Аритмия — гетерогенная группа нарушений ритма электрической активности сердца: нерегулярное сердцебиение, слишком частое (тахикардия) или слишком редкое (брадикардия) и т.д. Некоторые аритмии просто вызывают кратковременные пальпитации (трепетания), а другие — требуют неотложной медицинской помощи, так как могут привести к остановке сердца и внезапной смерти. Осложнениями аритмии являются тромбозы и ишемия миокарда вследствие недостаточно эффективного транспорта крови.
В МКБ-10 выделены 3 основные группы аритмий: I.47 «Пароксизмальная тахикардия», I.48 «Фибрилляция предсердий», и I.49 «Другие нарушения ритма сердца» (такие, как I.49.0 фибрилляции желудочков, I.49.1 преждевременная деполяризация предсердий, I.49.9 неспецифические нарушения ритма сердца и т.д.). Особо следует отметить так называемую проаритмию, которая, как это ни парадоксально, зачастую является результатом антиаритмической терапии, т.е. побочным эффектом некоторых антиаритмических средств [1—5]. Поэтому поиск эффективных антиаритмических средств с минимальными побочными эффектами весьма актуален.
ω-3-Полиненасыщенные жирные кислоты (ω-3-ПНЖК) — эссенциальный микронутриент с выраженными антиаритмическими свойствами. Антиаритмические эффекты ω-3-ПНЖК стали очевидны в результате экспериментальных, молекулярно-биологических и крупных эпидемиологических исследований. Рандомизированные исследования случай—контроль и проспективные (лонгитудинальные) исследования показали, что прием ω-3-ПНЖК действительно снижает риск развития инфаркта миокарда (ИМ) и внезапной остановки сердца [6]. Например, исследование GISSI-Prevenzione, включившее наблюдения за 11 324 пациентами в течение 3,5 года, показало эффективность ω-3-ПНЖК (омакор) для снижения смертности у пациентов после недавнего ИМ. Положительный эффект терапии наблюдался независимо от сопутствующих заболеваний, рекомендаций по диете или других видов терапевтического вмешательства. Более того, снижение риска общей смертности в исследованиях GISSI-P и GISSI-HF было показано независимо от влияния ω-3-жирных кислот на липидный состав крови [7, 8]. Было отмечено, что потребление ω-3-жирных кислот снижает частоту сердечных сокращений (ЧСС) при тахиаритмии (один из основных факторов риска внезапной смерти) и дозозависимо снижает уровни тригицеридов на 10—33% [9]. Следует также отметить, что прием омакора был эффективен и у пациентов, соблюдавших средиземноморскую диету и имевших ω-3-индекс в 7,8% (т.е. у пациентов, не испытывавших дефицита ω-3-ПНЖК в диете).
Для объяснения положительных сердечно-сосудистых эффектов ω-3-ПНЖК (уменьшения воспаления эндотелия, стабилизации атеросклеротических бляшек [10], снижения тромбообразования, сосудорасширяющего эффекта и для объяснения антиаритмического эффекта) были предложены различные молекулярные фармакологические механизмы. Во-первых, вмешиваясь в каскад арахидоновой кислоты, ω-3-жирные кислоты подавляют синтез и высвобождение провоспалительных простагландинов и эйкозаноидов. Это приводит к уменьшению секреции провоспалительных цитокинов таких, как фактор некроза опухолей (ФНО), интерлейкинов-1 и -2, повышенные уровни которых сопутствуют ишемической болезни сердца (ИБС) [11]. Во-вторых, ω-3-ПНЖК ингибируют определенные кальциевые каналы. В-третьих, ω-3-ПНЖК регулируют цитокин-индуцированную экспрессию индуцибельной синтазы оксида азота, снижая тонус сосудов и апоптоз гладких мышечных клеток [12].
Несмотря на то что антиаритмические эффекты ω-3-ПНЖК были продемонстрированы в многочисленных клинических и экспериментальных исследованиях, молекулярные механизмы антиаритмического действия неясны. В данной работе мы проводим систематический анализ результатов биохимических, молекулярно-биологических, экспериментальных, эпидемиологических и клинических исследований с целью выяснения наиболее «биологичных» молекулярных механизмов антиаритмического действия ω-3-жирных кислот, представленных в работах.
Поиск достоверных публикаций в базе данных MEDLINE для проведения систематического анализа [6—77] проводили с использованием компъютерной программы, разработанной на основе математической теории классификации значений признаков. Данная теория представляет собой современный подход к проблемам распознавания и развивается в научной школе академика РАН Ю.И. Журавлева [78, 79].
Эпидемиология
Имеющиеся эпидемиологические исследования представляют собой ценнейшую базу косвенных доказательств положительного влияния ω-3-ПНЖК на ЧСС, риск развития аритмии и внезапной смерти. Большинство эпидемиологических исследований основаны на анализе питания пациентов. Опросники питания позволяют оценить потребление продуктов, богатых ПНЖК (рыба, морепродукты) и рассчитать суммарное потребление ПНЖК. Затем анализируется корреляция между параметрами диеты и риском развития патологии. Например, внезапная смерть от остановки сердца встречается в 20 раз реже среди населения Японии, чем среди населения Германии. В Японии уровень эйкозапентаеновой (ЭПК) + докозапентаеновой (ДГК) кислот, по эпидемиологическим оценкам, довольно высок (ω-3-индекс в эритроцитах 11%), тогда как в Германии — гораздо ниже (4%) [13, 14]. Имеющиеся эпидемиологические данные охватывают различные географические регионы и различные популяции людей.
В ряде исследований выявлена корреляция между уровнем потребления рыбы и параметрами ритма сердца. В популяционном исследовании с участием 5096 мужчин и женщин оценивали потребление запеченной рыбы (в которой, в отличие от жареной, сохраняются наибольшие количества ω-3-ПНЖК). Сравнивали группы с максимальным и минимальным потреблением. Установлено, что снижение ЧСС ассоциировано с более высоким потреблением запеченной рыбы (–3,2 уд/мин при 95% доверительном интервале — ДИ от 1,3 до 5,1 уд/мин; р<0,001). У пациентов, употреблявших бо́льшие количества запеченной рыбы, также была существенно более низкой вероятность удлиненного интервала QT (относительный риск — ОР 0,5 при 95% ДИ от 0,27 до 0,95; р=0,03) [15].
В когорте 4815 взрослых старше 65 лет потребление тунца и другой запеченной рыбы коррелировало с уровнями ω-3-ПНЖК в фосфолипидах плазмы, в то время как для потребления жареной рыбы или рыбных котлет достоверные корреляции отсутствовали. За 12 лет наблюдений диагноз «фибриляции предсердий» был поставлен 980 пациентам. При многофакторном анализе потребление тунца или другой запеченной рыбы было обратно пропорционально риску развития фибрилляции предсердий — ФП (ОР 0,72 при, 95% ДИ от 0,58 до 0,91; р=0,005) [16].
В когорте из 1514 мужчин и 1528 женщин (от 18 до 89 лет) участникам были проведены электрокардиография и оценка питания посредством опросника. Как известно, риск развития аритмии возрастает с удлинением интервала QTc. В группе людей, употреблявших более 300 г рыбы в неделю, наблюдались на 14% более короткие интервалы QTc (р<0,01), чем в группе не употребляющих рыбу. Корреляция сохранилась после учета возраста, пола, физического состояния активности, индекса массы тела, курения, потребления орехов, и других вмешивающихся факторов [17].
В некоторых исследованиях предпринимаются попытки рассчитать потребление ω-3-ПНЖК на основе опросников рациона. Однако без дополнительной биохимической верификации уровня ω-3-ПНЖК в пище и в крови оценки такого рода заведомо неточны и, следовательно, могут приводить к ложноотрицательным или ложноположительным результатам. Например, в когорте «Women´s Health Initiative» из 44 720 участниц за 6 лет было диагностировано 378 случаев ФП. Потребление рыбы и ω-3-ПНЖК оценивали по опроснику и никаких корреляций между уровнями ω-3-ПНЖК и ФП найдено не было [18]. Отметим, что в данном исследовании оценивали потребление нежаренной рыбы, что не вполне корректно (так как, например, при варке рыбы также происходят потери ω-3-ПНЖК).
Наиболее важны эпидемиологические исследования, в которых проводится непосредственное измерение уровней ω-3-ПНЖК в крови и анализируются корреляции между измеренными уровнями и риском развития аритмии. Например, весьма показательно исследование, проведенное в когорте эскимосов Аляски (316 мужчин, 391 женщины, 35—74 лет) [19]. В связи с интервенцией так называемого цивилизованного питания популяция эскимосов переживает сдвиг традиционной диеты от преимущественно ненасыщенных жиров (рыба) к насыщенным жирам (мясопродукты, маргарин и т.д.). Поэтому в данной популяции наблюдается широкий диапазон обеспеченности ω-3-ПНЖК. Данные о ЧСС у участников этого исследования сопоставляли с содержанием ω-3-ПНЖК в эритроцитах. Многомерная линейная регрессия отражала уменьшение ЧСС с увеличением содержания ДГК (р=0,004) и ЭПК (р=0,009) в мембране эритроцитов [19].
В Финляндии в течение 18 лет проводились наблюдения за когортой из 2174 мужчин 42—60 лет. В течение этого периода у 240 участников была зарегистрирована аритмия предсердий. В модели пропорциональных рисков Кокса сравнение подгрупп пациентов с самым низким и самым высоким содержанием ЭПК + ДГК показало снижение риска развития аритмий у пациентов с более высокими уровнями ПНЖК в крови (отношение шансов — ОШ 0,65 при 95% ДИ от 0,44 до 0,96; р=0,07). Снижение риска было связано, в основном, с уровнями ДГК в крови (ОШ 0,62 при 95% ДИ от 0,42 до 0,92; р=0,02). Исключение из когорты пациентов с ИМ или сердечной недостаточностью (n=233) усиливало достоверность ассоциаций между ПНЖК и риском развития аритмии [20]. Из рассмотренных исследований работа [20] представляет собой одно из наиболее надежных эпидемиологических доказательств взаимосвязи уровней ПНЖК и аритмтии поскольку это крупное исследование с весьма длительным сроком наблюдений — почти 20 лет, в нем были сделаны прямые измерения ПНЖК в сыворотке, и исследование было основано на изучении стабильного генетического изолята (финны), что в значительной степени снижает неоднородность выборки вследствие плохо изученных генетических факторов.
Экспериментальные и биохимические исследования аритмии и ПНЖК
Ряд экспериментальных исследований указывают на антиаритмические эффекты ПНЖК. Длительность потенциала действия в желудочках миоцитов крыс дозозависима от концентрации ДГК: при увеличении уровней ДГК от 1 до 100 мкмоль/л происходило пропорциональное увеличение длительности потенциала действия [21]. При экспериментальном исследовании на изолированных в физиологическом растворе сердцах кроликов моделировалась аритмия типа torsades de pointes. Предварительное скармливание животным ω-3-ПНЖК предотвращало аритмию [22]. Мониторинг функции сердца с помощью магнитно-резонансной томографии у 21 овцы с доксорубицин-индуцированной фибрилляцией показал, что ω-3-ПНЖК предотвращают развитие гипертрофии левого предсердия (р=0,001) и приводят к более короткой продолжительности эпизодов аритмии предсердий (р=0,02) [23].
В некоторых случаях экспериментальные исследования дополнялись оценками биохимических параметров, направленными на выяснение особенностей молекулярных механизмов антиаритмических эффектов ПНЖК. В результате было сформулировано несколько гипотез о молекулярных механизмах действия ПНЖК:
1) неспецифическое взаимодействие ПНЖК с ионными каналами кардиомиоцитов;
2) косвенное влияние ПНЖК через противовоспалительные и антитромботические эффекты их производных в каскаде арахидоновой кислоты — эйкозаноидов и докозаноидов;
3) вазодилаторные эффекты эйкозаноидов и докозаноидов;
4) эффекты продуктов биотрансформаций ПНЖК цитохромами.
Гипотеза 1: неспецифическое взаимодействие ПНЖК с ионными каналов кардиомиоцитов
ω-3-ПНЖК тормозят возникновение аритмии за счет снижения концентрации внутриклеточного кальция и реакции на норадреналин (р<0,05) [24]. Простейшим объяснением является предположение о том, что антиаритмические эффекты ПНЖК могут быть связаны с прямым, неспецифичным взаимодействием ω-3-ПНЖК с ионными каналами, такими как Na+/Ca2+-транспортер кардиомиоцитов (NCX1) [25] и сотнями других ионных каналов. ω-3-ПНЖК и ω-6 ПНЖК также влияют на функционирование калиевых каналов типа «шейкер» [26]. Однако эффекты взаимодействия ПНЖК с ионными каналами регистрируются только при очень высоких внеклеточных концентрациях ПНЖК и весьма неспецифичны — другие ненасыщенные жирные кислоты помимо ДГК и ЭПК (линоленовая, линолевая, арахидоновая и др.) также значительно тормозят ток ионов через каналы [27].
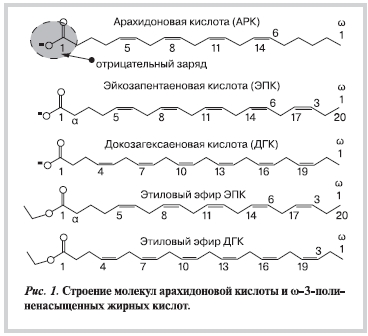
Скорее всего, эффект прямого взаимодействия с каналами обусловлен исключительно отрицательным зарядом атомов кислорода на карбоксильной группе ПНЖК (рис. 1). Действительно, незаряженные сложные эфиры (метиловые или этиловые) ПНЖК не влияют, например, на калиевые каналы [26]. Поэтому неспецифическое взаимодействие ПНЖК с ионными каналами является весьма поверхностным и, очевидно, недостаточным объяснением антиаритмического эффекта.
Гипотеза 2: противовоспалительные и антитромботические эффекты ПНЖК
Системное воспаление эндотелия сосудов и повышенная свертываемость крови также могут способствовать развитию аритмии. Поэтому ко второй группе гипотез относятся объяснения антиаритмических эффектов ПНЖК через торможение воспаления, атеросклероза и, следовательно, снижения стеноза артерий. Центральной идеей в этой группе объяснений антиаритмического эффекта является физическая проходимость сосудистого русла — чем более открыт просвет артерии, тем меньше вероятность турбулентного течения крови и тем меньше риск развития ФП.
ПНЖК характеризуются значительными противовоспалительными и вазодилататорными свойствами в связи с их влиянием на метаболизм простагландинов через каскад арахидоновой кислоты (АрК). ЭПК и ДГК конкурируют с АрК (см. рис. 1) через взаимодействия с циклооксигеназами и липоосигеназами, что снижает синтез провоспалительных простаноидов и одновременно стимулирует синтез антивоспалительных и нейропротекторных простаноидов, которые также способствуют вазодилатации [28, 29]. Каскад АрК следует рассмотреть более подробно, так как он является наиболее изученным механизмом воздействия ω-3-ПНЖК.
АрК — разновидность ω-3-ПНЖК присутствующая в значительном количестве в фосфолипидах составляющих клеточные мембраны. Биотрансформации АрК осуществляются посредством совокупности химических реакций известной под названием «каскад арахидоновой кислоты» (рис. 2). Сигнальные молекулы, образующиеся при превращениях АрК, контролируют функционирование иммунной, нервной и васкулярной систем.
На первом этапе АрК образуется из фосфолипидов посредством фосфолипаз, катализирующих гидролиз фосфолипидов до жирных кислот. Затем, АпК преобразуется либо в простаноиды (простагландины, простациклины, тромбоксаны) посредством циклооксигеназ, либо в лейкотриены через диоксигенацию жирных кислот с образованием гидропероксидов этих кислот посредством липооксигеназ.
В каскаде АрК сама АрК и ω-3-ПНЖК метаболизируются до важных сигнальных молекул, эйкозаноидов и докозаноидов. Эйкозаноиды — обширная группа биологически активных соединений, включающих простагландины, простациклины, тромбоксаны и лейкотриены. Эйкозаноиды осуществляют контроль над физиологическими системами тела, регулируя, главным образом, процессы воспаления, иммунного ответа и передачи сигнала в нервной системе. Известные докозаноиды менее многочисленны чем эйкозаноиды, и их область действия включает противовоспалительные реакции и нейропротективное действие [31].
ω-3-ПНЖК также трансформируются посредством описанного выше каскада АрК. Однако, в отличие от АрК, производные ПНЖК оказывают гораздо менее выраженное провоспалительное действие или даже просто ингибируют каскад АрК, предотвращая синтез провоспалительных молекул. Основной механизм действия ω-3-ПНЖК — ингибирование каскада АрК и синтез противовоспалительных эйкозаноидов (рис. 3).
Эйкозаноиды, синтезируемые в каскаде АрК, воздействуют на клетки целевых тканей через активацию/ингибирование специфических клеточных рецепторов. Большинство эйкозаноидных рецепторов передают сигнал через G-белки [32, 33]. Данные об известных типах рецепторов эйкозаноидов суммированы в табл. 1. Помимо G-белок-зависимых рецепторов, в табл. 1 также представлен рецептор PPARγ, внутриядерный рецептор стероидного типа который непосредственно воздействует на транскрипцию генов [34].
Таблица 1. Известные рецепторы эйкозаноидов*
Примечание. * — таблица упорядочена в соответствии с названиями генов рецепторов.
Как видно из табл. 1, большинство известных рецепторов эйкозаноидов влияют на бронхоконстрикцию/бронходилатацию и активацию клеток иммунной системы (хемотаксис лейкоцитов). Отметим, что бронхоконстрикция всегда провоцирует нарушения ритма (как правило, тахиаритмию, реже, экстрасистолы) из-за снижения кислородного обеспечения миокарда. Влияния эйкозаноидов на вазодилатацию также могут косвенно снижать риск развития аритмии (см. ниже).
Таким образом, ω-3-ПНЖК оказывают ярко выраженный противовоспалительный эффект, обусловленный биотрансформациями ω-3-ПНЖК в каскаде АрК. Снижение активности воспаления важно для торможения атеросклеротических процессов. Однако антиатеросклеротический эффект ω-3-ПНЖК проявляется при долговременном приеме и, вероятно, является далеко не самым важным механизмом антиаритмического воздействия ω-3-ПНЖК.
Гипотеза 3: ω-3-ПНЖК и вазодилатация
ω-3-ПНЖК (дозы 3—4 г/сут) способствуют снижению артериального давления (АД) [35, 36]. При солезависимой гипертонии, ω-3-ПНЖК усиливают положительные эффекты ограничения потребления поваренной соли. Эпидемиологические исследования указывают на взаимосвязь между уровнями потребления рыбы и параметрами вазодинамики [37, 38]. В эксперименте ДГК и ЭПК, принимаемые в микромолярных концентрациях, ингибировали провоцируемые агонистами α-адренорецепторов вазоконстрикторные реакции аорты [39]. Представляет интерес рассмотреть возможные молекулярные механизмы вазодилататорных эффектов, так как снижение АД вследствие вазодилатации способствует снижению риска аритмий.
Во-первых, следует отметить, что ω-6 ПНЖК (линоленовая, арахидоновая) также вызывают вазодилатацию [40]. Поэтому воздействие через простагландины — наиболее вероятное объяснение механизма вазодилатации и ω-6, и ω-3. Простациклин, синтезируемый из АрК, приводит к активации внутриклеточных G-белковых сигнальных каскадов, снижающих тонус сосудов. Анализ известных рецепторов эйкозаноидов (см. табл. 1) показывает, что наиболее вероятными рецепторами являются простагландин рецептор Е3 (ген PTGER3) и простациклин-рецептор (ген PTGIR). Продукты биотрансформаций ω-3 в каскаде АрК, вероятно, ингибируют рецептор Е3 и активируют рецептор простациклина. Однако вазодилатация, вызываемая продуктами ω-6 ПНЖК, дает побочные эффекты. Дело в том, что на промежуточных стадиях синтеза простациклина из ω-6 ПНЖК образуются другие простаноиды, приводящие к бронхо- и вазоконстрикции, констрикции гладкой мускулатуры желудочно-кишечного тракта и т.д. [41—43].
Во-вторых, другим возможным объяснением является воздействие ПНЖК на вазодилатацию через NO. Как известно, аргинин необходим для синтеза NO, причем последний синтезируется из аргинина посредством синтаз окиси азота. В эксперименте ω-3-ПНЖК способствовали экспрессии индуцибельной синтазы окиси азота (INOS), снижению экспрессии гена эндотелина (ЕТ1) и уровней эндотелина в плазме — изменения, соответствующие расширению сосудов [44]. В исследовании с участием 563 мужчин 64—76 лет потребление ω-3-ПНЖК сопровождалось значительным увеличением уровней аргинина в плазме (р<0,05) [45], что соответствует вазодилатации. ω-3-ПНЖК также снижали уровни Akt, EGF, JAM3, MHCalpha, что соответствует ослаблению неблагоприятного ремоделирования миокарда [44] и снижает риск аритмии.
В-третьих, антиаритмические эффекты ω-3-ПНЖК могут быть также связаны с модуляцией экспрессии в миокарде белка коннексин-43, который выступает посредником межклеточных контактов миокарда. Так как ω-3-ПНЖК и их производные являются лигандами для фактора транскрипции PPAR (см. табл. 1), то они воздействуют на экспрессию коннексина-43 что в долгосрочной перспективе способствовует уменьшению риска развития аритмии вследствие улучшения механических характеристик структуры миокарда [46].
В-четвертых, экспериментальные исследования показали, что сосудорасширяющий эффект ЭПК, ДГК и их производных сопровождается изменениями внутриклеточных концентраций кальция [47]. Производимый липоксигеназой продукт биотрансформаций ДГК, 17-гидро-ДГК, обладает гораздо более сильным вазодилататорным эффектом, чем сама ДГК. При этом известно, что 17-гидро-ДГК активирует особый вид кальций-зависимых каналов, BK(Ca)-каналов, которые и регулируют тонус сосудов [48]. ВК-каналы (Big Potassium conductance calcium-activated channel) обеспечивают проведение потоков калия (К) через мембрану кардиомиоцитов. Эти каналы активируются изменениями в потенциале мембраны или при изменении внутриклеточной концентрации кальция и модулируют возбудимость клеток.
В-пятых, продукты биотрансформаций ω-3-цитохромами, такие как эпоксиэйкозотетраеноевая кислота, также характеризуются отчетливым сосудорасширяющим эффектом, сопровождающимся активацией BK(Ca)-каналов и, возможно, K/АТФ-каналов [49]. Продукты биотрансформации ω-3-ПНЖК цитохромами заслуживают отдельного рассмотрения вследствие их ярко выраженных антиаритмических эффектов.
Гипотеза 4: Биотрансформации ПНЖК цитохромами
Отметим, что рассмотренные механизмы непосредственного и неспецифического торможения ионных каналов требуют миллимолярных (10–3 М, мМ) концентраций ω-3-ПНЖК в сыворотке крови. Эта концентрация соответствует потреблению взрослыми 10—20 г и более ω-3-ПНЖК с пищей. В то же время в клинических исследованиях антиаритмические эффекты ПНЖК наблюдаются уже при дозах 1—2 г, что соответствует микромолярным (10–6 М, мкМ) концентрациям ω-3-ПНЖК в крови. Уменьшение воспаления, несомненно, является значимым механизмом воздействия ПНЖК. Однако для развития этого эффекта требуется значительное время — недели и месяцы. При этом антиаритмический эффект ω-3-ПНЖК может проявляться в течение нескольких минут после приема. Последнее утверждение следует как из нашей клинической практики (например, прием стандартизированных по качественному и количественному составу этиловых эфиров ДГК и ЭПК, препарат омакор), так и из экспериментальных исследований (см. ниже).
Результаты новейших биохимических исследований показывают, что ЭПК и ДГК могут конкурировать с АрК не только в ее каскаде, но и в каскадах биотрансформаций поддерживаемых ферментами цитохромами P450 (CYP). В результате этих биотрансформаций образуются физиологически активные метаболиты, называемые «ω-3-эпоксидами» [50].
Цитохромы CYP2C и CYP2J преобразуют АрК в эпоксиэйкозотриеновые кислоты (ЭЭК), ω-3 ЭПК в 17,18-эпоксиэйкозотетраеновую (17,18-ЭЭТК) и ДГК в 19,20-эпоксидокозопентаеновую кислоты (19,20-ЭДПК) [51]. Цитохромы CYP4A и CYP4F трансформируют ЭПК в 20-гидроксиэйкозотетраеновую кислоту (20-ГЭТК). ЭЭТК и ГЭТК регулируют гладкую мускулатуру сосудов и функции почек [52—54] (рис. 4). Хотелось бы подчеркнуть, что ω-3 эпоксиды ЭДПК и ЭЭТК обладают характерными антиаритмическими свойствами, подавляющие Ca2+-индуцированный ритм кардиомиоцитов уже при наномолярных (10–9 М, нМ) концентрациях [55].
Исследование метаболизма ЭПК и ДГК с использованием радиоактивных меток показало, что цитохромы CYP2C8, CYP2C19 и CYP2C11 метаболизируют ДГК почти с такой же скоростью, как и АрК. Цитохром CYP4F2 метаболизирует ДГК в 2 раза быстрее, чем АрК, CYP2E1 также показали, в 2 раза выше, деятельность по ДГК, чем АрК. Активность CYP2J2 в 17 раз выше с ЭПК и в 4 раза выше с ДГК, чем с АрК (рис. 5) [55].
В эксперименте прием добавок с ЭПК/ДГК вызывал переход профиля ПНЖК от АрК-метаболитов к упомянутым ранее ЭПК- и ДГК-производным метаболитам (ЭЭК, ЭТК, ЭЭТК и др). Уровни ЭЭК, синтезируемой из АрК, были снижены на 52% в левом желудочке и на 78% в плазме. При этом наблюдалось значительное увеличение уровней эпоскидов ЭПК и ДГК (так называемые ЭЭТК и ЭДПК, см. выше) — на 60% в левом желудочке и на 40% в плазме [55].
Следует подчеркнуть, что соединения ЭЭТК (эпоксиметаболит ЭПК) и ЭДПК (эпокси-метаболит ДГК) непосредственно влияют на сократимость кардиомиоцитов. Кардиомиоциты реагируют на увеличение внеклеточного кальция увеличением ЧСС. Эта реакция в значительной степени подавляется после предварительной инкубации клеток (в течение 30 мин) с 3,3 мкМ ЭПК (см. рис. 5). Важно отметить, что для развития антиаритмического эффекта при приеме ЭПК требуется около 30 мин. В то же время эффект эпоксида ЭПК (ЭЭТК) наблюдался гораздо раньше — в течение 3—5 мин. Подчеркнем, что антиаритмический эффект ЭЭТК развивается при очень низких концентрациях — 30 нМ/л.
Кроме того, влияние 17,18-ЭЭТК стереоселективно (т.е. зависит от такой тонкой особенности структуры молекулы, как оптическая изомерия), что свидетельствует о высокой специфичности взаимодействия ЭЭТК с таргетными белками-рецепторами — по всей видимости, кальциевыми каналами кардиомиоцитов (рис. 6). В эксперимент, стереоизомер ЭЭТК R,S-типа приводил к снижению ритма кардиомиоцитов на 20—30 уд/мин, тогда как стереоизомер S,R-типа был неактивным [55]. Такие продукты трансформаций ω-3-ПНЖК, как ЭЭК также способствуют стерео-специфичной активации К/АТФ-зависимых ионных каналов, причем тоже в наномолярных концентрациях (40 нМ). Активация калиевых каналов посредством эпоксидов ЭПК и ДГК — еще один весьма вероятный молекулярный механизм воздействия ω-3-ПНЖК на электрическую активность сердца [56].
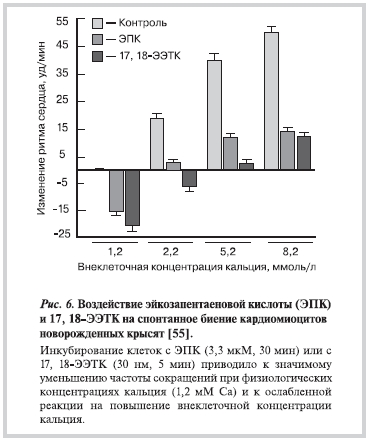
Как видно из данных, полученных в работах [50, 55, 56], формирование ω-3-эпоксидов — наиболее вероятное объяснение «быстрых» антиаритмических эффектов ω-3-ПНЖК. Во-первых, эпоксиды действуют в наномолярном (!) диапазоне, что соответствует дозе ПНЖК для взрослых в диапазоне 1—4 г/сут. Во-вторых, эти эффекты высоко специфичны для производных ЭПК и ДГК и не наблюдаются при метаболизировании цитохромами других ненасыщенных жирных кислот, таких как АрК. Кроме того, антиаритмический эффект зависит от стереохимии молекул ЭЭТК и ЭДПК, что указывает на высокую селективность взаимодействия с целевыми («таргетными») кальциевыми каналами. Столь высокая селективность взаимодействия характерна для специально разработанных ингибиторов (т.е. молекул-кандидатов на антиаритмические средства) и все же наблюдается в случае «всем известных» ω-3-ПНЖК. Особенно четко антиаритмический эффект по нашему опыту отмечен при приеме стандартизированного по качественному и количественному составу этиловых эфиров ДГК и ЭПК препарата омакор.
Клинические исследования антиаритмических эффектов ω-3-ПНЖК
Специфические молекулярные механизмы антиаритмического действия ПНЖК, сформулированные в [50, 55] и сопутствующих работах, позволяют предположить отчетливый клинический эффект молекул ω-3-ПНЖК в терапии и профилактике аритмий. Действительно, в ряде клинических исследований показаны положительные влияния ω-3-ПНЖК на сердечно-сосудистую систему в целом и на уменьшение риска развития аритмии, в частности.
Однако из-за отсутствия стандартизации ω-3-со держащих продуктов в составе многочисленных биологических добавок (БАД) и типичных проблем с анализом данных в биомедицинских исследованиях [57, 58], при клинических испытаниях ω-3-ПНЖК в составе БАД может не наблюдаться отчетливого эффекта. Отметим, что в большинстве клинических испытаний препараты ω-3-ПНЖК по-прежнему называют как рыбьим жиром (англ. fish oil), что является неточным термином, вульгаризмом. Отсутствие четкой стандартизации разнообразных добавок с ω-3-ПНЖК — наиболее важная причина неудач отдельных клинических исследований, претендующих на статус «доказательных». Среди клинических исследований ω-3-ПНЖК кажется надлежащим упомянуть, прежде всего, результаты хорошо известного исследования GlSSI-Prevenzione (Gruppo Italiano в Lo Studio делла Sopravvivenza nell√Infarto Miocardico), в которые были включены 11 323 пациентов. Долгосрочный прием ω-3-ПНЖК в форме этиловых эфиров ЭПК и ДГК по 1 г ЭПК+ДГК/сут приводило к достоверному снижению смертности, риска развития нефатального ИМ и инсульта [59]. Смертность от всех причин была значительно снижена после 3 мес лечения (ОШ 0,59 при 95% ДИ от 0,36 до 0,97; р=0,04). В частности, наблюдалось уменьшение в 2 раза риска развития аритмий, являющихся одной из основных причин внезапной смерти (ОШ 0,47 при 95% ДИ от 0,22 до 1,0; р=0,05) [60].
Популяционное исследование, проведенное в 6 округах Италии в течение 3 лет, включило более 1000 пациентов с ИМ (МКБ-9 диагноз 410). ω-3-ПНЖК снижали показатели ОР госпитализации по поводу ФП (ОШ 0,19 при 95% ДИ от 0,07—0,51) и соответствовали показателям по снижению смертности от всех причин (ОШ 0,15 при 95% ДИ от 0,05 до 0,46) [61].
В исследовании с участием 260 пациентов с острым ИМ потребление ω-3-ПНЖК оценивалось с помощью Гарвардского опросника; желудочковая эктопия оценивалась по 24-часовой записи электрокардиограммы. Бо́льшее потребление ω-3-ПНЖК было связано с более низким риском желудочковой эктопии (р=0,01), причем этот эффект был более выражен при исключении пациентов с другими сердечно-сосудистыми заболеваниями (р=0,003) [62].
Следует отметить, что для пациентов, проходящих подготовку к операциям на сердце, превентивный прием ω-3-ПНЖК весьма полезен в целях снижения риска послеоперационных осложнений — прежде всего, ФП. Важно подчеркнуть, что ПНЖК должны употребляться именно заранее до операции на сердце. Позднее назначение ω-3-ПНЖК, например, в день или за несколько дней до операции, а также использование с данной целью пищевых добавок не снижают риск развития ФП при приеме после операции [63,64]. Наблюдения за 160 пациентами, перенесшими коронарное шунтирование, показали, что предоперационный прием ПНЖК (во время пребывания в стационаре) существенно снижает частоту развития послеоперационной ФП (р=0,01) и связан с более коротким периодом пребывания в стационаре [65]. В другом исследовании 258 пациентов («случай» —129 пациентов, «контроль» — 129) подверглись катетерной аблации (т.е. устранению причин нарушений ритма сердца через катетер). У 35 (27%) пациентов в основной группе развился ранний рецидив аритмии по сравнению с 57 (44%) пациентами в контрольной группе (р<0,0001) [66]. В 4-летнем исследовании группы из 530 пациентов, прошедших операции на сердце (363 мужчин, 66±11 лет), предоперационный прием ПНЖК привел к 46% снижению риска раннего развития ФП (ОШ 0,54 при 95% ДИ от 0,31 до 0,92) [67].
Следует отметить, что отдельные исследования эффектов ω-3-ПНЖК стоят особняком. Например, несколько недавних (2009—2010) крупных исследований утверждают «неочевидность» полезности препаратов ПНЖК в терапии и профилактике аритмий [18, 68—70]. Исследование [18] мы уже упоминали ранее в связи с попытками оценки статуса ПНЖК на основе опросников по диете без биохимических анализов реального содержания ω-3-ПНЖК.
Отрицательные результаты (отсутствие выраженной ассоциации) ни доказывают, ни опровергают позитивные эффекты ПНЖК у пациентов с ИБС или аритмией [71]. Часто отрицательные результаты крупных исследований являются следствием неадекватного дизайна исследования или же неполноты использованных процедур статистического анализа данных [58, 72]. Однако весьма поучительно рассмотреть эти отрицательные результаты, поскольку они указывают на рациональный выбор наиболее подходящих препаратов ω-3-ПНЖК, режим назначения этих препаратов и необходимые дозировки.
Например, в проспективном рандомизированном многоцентровом исследовании с участием 663 пациентов с пароксизмальной (n=542) или персистентной (n=121) ФП, ω-3-ПНЖК (8 г/сут) или плацебо давались в течение первых 7 дней. Затем доза ω-3-ПНЖК была снижена до 4 г/сут в течение остальных 23 нед исследования. Уровни ЭПК и ДГК в крови, регистрируемые на 4-й и 24-й неделях исследования, были значительно выше в группе принимавших ω-3-ПНЖК. Тем не менее 24-недельное лечение «не снижало рецидивов ФП» [70].
Прежде чем перейти к пробелам, очевидным в дизайне данного исследования, хотелось бы отметить профессиональные интересы авторов исследования [70]. В течение десятилетий авторы данного исследования эффектов ω-3-ПНЖК занимаются изучением «тяжелых» фармакологических препаратов, таких как дронедарон [81, 82], дабигатран [83], дофетилид [84], вернакалант [85] и др. Возникает естественный вопрос — почему данная группа исследователей вдруг проводит крупное исследование по ω-3-ПНЖК и тут же получает отрицательные результаты?...
Проблемы анализа данных в биомедицинских исследованиях [57, 58, 72], которые приводят к ложноположительным или ложноотрицательным результатам, связаны с неточностями в дизайне исследования, отсутствием контроля за комплаентностью, недостаточно полным сбором анамнеза, лабораторных и прочих данных о каждом пациенте, отсутствием стратификационного анализа данных, повышением частоты неизвестных вмешивающихся факторов (англ. «unobserved confounder») в больших когортах пациентов и т.д. В результате собираемые данные характеризуются очень низким «полезным сигналом» на фоне высокого уровня «шума» и положительные эффекты терапии теряются в этом статистическом «шуме». При таких обстоятельствах клинические исследователи должны быть очень осторожны уже на стадии дизайна исследования и уделять особое внимание не только биологической активности препарата, но и фармакологической форме, и адекватности выбираемой дозы активного вещества, и длительности наблюдения.
Рассмотрим дизайн исследования [70]. Критерии отбора пациентов достаточно нетипичны и включают явную манипуляцию группами пациентов в зависимости от приема препарата. Во-первых, авторы ограничили срок исследования 6 мес — довольно короткий срок, принимая во внимание результаты большинства исследований по ω-3-ПНЖК. Во-вторых, авторы утверждают, что в исследование вошли пациенты с пароксизмальной ФП, не получавшие какой-то абстрактной «долговременной терапии антиаритмиками» (термин «долговременная» авторами не определяется, что ставит внимательного читателя публикации [70] в полное недоумение). Отметим, что произвольное, волюнтаристское определение группы объектов (в данном случае критерии отбора пациентов) — гарантия низкой аккуратности распознавания и отсутствия статистически значимых корреляций [78, 79]. В-третьих, значительная пропорция этих пациентов (почти 50%) почему-то принимала ингибиторы ангиотензинпревращающего фермента (АПФ), причем авторы не приводят никаких объяснений этому факту. В-четвертых, авторы исключили пациентов с постоянной ФП, вторичной ФП и полностью проигнорировали такие важные исходы, как сердечно-сосудистая смертность и смертность от других причин. В-пятых, авторы умалчивают о том, что статистически значимые эффекты ω-3-ПНЖК (р<0,05) наблюдались ими в подгруппе женщин и у пациентов, принимавших ингибиторы АПФ; тренды (р<0,07) наблюдались при изменении возраста. Стратификацию по возрастным группам авторы фактически не проводили.
Список очевидных пробелов дизайна исследования [70] можно продолжать. Сами авторы признают, что не было контроля за комплаентностью или способом приема ω-3-ПНЖК (до, после, во время еды), не были учтены показатели диеты (которые, как мы видели ранее, очень важны), авторы намеренно использовали произвольные допущения при анализе данных, подгоняя полученные ими результаты под критерии, разработанные для анализа эффективности синтетических антиаритмических средств (см. стр. 2371 в публикации [70]) и т.д. Поэтому полученный авторами отрицательный результат закономерен.
Рассмотрим другие причины неудач при проведении клинических исследований. Во-первых, следует отметить, что препараты ω-3-ПНЖК — это препараты природного происхождения. К сожалению, точный состав так называемого рыбьего жира (в частности, концентрация ДГК) редко принимается во внимание клиницистами. При использовании нестандартизированных БАД с ω-3-ПНЖК реально поступающая доза действующего вещества (ЭПК, ДГК) изменяется в широких пределах. В то же время для отчетливого клинического эффекта потребление чистых ЭПК+ДГК должно быть не менее 800—1000 мг/сут для пациентов с ИБС [73]. Более низкие дозы будут оказывать намного более слабое терапевтическое воздействие.
Например, в исследовании с участием 546 пациентов с имплантированными водителями ритма продолжали регистрироватся эпизоды злокачественной желудочковой тахикардии. Примение ω-3-ПНЖК в виде «рыбьего жира» не оказывало статистически значимых эффектов [69]. Суточная доза «рыбьего жира» (2 г/сут) содержала в среднем 961 мг ω-3-ПНЖК (464 мг ЭПК, 335 мг ДГК). Ключевым словом здесь является именно «в среднем», так как анализ различных препаратов «рыбьего жира» показывает значительные различия в реальном содержании ПНЖК — до 60%. Например, в работе [74] исследовалось 9 препаратов, большинство из которых не достигли рекомендуемой суточной дозы 1 г. Самый высокий процент ДГК и ЭПК был обнаружен в омакоре (96±0,6% от заявленного содержания) и перкуроре (77±7%) [74].
Во-вторых, значительный разброс в реальном содержании ω-3-ПНЖК определяется не только природным происхождением препаратов, но и тем, что ω-3-ПНЖК — сильные антиоксиданты. Как результат, ω-3-ПНЖК довольно легко окисляются при неправильных условиях хранения (свет, повышенная температура, открытый воздух) и концентрация активного вещества значительно падает. Поэтому передовые производители фармакологических препаратов используют специальные стабилизаторы ПНЖК (витаминные антиоксиданты, такие как витамин Е, специальные крахмальные матрицы, позволяющие стабилизировать ω-3-ПНЖК, использование этиловых или метиловых эфиров ПНЖК и.т.д). Однако не все производители препаратов на основе ПНЖК учитывают эти факторы. Поэтому разброс в реальной дозе ω-3-ПНЖК может привести к противоречивым результатам, особенно в случае крупных исследований.
Кроме того, более длительный срок исследования соответствует более высокой суммарной дозе ω-3-ПНЖК. Например, ранее мы цитировали исследование по ФП, в котором не было получено достоверных эффектов ПНЖК [69]. В аналогичном двойном слепом исследовании 402 пациента с имплантированными кардиовертерами-дефибрилляторами были рандомизированы в группу приема препарата либо ω-3-ПНЖК либо плацебо (оливковое масло) в течение 12 мес [75]. Суммарная суточная доза ЭПК + ДГК в расчете на «чистые ω-3-ПНЖК» была выше —2,6 г/сут, чем в «безрезультативном» исследовании [69], сроки приема — тоже. Как результат, применение ω-3-ПНЖК обеспечило тенденцию к снижению риска развития ИБС (28% снижение риска; р=0,057). Подтвержденный регулярный прием ω-3-ПНЖК в течение 11 мес еще более снизил риск развития аритмии (снижение риска на 38%; р=0,034) [75]. В-третьих, при планировании крупных исследований следует принимать во внимание фармакокинетические свойства различных форм ω-3-ПНЖК. В плохо спланированных исследованиях используется, как правило, «сырой», неочищенный от примесей и токсинов и, по-видимому, самый дешевый «рыбий жир». Однако в общеизвестных и наиболее успешных исследованиях, таких как GISSI-Prevenzione и GISSI-HF, ω-3-ПНЖК вводились как этиловые эфиры (а не как триглицериды, присутствующие в дешевых формах ПНЖК под названием «рыбий жир»). Этиловые эфиры ω-3-ПНЖК приводят к устойчивой кишечной адсорбции ЭПК и ДГК, лучшей биодоступности и, следовательно, более высоким уровням ПНЖК в крови [76].
Здесь отметим, что препарат омакор представляет высококонцентрированный препарат ω-3-ПНЖК (не менее 90% ПНЖК [74]) с одной из самых высоких степеней очистки от примесей. Кроме того, в состав омакора входят именно этиловые эфиры ЭПК и ДГК, что не только повышает стабильность ПНЖК, но и улучшает всасывание препарата. Высокоочищенные этиловые эфиры ЭПК и ДГК способствуют сохранению стабильных и воспроизводимых фармакологических эффектов препарата. И наоборот, быстрое окисление низкоочищенных и нестабилизированных форм ω-3-ПНЖК при воздействии солнечного света, длительном хранении и др. приводит к слабой эффективности некоторых БАД, а также к непредсказуемому результату при добавлении компонентов рыбьего жира в маргарин, йогурты и сухие смеси.
Поэтому следует отличать фармакологически стабилизированные формы ω-3-ПНЖК в составе препарата омакор от сотен и тысяч БАД к пище. Использование нестандартизированных (но дешевых) БАД на основе ω-3-ПНЖК приводит к потере бесценного времени для реабилитации, так как может не давать никаких клинически значимых результатов. Такая подмена крайне неэтична по отношению к пациентам, перенесшим ИМ или имеющим высокий риск развития ИМ. И, конечно же, доказательная база, полученная в клинических исследованиях стандартизированного препарата ω-3-ПНЖК 90% (например, омакор), не может быть перенесена на другие источники ω-3-ПНЖК.
В-четвертых, проблема неизвестных вмешивающихся факторов (англ. «unobserved confounder») будет всегда преследовать крупные исследования в связи с резким увеличением неоднородности когорты [58, 72]. Например, в эпидемическом исследовании с участием 47 949 пациентов в течение 6 лет ФП развилась у 556. Потребление ω-3-ПНЖК и здесь оценивалось по пищевому опроснику и «отчетливых корреляций» со снижением риска развития ФП не наблюдалось. Однако авторы открыто признали по крайней мере один «неизвестный фактор» — отсутствие информации о потребление пищевых добавок «рыбьего жира». Это фактор не был включен в дизайн исследования и, как следствие, остался неучтенным [68].
Заключение
Эффективность стандартизированных ω-3-полиненасыщенных жирных кислот 90% убедительно показана в многочисленных клинических исследованиях. В заключении совещания совета российских экспертов-кардиологов [77] указано, что высокое содержание ω-3-полиненасыщенных жирных кислот в препарате является защитным фактором, снижающим смертность от хронической сердечной недостаточности, желудочковой аритмии и фибрилляции предсердий. Хотя отдельные «доказательные» исследования ставят под сомнение эффективность ω-3-полиненасыщенных жирных кислот в профилактике и терапии аритмий, правильно спланированные и тщательно выполненные крупные исследования стандартизированных препаратов ω-3-поли ненасыщенных жирных кислот указывают на отчетливый положительный эффект.
Клинические и экспериментальные исследования поддерживаются вескими доказательствами, полученными из фундаментальных биохимических исследований эпокси-метаболитов эйкозапентаеновой и докозапентеновой, образующихся при биотрансформациях ω-3-полиненасыщенных жирных кислот цитохромами. Такие эпоксиды ω-3-полиненасыщенных жирных кислот проявляют характерные антиаритмические свойства уже при наномолярных концентрациях и оказывают антиаритмический эффект в течение считанных минут
Детальное изучение соответствующих молекулярных путей, идентификация потенциальных белков-мишеней (по всей видимости, определенных кальциевых каналов миокарда) необходимо не только для дальнейшего уточнения молекулярно-фармакологического механизма антиаритмического воздействия ω-3-полиненасыщенных жирных кислот, но и позволит осуществить разработку рационального дизайна более биодоступных и эффективных форм ω-3-полиненасыщенных жирных кислот с повышенной антиаритмической эффективностью.
Перспективным направлением биоинформационных исследований является установление наиболее вероятных кальциевых каналов, через которые осуществляются антиаритмические и вазодилататорные эффекты ω-3-полиненасыщенных жирных кислот и их производных. Определение этих рецепторов позволит перейти к следующему этапу исследований — моделированию взаимодействий различных форм ω-3-полиненасыщенных жирных кислот с пространственными структурами белков-рецепторов [80]. Существует четыре перспективных направления выбора белков-рецепторов для моделирования комплексов молекул в составе препарата Омакор и других ω-3-полиненасыщенных жирных кислот с рецепторами: 1) ферменты каскада арахидоновой кислоты, 2) цитохромы, преобразующие ω-3-полиненасыщенных жирных кислот, 3) рецепторы простагландинов и эйкозаноидов (см. табл. 1) и, конечно же 4) кальциевые каналы, обеспечивающие «быстрый» антиаритмический эффект препарата Омакор и ω-3-полиненасыщенных жирных кислот. Результаты расчета энергий связывания молекулы с рецептором для разных видов ω-3-полиненасыщенных жирных кислот, молекул арахидоновой кислоты и других молекул ω-3-полиненасыщенных жирных кислот, взятых из биологически активных добавок позволят определить количественную и качественную разницу взаимодействия с рецепторами, ответственными за развитие антиаритмического эффекта, выявить особенности связывания (степень сродства, воздействие на структуру самого рецептора и др.).
Работа выполнена при поддержке грантов РФФИ 09-07-12098, 09-07-00212-а и 09-07-00211-а.



