Острое повреждение почек (ОПП) нередко наблюдается у больных острым инфарктом миокарда (ОИМ) [1—3]. Так, анализ результатов лечения 59 970 пациентов с ОИМ в США продемонстрировал наличие ОПП у 16,1%, при этом в 96% случаев использовалась коронарография [3]. Применение рентгенконтрастных препаратов может вести к развитию контрастиндуцированного ОПП, частота которого может достигать 44% [4—6]. В этой связи трудно оценить вклад других факторов в развитие ОПП у пациентов с ОИМ.
Использование тромболитической терапии (ТЛТ) — важная тактика реперфузии у больных острым инфарктом миокарда с подъемом сегмента ST (ОИМпST), особенно там, где чреcкожное коронарное вмешательство (ЧКВ) не может быть доступным в пределах рекомендуемых сроков [7]. Европейским и Американским обществом кардиологов рекомендовано использование как фибринспецифических (алтеплаза, ретеплаза и тенектеплаза), так и фибриннеспецифических (стрептокиназа) тромболитических препаратов, однако первой группе следует отдавать предпочтение [7, 8]. При этом нужно отметить, что стоимость стрептокиназы ниже, чем других препаратов.
 Между тем введение стрептокиназы может сопровождаться развитием артериальной гипотензии, частота которой зависит от скорости введения препарата и достигает 54% [9, 10], что связывают с образованием брадикинина [11]. Для алтеплазы артериальная гипотензия не является частым осложнением и наблюдается значительно реже — в 3% случаев [12]. Важно отметить, что артериальная гипотензия — одна из частых причин острого кардиоренального синдрома [13]. Так, ОПП развивается у каждого второго больного ОИМ, осложнившимся кардиогенным шоком [2, 14]. В этой связи можно предположить, что на частоту и тяжесть ОПП при ОИМ может влиять тип используемого тромболитического препарата.
Между тем введение стрептокиназы может сопровождаться развитием артериальной гипотензии, частота которой зависит от скорости введения препарата и достигает 54% [9, 10], что связывают с образованием брадикинина [11]. Для алтеплазы артериальная гипотензия не является частым осложнением и наблюдается значительно реже — в 3% случаев [12]. Важно отметить, что артериальная гипотензия — одна из частых причин острого кардиоренального синдрома [13]. Так, ОПП развивается у каждого второго больного ОИМ, осложнившимся кардиогенным шоком [2, 14]. В этой связи можно предположить, что на частоту и тяжесть ОПП при ОИМ может влиять тип используемого тромболитического препарата.
Целью исследования явилась оценка частоты и тяжести ОПП у больных ОИМпST, которым выполнялся тромболизис алтеплазой или стрептокиназой. В исследование включены только больные, которым по тем или иным причинам в остром периоде инфаркта миокарда не выполнялась коронарография, что позволяет исключить развитие контрастиндуцированного ОПП.
Материал и методы
Обследованы 292 больных ОИМпST, которым в 2008—2012 гг. в отделении неотложной кардиологии Центральной городской клинической больницы Ульяновска был выполнен тромболизис, из них 170 (58%) — стрептокиназой, 122 (42%) — алтеплазой. Мужчин было 227 (78%), женщин 65 (22%), средний возраст больных составил 58±11 лет. Критерием исключения из исследования было проведение коронарографии в остром периоде инфаркта миокарда. Протокол обследования был утвержден Этическим комитетом ГУЗ «Центральная городская клиническая больница г. Ульяновска». В исследование включали больных, подписавших информированное согласие. Характеристика больных представлена в таблице.
Диагностику ОИМпST, наличие показаний и противопоказаний к тромболизису, а также оценку его эффективности осуществляли согласно Рекомендациям ВНОК (2007) [15]. Тяжесть острой сердечной недостаточности (ОСН) оценивали по Killip (1967). ОПП диагностировали и классифицировали согласно Рекомендациям KDIGO (2012) — в случае повышения уровня креатинина в сыворотке крови ≥26,5 мкмоль/л в течение 48 ч [16]. Мы не располагали информацией об уровне креатинина в сыворотке до заболевания, поэтому исходным считали уровень в момент госпитализации, до начала тромболизиса. В случае повышения уровня креатинина в сыворотке крови ≥26,5 мкмоль/л или в 1,5—1,9 раза по сравнению с исходным уровнем регистрировали I стадию тяжести ОПП, при увеличении в 2—2,9 раза — II стадию, в 3 раза и более или ≥ 353,6 мкмоль/л — III стадию. Диагностику ОПП по диурезу не осуществляли, поскольку у больных не было показаний к катетеризации мочевого пузыря, и почасовой учет диуреза был невозможен.
Статистическую обработку данных проводили с использованием программы Statistica for Windows 8.0. Достоверность различий несвязанных переменных определяли по критерию t Стьюдента, при нормальном распределении параметров, если распределение отличалось от нормального, использовали критерий U Манна—Уитни. Для сравнения зависимых групп использовали критерий Вилкоксона. Проводили однофакторный корреляционный анализ (в зависимости от вида распределения — Пирсона или Кендалла). Для сравнения 2 групп по качественному признаку использовали критерий χ2 Пирсона. Для исследования связи бинарного признака с несколькими количественными и качественными признаками применяли логистический регрессионный анализ. В случае приближенно нормального распределения данные представлены в виде M±SD, где M — среднее арифметическое, SD — стандартное отклонение, в противном случае данные представлены в виде Me (ИКР), где Me — медиана, ИКР — интерквартильный размах (25-й процентиль — 75-й процентиль). Различие считали достоверным при р<0,05.
Результаты
Время от появления клинических признаков ОИМ до госпитализации составило 2,5 ч (ИКР 1,67—4,00), при этом в течение первых 6 ч госпитализированы 256 (88%) больных. Тромболизис был эффективен у 213 (73%) пациентов. Достоверных различий по эффективности ТЛТ при использовании стрептокиназы (у 120 из 170 больных) и алтеплазы (у 93 из 122) не было (χ2=1,14; p=0,28).
Только у 25 (9%) пациентов при поступлении тяжесть ОСН соответствовала III и IV классу по Killip. Группы больных, в которых в качестве тромболитического препарата использовалась стрептокиназа или алтеплаза, по тяжести ОСН не различались (χ2=0,05; p=0,81).
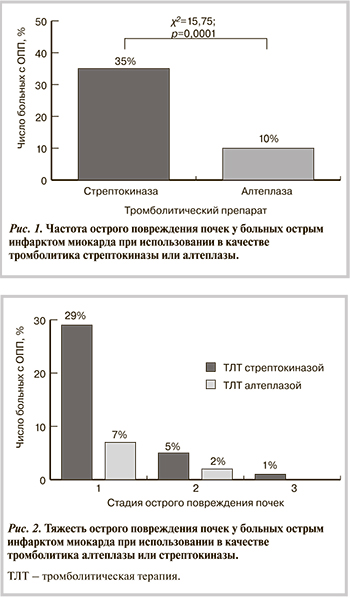
Уровень креатинина в сыворотке крови в момент госпитализации составил 99,3 (84,0—117,0) мкмоль/л, через 48 ч — 109,0 (97,9—129,3) мкмоль/л (p=0,0005). ОПП по динамике уровня креатинина диагностировано у 72 (25%) пациентов. При использовании стрептокиназы ОПП выявлялось чаще — у 60 из 170 больных, чем при введении алтеплазы — только у 12 из 122 (χ2=15,75; p=0,0001; рис. 1). У 49 (29%) пациентов, которым проводился тромболизис стрептокиназой, диагностирована I стадия, у 9 (5%) — II стадия и у 2 (1%) — III стадия ОПП. У 9 (7%) больных, которым вводилась алтеплаза, верифицирована I стадия, у 3 (2%) — II стадия ОПП (рис. 2). При этом тяжесть ОПП у больных, подвергнутых тромболизису стрептокиназой, была достоверно выше (χ2=14,93; p=0,0001).
 Снижение систолического артериального давления ниже 90 мм рт.ст. во время введения стрептокиназы наблюдалось чаще — у 26 (15%) больных, чем при введении алтеплазы — у 5 (4%) (χ2=9,38; p=0,002).
Снижение систолического артериального давления ниже 90 мм рт.ст. во время введения стрептокиназы наблюдалось чаще — у 26 (15%) больных, чем при введении алтеплазы — у 5 (4%) (χ2=9,38; p=0,002).
Логистический регрессионный анализ показал, что при использовании стрептокиназы независимо от пола, возраста, времени от возникновения инфаркта миокарда до госпитализации и тяжести ОСН относительный риск развития ОПП по сравнению с алтеплазой составил 2,25 при 95% доверительном интервале от 1,36 до 4,76. Проведение гемодиализа потребовалось только одной больной. В период пребывания в стационаре умерли 18 (6%) больных, госпитальная летальность была выше у больных с II—III стадией ОПП, чем у остальных пациентов (χ2=9,65; p=0,002).
Обсуждение
Современные Рекомендации KDIGO (2012) по диагностике и лечению ОПП предполагают оценку функции почек по динамике уровня креатинина в сыворотке крови относительно известного (на протяжении последних 7 дней до события) или базального, соответствующего скорости клубочковой фильтрации 75 мл/мин/1,73 м2, уровня и почасовому диурезу [16]. В настоящее время продолжают обсуждаться целесообразность диагностики ОПП по базальному креатинину (в связи с невозможностью исключения хронической болезни почек), а также адекватность оценки почасового диуреза, основываясь на сборе мочи при самостоятельном мочеиспускании за 6-часовой отрезок времени [17]. С учетом этого мы диагностировали ОПП по динамике уровня креатинина, относительно его уровня до начала тромболизиса.
Развитие ОПП у больных ОИМ связано с изменением системной и почечной гемодинамики, воздействием рентгенконтрастных препаратов и другими факторами [13]. ОПП ведет к повышению летальности в период пребывания больных в стационаре, в течение полугода, 1, 3, 5 и 10 лет после ОИМ, причем, чем тяжелее ОПП, тем выше вероятность смерти [3, 14, 18, 19].
Большинство исследований по оценке частоты ОПП у больных ОИМпST выполнено с участием пациентов, подвергнутых ЧКВ. Использование в этом случае рентгенконтрастных препаратов может у 1—44% больных вести к развитию контрастиндуцированной нефропатии [4—6] — одной из частых причин госпитального ОПП [16]. Современная тактика реперфузии у больных ОИМпST помимо ЧКВ предполагает ТЛТ [7, 15]. Исследования по оценке частоты ОПП у больных ОИМпST, подвергнутых ТЛТ, единичны. Так, по данным M.J. Kim и соавт., только у 3 (3%) из 114 больных азиатской расы диагностировано ОПП после тромболизиса [20]. При этом частота ОПП в зависимости от используемого тромболитического препарата не анализировалась.
По нашим данным, при использовании стрептокиназы отмечалась более высокая частота ОПП, чем при применении алтеплазы. Возможно, это связано с тем, что при введении стрептокиназы чаще регистрировалось снижение систолического артериального давления (15% в группе стрептокиназы против 5% в группе алтеплазы). Следует отметить, что в ряде исследований частота развития артериальной гипотензии при использовании стрептокиназы была еще выше. Так, в исследовании ASK-ROMANIA артериальная гипотензия при введении стрептокиназы развилась у 44,5% больных ОИМпST [9]. По данным S. Torres и соавт., на фоне введения стрептокиназы (1,5 млн единиц внутривенно в течение 1 ч) у 86% пациентов ОИМ систолическое артериальное давление снижалось на 15%, при этом у 54% — ниже 90 мм рт.ст. [12].
Артериальная гипотензия — одна из наиболее распространенных причин ОПП [16]. Так, у больных инфарктом миокарда при наличии кардиогенного шока ОПП наблюдается в 9 раз чаще, чем в случае клинической смерти и последующей успешной реанимации [2]. В крупном исследовании GUSTO установлено, что у больных, получавших терапию алтеплазой, кардиогенный шок развился в 5,5% случаев, а в группе больных, леченных стрептокиназой, в 6,9% [21].
Между тем в отсутствие эффекта от ТЛТ необходимо «спасающее» ЧКВ, а в случае успешного тромболизиса рекомендуется выполнение коронарографии в срок от 3 до 24 ч [7]. В этой ситуации очень важно знать исходное состояние функции почек перед введением рентгенконтрастного вещества.
Полученные нами данные свидетельствуют о высокой частоте ОПП у больных ОИМпST, подвергнутых ТЛТ, даже в отсутствие у них кардиогенного шока и введения рентгенконтрастных препаратов. Больные с заболеваниями сердца и сосудов относятся к группе повышенного риска развития ОПП, так как у 1/3 из них имеется хроническая болезнь почек [22]. Более того, согласно регистру National Cardiovascular Data Acute Coronary Treatment and Intervention Outcomes Network Registry (США) из 19 029 больных ОИМпST у 30,5% имелась хроническая болезнь почек, а среди больных ОИМ без подъема сегмента ST — у 42,9% [23]. Следует отметить, что госпитальное ОПП у больных с исходно сниженной функцией почек развивается в 3 раза чаще, чем у больных с нормальной функцией почек [24, 25].
Патогенез ОПП у больных с ОИМ многофакторный, и, безусловно, не может быть сведен только к действию тромболитических препаратов, однако полученные нами данные свидетельствуют, что частота ОПП при использовании стрептокиназы в качестве тромболитического препарата в 3 раза выше, чем при применении алтеплазы. При введении стрептокиназы также чаще наблюдалась артериальная гипотензия. В этой связи требуется осторожность при использовании стрептокиназы, особенно у больных с исходно сниженной функцией почек.
Заключение
У 1/4 больных острым инфарктом миокарда с подъемом сегмента ST, которым проводился тромболизис, имеется острое повреждение почек, частота и тяжесть которого при использовании в качестве тромболитического препарата стрептокиназы выше, чем при применении алтеплазы. Среди больных острым инфарктом миокарда с подъемом сегмента ST с острым повреждением почек II—III стадии госпитальная летальность выше, чем у остальных пациентов.
Работа выполнена при поддержке ФЦП «Научные и научно-педагогические кадры инновационной России» на 2009—2013 гг. (Соглашение №14.B37.21.1119 от 14.09.12).



