В условиях ишемии и последующей реперфузии в миокарде усиливается образование ряда присущих организму факторов — адипокинов, цитокинов и вазоактивных пептидов, опосредующих механизмы адаптации клеток к такому повреждению [1—3]. К их числу относится адипокин апелин — пептид, состоящий из 77 аминокислот и являющийся лигандом, сопряженного с Gi-белком APJ-рецептора [4, 5]. Апелин активно экспрессируется различными тканями, включая эндотелиальные и гладкие
мышечные клетки коронарных сосудов и кардиомиоциты [4]. Активация системы апелин—APJ-рецептор вызывает гипотензивный и положительный инотропный эффект [4, 6, 7], что указывает на ее важную роль в регуляции сердечно-сосудистого гомеостаза. В последние годы обнаружено, что 2 более коротких фрагмента пептида — апелин-36 и апелин-13 — обладают кардиопротекторной активностью и способны защищать сердце от ишемического и реперфузионного стресса. Под действием этих пептидов уменьшались размеры инфаркта и улучшалось восстановление сократительной функции изолированного перфузируемого сердца мышей и крыс после тотальной или регионарной ишемии [8—10]. Это сочеталось с увеличением активности в миокарде супероксид-дисмутазы, уменьшением образования продукта перекисного окисления липидов — малонового диальдегида — и меньшими повреждениями сарколеммы ишемизированных кардиомиоцитов [10]. В культуре неонатальных и зрелых кардиомиоцитов, подвергнутых ишемии и реоксигенации, апелин-13 усиливал экспрессию NO-cинтазы, образование NO и одновременно подавлял продукцию суперокид-аниона [10]. Получены экспериментальные подтверждения ингибирования апелином-13, и в меньшей степени апелином-36, открытия митохондриальной поры и апоптоза в кардиомиоцитах крыс при моделировании окигенационного стресса [8, 10]. Ряд авторов высказали гипотезу о том, что более физиологически активный апелин-13 инициирует механизмы запрограммированного клеточного выживания, которые запускаются каскадами реперфузионных киназ [11, 12]. Гипотеза была подтверждена отменой влияния апелина-13 на открытие митохондриальной поры и гибель кардиомиоцитов в присутствии ингибиторов фосфатидилинозитол-3-киназы, Akt-киназы (PI3K-Akt) и митоген-акивируемой p44/42 киназы [8, 10, 11].
Эти данные свидетельствуют о возможности существенного улучшения метаболического состояния постишемического сердца под влиянием экзогенного апелина.
Целью настоящей работы было изучение кардиозащитных свойств апелина-12 — фрагмента пептида, полностью идентичного таковому у человека, — на модели изолированного работающего сердца крысы, подвергнутого тотальной ишемии. Предполагалось сопоставить влияние апелина-12 при его
введении до периода ишемии и в начале реперфузии на восстановление функции сердца, а также оценить его действие на метаболизм миокарда и повреждения клеточных мембран.
Материал и методы
Получение апелина-12 H-Arg-Pro-Arg-Leu-Ser-His-Lys-Gly-Pro-Met-Pro-Phe-OH. А-12 был получен путем автоматического твердофазного синтеза на пептидном синтезаторе фирмы Applied Biosystems 431A (Германия) с использованием Fmoc-методологии на полимере Ванга по стандартным программам. Твердофазный синтез проводили исходя из 0,25 ммоль коммерческого Fmoc-Phe-полимера (Bachem, Швейцария), путем последовательного удлинения пептидной цепи с С-конца. На первой стадии синтеза с целью предотвращения побочной реакции образования дикетопиперозина из пролинсодержащего дипептидилполимера присоединяли дипептидный блок Fmoc-Met-Pro-OH. После
этого цепь наращивали по одной аминокислоте. Для создания амидной связи применяли карбодиимидный метод. Конечный продукт отщепляли от полимерного носителя одновременно
с удалением защитных групп боковых функций аминокислот действием трифторуксусной кислоты со скавенджерами. Пептид был очищен с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) до 98% чистоты и охарактеризован с помощью 1Н-ЯМР-спектроскопии и MALDI-масс-спектрометрии (m/z 1423,5; расчетная молекулярная масса 1422,7). В работе использованы производные аминокислот, реагенты и растворители фирм Bachem и Fluka (Швейцария).
Перфузия изолированного сердца крысы. Опыты выполнены на сердце крыс-самцов линии Wistar (290—340 г). У наркотизированных уретаном (внутрибрюшинно 1,25 мг на г массы тела) животных извлекали сердце и перфузировали ретроградно в течение 15—20 мин раствором Кребса (РК)
с 11 мМ глюкозой, насыщенным карбогеном (95% О2±5% СО2) рН 7,4±0,1 при температуре 37 °С, при постоянном перфузионном давлении 60 мм рт.ст. После этого сердца перфузировали антеградно по Нийли при постоянном давлении наполнения левого предсердия 15 мм рт.ст. и среднем перфузионном давлении в аорте 60 мм рт.ст. [13].
Давление в аорте и левом желудочке регистрировали при помощи тензометрических датчиков Р50, монитора SP1405 и регистратора SP2010 (Gould Statham, США). Показателем интенсивности сократительной функции (ИСФ) левого желудочка служило произведение частоты сокращений сердца на развиваемое давление (разность между систолическим и минимальным диастолическим давлением).
Насосную функцию левого желудочка оценивали по величине минутного (сумма коронарного потока и аортального объема) и ударного (отношение минутного объема к частоте сокращений сердца) объемов. Коронарное сопротивление рассчитывали из отношения аортального давления к коронарному потоку.
После перфузии сердца по Нийли в течение 15—20 мин регистрировали показатели функции сердца и коронарных сосудов (исходное состояние). Затем осуществляли 5-минутную инфузию РК с постоянной скоростью 4 мл/мин и подвергали сердца глобальной нормотермической (37 °С) ишемии в течение 35 мин. За ишемией следовала 5-минутная ретроградная инфузия РК со скоростью 4 мл/мин и реперфузия
по Нийли в течение 25 мин.
Влияние A-12 на восстановление показателей функции сердца было изучено при его введении до ишемии или во время ранней реперфузии после периода глобальной ишемии. Растворенный в РК A-12 до концентрации 35, 70, 140, 280 или 560 мкМ вводили со скоростью 4 мл/мин в течение 5 мин
до ишемии (А-12-И) или в течение 5 мин перед реперфузией (А-12-Р). При выборе концентраций А-12 нами были приняты во внимание данные работы [14] о содержании эндогенного апелина в плазме крови крысы, а также собственные предварительные результаты, в которых положительное
инотропное действие А-12 на интактное перфузируемое сердце крысы было обнаружено в диапазоне концентраций 0,5— 20 мкМ. В отдельных сериях было изучено влияние инфузии 140 мкМ A-12 перед ишемией на выход в перфузат лактатдегидрогеназы (ЛДГ) и энергетическое состояние сердца. В контроле инфузию РК проводили без А-12.
Повреждение мембран кардиомиоцитов оценивали по увеличению активности ЛДГ в оттекающем от сердца перфузате, который собирали в охлажденные льдом пробирки в течение 5 мин перед ишемией (исходное состояние) и в течение первых 5 мин реперфузии. Активность ЛДГ определяли, используя в качестве субстрата пируват, на спектрофотометре Yanako UO-2000 (Япония) при λ=340 нм.
Метаболическое состояние сердца. Сердца замораживали охлажденными в жидком азоте щипцами Волленбергера в исходном состоянии или в конце реперфузии. Ткань гомогенизировали в холодной 6% HClO4 (10 мл на 1 г ткани) в гомогенизаторе Ultra-Turrax T-25 (IKA-Labortechnik, Германия). Белки осаждали центрифугированием при 3000 g и 4 °С в течение 10 мин. Супернатанты нейтрализовали 5 М К2СО3 до рН 7,4. Осадок KСlO4 отделяли центрифугированием в тех же условиях. Безбелковые экстракты хранили при температуре –20 °С до определения метаболитов. Сухой вес гомогенизированной ткани определяли после высушивания образцов в течение суток при температуре 110 °С. АТФ и фосфокреатин (ФКр) в тканевых экстрактах определяли спектрофотометрически, используя глюкозо-6-фосфатдегидрогеназу, гексокиназу и креатинкиназу [15]. Содержание АДФ и АМФ в тканевых экстрактах определяли с помощью миокиназы, пируваткиназы и лактатдегидрогеназы [16]. Для определения креатина (Кр) использовали сопряженные реакции с креатинкиназой, пируваткиназой и лактатдегидрогеназой [17]. Лактат и пируват определяли с помощью ЛДГ [18, 19]. Содержание метаболитов выражали в мкмоль/г сухого веса.
Приведенные показатели выражены как средняя ± ошибка средней. Различия между группами оценивали с помощью t-критерия Стьюдента и считали статистически значимыми при р<0,05.
Результаты
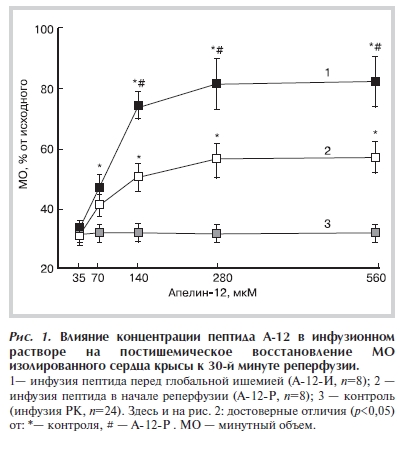
Восстановление функции сердца и коронарных сосудов при реперфузии. Инфузия А-12 до или после ишемии улучшала восстановление насосной функции сердца при реперфузии. На рис. 1 показано восстановление минутного объема (МО) в конце реперфузии в опытах с введением А-12 до и после ишемии. Достоверное увеличение его восстановления по сравнению с контролем было
отмечено при инфузии 70 мкМ А-12 в обеих группах. В дальнейшем по мере увеличения концентрации А-12 в РК различия между восстановлением МО в группах А-12 и контролем возрастали. При инфузии 140 мкМ А-12 скорость восстановления МО снижалась, а после введения 280 мкМ А-12 кривая дозозависимости выходила на плато в обеих группах. Во всем диапазоне исследованных концентраций введение пептида до ишемии было более эффективно, чем после ишемии. Так, максимальное восстановление МО после инфузии 560 мкМ в группе А-12-И и А-12-Р составляло 86±9 и 59±6% от исходного значения соответственно по сравнению с 32±2 в контроле (р<0,02—0,01). По существу ана-
логичные дозозависимости были получены для восстановления показателя ИСФ при реперфузии (рис. 2).
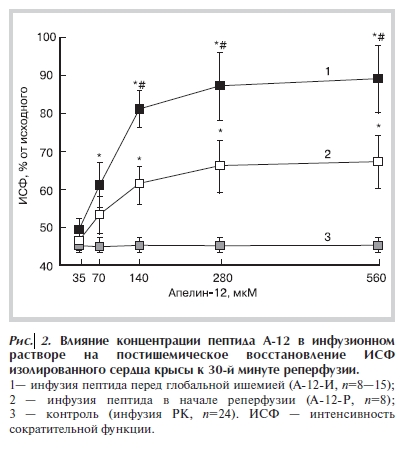
В табл. 1 сопоставлено восстановление показателей насосной, сократительной и коронарной функции сердца при введении 140 мкМ А-12 до и после ишемии. Видно, что восстановление аортального объема (АО) и ударного объема также было более высоким в группе А-12-И, чем в группе А-12-Р и в контроле. Особенно существенные различия между группами отмечены для АО, степень восстановления которого в группе А-12-И была в 2 раза больше, чем в А-12-Р, и в 30 раз выше контрольной. Более эффективное улучшение насосной функции под действием А-12 сопровождалось увеличением восстановления показателя ИСФ (см. рис. 2). В обеих А-12 группах это обеспечивалось более высоким развиваемым давлением (в большей степени, чем частота сердечных сокращений), которое в свою очередь было обусловлено устранением ишемической и реперфузионной контрактуры.
Действие А-12 не было прямо связано с его влиянием на коронарную систему. Так, несмотря на явное улучшение восстановления показателей сократительной и насосной функции, в группе А-12-Р была отмечена только тенденция к увеличению коронарного потока и снижению коронарного сопротивления по сравнению с контролем (см. табл. 1). В то же время при введении А-12 до ишемии показатели коронарной функции восстанавливались достоверно лучше контрольных, что позволяет предполагать участие коронарных сосудов в защите ишемизированного сердца А-12.
Энергетическое состояние реперфузированного миокарда. Изменения в содержании адениннуклеотидов и конечных продуктов гликолиза — лактата и пирувата — в конце реперфузии, вызванные предишемической инфузией 140 мкМ А-12, сопоставлены с исходными уровнями этих метаболитов в сердце в табл. 2 и 3. В контроле под действием ишемии и последующей реперфузии происходило снижение содержания АТФ до 37±7% от исходного с одновременным увеличением содержания АДФ и АМФ в среднем в 1,7 и 5,6 раза соответственно. Эти изменения указывали на преимущественный распад адениннуклеотидов, общий фонд которых (ΣАН) был снижен
до 58±3% от предишемического значения. Содержание лактата и пирувата в миокарде было увеличено соответственно в 5 и 1,3 раза по сравнению с нормой, что свидетельствовало
об ингибировании окисления глюкозы при реперфузии.
Таблица 1. Влияние инфузии 140 мкМ А 12 на восстановление показателей сократительной, насосной и коронарной функции изолированного сердца крысы после глобальной ишемии.
Таблица 2. Влияние инфузии 140 мкМ апелина 12 перед ишемией на содержание адениннуклеотидов (в мкмоль/г сухого веса) в сердце крысы в конце реперфузии.
Таблица 3. Влияние инфузии 140 мкМ апелина 12 перед ишемией на содержание конечных продуктов гликолиза (в мкмоль/г сухого веса) в сердце крысы в конце реперфузии.
Таблица 4. Влияние инфузии апелина 12 перед ишемией на выведение ЛДГ из сердца в перфузат до и после ишемии.
Под действием 140 мкМ А-12 содержание АТФ к концу реперфузии достоверно увеличивалось в 1,6 раза при двукратном снижении уровня АМФ. В результате фонд ΣАН в группе А-12-И был сохранен значительно лучше, чем в контроле и составлял 81±6% от предишемического значения.
Перераспределение в содержании адениннуклеотидов достоверно увеличивало энергетический заряд кардиомиоцитов в реперфузированных сердцах группы А-12-И по сравнению с контролем. Обнаруженное улучшение энергетического состояния реперфузированного миокарда сочеталось с уменьшением содержания лактата в ткани сердца до исходного значения (см. табл. 3). Хотя уровень пирувата в группе А-12-И оставался повышенным в конце реперфузии, отношение лактат/пируват в сердце было в 5 раз ниже, чем в контроле, и достоверно не отличалось от этого показателя в исходном состоянии.
Предишемическая инфузия 140 мкМ А-12 не приводила к достоверному увеличению восстановления фосфокреатина: его содержание в реперфузированном сердце составляло 14,77±1,41 мкмоль/г сухого веса по сравнению с 12,14±2,80 мкмоль/г сухого веса в контроле. Содержание общего креатина в группе А-12-И в конце реперфузии достоверно не отличалось от этого показателя в контроле и в исходном состоянии (59,65±1,56; 56,65±3,89 и 59,26±1,87 мкмоль/г сухого веса соответственно).
Влияние А-12 на выведение ЛДГ из сердца. Способность апелина влиять на повреждение клеточных мембран оценивали по изменению активности ЛДГ в перфузате до и после глобальной ишемии
в группе А-12-И (см. табл. 2). В течение 5-минутной инфузии 140 мкМ А-12 до ишемии выход ЛДГ из миокарда в перфузат был таким же, как в контроле при инфузии РК. Таким образом, инфузия А-12 не вызывала повреждения сарколеммы кардиомиоцитов неповрежденного сердца. В течение 5-минутного периода после ишемии выведение ЛДГ в контрольной группе увеличивалось в среднем в 2,6 раза по сравнению с этим показателем до ишемии, указывая на повреждение мембран. Инфузия 140 мкМ А-12
перед ишемией снижала активность ЛДГ в перфузате в 1,4 раза по сравнению с контролем. Это свидетельствовало о меньших дефектах мембран постишемических кардиомиоцитов, определяющих выведение цитоплазматической ЛДГ из миокарда.
Обсуждение
Впервые на модели изолированного работающего сердца крысы, подвергнутого глобальной ишемии, продемонстрированы кардиопротекторные свойства экзогенного А-12. Они проявлялись в значительном улучшении восстановления сократительной и насосной функции, а также коронарного потока при реперфузии, которое было наиболее эффективным при введении пептида перед ишемией, а не в начале реперфузии (см. рис. 1, см. табл. 1). Полученные данные принципиально согласуются
с результатами работы [10], в которой было показано, что введение апелина-13 в изолированное перфузируемое по Лангендорфу сердце увеличивало восстановление после ишемии конечного
систолического давления в левом желудочке (LVESP), максимальную скорость сокращения (±LV/dtmax) и расслабления (–LV/dtmax) при одновременном снижении конечного диастолического давления (LVEDP). Существенно, что более высокому функциональному уровню реперфузированных сердец, защищенных А-12 в наших опытах, соответствовало их лучшее метаболическое состояние. Оно было связано с восстановлением окисления глюкозы — основного энергетического субстрата изолирован-
ного перфузируемого сердца. Прямым следствием этого явилось достоверное увеличение содержания АТФ, ΣАН в миокарде и энергетического потенциала кардиомиоцитов в конце реперфузии по сравнению с этими показателями в контроле (см. табл. 2). Улучшение энергетического обмена миокарда под действием А-12 сопровождалось лучшим сохранением сарколеммы кардиомиоцитов, что было подтверждено меньшим выведением активности ЛДГ из сердца в перфузат на стадии ранней реперфузии (табл. 4). Полученные результаты прямо свидетельствуют о влиянии А-12 на энергетический обмен ишемизированного сердца крысы. Они согласуются с гипотезой об активации апелином-13 PI3K-Akt и митоген-активируемых MEK-Erk1/2 киназ, результатом которой является блокирование открытия митохондиальной поры [8, 10, 11], замедляющее катаболизм адениннуклеотидов в постишемических кардиомиоцитах.
Увеличение экспрессии эндотелиальной NO-синтазы (e-NOS) под действием апелина-13, являющейся одной из мишеней реперфузионных PI3K-Akt и MEK-Erk1/2 киназ [8, 10, 20], приводит к возрастанию образования NO. В наших опытах это косвенно подтверждалось достоверным улучшением коронарного потока в группе А-12-И во время реперфузии (см. табл. 1), а также улучшением коронарной функции постишемического сердца под действием донора NO — динитрозильного комплекса железа — на этой же экспериментальной модели, которое было обнаружено нами ранее [21, 22]. Включение образования NO в физиологические механизмы действия А-12 было отмечено К. Tatemoto и соавт. [6]. Ими было показано, что у наркотизированных крыс гипотензивный эффект А-12 (в большей степени, чем апелина-13 и апелина-36) сопровождается увеличением общего содержания
в плазме нитритов и нитратов и отменяется в присутствии ингибитора NOS метилового эфира Nω-нитро-L-аргинина (L-NAME). Впоследствии дозозависимый характер снижения среднего артериального давления при инфузии А-12 был документирован на бодрствующих крысах [23]. Известно, что NO обладает не только свойствами вазодилататора, но и скавенджера супероксидных радикалов, образование которых инициируется окислительным стрессом [24, 25]. Роль NO, образующегося под действием А-12, в снижении продукции активных форм кислорода (АФК)
до настоящего времени остается невыясненной. В то же время антиоксидантные свойства экзогенного апелина-13 были подтверждены снижением генерации АФК одновременно с уменьшением содержания малонового диальдегида в изолированном сердце крысы и в культуре кардиомиоцитов при моделировании ишемического и реперфузионного стресса [10]. Не исключено, что эти эффекты были обусловлены не только экспрессией e-NOS, но и увеличением активности супероксид-дисмутазы под влиянием апелина-13, которая снижалась в ткани сердца и кардиомиоцитах под влиянием ишемии и реперфузии [10, 26].
Таким образом, лучшее восстановление функции постишемического сердца и сохранение клеточных мембран под действием экзогенного А-12 могло быть вызвано улучшением аэробного обмена и антиоксидантной защиты миокарда. Существенно, что в опытах in vitro и in vivo было обнаружено увеличение экспрессии апелина и APJ-рецептора (на уровне мРНК и продукции белка) на моделях ишемии и гипоксии в периферических тканях и сердце [9, 10, 27—29]. Однако последующая инфузия С-концевых фрагментов пептида значительно повышала восстановление функции сердца и снижала повреждения, вызванные окислительным стрессом. Это указывает на то, что возрастание продукции эндогенного апелина недостаточно для активации APJ-рецептора и служит хорошим обоснованием применения его экзогенных лигандов для защиты сердца при ишемии и реперфузии.
Заключение
Результаты настоящей работы демонстрируют снижение нарушений функции и метаболизма постишемического сердца с помощью экзогенного А-12 на модели in vitro. Хотя короткие С-концевые фрагменты апелина обладают более высокой активностью по сравнению с апелином-36, представляется важным оценить возможность их использования в качестве кардиопротектора в условиях in vivo. Вероятно, что синтез модифицированных аналогов А-12 способен повысить его резистентность к действию аминопептидаз и привести к созданию фармакологических агонистов АPJ-рецептора. Такой подход может оказаться перспективным для регуляции активности системы апелин—АPJ-рецептор у пациентов с острым коронарным синдромом и сердечной недостаточностью.



