Внезапная сердечная смерть (ВСС) встречается у детей, подростков и молодых лиц относительно редко, составляя около 5—11% всех причин смерти в возрасте до 20 лет [1, 2] и до 20% в возрасте до 45 лет [3]. ВСС оказывает шокирующее действие не только на родных и близких, но и на врача, так как нередко служит первым и последним проявлением заболевания сердца у ребенка, до этого считавшегося абсолютно здоровым. В настоящей статье мы приводим семейный случай сочетанного прогрессирующего поражения проводящей системы сердца у 3 сестер.
В Центр синкопальных состояний и сердечных аритмий (ЦСССА) у детей и подростков ФМБА России была направлена на обследование Виктория П. в возрасте 11 мес для исключения предполагаемой надпочечниковой недостаточности. Девочка от второй беременности, срочных родов кесаревым сечением. Первая беременность и роды закончилась рождением 2 девочек, разнояйцевых близнецов, которые внезапно умерли в возрасте 4 и 5 лет. Масса тела Виктории при рождении 4750 г, рост 58 см. Оценка по шкале Апгар 8—9 баллов. Период новорожденности протекал без особенностей. До 8 мес жизни трижды возникали приступы бледности, вялости. Первый приступ — в возрасте 2 мес, на фоне ОРВИ, при нормальной температуре тела возникла внезапная вялость, выступил холодный пот, сознание не теряла. Второй приступ возник в возрасте 7 мес. На фоне приема гидрокортизона и течения ОРВИ с лихорадкой 39 °С, во сне, возникли одышка, тахикардия, бледность кожных покровов. Для уточнения природы пароксизмов девочка была консультирована кардиологами в нескольких клиниках и институтах Москвы. Обобщенное заключение: «Данных, подтверждающих структурные и органические заболевания сердца, не выявлены, отмечена умеренная брадикардия. Данных за синдром удлиненного интервала QT нет. В специализированном кардиологическом лечении не нуждается». В связи с неясной природой симптоматики, смертью сестер Виктории П. рекомендовали консультацию в ЦСССА ФМБА России для уточнения диагноза и исключения аритмогенного характера пароксизмов.
Данные обследования в ЦСССА ФМБА России. В семейном анамнезе отмечена смерть двух сестер Виктории, Ксении и Насти П. Девочки от первой беременности, протекавшей на фоне легкого микоплазмоза, маловодия (лечение с 22 нед), роды на 36-й неделе кесаревым сечением. Вес первой из двойни, Ксении при рождении 2420 г, второй, Насти — 2370 г. На 1-м месяце жизни Настя перенесла пневмонию, Ксения — острый бронхит. В связи с выявленной тимомегалией II степени обеим сестрам проводился 10-дневный курс терапии преднизолоном, обе находились на учете у эндокринолога. К году размеры тимуса у обеих девочек нормализовались.
С 3 мес жизни до года у обеих девочек отмечались приступы, которые мама описывает как «внезапный крик, закатывание, дети сильно выгибались, откидывали голову назад, краснели». Иногда приступы возникали во время сна, но даже при пробуждении могли продолжаться до 20—30 мин. Периодически мама и бабушка отмечали сердцебиение (примерно 1 раз в неделю), но точно описать характер изменений ритма сердца не могли. К году жизни приступы прекратились. После года росли и развивались нормально, синкопе, приступов сердцебиения не отмечалось.
В январе 2006 г. в возрасте 4,5 года Ксения шла с матерью в детский сад, прошла несколько шагов, упала и перестала дышать. Рядом оказалась другая мама, врач, которая немедленно стала проводить реанимационные мероприятия: непрямой массаж сердца, искусственное дыхание, вызвана бригада скорой помощи, которая приехала через 20 мин, была проведена электрическая дефибрилляция сердца, однако оживить девочку не удалось. После судебно-медицинского вскрытия был поставлен диагноз: «Синдром внезапной детской смерти, обусловленный иммунодефицитным состоянием с недостаточностью коры надпочечников (первичным гипокортитизмом)».
В связи с этой внезапной смертью, сестре погибшей девочки Насте П. в апреле 2006 г. было проведено комплексное педиатрическое обследование в краевой детской клинической больнице. Клинический диагноз при выписке: «Иммунодефицитное состояние, вторичное, умеренно выраженная недостаточность Т-клеточного звена иммунитета. Дисметаболическая кардиопатия с брадикардией. Резидиудальная энцефаломиелопатия после натальной травмы шейного отдела позвоночника, синдром цервикальной периферической недостаточности, синдром гиперактивности с дефицитом внимания. Неврозоподобное состояние. Диффузный нетоксический зоб I степени. Вестибулит».
Данных, подтверждающих наличие каких-либо заболевания с риском угрожающих жизни состояний, выявлено не было. Со стороны сердца в многочисленных осмотрах и эхокардиографических исследованиях кардиолога отмечались только аномально расположенная хорда, открытое овальное окно и «неспецифическая внутрижелудочковая блокада» на ЭКГ. Через 8 мес после выписки, в возрасте 5 лет Настя эмоционально встретила маму, пришедшую в детский сад на собрание, но ее попросили подождать окончания собрания, посадили за стол смотреть книжку. Как только она села внезапно упала, перестала дышать, посинела, было непроизвольное испражнение и мочеиспускание. Реанимационные мероприятия, начатые сразу же прибежавшими родителями и персоналом, оказались неэффективными. Судебно-медицинский диагноз: генерализованная РНК-вирусная инфекция. Острая полиорганная недостаточность (надпочечниковая, бульбарная, ствола головного мозга). ДВС-синдром. Врожденные диспластические тканевые пороки: дисплазия надпочечников, тимомегалия, иммунодефицитное состояние.
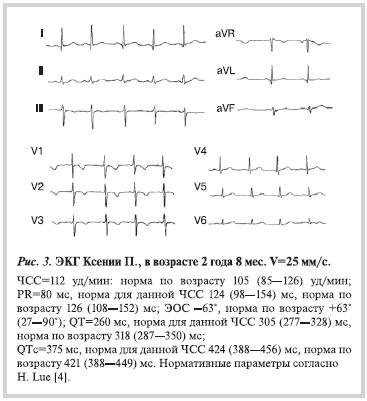
Данные семейного электрокардиологического обследования. ЭКГ умерших сестер в возрасте 8 мес представлены на рис. 1 и 2, ЭКГ Ксении П. в возрасте 2 года 8 мес — на рис. 3. Практически все параметры ЭКГ соответствовали возрастной норме [4], за исключением электрической оси сердца (ЭОС), которая была значительно отклонена влево/вверх. В возрасте 8 мес угол α QRS, отражающий ЭОС, составил –41° у Насти и –43° у Ксении при возрастной норме +60° (от +17° до +96°) [4]. ЭКГ Насти, снятая через 2 года, демонстрирует еще более выраженное отклонение ЭОС влево (угол α –63°), при возрастной норме от 27° до 90° [4], что является основным критерием блокады передней ветви левой ножки пучка Гиса у детей [4] и требует исключения заболеваний, сопровождающихся прогрессирующим поражением проводящей системы сердца.
При обследовании третьей сестры Виктории П. изменений сердечно-сосудистой системы не выявлено. При холтеровском мониторировании (ХМ) отмечались только единичные желудочковые экстрасистолы и небольшое транзиторное удлинение интервала PR — 0,16 с при ЧСС 94 уд/мин (при норме для данной ЧСС до 0,15 с) [4].
Были также проанализированы новые неинвазивные показатели риска развития угрожающих жизни аритмий и ВСС — показатели динамики интервала QT, турбулентность ритма сердца (ТРС) после желудочковой экстрасистолии [5], временной анализ микровольтной альтернации волны Т (МВТА) и оценка тенденций ритма сердца к ускорению и замедлению (AC/DC анализ), которые показали в последнее время высокую информативность в стратификации риска ВСС у взрослых [5—7].
Максимальные значения МВТА у Виктории П. составили 39 мкВ (норма у детей до 55 мкВ [6, 8]), параметры QT не изменены, в показателях ТРС отмечалась редукция ранней фазы турбулентности, параметры AC/DC анализа были симметричны, в пределах возрастной нормы [5, 6] и не выходили за границы стратификационных значений высокого риска (рис. 4) [6, 7]. Ребенку был поставлен диагноз: транзиторная АВ-блокада I степени. Семейный вариант прогрессирующего поражения проводящей системы сердца (болезнь Лева—Ленегра).
В связи с отсутствием данных, подтверждающих структурную патологию сердечно-сосудистой системы, наличием минимальных аритмических проявлений (транзиторная АВ-блокада I степени и единичные желудочковые экстрасистолы) от имплантации антиаритмических устройств или назначения антиаритмической терапии решено воздержаться. Рекомендовано регулярное наблюдение кардиолога, включающее контроль ЭКГ 1 раз в месяц, ХМ каждые 3 мес, эхокардиографию через 1 год. Имплантация электрокардиостимулятора (ЭКС) показана в случае увеличения степени АВ-блокады, брадикардии на уровне 5‰ возрастной нормы [4], появления фасцикулярных блокад, увеличения пауз ритма более 1,5 с. Рекомендовано проведение молекулярно-генетического анализа с целью выявления мутаций в гене SCN5A как основном гене-кандидате при болезни Лева—Ленегра и других прогрессирующих наследственных заболеваниях проводящей системы сердца.
В возрасте 1 год 2 мес при проведении ХМ у ребенка перед сном возник приступ беспокойства, слабости, во время которого на ЭКГ зарегистрирована остановка синусового узла, продолжительностью 3,3 с. Во время исследования также периодически регистрировались выскальзывающие идиовентрикулярные ритмы (рис. 5). С учетом выявленных изменений, данных семейного анамнеза больной был имплантирован ЭКС, после чего приступы не возникали. На ЭКГ покоя в возрасте 2 года 5 мес зарегистрирована АВ-блокада I степени с удлинением интервала PR до 180 мс при норме по ЧСС — 124 (98—154) мс [4], которая сохранялась постоянно в течение суток при ХМ.
С учетом данных семейного анамнеза (внезапная смерть двух сестер близнецов в течение года), отсутствия у них органических изменений сердца или других очевидных заболеваний при вскрытии, которые могли быть причиной смерти, можно предположить наличие у них наследственных заболеваний с высоким риском угрожающих жизни аритмий. К ним относятся поражения функции ионных каналов кардиомиоцита (аритмогенные каналопатии, или первичные электрические заболевания сердца): синдром удлиненного интервала QT, катехоламинергическая желудочковая тахикардия, синдром Бругада, синдром короткого интервала QT, заболевания с прогрессирующим поражением проводящей системы сердца, начальные стадии аритмогенной дисплазии/кардиомиопатии правого желудочка, идиопатическая фибрилляция желудочков. В практике отечественной судебной медицины, при этих заболеваниях обычно ставится судебно-медицинский диагноз недифференцированной кардиопатии и острой сердечно-сосудистой недостаточности.
На стандартной ЭКГ покоя маркеров перечисленных выше аритмогенных каналопатий не было. Выраженное отклонение ЭОС влево/вверх (угол α QRS комплекса более –30°), маленький зубец q и высокий зубец R в отведениях I и aVL соответствуют признакам блокады передней ветви левой ножки пучка Гиса у детей [9,10], что может служить первым проявлением врожденных заболеваний с прогрессирующим дегенеративным поражением проводящей системы сердца. Данная группа заболеваний включает множество нозологий, наиболее известными из которых являются заболевания синусного и атриовентрикулярного узлов (синдром слабости синусного узла и АВ-блокады разных степеней, бинодальная болезнь), поражения в нижележащих отделах системы Гиса—Пуркинье [11]. В 1964 г., независимо друг от друга, M. Lev [12] и J. Lenegre [13] описали схожие клинические, электрокардиографические и патоморфологические варианты поражения проводящей системы сердца (ПСС). Иногда оба заболевания объединяют в один синдром или болезнь Лева—Ленегра, при которой часто отмечается верхний фасцикулярный блок в сочетании с полной АВ-блокадой сердца и ВСС. В патогенезе поражения ПСС лежит дегенеративный процесс, который приводит к фиброзу волокон Гиса—Пуркинье и его распространенность определяет тяжесть заболевания. При болезни Ленегра диффузная фиброзная дегенерация ограничена волокнами ПСС, в то время как при болезни Лева дегенеративный процесс может поражать как специализированные волокна ПСС, так и ткани рабочего миокарда. Данный вариант болезни также описывается преимущественно у пожилых лиц и иногда рассматривается как нормальный процесс старения [11]. Нередко описываются семейные случаи комплексного поражения ПСС, комбинация фасцикулярных и АВ-блокад [14—22].
Нередко поражения ПСС встречаются у близнецов. Согласно данным датского Регистра с 1982 по 2000 г. в Дании зарегистрированы 159 близнецов с врожденным поражением ПСС [23]. В большинстве случаев этиология поражения оставалась неизвестной. Среди этих больных в 5 парах был имплантирован ЭКС у обоих близнецов. Генетические основы прогрессирующих заболеваний ПСС многообразны [24—26]. При болезни Лева—Ленегра молекулярно-генетической основой считаются мутации в гене SCN5A, кодирующем функцию натриевых каналов кардиомиоцита [24—27]. В этом же гене находят мутации, типичные для синдрома Бругада [28] и третьего варианта синдрома удлиненного интервала QT [27], что определяет возможность возникновения смешанных форм заболеваний и полиморфизма клинической картины. В нашем наблюдении у Виктории имелись 3 приступа слабости, 2 из которых были связаны с подъемом температуры тела, один произошел во сне, что типично и для клинической картины данных заболеваний. Описаны случаи развития угрожающих жизни тахиаритмий у больных с врожденными прогрессирующими дегенеративными поражениями ПСС [29], что может определить необходимость имплантации не только ЭКС, но и кардиовертера-дефибриллятора.
Мы считаем, что внезапная смерть первой сестры должна была послужить основанием для углубленного кардиологического исследования другой сестры (холтеровское мониторирование, возможно инвазивное электрофизиологическое исследование или имплантация петлевого регистратора ЭКГ). И даже в случае отсутствия у нее угрожающих жизни бради- или тахиаритмий идентичная электрокардиографическая картина поражения ПСС у сестер (левый передний гемиблок) могла быть показанием для имплантации ЭКС. Хочется отметить еще один момент. При ранее проведенных обследованиях (начиная с 8 месяцев!), стационарном обследовании Виктории после смерти сестры, проводились ЭКГ исследования, которые были описаны врачами функционалистами соответственно существующим стандартным протоколам, с измерением всех требуемых интервалов и углов, но без указания половозрастных норм показателей и что самое важное - без попытки сделать какое либо клиническое резюме по результатам исследования. Несомненно заключение в ЭКГ исследовании о наличии блокады передней ветви левой ножки пучка Гиса привлекло бы большее внимание к кардиологической направленности обследования ребенка. В данном случае в краевом стационаре девочке даже не провели холтеровское мониторирование.
Единственным отклонением при первом обследовании у третьей сестры Виктории можно считать умеренное транзиторное удлинение интервала PR относительно нормы при ХМ. Эти минимальные изменения не могли служить для нас объективными показаниями для постановки ЭКС. Однако, выявленный через несколько месяцев при ХМ клинически манифестный эпизод остановки синусного узла продолжительностью более 3 с послужил показанием 1 класса к имплантации ЭКС. Обнаруженная АВ-блокада I степени также прогрессировала и через 6 мес регистрировалась постоянно на стандартной ЭКГ покоя и ХМ. Несмотря на различия в локализации выявленных дефектов ПСС (фасцикулярные блокады у погибших сестер и поражение синусового и АВ узлов у Виктории), мы считаем оправданным предположить наличие в семье общего заболевания с прогрессирующим поражением различных участков ПСС.
Позволим себе высказать еще несколько соображений по данному случаю. Сестры Ксения и Настя в нашем наблюдении погибли в детском дошкольном учреждении или непосредственной близости от него, во время физической и эмоциональной активности. Несмотря на быстрое начало сердечно-легочной реанимации, со стороны родителей, в том числе медиков, она оказалась безуспешной. Согласно данным статистики ежегодно в школах США происходит один случай остановки сердца на 111 школ [30]. По данным американского Регистра остановок сердца и ВСС у детей и подростков, связанных с нагрузкой, в период с 2000 по 2006 г. в США произошел 521 подобный случай в школах и детских учреждениях у детей, подростков и молодых лиц в возрасте от 5 до 20 лет. Анализируя исходы оказания медицинской помощи и реанимационных мероприятий в этих случаях, авторы отмечают, что без быстрого применения электрической дефибрилляции выживаемость детей несравнимо ниже, чем при ее использовании. В последние годы в США эффективность наружных автоматических дефибрилляторов, расположенных в школах, сравнялась с эффективностью дефибрилляции, выполняемой специализированными бригадами скорой помощи [31]. Наибольшая эффективность отмечается при проведении электрической дефибрилляции в первые 3—7 мин от начала приступа [31, 32], что возможно только при расположении наружных автоматических дефибрилляторов в непосредственной близости к возможному месту происшествия (у детей это часто школьные и дошкольные учреждения, спортивные залы, в которых проводятся подвижные игры или спортивные занятия и соревнования [33]) и наличии соответствующих навыков у педагогов, медперсонала учреждения или самих спортсменов и тренеров. Соответствующее обеспечение наружными автоматическими дефибрилляторами детских и школьных учреждениях России и обучение максимального количества персонала и населения в целом приемам первой помощи также может быть одним из компонентов мероприятий снижающих риск ВСС у детей и подростков.
Выводы
Прогрессирующие фасцикулярные блокады у детей раннего возраста могут быть первым проявлением наследственных заболеваний с поражением проводящей системы сердца и требуют дополнительного кардиологического обследования для их исключения.
Внезапная смерть ребенка в семье должна служить основанием для тщательного семейного обследования и наблюдения с исключением возможных наследственных заболеваний с высоким риском ВСС. При этом особое внимание следует обращать на минимальные изменения ЭКГ, с учетом половозрастных нормативных показателей. которые могут быть первым проявлением болезни.



