В настоящие дни кардиоресинхронизирующая терапия (КРТ) доказала свою эффективность у взрослых пациентов с сердечной недостаточностью (СН), обусловленной ишемической и неишемической кардиомиопатией (КМП), ассоциированной с электромеханической диссинхронией (ЭМД), и вошла в стандарты ее лечения. В ряде исследований показано улучшение функции левого желудочка (ЛЖ), его обратное ремоделирование, улучшение функционального состояния пациента и снижение общей смертности на фоне применения данного вида лечения. Разработаны рекомендации, регламентирующие применение КРТ у взрослых пациентов [1–5]. Сегодня все чаще КРТ начинает применяться в педиатрической практике. В представленной статье анализируются патофизиологические механизмы ЭМД, обобщены результаты проведенных исследований, посвященных применению КРТ у детей, приводятся критерии отбора пациентов для данного вида лечения, рассматриваются особенности имплантации устройств в детском возрасте, а также опыт применения КРТ у детей в ФГБУ «НИИ кардиологии» СО РАМН.
Патофизиология электромеханической диссинхронии
ЭМД запускает последовательность событий, которые могут вызвать патологическое ремоделирование желудочка, ведущее к СН. Данный факт был установлен в опытах на животных [6–9] и впоследствии подтвержден клинически. Раннее электрическое возбуждение и сокращение вызывают растяжение сегментов миокарда желудочков, которые активируются позднее. Когда запаздывающие сегменты сокращаются, сегменты, сократившиеся ранее, расслабляются. Локальная работа миокарда снижена в зонах с ранним сокращением в связи с их уменьшенным наполнением и усилена в зонах запаздывающих сегментов, в которых наполнение повышено из-за предшествующего растяжения [10]. Это может привести к асимметричной гипертрофии: уменьшению объема и толщины стенки желудочка в областях раннего сокращения и увеличению в зонах позднего сокращения [10]. Клинические наблюдения у детей подтвердили экспериментально описанные модели сокращения [11] и эмпирически доказали факт ослабления работы миокарда при наличии внутрижелудочковой диссинхронии. Запаздывающее сокращение отдельных сегментов миокарда, возникшее после закрытия аортального клапана (АК), не вносит вклад в формирование ударного объема ЛЖ.
Вслед за внутрижелудочковой диссинхронией происходит частичное асимметричное клеточное ремоделирование [12], которое может закрепить первоначальное нарушение возбуждения и способствовать прогрессированию внутрижелудочковой механической задержки. Основными компонентами этих клеточных изменений являются:
- Повышение уровней медиаторов фиброза и апоптоза в сегментах позднего сокращения миокарда [10];
- Снижение внутриклеточного обмена ионов кальция между саркоплазматическим ретикулумом и цитозолем с негативным влиянием на электромеханическое сопряжение [13];
- Понижение экспрессии генов, кодирующих β-адренорецепторы, что приводит к слабому ответу миокарда на адренергическую стимуляцию [14];
- Супрессия и латерализация белка межклеточных щелевых контактов коннексин-43 в поздно сокращающихся сегментах, которые приводят к снижению скорости проведения по миокарду [15].
ЭМД, являющаяся результатом задержки желудочковой активации, связанной с блокадой левой ножки пучка Гиса (БЛНПГ) или электрокардиостимуляцией правого желудочка (ПЖ), обычно характеризуется формированием групп сегментов раннего и позднего сокращения миокарда. Такая диссинхрония хорошо корригируется КРТ, которая заключается в электрической стимуляции области позднего сокращения, состоящей из нескольких сегментов миокарда. Однако ЭМД может быть вызвана также неравномерностью или разностью в силе сокращений отдельных сегментов миокарда [16]. Сегменты с лучшей сократимостью предрастягивают те сегменты, у которых сократимость исходно снижена, тем самым оттягивая пик их сокращения. Сегменты с высокой и низкой силой сокращения могут чередоваться друг с другом. Этот тип диссинхронии встречается, к примеру, при идиопатической дилатационной КМП (ДКМП) или ишемической КМП при наличии узкого комплекса QRS по данным ЭКГ. Такая диссинхрония не поддается коррекции с помощью КРТ по двум причинам: отсутствие задержки электрической активации и недостаточные возможности технологии КРТ в коррекции дисперсной механической диссинхронии (ограниченное количество желудочковых электродов для стимуляции). Таким образом, дифференциальная диагностика типа желудочковой диссинхронии является важным условием для определения показаний к КРТ.
Кардиоресинхронизирующая терапия в педиатрии: опыт и показания
Эффективность КРТ у детей может варьировать в зависимости от лежащего в основе диссинхронии структурного и функционального субстрата, такого как анатомия системного желудочка (правый, левый или единственный), наличие и степень регургитации на системном атриовентрикулярном клапане, наличие первичного органического заболевания миокарда или рубцевания миокарда, а также задержки проводимости. Имеющиеся данные об эффективности КРТ у детей были получены в двух мультицентровых исследованиях [17, 18], одном крупном ретроспективном одноцентровом [19, 20] и в нескольких менее масштабных исследованиях. Ни одно из этих исследований не было рандомизированным или проспективным, амбулаторное наблюдение было слишком коротким для анализа долговременного результата КРТ, конечные точки в основном были сфокусированы на функции системного желудочка и не включали в себя данные по заболеваемости и смертности. Несмотря на эти ограничения, эффект КРТ относительно обратного ремоделирования желудочка сходен с таковым у взрослых. Результаты доступных исследований в детской популяции могут быть резюмированы следующим образом:
- Общепринятая одноэлектродная правожелудочковая стимуляция была самой распространенной (63%) причиной диссинхронии системного желудочка [17–19].
- Большей части пациентов (58%) был присвоен функциональный класс (ФК) II по классификации Нью-Йоркской ассоциации сердца (NYHA), что отражает более активный подход к КРТ у детей, в то время как среди пациентов взрослой популяции превалирует ФК III или IV по NYHA.
- На фоне КРТ было отмечено увеличение фракции выброса (ФВ) системного желудочка на 6–14% [17–20].
- Наличие в системной позиции ЛЖ было независимым предиктором улучшения систолической функции желудочка на фоне КРТ [18].
- Наилучший ответ на КРТ с почти полным обратным ремоделированием наблюдался у пациентов с системным ЛЖ, которым КРТ выполнялась после обычной электрокардиостимуляции ПЖ [20].
- КРТ была эффективна в сочетании с другой коррекционной или паллиативной кардиохирургией, в частности, когда целью было снижение регургитации на системном атриовентрикулярном клапане [18, 21].
- Доля систем КРТ с функцией дефибрилляции (КРТ-D) в общей структуре имплантаций была низкой (18–25%). Данные регистра трансплантации сердца у детей показали очень низкую встречаемость внезапной смерти среди ожидающих трансплантацию [22], что косвенно свидетельствует против шаблонного использования такого показателя, как ФВ ЛЖ≤35%, в качестве критерия для первичной профилактической имплантации дефибриллятора у маленьких пациентов с ДКМП.
- Почти 40% детей-кандидатов на трансплантацию сердца, направляемых на КРТ, в последующем были удалены из списка ожидания по причине эффективности данного вида лечения [20]. Это говорит о том, что юные пациенты, ожидающие трансплантацию сердца, предварительно должны проходить специальный скрининг на наличие ЭМД как потенциального субстрата для улучшения функции сердца посредством ресинхронизации.
- Доля детей, не восприимчивых к КРТ (14%), была ниже соответствующего показателя, полученного в проспективных исследованиях у взрослых, что скорее отражает ретроспективную природу педиатрических исследований и особенности критериев для оценки результатов применения КРТ, нежели её более высокую эффективность [17–20].
- Наличие первичной ДКМП и высокого ФК СН по NYHA, по-видимому, является предиктором невосприимчивости к КРТ [18].
- Оценка ЭМД не требуется для определения показаний к КРТ у взрослых с идиопатической ДКМП и ишемической КМП. Единственное проспективное исследование, доступное в настоящее время [23], не смогло показать достаточную воспроизводимость и предсказательную способность эхокардиографии (ЭхоКГ) как эффективного метода при определении показаний к КРТ. Однако у пациентов с врожденными пороками сердца (ВПС) наряду с многообразием структурных и функциональных субстратов для диссинхронии (наличие системного ПЖ или функционально единственного желудочка, блокады правой ножки пучка Гиса (БПНПГ)) длительность QRS может быть даже более худшим предиктором диссинхронии системного желудочка, чем у пациентов с нормальной структурой сердца. Таким образом, индивидуальная оценка ЭМД с помощью ЭхоКГ-исследования сердца в контексте с другими фактами может быть ценной для детской популяции [24–27].
Таким образом, каждый пациент с СН должен быть обследован на наличие показаний к КРТ. При наличии широкого комплекса QRS с морфологией блокады ножки пучка Гиса (БНПГ) необходимо провести ЭхоКГ-исследование для оценки типа ЭМД. Если ребенку планируется имплантация устройства КРТ, необходимо также рассмотреть вопрос о необходимости функции дефибрилляции.
Показания к КРТ у детей к настоящему времени так и не определены. Наши предложения основаны на современных рекомендациях по КРТ у взрослых с учетом доступных данных по детской популяции.
Предлагаемые показания к КРТ у детей
Класс I. Показания к КРТ имеют пациенты со структурно нормальным сердцем или структурным заболеванием сердца, с ФВ ЛЖ ≤35%, синусовым ритмом, широким QRS-комплексом, имеющим морфологию, характерную для полной БЛНПГ (спонтанной или стимулированной), с СН ФК II / у амбулаторных пациентов с СН ФК IV по NYHA. Уровень обоснованности (согласно руководству по КРТ для соответствующей взрослой группы пациентов) А для СН III ФК / у амбулаторных пациентов с СН ФК IV по NYHA; уровень обоснованности В для ФК II по NYHA [17–19, 28–31]. «Широкий QRS-комплекс» у подростков определяется как QRS≥150 мс, согласно опубликованным рекомендациям для взрослых пациентов [28–31]. У более юных пациентов в качестве показаний к КРТ могут быть приняты меньшие значения ширины QRS-комплекса при наличии полной БНПГ [32].
1. КРТ показана пациентам, имеющим ФВ системного желудочка ≤35%, узкий QRS-комплекс при самостоятельном сокращении сердца, СН ФК I / у амбулаторных пациентов с СН ФК IV по NYHA, которым проводится имплантация нового или замена старого электрокардиостимулятора (ЭКС) с ожидаемой потребностью в значительной (>40%) желудочковой стимуляции. Одноэлектродная ЭКС из верхушки/середины боковой стенки системного желудочка может считаться альтернативой КРТ. Уровень обоснованности С [17–20, 28–31, 33–49].
Класс IIa. КРТ может быть полезна пациентам со структурно нормальным сердцем или структурным заболеванием сердца, с ФВ системного ЛЖ ≤35%, синусовым ритмом, широким QRS-комплексом, имеющим морфологию, характерную для полной БЛНПГ (спонтанной или стимулированной), и СН ФК II / у амбулаторных пациентов с СН ФК IV по NYHA. Уровень обоснованности В (согласно руководству по КРТ для соответствующей взрослой группы пациентов) [17–19, 28–31]. В данном классе показаний «широкий комплекс QRS» у подростков определяется как QRS 120–149 мс, согласно опубликованным рекомендациям для взрослых пациентов [28–31]. У более юных пациентов в качестве показаний к КРТ могут быть приняты меньшие значения ширины QRS- комплекса при наличии полной БНПГ [32].
2. КРТ может быть полезна пациентам с системным ПЖ с ФВ ≤35% и дилатацией желудочка, СН ФК II / у амбулаторных пациентов с СН ФК IV по NYHA и широким QRS-комплексом, имеющим морфологию, характерную для полной БПНПГ (спонтанной или стимулированной). Для оценки ФВ ПЖ и его размеров предпочтительнее использовать магнитно-резонансную томографию. Не исключено, что значение ФВ системного ПЖ как одного из показаний к КРТ может быть пересмотрено в сторону увеличения. Необходимо рассмотреть вопрос о применении методов медицинской визуализации для подтверждения паттерна механической активации, согласующегося с электрической активацией и поддающегося ресинхронизации. Уровень обоснованности С [17–21, 50–52]. Понятие «широкий QRS-комплекс» соответствует указанному ранее (класс I, п.1).
3. КРТ может быть полезна для пациентов с функционально единственным желудочком сердца с ФВ ≤35% и дилатацией желудочка, СН ФК II / у амбулаторных пациентов с СН ФК IV по NYHA и широким QRS-комплексом из-за выраженной задержки электрической активации внутри желудочка, что обусловливает морфологию комплекса QRS с полной БПНПГ или БЛНПГ (спонтанной или стимулированной). Необходимо рассмотреть вопрос о применении методов медицинской визуализации для подтверждения паттерна механической активации, согласующегося с электрической активацией и поддающегося ресинхронизации. Уровень обоснованности С [19, 20]. Понятие «широкий QRS-комплекс» соответствует указанному ранее (класс I, п.1).
4. КРТ может быть полезна для пациентов с ФВ системного желудочка >35%, узким QRS-комплексом, СН ФК I / у амбулаторных пациентов с СН ФК IV по NYHA, которым проводится имплантация нового или смена старого ЭКС с ожидаемой необходимостью значимой (>40%) желудочковой стимуляции. Одноэлектродная ЭКС из верхушки/середины боковой стенки системного желудочка может считаться альтернативой КРТ. Уровень обоснованности С [17–20, 29–31, 33–49, 53, 54].
Класс IIb. КРТ может быть назначена пациентам со структурным заболеванием сердца независимо от морфологии системного желудочка при прогрессировании систолической дисфункции системного желудочка и/или его дилатации или высокой вероятности прогрессирования без конкретного значения ФВ; при СН ФК I / у амбулаторных пациентов с СН ФК IV по NYHA, с широким QRS-комплексом, имеющим морфологию полной БПНПГ или БЛНПГ (спонтанной или стимулированной) из-за значительной задержки электрической активации внутри желудочка; в случае выполнения другого хирургического вмешательства на сердце, открывающего возможность имплантации электрода при торакотомии. Необходимо рассмотреть вопрос о применении методов медицинской визуализации для подтверждения паттерна механической активации, согласующегося с электрической активацией и поддающегося ресинхронизации. Уровень обоснованности С [17–19]. Понятие «широкий QRS-комплекс» соответствует указанному ранее (класс I, п.1).
1. Можно рассмотреть вопрос о назначении КРТ пациентам с системным ПЖ, имеющим значительную регургитацию на трехстворчатом клапане (ТК), без снижения ФВ, с СН ФК I / у амбулаторных пациентов с СН ФК IV по NYHA, широким QRS-комплексом, при наличии морфологии полной БПНПГ (спонтанной или стимулированной), которым предстоит хирургическое лечение значительной трикуспидальной регургитации. Остается актуальным вопрос о применении методов медицинской визуализации для подтверждения паттерна механической активации, согласующегося с электрической активацией и поддающегося ресинхронизации. Уровень обоснованности С [18, 21]. Понятие «широкий QRS-комплекс» соответствует указанному ранее (класс I, п.1).
2. КРТ может быть использована у пациентов после хирургической коррекции врожденных пороков сердца (ВПС) с тяжелой дисфункцией ПЖ и его дилатацией, несмотря на вмешательство с целью снижения объемной перегрузки ПЖ, с СН ФК II / амбулаторным пациентам с СН ФК IV по NYHA и широким QRS-комплексом вследствие полной БПНПГ. Решение о КРТ ПЖ может быть принято на основании результатов временной ресинхронизации ПЖ. Исследование с визуализацией необходимо использовать в качестве подтверждения механической активации модели, соответствующей электрической активации и восприимчивой к ресинхронизации. Уровень обоснованности [55–57]. Понятие «широкий QRS-комплекс» соответствует указанному ранее (класс I, п.1).
3. Необходимо тщательно и индивидуально подходить к назначению КРТ у пациентов со специфическими прогрессирующими формами ДКМП (некомпактный миокард желудочков, нейромышечные и митохондриальные болезни), при которых эффект КРТ еще точно не определен. Уровень обоснованности С.
4. Необходимо тщательно и индивидуально подходить к назначению КРТ у пациентов с СН ФК IV по NYHA и тяжелой желудочковой дисфункцией, которые в противном случае были бы кандидатами на трансплантацию сердца или механическую поддержку кровообращения. У таких пациентов применение КРТ может вызывать задержку или стать помехой в использовании альтернативных методов лечения (трансплантация сердца). Уровень обоснованности С [18].
Класс III. КРТ не показана пациентам с узким QRS-комплексом без существенной задержки электрической активации внутри пораженного желудочка. Уровень обоснованности В [57, 58]. КРТ не показана пациентам, у которых предполагаемая продолжительность жизни с хорошей функциональной активностью составляет менее 1 года в силу сопутствующих заболеваний. Уровень обоснованности С [59].
Оптимальная лекарственная терапия должна быть неотъемлемой частью лечения СН перед тем, как определять показания к КРТ [28–31].
Необходимость функции дефибрилляции в имплантируемом устройстве (КРТ-D) должна оцениваться индивидуально, с использованием всех доступных критериев [28–31], а не только на основании значения ФВ системного желудочка [22]. Уровень обоснованности С.
Особенности имплантации устройств КРТ у детей
Наряду с определением показаний к имплантации устройства, специалисту необходимо решить, какая система ЭКС – эпикардиальная или эндокардиальная – будет наиболее оптимальной для данного пациента. Определяясь с методом, специалист должен принимать во внимание ряд особенностей, свойственных организму ребенка.
Особенности венозной системы. Диаметр сосудов ребенка весьма мал при рождении и увеличивается с возрастом. Известно, что диаметр подключичных вен, используемых при эндокардиальной имплантации электродов, к возрасту 4–6 лет в среднем составляет 4–5 мм, что существенно меньше суммарного диаметра трех электродов ЭКС [60–63].
Вены ребенка обладают развитой системой клапанов. Так, в частности, хорошо развитый тебезиев клапан, располагающийся в устье коронарного синуса (КС), может стать серьезным препятствием к его канюляции. Также характерно для детского возраста наличие системы клапанов на протяжении всей системы КС, особенно в местах отхождения вен меньшего порядка [64]. Сложность для канюляции КС может составлять субевстахиев чехол, являющийся частью миокарда правого предсердия и располагающийся между евстахиевым гребнем и ТК, прикрывая вход в устье КС. Узость КС, небольшой диаметр вен, обилие коллатералей, хрупкость стенки сосудов у детей – все это может приводить к диссекции сосудов и развитию осложнений. Эффективность КРТ во многом зависит от точки приложения левожелудочковой стимуляции. При трансвенозной постановке электрода искомой веной является латеральная желудочковая, остро-угольное отхождение которой, характерное для детского возраста, делает затруднительной или невозможной её канюляцию [65, 66]. Известно также, что у ряда пациентов после операций по гемодинамической коррекции ВПС (операции Фонтена, Мастарда, Сеннинга) трансвенозный доступ для имплантации электродов антиаритмических устройств невозможен [67].
Антропометрические особенности детского возраста, темпы роста. Отсутствие выраженной подкожной жировой клетчатки и развитой скелетной мускулатуры у детей, в основном дошкольного возраста, создает определенные сложности при выборе расположения генератора устройства. Так, имплантация генератора в подключичной области подкожно или под большой грудной мышцей может приводить к значительному косметическому дефекту, повышенному риску повреждения устройства, его дислокации и пролежням. Альтернативной локализацией генератора в данном случае является абдоминальная, когда ложе формируется под прямой мышцей живота или под апоневрозом наружной косой мышцы живота [68, 69].
Темпы роста ребенка за несколько лет могут составлять десятки сантиметров. Данный факт обусловливает высокую вероятность нарушения целостности или дислокации электрода в случае трансвенозного метода имплантации, особенно в период интенсивного роста. Имплантация эндокардиальных электродов «с запасом» путем формирования петли в полости сердца себя не оправдала ввиду высокой вероятности нарушения функции ТК и нередко клапана легочной артерии при дислокации петли в выводной отдел ПЖ, а также адгезии электродов к стенке сосудов и камер сердца [60–63,70].
Необходимость длительной терапии
КРТ в большинстве случаев носит длительный, а иногда и пожизненный характер. Учитывая заявленный срок службы генератора ЭКС (7–11 лет), обусловленной емкостью элемента питания устройства, пациенту может потребоваться несколько его реимплантаций. Срок службы электродов таких ограничений не имеет. Выживаемость эпикардиальных и эндокардиальных электродов, согласно исследованию E.B. Fortescue и соавт. [71], существенно не отличается, но как у одних, так и у других существует целый ряд непредотвратимых осложнений, связанных с функцией электродов. Для эпикардиальных электродов это блок импульса на выходе (относительный риск (ОР) 3,6; p=0,01), разрыв электрода (ОР 2,1; p=0,06), а для эндокардиальных – это дислокация электрода (ОР 3,7; p=0,007) и нарушение его изоляции (ОР 2,6; p=0,007) [71]. При выходе из строя электрода потребуется его замена. Известно, что транскатетерное удаление эндокардиальных электродов крайне затруднительно, сопряжено с высоким риском осложнений вплоть до летального исхода, может выполняться только в экспертных центрах с опытом не менее 50 процедур ежегодно, а также весьма дорого. Риск катетерного удаления электрода возрастает пропорционально времени с момента его имплантации [72]. Установка же дополнительных электродов без удаления уже нефункционирующих чревата нарушением функции ТК, повышением вероятности полной окклюзии сосудов системы верхней полой вены. Выход из строя электродов эпикардиальной системы ЭКС потребует повторного хирургического вмешательства для его замены [60–71].
Клиническая эффективность кардиоресинхронизирующей терапии у детей
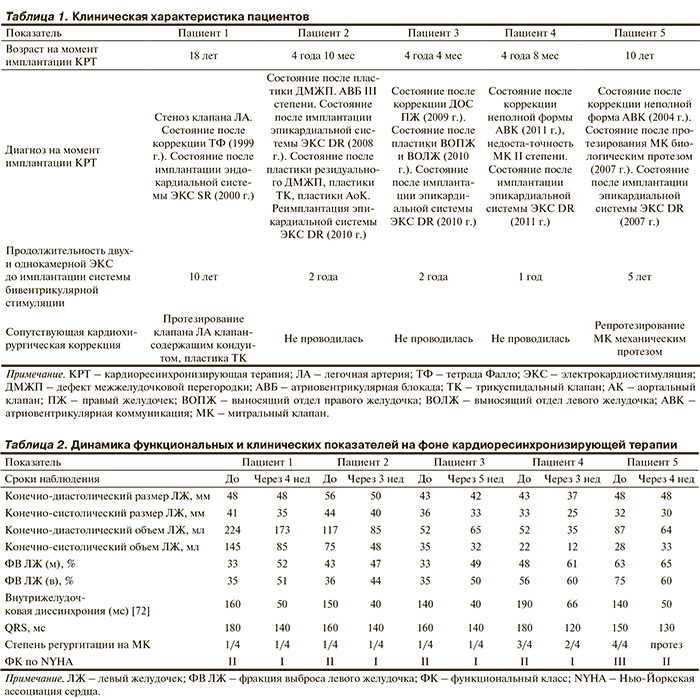
Эффективность КРТ в детском возрасте, при условии строгого следования показаниям к её проведению, наглядно демонстрируют результаты лечения пациентов в ФГБУ «НИИ кардиологии» СО РАМН. За период с 2008 по 2013 гг. устройства КРТ были имплантированы 5 пациентам – детям в возрасте от 4 до 18 лет (средний возраст 8,4±5,7 года). Все пациенты ранее в различные сроки были прооперированы по поводу ВПС: тетрады Фалло (ТФ), дефекта межжелудочковой перегородки (ДМЖП), двойного отхождения сосудов (ДОС) от ПЖ и двух случаев неполной формы атриовентрикулярной коммуникации (АВК) (табл. 1). У всех пациентов хирургическая коррекция ВПС осложнилась развитием полной атриовентрикулярной блокады (АВБ), что потребовало имплантации двухкамерной эпикардиальной (у 4) и однокамерной эндокардиальной (у 1) системы ЭКС. В течение 1–3 лет после выполнения коррекции ВПС и имплантации ЭКС у всех пациентов возникли признаки СН, сохраняющиеся на фоне адекватной медикаментозной терапии, по поводу чего они были госпитализированы в ФГБУ «НИИ кардиологии» СО РАМН. По данным трансторакальной ЭхоКГ с допплеровским сканированием, у всех пациентов определялось увеличение полостей сердца, снижение ФВ ЛЖ и выраженные признаки ЭМД, заключавшейся в асинхронном движении стенок ЛЖ, межжелудочковой диссинхронии со значительным отставанием сегментов свободной стенки ЛЖ от ПЖ. По данным электрокардиографии отмечалось расширение комплекса QRS до 150–180 мс (166±13,4 мс). Выявленная диссинхрония не была единственной причиной СН у детей. Значительный вклад в её развитие внесли проблемы, возникшие вследствие хирургической коррекции ВПС: резидуальный ДМЖП, недостаточность митрального клапана (МК) и ТК, клапана аорты, стеноз выходного отдела ПЖ (ВОПЖ). В связи с вышеизложенным всем пациентам были имплантированы эпикардиальные системы бивентрикулярной стимуляции – КРТ. Двум из пяти пациентов потребовалась одновременная коррекция сопутствующих аномалий: протезирование МК механическим протезом, пластика ТК и АК, протезирование легочной артерии клапансодержащим кондуитом и удаление эндокардиальных электродов (см. табл. 1). Осложнений в раннем послеоперационном периоде не было, нарушений внутрисердечной гемодинамики, функции ЭКС и электродов не выявлено, ритмовождение было устойчивое. После оптимизации A-V и V-V задержки у всех пациентов отмечено уменьшение полостей сердца, увеличение ФВ ЛЖ, а также уменьшение продолжительности комплекса QRS до 120–140 мс (134±9 мс) и улучшение функционального статуса пациента (табл. 2). При дальнейшем динамическом наблюдении продолжительностью от 6 до 24 мес сохранялся стойкий эффект КРТ. Все пациенты включены в регистр Европейского общества детских кардиологов (European Registry for ICD and CRT Devices in Pediatrics and Adults with Congenital Heart Disease).
Таким образом, результаты применения КРТ у детей в ФГБУ «НИИ кардиологии» СО РАМН следует оценить как положительные. Мы применяли данный вид лечения у пациентов с диссинхронией, вызванной предвозбуждением ПЖ, обусловленным работой двухкамерной и однокамерной системы ЭКС, установленной по поводу послеоперационной полной АВБ. Причиной диссинхронии был неверный выбор точки имплантации желудочкового электрода – выходной отдел ПЖ [42]. Сопутствующая имплантации аппарата КРТ хирургическая коррекция дефектов структур сердца, безусловно, потенцировала положительный эффект КРТ.
Заключение
Кардиоресинхронизирующая терапия (КРТ) у взрослых сделала возможным лечение таких пациентов, хроническая СН у которых ранее считалась рефрактерной. Строго следуя рекомендациям, специалистам удается добиваться впечатляющих успехов в их лечении [1–5].
Согласно проведенным исследованиям, наилучший эффект от КРТ возникает в том случае, когда имеет место кластерный тип диссинхронии, а именно задержка электрической активации сегментов миокарда, расположенных по соседству. Диссинхрония, при которой нет задержки электрической активации, а ее появление вызвано разницей в сократительной способности участков миокарда, не может быть корригирована методом КРТ [6–12, 16].
Применение КРТ у детей уже показало свою состоятельность и эффективность. Тем не менее, лишь небольшое число пациентов в педиатрии строго подходит под критерии, разработанные для взрослых. Данный факт делает необходимым оптимизацию подходов отбора пациентов для детской практики. В настоящее время установлено, что наилучший результат дает применение КРТ в группе пациентов, СН у которых является следствием ЭМД, обусловленной одно- и двухкамерной стимуляцией с имплантацией желудочкового электрода в ПЖ. Напротив, наличие у пациента ДКМП, а также СН III–IV ФК является предиктором неэффективности КРТ [17–19, 28–31].
Особенности детского возраста определяют необходимость индивидуального подхода к каждому пациенту. Это касается определения как показаний к проведению КРТ, так и метода имплантации устройства. Выбор метода имплантации должен быть основан не только на физических параметрах пациента, но и на особенностях анатомии сердечно-сосудистой системы в разные периоды жизни ребенка, наличии корригированного ВПС в анамнезе, наличии ранее установленной одно- или двухкамерной системы ЭКС. Учитывая также долгосрочную перспективу лечения, следует признать целесообразным применение эпикардиальной бивентрикулярной стимуляции у детей с целью максимально длительного сохранения вен интактными [60–72].
Таким образом, определение вида диссинхронии, предикторов эффективности и неэффективности, показаний к КРТ у детей, а также метода имплантации устройства требует индивидуального, «клиентского» подхода в каждом конкретном случае с оценкой долгосрочных перспектив и слаженной работы детских кардиологов, специалистов по эхокардиографии, электрофизиологов, кардиохирургов.



