Список сокращений:
АГМА – антитела к гладкой мускулатуре
АЛТ – аланиновая аминотрансфераза
АНФ – антинуклеарный фактор
АСТ – аспарагиновая аминотрансфераза
ГГТП – гамма-глутамилтранспептидаза
ГЦК – гепатоцеллюлярная карцинома
ИМТ – индекс массы тела
ИР – инсулинорезистентность
КТ – компьютерная томография
ЛПВП – липопротеины высокой плотности
ЛПНП – липопротеины низкой плотности
ЛПОНП – липопротеины очень низкой плотности
МРТ – магнитно-резонансная томография
МС – метаболический синдром
НАЖБП – неалкогольная жировая болезнь печени
НАСГ – неалкогольный стеатогепатит
НТГ – нарушение толерантности к глюкозе
ПОЛ – перекисное окисление липидов
СД – сахарный диабет
СЖК – свободные жирные кислоты
СИБР – синдром избыточного бактериального роста в кишечнике
ТГ – триглицериды
УДХК – урсодезоксихолевая кислота
УЗИ – ультразвуковое исследование
ХС – холестерин
ЦП – цирроз печени
ЩФ – щелочная фосфатаза
ЭГДС – эзофагогастродуоденоскопия
TNF-α – фактор некроза опухоли-α
По данным Всемирной организации здравоохранения, в последние годы регистрируется неуклонный рост числа хронических заболеваний печени, в частности неалкогольной жировой болезни печени (НАЖБП). Являясь самостоятельной нозологической единицей, НАЖБП служит фактором риска сердечно-сосудистых заболеваний, ассоциирована с абдоминально-висцеральным ожирением, периферической инсулинорезистентностью, артериальной гипертензией и дислипидемией и рассматривается как печеночный компонент метаболического синдрома (МС).
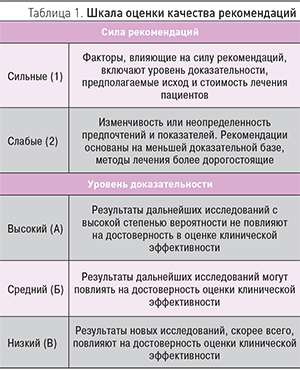
В России отсутствуют общепринятые российские стандарты по диагностике и лечению НАЖБП для терапевтов, что продиктовало необходимость их разработки. Настоящие методические рекомендации основаны на обзоре и анализе публикаций последних лет по данной тематике в мировой и отечественной литературе, а также на опыте авторов по лечению пациентов с НАЖБП. Методические рекомендации предназначены для терапевтов и содержат описание предпочтительных подходов к оказанию диагностической, лечебной и профилактической помощи больным НАЖБП. Для оценки качества рекомендаций используется шкала GRADE (табл. 1), в которой сила рекомендаций подразделяется на сильную и слабую, а также учитывается уровень доказательности.
НАЖБП – хроническое заболевание, объединяющее целый спектр клинико-морфологических изменений в печени (стеатоз, стеатогепатит, фиброз и цирроз) у лиц, не употребляющих в чрезмерном количестве алкоголь. НАЖБП диагностируется при накоплении липидов в виде триглицеридов (ТГ) в количестве более 5–10% массы гепатоцитов или при наличии более 5% печеночных клеток, содержащих депозиты липидов.
В МКБ-10 отсутствует единый код НАЖБП, отражающий полноту диагноза, в связи с чем целесообразно использовать один из нижеприведенных кодов:
- К 76.0 – жировая дегенерация печени, не классифицированная в других рубриках;
- К 73.0 – хронический персистирующий гепатит, не классифицированный в других рубриках;
- К 73.9 – хронический гепатит неуточненный;
- К 74.6 – другой и неуточненный цирроз печени (ЦП).
ЭПИДЕМИОЛОГИЯ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ
Распространенность НАЖБП в общей популяции в мире варьирует от 6,3 до 33%. НАЖБП выявляют в любой возрастной категории, а у лиц, страдающих ожирением, распространенность заболевания значительно выше, чем в общей популяции, и, по данным различных исследований, достигает 62–93%. При этом на стадии стеатогепатита НАЖБП диагностируют в 18,5–26%, фиброза – в 20–37%, ЦП – в 9–10% случаев. Имеются наблюдения, показывающие, что среди пациентов с НАЖБП 22% не имели избыточного веса и не страдали сахарным диабетом (СД), 64% – не соответствовали минимальным критериям МС, а в 12% случаев не было выявлено ни одного критерия МС. В исследовании Y. Chang и соавт. (2006) показано, что стеатоз печени может развиваться при повышении массы тела, не сопровождающемся повышением индекса массы тела (ИМТ). Предполагается, что даже незначительное увеличение массы тела способствует перераспределению содержания липидов в тканях и нарушению их нормального метаболизма.
НАЖБП занимает лидирующее место в структуре заболеваний внутренних органов в РФ (сила – 1, уровень – Б). В России 30% трудоспособного населения имеет избыточную массу тела и 25% страдает ожирением. По результатам исследования DIREGL09103 (2007), распространенность НАЖБП в России составляет 27%, при этом у 80,3% пациентов диагностирован стеатоз, у 16,8% – стеатогепатит, у 2,9% – ЦП.
 У 90% пациентов с НАЖБП выявляется 1 компонент МС и более, а у 30% – все составляющие МС. При этом НАЖБП как составляющая МС служит фактором риска развития заболеваний сердечно-сосудистой системы и определяет их исход даже в большей степени, чем исход заболевания печени. Частота НАЖБП у больных СД 2 типа и ожирением, по данным различных исследований, варьирует от 70 до 100%, при этом СД 2 типа или нарушение толерантности к глюкозе (НТГ) выявляют у 10–75%, ожирение – у 30–100%, гипертриглицеридемия – у 20–92% пациентов с НАЖБП.
У 90% пациентов с НАЖБП выявляется 1 компонент МС и более, а у 30% – все составляющие МС. При этом НАЖБП как составляющая МС служит фактором риска развития заболеваний сердечно-сосудистой системы и определяет их исход даже в большей степени, чем исход заболевания печени. Частота НАЖБП у больных СД 2 типа и ожирением, по данным различных исследований, варьирует от 70 до 100%, при этом СД 2 типа или нарушение толерантности к глюкозе (НТГ) выявляют у 10–75%, ожирение – у 30–100%, гипертриглицеридемия – у 20–92% пациентов с НАЖБП.
В настоящее время НАЖБП в рамках МС рассматривается как фактор риска развития и прогрессирования заболеваний печени и сердечно-сосудистой системы (сила – 1, уровень – Б). При этом жировая дегенерация печени у больных НАЖБП может возникнуть задолго до развития МС и создавать существенные предпосылки для развития возможных метаболических нарушений (сила – 1, уровень – В).
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ
В основе развития МС и НАЖБП лежит нарушение чувствительности и количества рецепторов к инсулину – инсулинорезистентность (ИР). ИР приводит к нарушению липидного, углеводного и жирового обменов, результатом которого является избыток свободных жирных кислот (СЖК). ТГ откладываются в виде жировых вакуолей в гепатоцитах, что приводит к развитию жировой инфильтрации печени – стеатоза. В основе стеатоза лежит дисбаланс между потреблением и утилизацией липидов. Накопление жира в клетках печени является следствием: повышения поступления СЖК в печень, снижения скорости β-окисления СЖК в митохондриях, избыточного их синтеза, снижения синтеза или секреции липопротеинов очень низкой плотности (ЛПОНП).
Механизмами трансформации стеатоза в стеатогепатит являются: повышение продукции TNF-α жировой тканью, увеличение концентрации СЖК, которые оказывают прямой повреждающий эффект на мембраны гепатоцитов, активация цитохрома Р450, повышение ПОЛ, накопление реактивных форм кислорода (оксидативный стресс) с образованием избыточного количества высокотоксичных ксенобиотиков. Результатом этих патологических реакций является хроническое воспаление (неалкогольный стеатогепатит; НАСГ), стимуляция коллагенообразования и прогрессирование фиброза в печени. У 15–50% больных НАЖБП имеется фиброз печени, который может трансформироваться в цирроз и гепатоцеллюлярную карциному (ГЦК).
Признаки НАЖБП также обнаруживают у 10–15% людей без клинических проявлений МС, что может быть обусловлено другими причинами, например, синдромом избыточного бактериального роста в кишечнике (СИБР) и/или эндотоксемией. Основные механизмы развития НАЖБП при этих состояниях связаны с активацией ПОЛ и развитием окислительного стресса на фоне нарушения синтеза аполипопротеинов классов А и С, являющихся транспортной формой для ТГ в процессе образования ЛПОНП. Кроме этого, СИБР является причиной повышенного выброса эндотоксина, повреждающего гепатоцит и сосудистый эндотелий. При нарушении функционирования гепатоцита развивается дисбаланс в долях выводимого через основной и дополнительный пути холестерина (ХС; = атерогенная дислипидемия, холестероз желчного пузыря, желчнокаменная болезнь, НАЖБП), что при наличии т.н. факторов риска (в т.ч. гиперэндотоксинемии) является условием формирования атеросклероза.
Имеется также гипотеза о том, что одним из путей развития атеросклероза является первоначальное отложение липидов в стенке желчного пузыря с развитием его холестероза на фоне нарушения обмена холестерина в гепатоците и последующим инициированием отложения липидов в стенке сосудов. Это подтверждается сходством гистологической картины стенки желчного пузыря при холестерозе и стенки сосудов при атеросклерозе в виде образования большого количества пенистых клеток.
ФАКТОРЫ РИСКА РАЗВИТИЯ И ПРОГРЕССИРОВАНИЯ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ
Выделяют первичные и вторичные факторы, способствующие развитию и прогрессированию НАЖБП.
К первичным факторам относят: малоподвижный образ жизни, низкую физическую активность, МС, СД, висцеральное ожирение, дислипидемию.
Вторичные факторы: прием лекарственных препаратов (глюкокортикоиды, амиодарон, эстрогены, тамоксифен, тетрациклин, ацетилсалициловая кислота, индометацин, бруфен, антибиотики), нарушение питания (голодание, резкое сокращение или увеличение калорийности пищи, чрезмерное потребление углеводов, парентеральное питание, недостаток белков, витаминов и микроэлементов), нарушение процессов пищеварения и всасывания (хронические заболевания органов желудочно-кишечного тракта с секреторной недостаточностью пищеварительных ферментов), болезни обмена (Вильсона–Коновалова, Вебера–Крисчена, подагра), гипотиреоз, беременность, нарушение микробиоценоза кишечника.
РОЛЬ ГЕНЕТИЧЕСКОГО ПОЛИМОРФИЗМА В ПАТОГЕНЕЗЕ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ
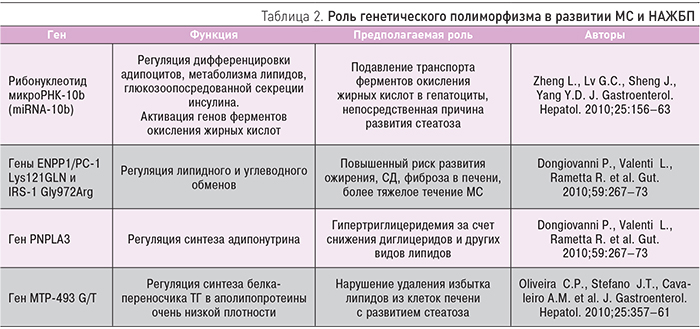
Описано несколько генов, участвующих в регуляции метаболизма липидов и углеводов, имеющих значение в патогенезе НАЖБП (табл. 2)
Имеются случайные наблюдения и данные некоторых исследований о семейной природе заболевания, однако достоверных сведений о семейной природе и наследуемости НАЖБП у взрослых пациентов нет. В связи с этим у взрослых пациентов с НАЖБП скрининг ближайших родственников на наличие заболевания нецелесообразен (сила – 1, уровень – Б).
КЛИНИЧЕСКАЯ КАРТИНА НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ
В целом для НАЖБП характерно бессимптомное течение, поэтому наиболее часто в практике врач сталкивается со случайно обнаруженным при биохимическом исследовании синдромом цитолиза. Зачастую пациенты обращаются к врачу по поводу жалоб, не связанных с заболеванием печени, а именно по поводу артериальной гипертензии, ишемической болезни сердца, заболеваний периферических сосудов, ожирения, СД 2 типа и др.
Основные клинические симптомы:
- астенический синдром: слабость, повышенная утомляемость, нарушение сна;
- диспепсический синдром: метеоризм, тошнота, нарушения стула;
- болевой синдром: тупые боли и/или тяжесть в правом подреберье;
- гепатомегалия и/или спленомегалия.
Необходимо учитывать, что интенсивность предъявляемых жалоб, данные лабораторно-инструментального обследования не коррелируют со степенью активности процесса.
Показатели биохимического анализа крови у пациентов на стадии стеатоза печени обычно не превышают границ нормы. При лабораторном обследовании пациентов на стадии стеатогепатита выявляют изменения биохимических показателей: повышение активности аланиновой (АЛТ) и аспарагиновой (АСТ) аминотрансфераз до уровня 4–5 норм с преобладанием АЛТ, повышение активности щелочной фосфатазы (ЩФ) и гамма-глутамилтранспептидазы (ГГТП), гиперхолестеринемия, гипергликемия (НТГ или СД 2 типа), гипоальбуминемия, повышение уровня билирубина.
Спутником НАЖБП является дислипидемия (проатерогенный сывороточный липидный профиль, включающий низкий уровень ХС липопротеинов высокой плотности (ЛПВП), высокий уровень ТГ, ЛПНП и аполипопротеина В100), способствующая прогрессированию поражения печени и развитию заболеваний сердечно-сосудистой системы (сила – 1, уровень – Б).
При трансформации фиброза в ЦП наблюдается преобладание АСТ над АЛТ, а также снижение белково-синтетической функции печени в виде снижения уровня общего белка, альбумина, ХС, холинэстеразы и протромбинового индекса, повышение уровня билирубина и тромбоцитопения. Наличие фиброза характеризуется изменением сывороточных маркеров: гиалуроновой кислоты, проколлагена III типа, N-терминального пептида проколлагена III, ламинина и др. На этом фоне постепенно формируется портальная гипертензия (расширение воротной и селезеночной вен, варикозное расширение вен пищевода, асцит).
Отсутствие изменений лабораторных показателей, характеризующих функциональное состояние печени, не исключает наличия воспалительно-деструктивного процесса и фиброза.
ДИАГНОСТИКА НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ
Основное условие диагностики НАЖБП – установление наличия избыточного содержания жира в печени по данным инструментальных и/или морфологических исследований.
У больных с подозрением на НАЖБП рекомендуется исключить конкурирующие этиологические факторы и сопутствующие хронические заболевания печени (сила – 1, уровень – А):
- алкогольную болезнь печени;
- хронический вирусный гепатит (исследование на маркеры вирусных гепатитов В и С);
- болезнь Вильсона–Коновалова (исследование прямой фракции меди и церулоплазмина в сыворотке крови, меди в суточной моче);
- гемохроматоз (исследование показателей обмена железа: ферритин, трансферрин, степень насыщения трансферрина);
- аутоиммунные заболевания печени (исследование аутоантител: антинуклеарные, антигладкомышечные, антинейтрофильные, антимитохондриальные, печеночно-почечные);
- врожденную недостаточность α1-антитрипсина (определение фермента в сыворотке крови).
Необходимо исключить вторичные факторы развития НАЖБП: прием лекарственных препаратов (амиодарон, аспирин, глюкокортикоиды, кокаин, дилтиазем, нифедипин, тамоксифен, метотрексат и др.), парентеральное питание, голодание, быстрое снижение массы тела, СИБР, воспалительные заболевания кишечника, хирургические вмешательства (гастропластика, еюноилеальное шунтирование, обширная резекция тонкой кишки).
Исключение алкогольной этиологии является одной из первых задач в диагностике НАЖБП. Приемлемой дозой употребления алкоголя у пациентов, которым диагностируется НАЖБП, следует считать не более 210 мл этанола в нед для мужчин и не более 140 мл в нед для женщин (сила – 2, уровень – В).
Для исключения алкогольной этиологии рекомендованы:
- опрос ближайших родственников пациента;
- апробированные опросники для количественной оценки потребления алкоголя;
- определение лабораторных маркеров злоупотребления алкоголем: уровня сывороточной ГГТП, АСТ, соотношения АСТ/АЛТ, среднего объема эритроцитов, уровня ТГ, углеводдефицитного трансферрина;
- определение алкогольного стеатоза с помощью диагностической панели «ФиброМакс» («АшТест»).
РОЛЬ ВИЗУАЛИЗИРУЮЩИХ МЕТОДОВ В ДИАГНОСТИКЕ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ
С целью верификации наличия и степени выраженности жировой инфильтрации печени и портальной гипертензии рекомендовано инструментальное обследование: ультразвуковое исследование (УЗИ), компьютерная томография (КТ), магнитно-резонансная томография (МРТ).
Среди визуальных методов диагностики НАЖБП наибольшее распространение в виду своей доступности получило УЗИ, дающее возможность заподозрить стеатоз в печени и оценивать изменения в динамике.
Основные ультразвуковые признаки стеатоза печени:
- дистальное затухание эхосигнала;
- диффузная гиперэхогенность печени («яркая белая печень»);
- увеличение эхогенности печени по сравнению с почками;
- нечеткость и обеднение сосудистого рисунка.
Основные признаки стеатоза печени по данным КТ:
- снижение рентгеноплотности печени до 3–5 единиц (норма 50–75 единиц);
- рентгеноплотность печени при стеатозе меньше рентгеноплотности селезенки;
- внутрипеченочные сосуды (воротная, нижняя полая вена) визуализируются как более плотные структуры по сравнению с печеночной тканью;
- для очаговой жировой инфильтрации характерно пересечение нормальными кровеносными сосудами печени зон пониженной рентгеноконтрастности.
 При необходимости применяется современная высокопольная МРТ, преимуществами которой являются: высокая тканевая контрастность изображения за счет выгодного соотношения сигнал–шум, возможность получения целостного изображения органа в любой проекции, большие ресурсы программного обеспечения, используемые для дифференциальной диагностики.
При необходимости применяется современная высокопольная МРТ, преимуществами которой являются: высокая тканевая контрастность изображения за счет выгодного соотношения сигнал–шум, возможность получения целостного изображения органа в любой проекции, большие ресурсы программного обеспечения, используемые для дифференциальной диагностики.
НЕИНВАЗИВНАЯ ДИАГНОСТИКА ФИБРОЗА ПЕЧЕНИ ПРИ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ
Для установления степени выраженности некровоспалительных изменений и стадии фиброза печени для больных НАЖБП разработан неинвазивный диагностический тест. По ряду биохимических показателей, с учетом пола, возраста, роста и веса пациента, на основании математического анализа производится расчет индекса, соответствующего той или иной шкале.
Для определения степени фиброза при НАЖБП возможно также использование следующих неинвазивных сывотороточных тестов:
- Fibro Test дает возможность определения сывороточных маркеров фиброза (α2-макроглобулин [АМГ], гаптоглобин, аполипопротеин А1 [ApoAl], ГГТП, общий билирубин) с последующим расчетом индекса фиброза по специальной формуле. Тест имеет высокую надежность при выраженных стадиях фиброза – прогностическая ценность отрицательного (NPV – negative predictive value) и положительного (PPV – positive predictive value) результата составляет 90 и 70% соответственно. Синдром Жильбера, высокий цитолиз, высокая концентрация ЛПВП делает Fibro Test неэффективным.
- Шкала оценки фиброза при НАЖБП (NAFLD fibrosis score) основана на ряде показателей: возраст (количество лет), нарушение толерантности к глюкозе (НТГ; есть = 1, нет = 2), ИМТ (ИМТ = масса тела в кг/рост в м2), количество тромбоцитов (1х109/л), уровень альбумина (г/дл), соотношение АСТ/АЛТ. Степень фиброза рассчитывается по формуле: - 1,675 + 0,037возраст + 0,094 ИМТ + 1,13 НТГ + 0,99 АСТ/АЛТ– 0,013 тромбоциты – 0,66 альбумин. При значении менее 1,455 фиброз отсутствует, более 0,676 – выраженный фиброз (чувствительность шкалы 90%).
- Original European Liver Fibrosis (OELF) test (чувствительность 90%) включает ряд показателей: возраст, уровень тканевого ингибитора металлопротеиназы-1, концентрация гиалуроновой кислоты, концентрация N-терминального пропептида коллагена III типа.
Для выявления фиброза и оценки степени фиброза используется также транзиентная эластография печени, с помощью которой определяется эластичность печени. Наиболее высокая диагностическая точность метода наблюдается при выраженных стадиях фиброза. Недостатком метода является отсутствие возможности оценки выраженности некровоспалительного процесса, неинформативность у пациентов с избыточной массой тела, искажение значения результатов у пациентов в стадии биохимической ремиссии, с острым гепатитом, невозможность оценки состояния печени на стадиях стеатоза, стеатогепатита и ранних стадиях фиброза.
Значение (интерпретация) полученных при обследовании результатов
У пациента со случайно выявленным при инструментальном обследовании стеатозе печени (при отсутствии признаков или симптомов печеночного заболевания и нормальных биохимических показателях) целесообразно провести оценку метаболических факторов и альтернативных причин возникновения стеатоза (сила – 1, уровень – А).
Случайно выявленные при инструментальном обследовании признаки или симптомы и изменения биохимических показателей сыворотки крови, характерные для НАЖБП, дают основание предполагать наличие заболевания и проводить дальнейшее исследование (сила – 1, уровень – А).
Наличие метаболического синдрома, положительные результаты диагностических тестов NFS-индекса могут быть использованы для верификации лиц с высоким риском развития НАЖБП и прогрессирующего фиброза печени (сила – 1, уровень – В).
При обнаружении у пациентов НАЖБП в сыворотке крови высоких титров аутоантител в сочетании с другими признаками иммунного воспаления необходимо провести полное обследование для исключения аутоиммунного заболевания (сила – 1, уровень – В).
Перспективным биомаркером для диагностики НАЖБП может быть концентрация цитокератина 18 (СК18) в сыворотке, однако в повседневной клинической практике его исследование не рекомендовано для широкого использования (сила – 1, уровень – В).
Пациентам с ЦП в исходе НАЖБП целесообразно проведение скрининга для верификации портальной гипертензии (варикозного расширения вен пищевода и желудка) (сила – 1, уровень – Б).
БИОПСИЯ ПЕЧЕНИ В ДИАГНОСТИКЕ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ
Пункционная биопсия печени является «золотым стандартом» диагностики НАЖБП, особенно в случаях, когда другие методы диагностики не дают возможности убедительно верифицировать заболевание.
Показания к биопсии печени при НАЖБП:
- возраст старше 45 лет и хронический цитолиз неустановленной этиологии;
- сочетание хронического цитолиза неустановленной этиологии по крайней мере с двумя проявлениями МС, независимо от возраста.
Биопсия с целью дифференциальной диагностики показана:
- в случае невозможности другими методами исключить наличие конкурирующих этиологических факторов и сопутствующих хронических заболеваний печени (сила – 1, уровень – В);
- при высокой вероятности наличия стеатогепатита и прогрессирующего фиброза печени (сила – 1, уровень – В);
- при подозрении на НАЖБП в сочетании с устойчивым выраженным увеличении содержания железа и сывороточного ферритина на фоне гомозиготной или гетерозиготной мутации С282У в гене НFE (сила – 1, уровень – В).
 Биопсия печени не показана лицам с НАЖБП со стеатозом, выявленным при инструментальном обследовании, в случае отсутствия признаков или симптомов печеночного заболевания и нормальных биохимических показателях (сила – 1, уровень – В), а также пациентам с установленным НАЖБП в рутинном обследовании для динамического наблюдения (сила – 2, уровень – В).
Биопсия печени не показана лицам с НАЖБП со стеатозом, выявленным при инструментальном обследовании, в случае отсутствия признаков или симптомов печеночного заболевания и нормальных биохимических показателях (сила – 1, уровень – В), а также пациентам с установленным НАЖБП в рутинном обследовании для динамического наблюдения (сила – 2, уровень – В).
КЛАССИФИКАЦИЯ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ
По гистологическим признакам выделяют стеатоз, стеатогепатит (НАСГ) и ЦП в исходе НАЖБП. Стеатоз печени определяется при наличии накопления жира в печени без признаков гепатоцеллюлярного повреждения в виде баллонной дистрофии гепатоцитов. НАСГ характеризуется наличием воспалительной инфильтрации на фоне стеатоза с фиброзом или без фиброза. На стадии ЦП выявляются морфологические признаки цирроза в сочетании с жировой инфильтрацией печени.
Основные морфологические критерии НАЖБП:
- крупнокапельный стеатоз, преимущественно в 3-й зоне ацинуса, характеризующийся наличием крупных липидных капель в цитоплазме со смещением ядра к периферии дольки;
- баллонная дистрофия гепатоцитов;
- преобладание лобулярного воспаления, представленного полиморфноядерными лейкоцитами и мононуклеарами;
- перисинусоидальный фиброз в 3-й зоне ацинуса – месте наихудшего кровоснабжения.
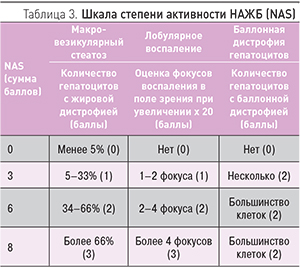
С целью определения активности заболевания разработана специальная шкала для определения активности НАЖБП (NAFLD activity score, NAS), которая представляет собой комплексную оценку морфологических изменений в баллах и объединяет такие критерии, как стеатоз, лобулярное воспаление и баллонную дистрофию гепатоцитов (табл. 3).
При сумме баллов менее 3 – НАСГ отсутствует, 3–5 баллов – пограничное значение, более 5 баллов – имеется НАСГ.
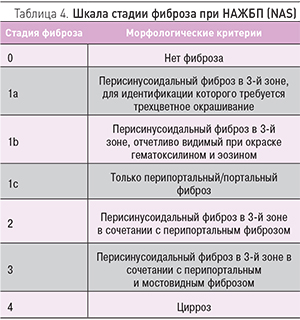
Аналогичная шкала разработана и для определения стадии фиброза при НАЖБП (табл. 4).
Скрининг на наличие НАЖБП целесообразен среди взрослых пациентов с СД, ожирением, МС в связи с высоким риском возникновения у них заболеваний печени и сердечно-сосудистой системы (сила – 1, уровень – В).
План обследования пациентов с метаболическими нарушениями, обращающихся к врачу по поводу ишемической болезни сердца, СД 2 типа, артериальной гипертензии, гипотиреоза, холелитиаза и т.д.
- Сбор анамнеза (наследственность, образ жизни, пищевые привычки, физические нагрузки).
- Антропометрические измерения (ИМТ, объем талии [ОТ] и бедер [ОБ], индекс ОТ/ОБ).
- Объективный осмотр (выявление малых печеночных знаков: телеангиоэктазий, пальмарной эритемы, оценка размеров и консистенции печени, размеров селезенки).
- Мониторинг артериального давления, электрокардиографическое исследование.
- Оценка липидограммы: ТГ, общего ХС, ХС ЛПВП и ЛПНП, апо-В ЛП.
- Определение уровня глюкозы натощак, глюкозотолерантный тест по показаниям.
- Инсулин крови натощак.
- Оценка наличия и выраженности ИР – определение индекса HOMA-IR (HOmeostasis Model Assesment) по формуле: HOMA-IR = I0 х G0/22,5, где I0 – уровень инсулина натощак (мкМЕ/мл), G0 – уровень глюкозы натощак (ммоль/л) (значение HOMA-IR у здоровых лиц менее 2,7, при нарушении толерантности к глюкозе, СД 2 типа – более 4, значимую диагностическую ценность при НАЖБП имеет увеличение индекса HOMA-IR более 5).
- Клинический анализ крови (наличие тромбоцитопении, анемии).
- Оценка биохимических показателей, отражающих функциональное состояние печени (АЛТ, АСТ, ГГТП, ЩФ, общий билирубин, протромбин, протеинограмма).
- УЗИ органов брюшной полости (размеры печени и селезенки, наличие и выраженность портальной гипертензии).
- Эзофагогастродуоденоскопия (ЭГДС; скрининг на наличие варикозно расширенных вен пищевода).
- КТ (МРТ) печени.
- Пункционная биопсия печени.
ОЦЕНКА ПРОГРЕССИРОВАНИЯ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ
Предикторами высокого риска прогрессирования НАЖБП с развитием гепатита и фиброза являются: возраст старше 45 лет, женский пол, ИМТ более 28 кг/м2, постоянное увеличение уровня АЛТ более 2 норм, уровень ТГ более 1,7 ммоль/л, артериальная гипертензия, СД 2 типа, индекс ИР (НОМА-IR) более 5. Наличие 2 и более критериев свидетельствует о высоком риске фиброза печени.
ЛЕЧЕНИЕ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ
Основной целью терапии является профилактика прогрессирования болезни: уменьшение выраженности стеатоза и предотвращение прогрессирования заболевания в стеатогепатит, фиброз и цирроз, а также снижение риска сердечно-сосудистых осложнений. В ряде исследований показано, что комплексные меры по изменению образа жизни пациентов с НАЖБП способствуют снижению смертности от сердечно-сосудистых осложнений на 40%, что сопоставимо с эффективностью медикаментозной коррекции.
Основные принципы лечения НАЖБП:
- снижение массы тела (диета и физические нагрузки);
- обязательная отмена потенциально гепатотоксичных препаратов;
- коррекция метаболических нарушений – дислипидемии, гипергликемии:
- повышение чувствительности клеточных рецепторов к инсулину (метформин, тиазолидиндионы);
- коррекция нарушений липидного обмена;
- снижение концентрации TNF-α (пентоксифиллин);
- гипотензивная терапия (антагонисты рецепторов ангиотензина II).
Не существует унифицированного немедикаментозного подхода в лечении пациентов c НАЖБП, целесообразным является приспособление диеты, снижение веса и увеличение физической нагрузки к индивидуальным потребностям пациента. Постепенное снижение веса и увеличение физической нагрузки является ведущими факторами в лечении НАЖБП (сила – 1, уровень – А), потеря веса при использовании гипокалорийной диеты или ее сочетание с повышенной физической активностью способствует уменьшению проявлений стеатоза (сила – 1, уровень – А). Установлено, что для уменьшения выраженности стеатоза при НАЖБП требуется снижение веса тела не менее чем на 3–5%, а для устранения некротических и воспалительных изменений в печени при стеатогепатите необходимо снижение веса не менее чем на 10% (сила – 1, уровень – В). У взрослых пациентов физическая нагрузка уменьшает выраженность стеатоза даже при отсутствии дополнительных медикаментозных воздействий, однако ее влияние на нормализацию других гистологических изменений в печени остается неизвестной (сила – 1, уровень – В). Пациентам с НАЖБП противопоказано злоупотребление алкоголем (сила – 1, уровень – В).
ФАРМАКОЛОГИЧЕСКАЯ КОРРЕКЦИЯ ИНСУЛИНОРЕЗИСТЕНТНОСТИ
В клинических исследованиях по изучению эффективности метформина показано снижение резистентности к инсулину, уменьшение активности трансаминаз и выраженное снижение веса (более 10 кг) у 19% больных НАЖБП. Однако улучшение гистологической картины печени было незначительным: уменьшения выраженности стеатоза удается достигнуть только у 30% пациентов. Данные мета-анализа показали, что применение метформина в течение 6–12 мес на фоне изменений образа жизни не снижало выраженности цитолиза и улучшало гистологическую картину печени только по сравнению с изменением образа жизни. В связи с полученными данными метформин не рекомендуется в качестве специфического средства для лечения НАЖБП с синдромом ИР, поскольку не оказывает существенного влияния на гистологическую структуру печени (сила – 1, уровень – В). Метформин в дозе 20 мг/кг/сут (дозу наращивать постепенно, начиная с 500–850 мг/сут) курсами не менее года назначается пациентам с НАЖБП для лечения сопутствующего нарушения толерантности к углеводам и профилактики развития СД 2 типа.
Пиоглитазон может быть использован для лечения морфологически подтвержденного НАСГ, однако его безопасность и эффективность при длительной терапии не доказана (сила – 1, уровень – В).
ФАРМАКОЛОГИЧЕСКАЯ КОРРЕКЦИЯ ГИПЕРЛИПИДЕМИИ
Гиполипидемическую терапию следует проводить с учетом стадии НАЖБП, при необходимости – в комбинации с гепатопротекторами. Наиболее распространенными и изученными гиполипидемическими препаратами являются ингибиторы ГМК-КОА-редуктазы – статины.
У больных НАЖБП при отсутствии данных о повышенном гепатотоксическом риске под воздействием статинов они могут быть использованы для коррекции дислипидемии (сила – 1, уровень – В). Однако для специфического лечения НАСГ статины не рекомендуется применять до морфологического подтверждения их эффективности РКИ (сила – 1, уровень – В). В исследованиях показано, что прием статинов в комбинации с препаратами уродезоксихолевой кислоты (УДХК) в дозе 10–15 мг/ кг/ сут сопровождается более выраженным снижением уровня ХС ЛПНП. Такая комбинация предупреждает развитие цитолиза и способствует снижению исходно повышенных трансаминаз.
На фоне лечения статинами рекомендуется активный мониторинг каждые 3–4 нед:
- определение сывороточных печеночных тестов (билирубин, трансаминазы, ГГТП, ЩФ);
- определение показателей углеводного и липидного обменов (глюкоза, ТГ, общий ХС, ХС ЛПНП, ХС ЛПВП, инсулин).
В качестве средства первой линии у пациентов НАЖБП с триглицеридемией показаны омега-3 жирные кислоты (сила – 1, уровень – В).
Кроме статинов, при нарушении липидного обмена у больных НАЖБП рекомендованы: производные фиброевой кислоты (фибраты), никотиновая кислота (ниацин), секвестранты желчных кислот (ионно-обменные смолы). Однако в настоящее время отсутствуют РКИ по их использованию у больных НАЖБП.
ЛЕЧЕНИЕ ОКИСЛИТЕЛЬНОГО СТРЕССА
В лечении НАЖБП патогенетически оправдано назначение лекарственных средств метаболического действия с антиоксидантной активностью, таких как витамин Е, УДХК, эссенциальные фосфолипиды, метадоксин, адеметионин, липоевая кислота.
Витамин Е в лечении больных НАЖБП
Витамин Е в суточной дозе 800 МЕ у пациентов с НАЖБП, не страдающих СД, улучшает гистологическую картину печени. Препарат можно отнести к средствам терапии первой линии в качестве антиоксиданта в лечении данной категории больных (сила – 1, уровень – В). Однако до получения убедительных данных об эффективности и безопасности витамина Е его не следует назначать пациентам с НАЖБП, страдающим СД, не подтвержденной гистологическим исследованием, а также при ЦП в исходе НАЖБП (сила – 1, уровень – С).
Урсодезоксихолевая кислота в лечении НАЖБП
УДХК как препарат, обладающий антиоксидантным, мембраностабилизирующим и иммуномодулирующим действиями, может быть использована для лечения НАЖБП с признаками стеатоза и стеатогепатита (сила – 1, уровень – В). УДХК назначается в дозе 10–15 мг/кг/сут в 2 приема не менее года, иногда до 2-х лет и более. Имеются данные о снижении цитолитического синдрома и уменьшении выраженности стеатоза печени при лечении больных НАЖБП УДХК.
Другие препараты в лечении НАЖБП
В настоящее время отсутствуют РКИ по использованию у больных НАЖБП пентоксифиллина, антагонистов рецепторов ангиотензина II, эссенциальных фосфолипидов, силимарина, адеметионина, метадоксина. Однако применение этих препаратов патогенетически обосновано с учетом имеющихся у них антиоксидантного, противовоспалительного механизмов действия.
Эссенциальные фосфолипиды (1–2 капсулы 2–3 раза/ сут) стабилизируют мембраны и антитоксическую функцию печени; усиливают элиминацию и снижение внутрипеченочного синтеза холестерина; активируют синтез белка; оказывают желчегонное, мочегонное и гипоазотемическое действие, нормализуют клеточную структуру печени и фосфолипидзависимые энзиматические системы, тормозят формирование соединительной ткани и вызывают регресс жировых вакуолей в гепатоцитах, предотвращают окисление жира, ведущее к воспалению и фиброзу.
Силимарин (140 мг 3 раза/сут курсами до 6 мес) предотвращает активацию звездчатых и Купферовских клеток (путем снижения содержания реактивных форм кислорода [ROS] и синтеза лейкотриенов B4 и PDE4).
Метадоксин (500 мг 3 раза/сут), являясь мощным антиоксидантом, усиливает антитоксическую функцию печени, способствует уменьшению жировых отложений в печени, снижает коллагенообразование.
Имеется опыт применения адеметионина (400 мг 3 раза/сут) у больных с НАЖБП, в результате которого получено снижение активности ферментов цитолиза и регрессия клинических симптомов.
ВОССТАНОВЛЕНИЕ НАРУШЕНИЙ МИКРОБИОЦЕНОЗА КИШЕЧНИКА У БОЛЬНЫХ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНЬЮ ПЕЧЕНИ
Нарушение микробиоценоза кишечника у больных НАСГ является показанием для проведения его санации антибактериальными препаратами (рифаксимин 400 мг 2 раза/сут после еды, метронидазол 250 мг 3 раза/сут, ципрофлоксацин 250 мг 2 раза/сут 5–7 дней) с последующим назначением пробиотиков, пребиотиков, симбиотиков, синбиотиков на 3–4 нед (сила – 1, уровень – С).
БАРИАТРИЧЕСКАЯ ХИРУРГИЯ ВЕРХНИХ ОТДЕЛОВ ПИЩЕВАРИТЕЛЬНОГО ТРАКТА
Больным НАЖБП в качестве метода специфического лечения преждевременно рекомендовать бариатрическую хирургию верхних отделов пищеварительного тракта (сила – 1, уровень – В). При этом у тучных пациентов НАЖБП без верифицированного ЦП отсутствуют противопоказания для бариатрического хирургического лечения верхних отделов пищеварительного тракта (сила – 1, уровень – А). У больных НАСГ с исходом в ЦП и избыточным весом пока не определены вид, безопасность и эффективность методов бариатрической хирургии верхних отделов пищеварительного тракта (сила – 1, уровень – В).
ДИНАМИЧЕСКОЕ НАБЛЮДЕНИЕ ЗА БОЛЬНЫМИ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНЬЮ ПЕЧЕНИ
Динамическое наблюдение за больными НАЖБП осуществляет терапевт (врач общей практики).
Каждые 6 мес рекомендуется:
- определение антропометрических данных (масса тела, ИМТ, окружность талии);
- определение сывороточных печеночных тестов (трансаминазы, ГГТП, ЩФ).
- определение показателей углеводного и липидного обменов (глюкоза, ТГ, общий ХС, ХС ЛПНП, ХС ЛВП, инсулин);
- определение степени фиброза печени с помощью неинвазивных методов диагностики (фиброэластометрия, сывороточные тесты).
Каждые 12 мес рекомендуется проведение УЗИ органов брюшной полости, при необходимости ЭГДС.
НЕАЛКОГОЛЬНАЯ ЖИРОВАЯ БОЛЕЗНЬ ПЕЧЕНИ У ПАЦИЕНТОВ ПОЖИЛОГО И СТАРЧЕСКОГО ВОЗРАСТА
У лиц пожилого и старческого возраста жировая инфильтрация печени встречается в 25,2–86,3% случаев. Частота и выраженность стеатоза нарастает с возрастом и достигает пика в 40–60 лет. НАЖБП у пациентов пожилого и старческого возраста следует рассматривать как печеночное проявление МС (сила – 1, уровень – В).
Особенности диагностики НАЖБП у пациентов пожилого и старческого возраста
Пациенты гериатрического возраста с ишемической болезнью сердца атеросклеротического генеза нуждаются в проведении дополнительного исследования на выявление жирового перерождения печени (сила – 1, уровень – В). Жировая инфильтрация печени у пожилых и старых мужчин сопровождается повышением в сыворотке крови уровня мочевой кислоты, снижением ЛПНП при нормальной активности трансаминаз. У пожилых и старых пациентов НАЖБП активность аминотрансфераз не является абсолютным критерием диагностики заболевания, поскольку известно, что с увеличением возраста активность АЛТ и АСТ уменьшается (сила – 1, уровень – В).
Биопсия печени для пожилых и, особенно, старых пациентов не имеет строго регламентированных показаний и противопоказаний, однако ее проведение ограничено (сила – 1, уровень – В).
Лечение НАЖБП у пациентов пожилого и старческого возраста
Гериатрическому больному НАЖБП показаны ежедневные 30–50-минутные физические упражнения с преимущественно аэробной нагрузкой (сила – 1, уровень – В). Снижение массы тела необходимо проводить в течение нескольких месяцев при соблюдении принципов геродиететики (сила – 1, уровень – В), рекомендуемый безопасный темп снижения массы тела должен соответствовать 2,0–3,0 кг/мес.
Коррекция декомпенсированного СД 2 типа у пожилых и старых пациентов с НАЖБП требует назначения инсулинотерапии, несмотря на то, что терапия может интенсифицировать жировое перерождение печени (сила – 1, уровень – С).


