Артериальная гипертензия (АГ) является глобальной проблемой общественного здравоохранения, от которой страдает четверть взрослого населения мира, как в развитых, так и развивающихся странах [1]. Более 40% населения России имеют диагноз АГ [2, 3].
Этиология АГ включает генетические и поведенческие факторы, оказывающие влияние на функционирование вегетативной нервной системы и регуляцию тонуса сосудов [4].
В исследованиях показано, что высокий уровень стресса способствует росту артериального давления (АД), частоты сердечных сокращений (ЧСС), увеличению уровня холестерина, триглицеридов и фибриногена в крови [1, 5–8]. Повышенное АД, наряду с нарушением липидного обмена и изменением параметров свертываемости крови, служит значимым фактором риска развития сердечно-сосудистых заболеваний (ССЗ), цереброваскулярных болезней (ЦВБ), хронической болезни почек, инвалидности и преждевременной смерти [9].
Продолжительное воздействие стресса приводит к нарушению функционирования гипоталамо-гипофизарно-адреналовой и вегетативной нервной систем. Срыв адаптационных механизмов способствует развитию тревоги и депрессии [10, 11]. Более чем в половине случаев у пациентов с ССЗ тревожно-депрессивные расстройства вносят вклад в развитие основного заболевания, осложняют его течение и терапию [11, 12]. У каждого пятого пациента с АГ или ишемической болезнью сердца (ИБС) диагностирована депрессия, распространенность которой в среднем в 3 раза выше, чем среди населения в целом [13–15].
Лечение тревожно-депрессивных расстройств, ассоциированных с ССЗ, требует специальных психофармакологических подходов по сравнению с терапией эмоциональных нарушений у пациентов без сопутствующих соматических заболеваний [11, 16]. Использование препаратов из групп антидепрессантов более эффективно у пациентов с клинически завершенной депрессией. Применение бензодиазепинов и нейролептиков ограничено в связи высокой вероятностью возникновения нежелательных явлений или риска межлекарственного взаимодействия у пациентов с АГ и другими ССЗ [11]. В связи с этим становится очевидной необходимость оптимизации терапии реакций тревожно-депрессивного спектра у больных АГ.
Препарат Тенотен, созданный на основе технологически обработанных антител к мозгоспецифическому белку S100 (высокие разведения) [16], обладает противотревожным, антистрессорным и антидепрессивным эффектами, доказанными в доклинических и клинических исследованиях (КИ) [16]. В ранее проведенных КИ показана высокая эффективность и безопасность Тенотена в терапии тревоги у пациентов с АГ 1–3 степени, ИБС, нарушениями ритма сердца (НРС) [16, 17].
Целью настоящей наблюдательной программы ТЕАТР стала оценка эффективности и безопасности препарата Тенотен у пациентов с АГ и тревожно-депрессивными расстройствами в реальной клинической практике.
МАТЕРИАЛ И МЕТОДЫ
Дизайн и процедуры исследования
Всероссийская открытая проспективная наблюдательная программа ТЕАТР была одобрена этическим комитетом (протокол от 20.09.2019 № 14, Независимый междисциплинарный комитет по этической экспертизе клинических исследований) и проведена в соответствие с правилами надлежащей клинической практики (Good Clinical Practice) и Хельсинской декларацией в период с 2019 по 2020 г. В программе приняли участие 571 врач-терапевт из 8 регионов России.
В исследование включались амбулаторные пациенты обоего пола в возрасте 18–70 лет с невротическими расстройствами и расстройствами адаптации на фоне АГ. Диагноз АГ был установлен терапевтом в соответствии с Международной классификацией болезней-10 (МКБ-10) до включения в исследование. Наличие тревожного, депрессивного или смешанного расстройств подтверждалось результатами оценки по Госпитальной шкале тревоги и депрессии Hospital Anxiety and Depression Scale HADS (HADS-A и/или HADS-D ≥11 баллов). Всем пациентам в дополнение к неизменной базовой антигипертензивной терапии был назначен анксиолитический препарат Тенотен по 2 таблетки 3 раза/сут в течение 12 нед.
На этапе включения в программу и завершения терапии проводилась оценка жизненно важных показателей (ЧСС, систолического и диастолического АД), выраженности тревожного, депрессивного или смешанного расстройства по HADS и клинического впечатления врача о состоянии пациента по шкале Общего клинического впечатления (Clinical Global Impression-Severity, CGI-S). Регистрировались сопутствующие заболевания и терапия, факторы риска ССЗ, наличие поражения органов-мишеней и ассоциированных с АГ заболеваний (ЦВБ, перенесенный инсульт, ИБС, стенокардия, постинфарктный кардиосклероз, НРС, хроническая сердечная недостаточность, безболевая ишемия миокарда, почечная недостаточность, заболевания периферических артерий, гипертоническая ретинопатия), рассчитывался индекс коморбидности Чарлсон (ИКЧ, Charlson comorbidity index).
Определение размера выборки
Планировалось включение в программу 7000 пациентов из 40 городов России. Набор пациентов производился в произвольной демографической пропорции.
Критерии эффективности и безопасности
Первичным критерием эффективности терапии служила оценка доли пациентов с отсутствием тревожно-депрессивных симптомов (≤7 баллов по подшкалам тревоги/депрессии шкалы HADS) через 12 нед применения препарата Тенотен. В качестве дополнительных критериев эффективности были проанализированы:
- средний балл и динамика среднего балла по шкале HADS, подшкалам HADS-A и HADS-D по сравнению с исходным;
- динамика жизненно важных показателей (ЧСС, АД);
- динамика среднего балла по шкале CGI-S;
- величина ИКЧ и его влияние на жизненно важные показатели и выраженность тревоги по шкале HADS.
Безопасность терапии оценивалась по частоте и выраженности нежелательных явлений.
Статистический анализ
Анализ суммарного балла шкалы HADS и ее подшкал, шкалы CGI-S, а также динамики АД осуществлялся с помощью ковариационной модели. Интересующими фиксированными факторами служили «Основной диагноз», «Характер тревожно-депрессивных расстройств» и их взаимодействие. В качестве ковариаты выступал ИКЧ.
Для оценки ЧСС был применен дисперсионный анализ с теми же фиксированными факторами, описанными выше.
Доля пациентов с отсутствием симптомов анализировалась с помощью логистической регрессии, интересующие факторы были аналогичны вышеуказанным.
Данные по общей характеристике, клинической картине, комплаентности, показателям безопасности представлены в рамках описательной статистики.
РЕЗУЛЬТАТЫ
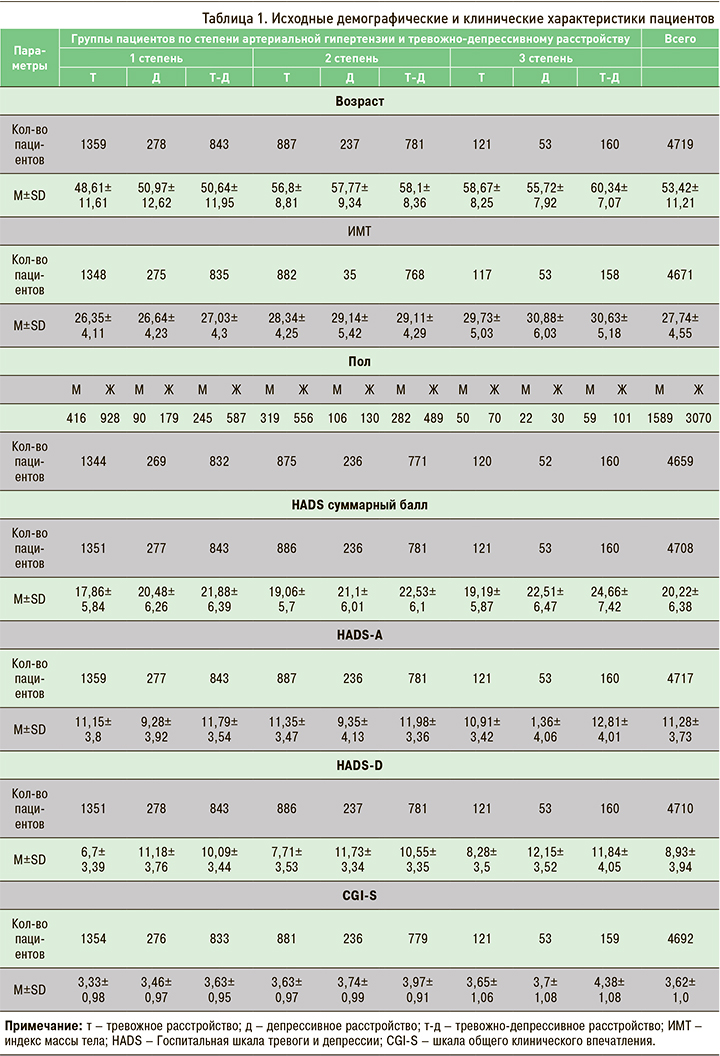
Исходные демографические и клинические данные пациентов
В КИ принимали участие 6933 пациента. Анализ безопасности и приверженности терапии проводили с учетом данных 4719 человек (2214 человек не соответствовали критерию включения «возраст от 18 до 70 лет» или имели низкие показатели комплаентности). Клинические и демографические характеристики некоторых пациентов, завершивших курс терапии, частично отсутствовали, в связи с чем в анализ эффективности включены только полные данные по каждому критерию эффективности и демографическому показателю.
Данные пациентов были распределены по группам в соответствии со степенью АГ (1–3) и характером эмоционального расстройства (тревожное, депрессивное и смешанное расстройство).
Возраст пациентов (n=4719) во всех группах превышал 45 лет и в среднем для всех пациентов составил 53,4±11,2 лет.
Большую часть участников во всех группах составили женщины. Всего среди всех проанализированных пациентов (n=4659) женщин (n=3070) было в 2 раза больше, чем мужчин (n=1589).
Для пациентов (n=4671) была характерна избыточная масса тела: во всех группах индекс массы тела (ИМТ) превышал 26 кг/м2 (среднее 27,74±4,55 кг/м2). Наибольшим показатель ИМТ был в группе пациентов с АГ 3 степени (табл. 1).
Комплаентность
По результатам КИ, приверженность лечению среди 4719 пациентов составила 106,81%.
Факторы риска и ассоциированные с артериальной гипертензией заболевания
Более 40% всех участников имели сопутствующие факторы риска, такие как гиперхолестеринемия (56,3% пациентов из 4693) и наличие ССЗ в семейном анамнезе (51,7% из 4657). Сахарный диабет (СД) встречался в 13,7% случаев (из 4620), метаболический синдром – в 32,3% (из 4628). Наиболее часто у пациентов наблюдалась сопутствующая гипертрофия левого желудочка (43,1% из 4681). Остальные варианты поражения органов мишеней встречались реже: атеросклеротическое поражение магистральных сосудов было характерно для 23,5% пациентов (из 4625), гиперкреатинемия – для 7,3% (из 4611). Среди ассоциированных с АГ заболеваний 30,5% (из 4673) участников КИ имели ЦВБ, 17,9% (из 4629) – гипертоническую ретинопатию. ИБС присутствовала у 15,9% пациентов (из 4644).
Сопутствующие заболевания
Сопутствующие заболевания, не связанные с АГ, имели 1479 (31,3%) участников исследования. У 448 (9,5%) из них наблюдались расстройства питания и нарушения со стороны обмена веществ, у 170 (3,6%) – болезни системы кровообращения (наряду с АГ), у 301 (6,4%) – болезни желудочно-кишечного тракта (ЖКТ), у 143 (3,0%) – болезни органов дыхания. Доля пациентов с болезнями нервной системы составила 6,1%, костно-мышечной и соединительной ткани – 3,2%.
Сопутствующая терапия
В качестве сопутствующей терапии хотя бы один препарат принимали 4220 (89,4%) участников КИ. Из них антигипертензивные препараты получали 103 пациента (2,2%), антитромботические – 285 (6,0%), бета-адреноблокаторы – 982 (20,8%), блокаторы кальциевых каналов – 531 (11,3%), диуретики – 562 (11,9%), гиполипидемические средства – 183 (3,9%), средства, действующие на ренин-ангиотензиновую систему, – 3647 (77,3%), препараты для лечения болезней сердца – 67 (1,4%). Более 500 пациентов (n=515) не применяли ни одного препарата из группы «препараты для лечения заболеваний сердечно-сосудистой системы» (АТХ С). Отдельные участники исследования использовали витамины, минеральные добавки, препараты для лечения заболеваний ЖКТ и СД.
Первичный критерий эффективности терапии
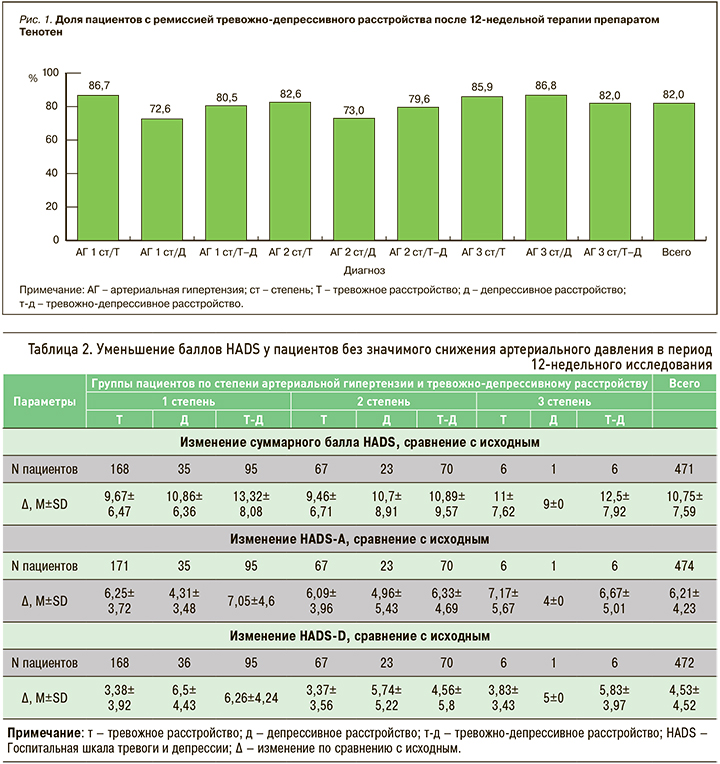
После 12 нед приема препарата Тенотен симптомы тревожно-депрессивного расстройства отсутствовали у 82% пациентов (из 4719). Доля пациентов в ремиссии после лечения оказалась зависима только от изначального характера эмоционального расстройства (p=0,009), но не от основного диагноза АГ (р=0,053). Наибольший процент пациентов с отсутствием симптомов наблюдался в группе участников с тревожным расстройством (82,6; 85,9; 86,7%) и пациентов с депрессией и АГ 3 степени (86,8%) (рис. 1).
Дополнительные критерии эффективности
Исходная величина среднего суммарного балла по шкале HADS находилась в зависимости от степени АГ: у пациентов с более высоким систолическим АД (САД) отмечен больший балл HADS. Участники с тревожным расстройством имели самые низкие баллы HADS среди всех пациентов с эмоциональными нарушениями.
Через 12 нед терапии препаратом Тенотен у всех проанализированных пациентов (n=4694) суммарный балл HADS уменьшился на 62,2% (с 20,22±6,38 до 7,26±5,6 баллов; p <0,0001). Наибольшее снижение среднего суммарного балла отмечалось у пациентов с тревожно-депрессивным (на 17,34±8,65 баллов) и депрессивным (на 16,19±7,18 баллов) расстройствами и АГ 3 степени. В соответствии с результатами дисперсионного анализа, степень АГ и характер эмоционального нарушения значимо повлияли на динамику суммарного балла HADS (фактор «степень АГ» – p <0,0001; фактор «тревожно-депрессивное расстройство» – р <0,0001; фактор «АГ × фактор тревожно-депрессивное расстройство» – р=0,04) (рис. 2а). Результаты ковариационного анализа продемонстрировали различия в зависимости изменения балла HADS от величины САД между группами пациентов с тревожными, депрессивными и смешанными расстройствами. Тем не менее было установлено, что даже в отсутствие снижения АД (изменение САД и диастолического АД ≤5 мм рт.ст.) после 12 нед приема Тенотена у более чем 470 пациентов (≈10%) происходит снижение выраженности симптомов эмоциональных нарушений по шкале HADS (табл. 2).
Изменение суммарного балла HADS-А и HADS-D во всех подгруппах, ранжированных по степени АГ, оказалось статистически значимым по сравнению с исходным (HADS-A и HADS-D: р <0,0001 для каждой из подгрупп). Средний суммарный балл HADS-A у всех участников (n=4705) уменьшился на 63,5% (с 11,28±3,73 до 3,83±3,02 баллов; рис. 2б). Изменение среднего балла HADS-D составило 56,5% (-5,49±4,27 баллов) у всех пациентов (n=4696; рис. 2в).
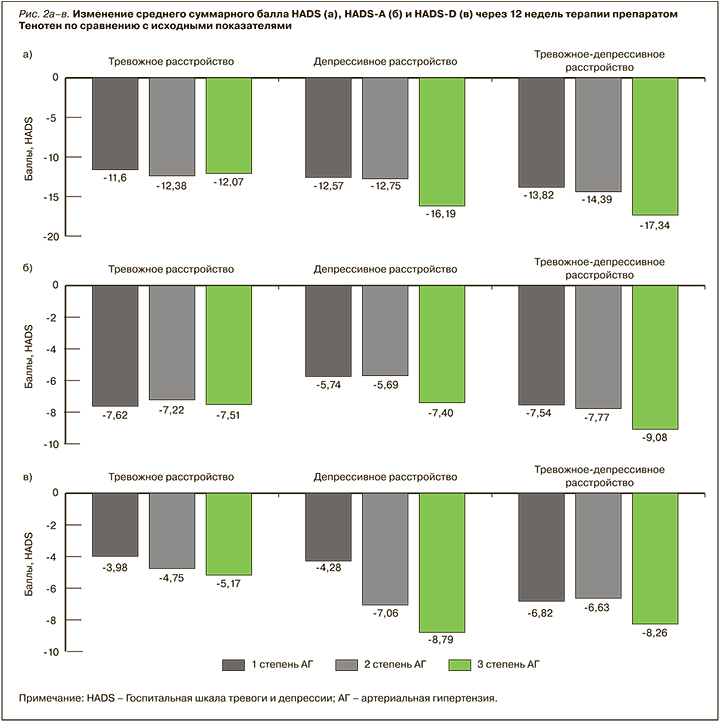
Динамика суммарного балла подшкалы тревоги была выраженной в группах участников КИ со смешанным, тревожно-депрессивным, расстройством и АГ 2 (-7,77±4,23) и 3 (-9,08±4,71) степеней, а также у тревожных пациентов с АГ 1 степени (-7,62±4,47).
Наиболее выраженное снижение суммы баллов HADS-D было характерно для пациентов с тревожно-депрессивным (-8,26±4,57) и депрессивным (-8,79±4,11) расстройствами и АГ 3 степени.
После курсового применения препарата Тенотен у части пациентов (n=515), не принимавших препараты для лечения сердечно-сосудистой системы в качестве сопутствующей терапии, отмечено значимое снижение выраженности тревоги (на 7,67±4,79 баллов по подшкале HADS-A) и депрессии (на 6,01±4,62 баллов по HADS-D) (р <0,0001 для каждой из подгрупп, ранжированной по степени АГ).
Результаты дисперсионного анализа показали, что на изменение суммарного балла HADS-A и HADS-D значимо влияют как факторы «степень АГ» (р <0,01) и «тревожно-депрессивное расстройство» (р <0,0001), так и их взаимодействие (р <0,01). Динамика балла HADS-D у пациентов, не получавших препараты для лечения сердечно-сосудистой системы в качестве сопутствующей терапии, зависит только от характера эмоциональных нарушений (фактор «тревожно-депрессивное расстройство» – р=0,04).
Значимое изменение балла CGI-S наблюдалось у участников с АГ 1–3 степеней через 12 нед терапии Тенотеном (р <0,0001 для каждой из подгрупп). Среднее снижение балла CGI-S составило 1,66±1,23 для всех проанализированных пациентов (n=4642). Выраженная динамика клинического впечатления наблюдалась при наличии АГ 3 степени у участников с любым типом эмоционального нарушения. Как степень АГ, так и характер тревожно-депрессивного расстройства значимо влияли на изменение балла CGI-S (фактор «степень АГ» – p=0,0001; фактор «тревожно-депрессивное расстройство» – р=0,0017).
Изменение САД, диастолического АД (ДАД) и ЧСС во всех подгруппах оказалось статистически значимым (р <0,0001). Через 12 нед приема препарата Тенотен среднее снижение САД и ДАД (для 4541 пациента) составило 17,28±12,82 (на 11,2%) и 9,5±8,81 мм рт.ст. (на 10%) соответственно. Значимое снижение этих показателей отмечено у 10% пациентов с АГ (n=490), не принимавших препаратов для лечения сердечно-сосудистых заболеваний (р <0,001 для каждой из подгрупп, ранжированных по степени АГ и характеру эмоционального нарушения) (табл. 3).
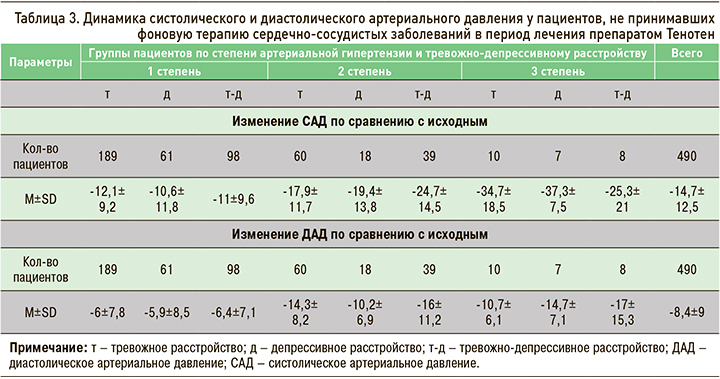
Уменьшение ЧСС на 6,9±8,98 уд./мин (на 8%) наблюдалось у 4614 участников. Значимое снижение ЧСС (на 7,37±9,5 уд./мин в среднем) было характерно для тревожных и депрессивных пациентов с АГ 1–2 степени (n=479), не получавших терапию ССЗ (р <0,05),
Согласно результатам дисперсионного анализа, на изменение САД и ДАД значимо повлияли как степень АГ (САД и ДАД – р <0,0001), так и характер эмоционального расстройства (САД – р=0,03; ДАД – р=0,005) и их взаимодействие (САД – р=0,04; ДАД – р=0,0002). На изменение ЧСС оказала влияние только степень АГ (p <0,001) и взаимодействие факторов (p=0,03).
Индекс коморбидности Чарлсона не оказал статистически значимого влияния на изменение АД и на изменение балла HADS, HADS-A и HADS-D. Индекс коморбидности, равный 0, имели 48,75% всех проанализированных пациентов (n=4685). ИКЧ 7–15 был характерен менее чем для 1% участников исследования.
Безопасность
Всего у 4719 пациентов зарегистрировано 34 нежелательных явления, из них 33 были легкой степени тяжести. По мнению исследователей, 15 неблагоприятных реакций (44,1%) были связаны с приемом Тенотена, 18 (52,9%) не имели связи с терапией. Для 1 пациента степень тяжести нежелательных явлений и связь с терапией не была указана. У 0,2% пациентов побочные эффекты относились к группе болезней нервной систем (6 пациентов указали на головные боли, 7 – на головокружение, 2 – на сонливость) и заболеваниям пищеварительной системы (10 пациентов отметили эпизоды тошноты, 1 – диареи), у 0,1% пациентов отмечались нежелательные явления из группы дерматологических заболеваний (4 пациента сообщили о реакции в виде кожных высыпаний или зуда).
ОБСУЖДЕНИЕ
В результате Всероссийской наблюдательной программы ТЕАТР была показана эффективность и безопасность применения анксиолитического препарата Тенотен с антидепрессивными свойствами у большого числа пациентов с невротическими расстройствами, нарушениями адаптации и с АГ 1–3 степени в реальной клинической практике. Доля пациентов в ремиссии тревожно-депрессивного расстройства превысила 80% по окончанию 12-недельного курса лечения. Добавление Тенотена к базовой терапии АГ и других сопутствующих соматических заболеваний приводило к значимому снижению выраженности симптомов тревоги и депрессии у всех проанализированных пациентов к окончанию КИ, согласно оценке по шкале HADS. Наибольшее уменьшение тревожных и депрессивных симптомов было отмечено у участников исследования с АГ 3 степени. Значимая редукция тревожно-депрессивных расстройств на фоне приема препарата Тенотен наблюдалась в том числе и у пациентов с эмоциональными нарушениями и АГ, не принимавших препараты для лечения ССЗ в течение исследования.
Снижение выраженности тревоги и депрессии оказало положительное влияние на нормализацию АД у пациентов с АГ 1–3 степени: в среднем установлено снижение показателей САД, ДАД и ЧСС. Наибольшая положительная динамика жизненно важных показателей наблюдалась у пациентов с более высокой степенью АГ.
Нормализация САД и ДАД на фоне приема препарата Тенотен также была характерна для более чем 500 участников исследования, не использовавших препараты для лечения ССЗ в течение исследования. Возможность препарата Тенотен улучшать эмоциональное состояние пациентов с АГ даже в отсутствии гипотензивной терапии способствует усилению контроля и уменьшению степени этого заболевания.
Участники, которые не отметили снижения АД в ходе 12-недельного исследования, сообщали об улучшении эмоционального состояния и демонстрировали уменьшение суммарного балла HADS, HADS-A и HADS-D, что свидетельствует о позитивном влиянии Тенотена на выраженность тревожно-депрессивных нарушений, которое не зависит от эффективности базовой терапии АГ и величины снижения АД.
Тяжесть тревожно-депрессивных расстройств до лечения не соответствовала степени коморбидности. Согласно оценке влияния ИКЧ на результаты HADS и показатели АД и ЧСС, эффективность препарата Тенотен была одинаковой у всех пациентов и не зависела от наличия сопутствующих заболеваний.
Клиническое впечатление врачей-исследователей о состоянии участников КИ значимо улучшилось через 12 нед терапии Тенотеном.
Анксиолитическое действие препарата Тенотен, наблюдаемое в программе ТЕАТР, соответствует результатам проведенных ранее сравнительных и рандомизированных КИ у больных ССЗ [11, 16]. У большинства пациентов в исследованиях отмечалось снижение АД при добавлении Тенотена к стандартной терапии АГ.
Данные о снижении АД на фоне улучшения эмоционального состояния после медикаментозного лечения анксиолитиками согласуются с результатами исследований Mendelson N. et al., Grossman E. et al. и Yilmaz S. et al. [18–20]. Тем не менее во многих работах подчеркивается высокая вероятность развития привыкания, миорелаксации и межлекарственного взаимодействия у пациентов с ССЗ при приеме традиционных анксиолитиков в сочетании с базовой терапией [18, 21].
Как показывают результаты рандомизированного контролируемого исследования и метаанализа, использование трициклических антидепрессантов и ингибиторов обратного захвата серотонина и норадреналина с целью улучшения эмоционального состояния пациентов с АГ сопряжено с увеличением показателей АД, что ограничивает их применение у пациентов с повышенным АД [22, 23]. Применение селективных ингибиторов обратного захвата серотонина возможно только у пациентов, не получающих антитромботическую терапию [24].
В отличие от указанных препаратов, Тенотен, согласно данным программы ТЕАТР, способствует снижению повышенных САД и ДАД и достижению нормальных значений АД в сочетании с базовой антигипертензивной терапией. Высокая безопасность Тенотена, отсутствие привыкания и взаимодействия с другими лекарственными средствами, продемонстрированные в программе ТЕАТР и предыдущих клинических и экспериментальных исследованиях, позволяют использовать препарат при эмоциональных нарушениях и соматической патологии с минимальной вероятностью развития нежелательных реакций. По эффективности в лечении эмоциональных расстройств Тенотен не уступает некоторым анксиолитическим препаратам: клоназепаму, феназепаму (при 7-дневной длительности терапии) и тофизопаму [16].
Отсутствие полных данных и связанное с этим исключение из анализа результатов оценки многих пациентов являются ограничениями исследования. К преимуществам наблюдательной программы ТЕАТР можно отнести большое количество участников из разных регионов России и многоцентрового дизайн-исследования, которые позволили получить дополнительные данные по безопасности и эффективности препарата в реальной клинической практике.
Оптимальное соотношение безопасности и эффективности позволяет предположить возможность использования Тенотена в качестве препарата выбора для лечения тревожно-депрессивных реакций у пациентов с АГ.
ЗАКЛЮЧЕНИЕ
1. Доля пациентов в ремиссии тревожно-депрессивного расстройства превысила 80% по окончании 12-недельного курса лечения с применением препарата Тенотен.
2. Через 12 нед терапии Тенотеном у всех проанализированных пациентов средний суммарный балл HADS уменьшился на 62,2%.
3. Среднее снижение САД и ДАД составило более 10% от исходного на фоне добавления Тенотена к базовой терапии.
4. Значимое снижение выраженности симптомов эмоционального расстройства отмечено у 10% пациентов с АГ, получавших Тенотен в отсутствии базовой терапии ССЗ.
5. У 10% пациентов с АГ и тревожно-депрессивным расстройством, принимавших Тенотен, АД нормализовалось даже в отсутствие гипотензивной терапии через 12 нед лечения.



