ВВЕДЕНИЕ
Вакцинопрофилактика по праву считается одним из самых важных и эффективных достижений медицины. Иммунизация, по разным оценкам, ежегодно спасает от 3 до 6 млн жизней во всем мире [1]. Проведение массовых прививок по-прежнему является одним из экономически оправданных инструментов профилактики вакциноуправляемых инфекционных заболеваний [2, 3].
Программы по первичной профилактике инфекционных заболеваний, начинающиеся в детском возрасте и продолжающиеся на протяжении всей жизни человека, относят к приоритетным направлениям развития современной системы здравоохранения. С одной стороны, иммунизация позволяет управлять заболеваемостью и смертностью населения от инфекционных болезней, а с другой ‒ служит мощным инструментом в снижении смертности от ведущих хронических неинфекционных заболеваний (ХНИЗ) [2, 4].
Иммунизация населения на протяжении всей жизни человека рассматривается как ключ к решению глобальных проблем здравоохранения, которые сопровождают демографические изменения [5]. Иммунопрофилактика позволила достичь ликвидации оспы и полиомиелита во многих странах мира, в том числе в России, существенно снизить смертность и заболеваемость населения инфекционными болезнями, а также обеспечить эффективную защиту населения в очагах инфекций, включая особо опасные болезни, и ограничить распространение ряда бактериальных и вирусных заболеваний [6, 7].
Глобальный охват вакцинацией детей – яркий пример бережного отношения к сохранению устойчивого демографического потенциала населения планеты [8]. Однако в отличие от детей, применительно к которым отработаны организационные и методические приемы и принципы иммунизации, в вопросах необходимости и порядка проведения вакцинации взрослого населения существуют определенные противоречия [9].
ЗАДАЧИ И ПРОБЛЕМЫ ВАКЦИНАЦИИ ВЗРОСЛОГО НАСЕЛЕНИЯ
Национальные календари вакцинации традиционно были ориентированы на детей, однако в связи с увеличением продолжительности жизни и доли населения, относящейся к старшей возрастной категории, остро встал вопрос о разработке национальных программ вакцинации взрослых [10]. По прогнозам Всемирной организации здравоохранения (ВОЗ), в период с 2000 по 2050 г. доля лиц в возрасте 60 лет и старше составит более трети всего населения планеты [11, 12].
Такие инфекционные заболевания, как грипп, пневмококковая инфекция, коклюш, корь, дифтерия, столбняк выявляются у пациентов всех возрастных групп. В результате традиционно эффективной профилактики инфекционных заболеваний у детей именно взрослое население оказалось в зоне риска возникновения болезней, предупреждаемых с помощью вакцин. Однако охват взрослого населения иммунизацией с применением рекомендованных для этой возрастной категории вакцин остается ниже целевых показателей, обозначенных в рекомендованных документах [13, 14].
Расширение преимуществ вакцинации против инфекционных заболеваний с детства на протяжении всей жизни становится все более насущным приоритетом в силу возможности управления иммунным ответом у лиц старшей возрастной категории для формирования эффективного профилактического стандарта оказания медицинской помощи [15].
В современном мире программы иммунизации взрослого населения приносят значительную выгоду на индивидуальном, общественном и социально-экономическом уровнях; они уже не только нацелены на предотвращение преждевременной смерти, но служат задачам улучшения общего состояния здоровья и благополучия на протяжении всей жизни. Как для общества, так и отдельных людей важно не только увеличение продолжительности жизни, но и количество лет, проведенных в хорошем состоянии здоровья [16, 17].
Взрослые нуждаются в вакцинации по целому ряду причин. Во-первых, иммунизация – безопасный и наиболее целесообразный способ выработки в организме человека иммунного ответа от управляемых с ее помощью патогенов. Другой весомый аргумент в пользу вакцинации – возможность защитить окружающих, которым ряд прививок может быть противопоказан, например, новорожденных, пациентов с тяжелой соматической патологией в определенные периоды ее течения, лиц с видами аллергии, зависимыми от компонентов, входящих в состав вакцин и др. [18].
Пожилые люди и лица, страдающие ХНИЗ, подвергаются более высокому риску заражения инфекционными болезнями и могут иметь серьезные осложнения в результате инфицирования. Вакцинация достоверно снижает риск развития и тяжелого течения инфекционной патологии, уменьшает вероятность развития осложнений заболеваний и летального исхода от них [19, 20].
Бустерные дозы вакцин могут потребоваться в том случае, если гарантией иммунитета от того или иного заболевания является высокий уровень нейтрализующих антител, который не может быть обеспечен механизмами иммунологической памяти (например, при столбняке) или не может быть достигнут своевременно для предотвращения заболевания, поскольку его инкубационный период короче, чем время на повышение иммунитета (например, менингококк). К важным направлениям в программах иммунизации взрослого населения относится формирование календаря прививок для выбранных целевых групп, определенных по возрасту, существующим хроническим заболеваниям, иммунодефициту или таким условиям, как беременность, профессиональная деятельность (например, работа в медицинских учреждениях) или поездки за границу [21, 22].
Ряд инфекций, например грипп, пневмококковая инфекция, имеют доказанную взаимосвязь с развитием или прогнозированием неблагоприятного исхода ХНИЗ, увеличением числа госпитализаций и риском смерти от других причин. Иммунизация может значительно снизить эти риски. Вакцинация взрослых пациентов с сердечно-сосудистой патологией, бронхолегочными заболеваниями улучшает течение ХНИЗ, позволяет снизить частоту обострений коморбидной патологии и смертность от сопутствующих заболеваний [23–25].
Исследования влияния вакцинации против гриппа у пожилых людей демонстрируют снижение частоты инсульта и острого инфаркта миокарда примерно на 20%, а исследования у пожилых пациентов из группы риска, по крайней мере с одной сопутствующей патологией, показывают четкий эффект дозы в течение нескольких сезонов гриппа [26, 27].
Взрослым может потребоваться вакцинация от управляемых инфекций, если они не были привиты полностью или частично в детстве или в связи с появлением новых важных вакцин в промежутке между детским и взрослым возрастом. Особый интерес вызывает возможность с помощью вакцинации управлять риском возникновения онкологических заболеваний. Согласно данным Международного агентства по изучению рака (International Аgency for Research on Cancer), выделяют 10 инфекционных агентов, для которых доказана роль в возникновении рака: это вирусы гепатита В и С, H. pylori, Opisthorchis viverrini, Clonorchis sinensis, Shistosoma haematabium, вирус иммунодефицита человека-1 (ВИЧ-1), вирус Эпштейна–Барр, герпесвирус, ассоциированный с саркомой Капоши, и вирус папилломы человека (ВПЧ). Прогнозные исследования утверждают, что проведение широкомасштабной вакцинации от ВПЧ приведет к реальному снижению заболеваемости и смертности, ассоциированной с этим вирусом, прежде всего от рака шейки матки [28]. В настоящее время вакцинация от ВПЧ входит в национальные календари прививок более чем 110 стран. В России обязательная вакцинация от ВПЧ установлена в ряде субъектов – Москве, Московской и Свердловской областях и др.
АДМИНИСТРАТИВНОЕ РЕГУЛИРОВАНИЕ ИММУНОВАКЦИНАЦИИ
Осуществление программ вакцинации на национальном уровне – ведущая стратегия в борьбе с болезнями, предупреждаемыми с помощью прививок. Успешная реализация иммунопрофилактики инфекционных болезней и распространение преимуществ вакцинации на все возрастные группы позволят снизить заболеваемость, смертность и расходы на здравоохранение. Приоритетным аспектом реализации программы ВОЗ по иммунизации до 2030 г. (Immunization Agenda 2030) является охват иммунизацией всех этапов жизни человека одновременно с другими медицинскими мероприятиями [29]. По мнению экспертов ВОЗ, формирование и укрепление в обществе антивакцинального лобби является одной из 10 глобальных угроз здравоохранению [30].
Документом, определяющим государственную политику по дальнейшему развитию иммунопрофилактики в России, является распоряжение Правительства РФ № 2390-р «Об утверждении Стратегии развития иммунопрофилактики инфекционных болезней на период до 2035 г.», утвержденное 18 сентября 2020 г. [31].
Одно из главных направлений программы реализации Стратегии ориентировано на развитие национального календаря прививок, куда планируется включить максимально полный перечень инфекционных заболеваний, контролируемых вакцинами. Национальный календарь прививок пополнят вакцины для профилактики ротавирусной инфекции, ветряной оспы, менингококковой инфекции, ВПЧ. Стратегия предусматривает разработку программ вакцинации для отдельных категорий граждан, в том числе для пациентов с ХНИЗ, беременных женщин, лиц старших возрастных групп, лиц призывного возраста, определенных профессиональных групп. Совершенствование программ вакцинации приоритетных групп населения позволит обеспечить оптимальный контроль заболеваемости, будет способствовать повышению качества и продолжительности жизни.
Приказ Минздрава России от 21.03.2014 № 125н «Об утверждении национального календаря профилактических прививок и календаря профилактических прививок по эпидемическим показаниям» (с изменениями и дополнениями) служит основой формирования плана профилактических прививок для взрослого населения. Национальный календарь прививок постоянно совершенствуется: добавляются вакцинации против новых инфекций, внедряются новые схемы применения, регистрируются современные препараты [32].
В ЗОНЕ ОСОБОГО ВНИМАНИЯ: ГРИПП
Один из примеров совершенствования вакцинации от управляемых вирусных инфекций – вакцинация от сезонного и эпидемического гриппа [33]. Прививки против гриппа эффективно предупреждают госпитализации, связанные с этим заболеванием, у людей пожилого возраста [34, 35]. Расчетное число смертей, предотвращенных с помощью ежегодной программы вакцинации против гриппа, является значительным, особенно среди пожилых людей [34]. По данным ВОЗ, смертность от респираторных осложнений сезонного гриппа составляет от 290 до 650 тыс. случаев в год [36]. В связи с этим ВОЗ рекомендует обеспечить ежегодную иммунизацию против сезонного гриппа лицам из групп высокого риска: беременным женщинам, детям в возрасте от 6 мес до 5 лет, пожилым людям (старше 65 лет), пациентам с хроническими заболеваниями, работникам здравоохранения [37].
Приказом Минздрава России от 14.09.2020 № 967н в национальный календарь профилактических прививок внесены изменения, расширяющие перечень категорий граждан, подлежащих вакцинации против гриппа. В число вакцинируемых от гриппа дополнительно включены работники сферы предоставления услуг; лица, работающие вахтовым методом; сотрудники правоохранительных и государственных контрольных органов в пунктах пропуска через государственную границу, работники организаций социального обслуживания и многофункциональных центров, государственные гражданские и муниципальные служащие [38].
Стратегия иммунопрофилактики инфекционных болезней на период до 2035 г. устанавливает целевые ориентиры вакцинации от гриппа в общей группе населения до 60%. В ежегодном Постановлении Главного государственного санитарного врача РФ в эпидемическом сезоне 2021–2022 гг. для пациентов, относящихся к группе риска, планируется обеспечить уровень противогриппозной вакцинации не менее 75%. Эти цифры согласуются с целевыми ориентирами по вакцинации от гриппа, установленными ВОЗ [31].
Прививки против гриппа снижают риск заражения гриппом, связанных с гриппом заболеваний и смерти у пожилых людей, пациентов с сопутствующей бронхолегочной патологией, эффективно предотвращают число госпитализаций, ассоциированных с обострением хронических болезней органов дыхания [33].
Мутация вирусов гриппа происходит постоянно, каждый год циркулируют разные штаммы. Выделяют 4 типа вирусов сезонного гриппа – A, B, C и D; среди них наибольшее значение имеют типы А и В [37]. Вакцина против гриппа наиболее эффективна, когда циркулирующие вирусы хорошо сочетаются с вирусами, содержащимися в вакцинах. В связи с высокой изменчивостью возбудителей гриппа состав сезонных вакцин каждый год обновляется, чтобы обеспечить наибольшую защиту от вирусов гриппа, которые, как показывают исследования, могут быть наиболее распространены в предстоящем сезоне. При проведении вакцинации населения используются прививки, содержащие актуальные для России антигены, которые позволяют обеспечить максимальную эффективность иммунизации [39].
Согласно рекомендациям ВОЗ по составу противогриппозных вакцин на предстоящий сезон по гриппу 2021–2022 гг. для Северного полушария, в состав трехвалентной противогриппозной вакцины (на основе куриных эмбрионов) включены штаммы вирусов гриппа A/Victoria/2570/2019 (H1N1)pdm09, A/Cambodia/e0826360/2020 (H3N2), B/Washington/02/2019. Для четырехвалентной вакцины, кроме указанных штаммов, введен штамм B/ Phuket/3073/201 [40].
В ЗОНЕ ОСОБОГО ВНИМАНИЯ: НОВАЯ КОРОНАВИРУСНАЯ ИНФЕКЦИЯ
В декабре 2019 г. в Ухане (провинция Хубэй, Китай) произошла вспышка новой коронавирусной инфекции, возбудителем которой стал вирус SARS-CoV-2, стремительно распространившейся по миру. 11 марта 2020 г. ВОЗ объявила пандемию COVID-19, охватившую к настоящему времени практически все страны и континенты, включая Антарктиду. На 11.10.2021 зарегистрировано более 237 млн заболевших, документировано 4 851 749 случаев смерти от COVID-19, что в среднем составляет 2,04% от общей заболеваемости [41].
Прививка против новой коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, внесена в календарь профилактических прививок по эпидемическим показаниям Приказом Минздрава Росси от 09.12.2020 № 1307н. В документе определены уровни приоритета при вакцинации от новой коронавирусной инфекции [42].
Приказом Минздрава России от 03.02.2021 № 47н «О внесении изменения в календарь профилактических прививок по эпидемическим показаниям, утвержденный приказом Министерства здравоохранения Российской Федерации от 21.03.2014 № 125н» пересмотрены уровни приоритета при вакцинации против коронавирусной инфекции, вызываемой вирусом SARS-CoV-2. К приоритету первого уровня отнесены лица в возрасте 60 лет и старше, взрослые, работающие по отдельным профессиям и должностям (работники медицинских, образовательных организаций, организаций социального обслуживания и многофункциональных центров), лица, проживающие в организациях социального обслуживания, пациенты с хроническими заболеваниями, в том числе с бронхолегочными, сердечно-сосудистыми патологиями, сахарным диабетом и ожирением, граждане, проживающие в городах с численностью населения 1 млн и более [43].
ЗНАЧЕНИЕ ВАКЦИНАЦИИ ПРОТИВ ГРИППА В УСЛОВИЯХ ПАНДЕМИИ COVID-19
Иммунизация против гриппа сохраняет свою актуальность в условиях пандемии новой коронавирусной инфекции в связи с тем, что одновременное инфицирование вирусом гриппа и SARS-CoV-2 способствует развитию более тяжелых форм заболевания и значительно повышает риск летального исхода [44].
В последнее время привлекает большое внимание возможное взаимодействие между вакцинами и инфекциями, не относящимися к целевому заболеванию. Несколько недавних исследований продемонстрировали потенциальное положительное влияние вакцинации против гриппа на восприимчивость к COVID-19 [45].
Немалый интерес представляют исследования о перекрестных защитных механизмах вакцинации против гетерологичных инфекций, при которых клетки иммунологической памяти способны быстро и эффективно уничтожать даже неродственные патогены. Гетерологичные иммунные ответы наиболее типичны для вирусных и других внутриклеточных инфекций, где ведущую роль в защите организма играют Т-клетки. В качестве основного механизма такого иммунного ответа рассматривают долгосрочное усиление врожденного иммунитета, который также называют «тренированный иммунитет». Иммунологическая память не является исключительной особенностью адаптивного иммунного ответа, функции иммунной памяти также могут быть обнаружены в клетках врожденного иммунитета [46].
Механизмы врожденного иммунного ответа могут запускаться как естественными инфекциями, так и вакцинами. Эпидемиологические исследования подтверждают, что, помимо эффектов, специфичных для конкретной патологии, вакцины против инфекционных заболеваний оказывают неспецифическое влияние на способность иммунной системы бороться с другими патогенами. Например, в рандомизированных исследованиях применение противотуберкулезных и противокоревых вакцин ассоциируется со значительным снижением общей детской смертности, что нельзя полностью объяснить профилактикой целевого заболевания [47]. Исследователи полагают, что неспецифические эффекты вакцин связаны с перекрестной реактивностью адаптивной иммунной системы с неродственными патогенами. Концепция «тренированного иммунитета» дает новое представление об иммунной системе и о том, как вакцины могут модулировать ее ответ, чтобы повлиять на общую сопротивляемость болезни [48].
Исследования продемонстрировали, что иммунизация от гриппа может обеспечить некоторую защиту от вируса SARS-CoV-2 за счет усиления именно врожденной иммунной системы, не нацеленной на конкретный патоген. Вакцинация против гриппа связана с более низкой смертностью среди пациентов с COVID-19 и потребностью в интенсивной госпитальной помощи у вакцинированных от гриппа пациентов [49].
Результаты популяционного исследования в Италии в 2019 г. с охватом лиц старше 65 лет показали более низкие показатели заболеваемости новой коронавирусной инфекцией среди привитых от гриппа лиц по сравнению с лицами, не получивших вакцину. Ученые отметили, что чем выше уровень охвата вакцинацией против гриппа среди пожилого населения, тем ниже распространение и легче течение COVID-19 [50].
Сведения о положительном влиянии вакцинации против гриппа на распространенность COVID-19 предполагают ее эффективное использование для защиты от обеих инфекций.
Центры по контролю и профилактике заболеваний США (CDC) рекомендуют совместить прививку от гриппа с получением одного из двух компонентов вакцины против COVID-19 либо ревакцинацией. По информации CDC, прививки от COVID-19 теперь можно делать без учета сроков введения других вакцин; рекомендовано одновременное введение вакцины COVID-19 и других вакцин в тот же день, а также совместное их введение в течение 14 дней [51].
Прививочная кампания против гриппа в 2021 г. в России проходит одновременно с вакцинацией от COVID-19. Роспотребнадзор рекомендует соблюдать интервал не менее 1 мес между прививками против этих заболеваний. Допускается совмещение антигриппозной вакцины с иммунизацией против пневмококковой и ряда других инфекций [52].
В ЗОНЕ ОСОБОГО ВНИМАНИЯ: ПНЕВМОКОККОВАЯ ИНФЕКЦИЯ
Пневмококковая инфекция вызывает больше смертей, чем все инфекции другой этиологии вместе взятые. Streptococcus pneumoniae – наиболее распространенная причина бактериальных инфекций, приводящих к значительной заболеваемости и смертности во всем мире. По данным ВОЗ, в 2017 г. смерть от инфекций нижних дыхательных путей в 203 104 случаях среди взрослых в возрасте 50–69 лет и 456 096 случаях в возрастной группе старше 70 лет была связана именно с пневмококком [53]. На основе клинических проявлений выделяют следующие формы пневмококковой инфекции: здоровое носительство, локальные (неинвазивные) формы, инвазивные формы заболевания.
Наиболее высокие уровни заболеваемости и смертности от тяжелых форм пневмококковой инфекции наблюдаются в группах детского возраста и среди пожилых пациентов [54]. Проблема пневмококковой инфекции усугубляется не только пожилым возрастом, но и хроническими заболеваниями легких, коморбидной патологией, иммуносупрессией, сочетанной вирусной инфекцией. К тяжелым проявлениям инвазивной пневмококковой инфекции относят пневмонию с бактериемией, менингит, септицемию. Инфекции среднего уха (острый средний отит), синуситы являются менее тяжелыми, но чаще диагностируемыми патологиями, связанным с пневмококком [55].
Наиболее значимым клиническим проявлением пневмококковой инфекции среди взрослых выступает пневмококковая пневмония. Бактериемия встречается у 25–30% пациентов с этим заболеванием [56]. Общий показатель смертности при пневмококковой бактериемии сохраняется высоким и достигает 15–20% среди взрослых и 30–40% среди пациентов пожилого возраста, несмотря на адекватное применение современных антибактериальных препаратов и интенсивное лечение [57].
Носительство пневмококка протекает чаще всего бессимптомно, возбудитель колонизирует слизистые оболочки полости рта и верхних дыхательных путей. В зависимости от популяции и условий примерно 5–10% взрослых и 20–60% детей школьного возраста могут быть носителями этого бактериального агента. Из ротоглотки и носоглотки могут одновременно выделять до четырех серотипов пневмококка, что с учетом роста резистентности к антибиотикам делает проблему особенно актуальной [58].
Существует около 100 известных серотипов S. pneumoniae, но большая часть инвазивных заболеваний вызывается 23 серотипами. Серотипы 1, 5, 6А, 6В, 14, 19F и 23F обычно вызывают инвазивные пневмококковые инфекции среди детей в возрасте до 5 лет. К малоинвазивным, но вызывающим тяжелые инфекции, относятся серотипы 3, 6A, 6B, 9N, 19A, 19F, 23F; к высокоинвазивным, но вызывающим легкие инфекции, – серотипы 1, 4, 5, 7F, 8. Некоторые серотипы, такие как 6B, 9V, 14, 19A, 19F и 23F, по сообщениям исследователей, более, чем другие, ассоциируются с резистентностью к противомикробным средствам [59].
Распространенность серотипов, вызывающих заболевание, варьирует в зависимости от времени и возраста, клинических проявлений заболевания, тяжести течения, географического региона и наличия устойчивости к антибиотикам [60].
Зарегистрированы сезонные и климатические тенденции в отношении инвазивной инфекции и приобретенной пневмонии, что совпадает с сезонной циркуляцией вируса гриппа, который предрасполагает к возникновению пневмококковой инфекции. Имеются сведения о том, что во время пандемий гриппа внебольничная пневмония становится одним из самых частых его осложнений [61].
В 2007 г. ВОЗ опубликовала рекомендацию включить пневмококковую конъюгированную вакцину (ПКВ) в календарь плановой иммунизации детей младшего возраста [62]. По состоянию на март 2020 г. 146 из 194 стран ‒ членов ВОЗ ввели ПКВ в программу иммунизации на национальном уровне, что позволило значительно снизить заболеваемость тяжелой (инвазивной) пневмококковой инфекцией и пневмонией. Однако даже в странах с высоким доходом охват вакцинацией от пневмококка пожилых людей зачастую остается низким [63].
В России вакцинация против пневмококковой инфекции с 2014 г. включена в обязательную часть национального календаря профилактических прививок. Все дети с двух месяцев жизни подлежат иммунизации с использованием ПКВ13 по схеме «2+1»: первая вакцинация в 2 мес, вторая – в 4,5 мес, ревакцинация против пневмококковой инфекции – в 15 мес. Национальным календарем профилактических прививок по эпидемическим показаниям (Приложение 2 к приказу Минздрава России от 21.03.2014 № 125н с изменениями и дополнениями) вакцинация против пневмококковой инфекции также рекомендована детям в возрасте от 2 до 5 лет, взрослым из групп риска (лица, подлежащие призыву на военную службу, лица старше 60 лет, страдающие хроническими заболеваниями легких, лица старше трудоспособного возраста, проживающие в организациях социального обслуживания) [64].
В качестве обязательного мероприятия вакцинация против гриппа и пневмококковой инфекции пациентов из групп риска включается в современные клинические рекомендации и стандарты оказания медицинской помощи по терапии, кардиологии, неврологии, онкологии, онкогематологии, нефрологии, пульмонологии, аллергологии, иммунологии, эндокринологии и трансплантологии [65]. Как пример можно привести рекомендации по вакцинации против гриппа и пневмококковой инфекции, которые включены в разделы реабилитации пациентов, подлежащих диспансерному наблюдению у терапевта, при хронической сердечной недостаточности [66], язвенном колите [67], болезни Крона [68], старческой астении [69], хронической обструктивной болезни легких [70] и др.
Расширение групп иммунизации против пневмококковой инфекции необходимо проводить за счет выявления лиц любого возраста, входящих в группы риска, относящихся к категориям иммунокомпетентных и иммунокомпрометированных лиц. Категория иммунокомпетентных лиц включает пациентов с сахарным диабетом, инсультом в анамнезе, сердечно-сосудистыми заболеваниями, хроническими заболеваниями легких, хроническими заболеваниями печени, ожирением, табачной зависимостью, лиц, работающих в условиях производственных факторов риска, находящихся в специальных условиях пребывания, лиц с поведенческими факторами риска, медицинских работников. В свою очередь, к иммунокомпрометированным лицам принадлежат больные с иммунодефицитными состояниями, включая инфицированных ВИЧ и микобактериями туберкулеза, пациенты после спленэктомии, пациенты, получающие иммуносупрессивную терапию, страдающие нефротическим синдромом, хронической почечной недостаточностью, при которой требуется заместительная почечная терапия, больные с кохлеарными имплантами, подтеканием спинномозговой жидкости, гемоглобинопатиями, пациенты, включенные в лист ожидания на трансплантацию органов и тканей [71].
В настоящее время в национальной программе иммунизации используются две разные пневмококковые вакцины: 13-валентная пневмококковая конъюгированная вакцина (ПКВ13) и 23-валентная пневмококковая полисахаридная вакцина (ППВ23). Полисахаридные вакцины действуют по механизму Т-независимого иммунного ответа. Инактивированная полисахаридная вакцина включает 23 серотипа пневмококка: 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20, 22F, 23F, 33F. Однако полисахаридные вакцины недостаточно иммуногены среди детей в возрасте младше 2 лет, поэтому не рекомендованы к применению в этой возрастной группе. В России вакцина ППВ23 разрешена к применению у детей с 2 лет, у взрослых в возрасте от 18 до 64 лет, входящих в группу риска, а также рекомендована всем людям в возрасте от 65 лет и старше в объеме одной дозы [72].
ПКВ формируют Т-зависимый иммунный ответ, который обусловлен набором пневмококковых капсульных полисахаридов, соединенных с иммуногенным белком-носителем, что позволяет усилить иммунный ответ. Особенность этого типа вакцин – хорошая распознаваемость конъюгированного антигена иммунной системой, стимуляция антительного ответа и выработка долговременной иммунологической памяти. ПКВ13 содержит капсульные полисахариды 13 серотипов, которые эффективны в отношении профилактики пневмококковой инфекции у детей за счет вакцинных серотипов 1, 3, 4, 5, 6А, 6В, 7F, 9V, 14, 18С, 19А, 19F и 23F. ВОЗ рекомендует использование ПКВ в программах детской иммунизации во всем мире [59].
По данным ВОЗ, обе вакцины обладают достаточной иммуногенностью для взрослых старше 50 лет [73].
Обзор исследований эффективности и действенности пневмококковой вакцины против пневмонии и инвазивной пневмококковой инфекции у пожилых людей показывает защитную эффективность обеих вакцин против пневмококков вакцинного типа [74].
Результаты крупномасштабного исследования CAPITA (Community-Acquired Pneumonia Immunization Trial in Adults), включившего 85 000 участников, продемонстрировали эффективность ПКВ13 у взрослых в возрасте 65 лет и старше в профилактике пневмококковой инфекции, вызванной вакцинными серотипами, включая инвазивные и неинвазивные случаи без анамнестических данных о предшествующей вакцинации против S. Pneumoniae [75]. Эффективность ПКВ13, согласно данным анализа в соответствии с протоколом исследования, составила 45,6% для предотвращения первого эпизода внебольничной пневмонии, вызванной вакциноспецифичными серотипами пневмококка, по сравнению с плацебо. При проведении модифицированного анализа в соответствии с назначенным вмешательством (ITT-анализ) эффективность вакцинации оказалась несколько ниже – 37,7%. Существует мнение, что результаты исследования CAPITA следует трактовать с оговорками, поскольку в него не включались пациенты с иммунодефицитом, и проект проводился до внедрения в Нидерландах массовой иммунизации против пневмококковой инфекции детей без анализа состояния коллективного эффекта вакцинации [76].
В одном из первых опубликованных метаанализов, посвященных эффективности ППВ23 (25 исследований), были получены убедительные доказательства эффективности этой вакцины при профилактике всех инвазивных пневмококковых инфекций (отношение шансов 0,26) и пневмонии в странах с невысоким уровнем доходов в общей популяции пациентов (отношение шансов 0,54) в отличие от стран с высоким уровнем доходов [77]. Более поздние метаанализы с включением исследований разного дизайна показали эффективность ППВ23 в профилактике пневмококковой пневмонии, вызванной любым серотипом пневмококка: она достигала 64% по данным 2 клинических исследований и 48% по результатам 2 когортных исследований. Более высокая эффективность вакцинации ППВ23 была выявлена в клинических исследованиях (период последующего наблюдения – 2,5 года), чем в обсервационных исследованиях (период последующего наблюдения – около 5 лет), что, возможно, связано со снижением иммунной защиты с течением времени [78].
СЕРОТИПЫ ПНЕВМОКОККА И ПЕРЕКРЫВАЕМОСТЬ ВАКЦИНАМИ: ДАННЫЕ ИССЛЕДОВАНИЙ
Эксперты ВОЗ предлагают расширить использование пневмококковых вакцин в национальных программах вакцинации взрослых пациентов для стран с так называемыми зрелыми программами вакцинопрофилактики у детей (т.е. когда вакцинация проводится на национальном уровне в течение ≥7 лет с охватом не менее 70% целевой детской популяции в течение каждого из последних 3 лет) [79]. Россия относится именно к таким странам, поскольку вакцинация против пневмококковой инфекции включена в национальный календарь профилактических прививок и календарь профилактических прививок по эпидемическим показаниям с 2014 г., а охват детского населения вакцинацией против пневмококка с 2018 г. превышает 90% [80].
Состав пневмококковых вакцин был разработан с учетом серотипов, наиболее часто вызывающих инвазивные пневмококковые заболевания, и может не отражать современное распределение серотипов в отдельных регионах. Широкое применение ПКВ для профилактики пневмококковых инфекций у детей привело к изменению распространенности серотипов пневмококка в тех странах, где они были включены в национальные календари прививок. Также постепенно начала увеличиваться доля невакцинных серотипов пневмококка как среди пациентов с инвазивными инфекциями, так и у носителей [81].
Использование ПКВ продолжает оказывать влияние на распространенность серотипов пневмококка, изменение чувствительности возбудителя к антибиотикам. Эпидемиология серотипов S. Pneumoniae для взрослой популяции изучена в исследовании SPECTRUM [82]. В это исследование были включены 500 изолятов S. pneumoniae, собранные в 29 медицинских центрах из 20 городов России в 2019–2020 гг. в рамках эпидемиологического исследования по определению спектра серотипов пневмококка, циркулирующих во взрослой популяции в различных регионах нашей страны. Изоляты S. pneumoniae были получены от лиц старше 18 лет: здоровых носителей, пациентов с синуситами/острым средним отитом, внебольничной пневмонией и инвазивными пневмококковыми инфекциями.
Результаты исследования SPECTRUM (рис. 1) показывают, что наиболее часто выявляемые серотипы S. Pneumoniae среди всех изолятов в рамках исследования относились к серотипам 19F (13,4%), 6ABCD (12,2%), 3 (12,0%), 23F (7,2%), 11AD (5,2%), 22AF (4,8%), 14 (4,6%). Доминирующими назофарингеальными серотипами S. pneumoniae во взрослой популяции являются 19F, 6A/B/C/D, 3, 11A/D, 23F и 22A/F, что в целом соответствует тенденциям циркуляции серотипов пневмококка в странах, где массовая пневмококковая вакцинация проводится менее 10 лет.
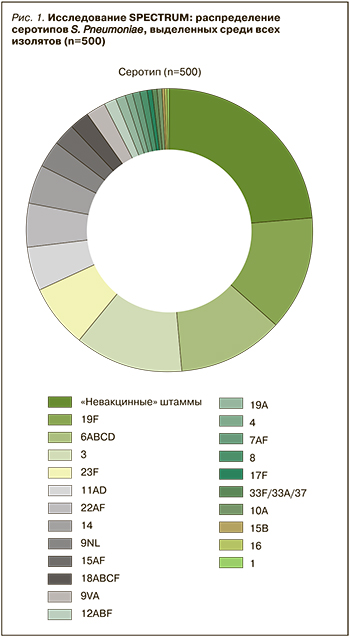
У взрослых пациентов с инвазивными пневмококковыми инфекциями на территории нашей страны показано преобладание серотипов 3, 23F, 6A/B/C/D, 19F, 12A/B/F, 15B, 4, 7A/F, 8, 9N/L и 9V/A. Исследователи отметили вариативность серотипов в группах в зависимости от клинического варианта инфекции, однако ряд серотипов доминирует в каждой из них: это серотипы 3, 23F, 6ABCD, 19F. У лиц с внебольничной пневмонией преобладают серотипы 19F, 6ABCD, 3, 23F, 14, 22AF и 11AD. На долю невакцинных штаммов пневмококка в группе внебольничной пневмонии приходится 28%, в группе инвазивных пневмококковых инфекций – 20%.
Особый интерес вызывают данные о перекрываемости зарегистрированными на территории России пневмококковыми вакцинами серотипов S. Pneumoniae, выделенных в исследовании SPECTRUM. Согласно полученным результатам, перекрываемость серотипов, полученных от пациентов с внебольничной пневмонией, составила 68,63% для ППВ23 и 51,82% для ПКВ13 (рис. 2). При этом у пациентов с инвазивными пневмококковыми инфекциями аналогичные показатели для тех же вакцин составили 86,0 и 62% соответственно (рис. 3). У здоровых носителей картина несколько иная: отмечается высокая перекрываемость выделенных серотипов S. pneumoniae как ПКВ13 (80,6%), так и особенно ППВ23 (90,3%).
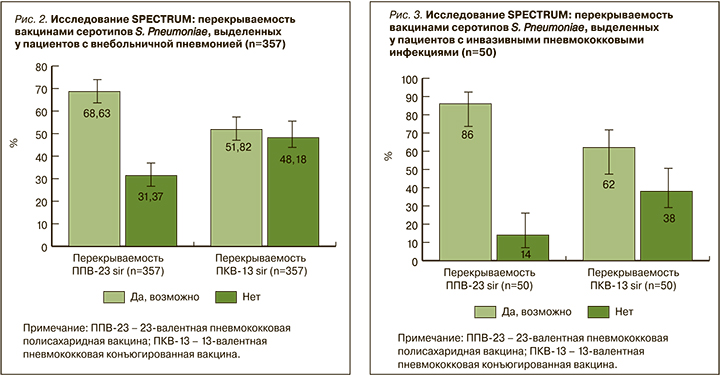
Результаты исследования SPECTRUM подчеркивают значимость данных о региональной эпидемиологии пневмококка для разработки эффективных схем вакцинопрофилактики от пневмококковой инфекции на национальном уровне.
В соответствии с провозглашенной в конце 2020 г. стратегией ВОЗ о расширении использования пневмококковых прививок в национальных программах вакцинации взрослых пациентов возникает вопрос как о необходимости определения новых показаний для проведения такой вакцинации, так и разработке эффективных вакцин с более широким валентным составом и возможным охватом наиболее значимых серотипов S. Pneumoniae.
ЗАКЛЮЧЕНИЕ
Таким образом, иммунизация взрослого населения от вакциноуправляемых инфекций остается одной из ключевых задач в практике врача-терапевта. Необходимость ее проведения регламентируется целым рядом постоянно обновляемых нормативных и методических документов. Выполнение вакцинопрофилактики рассматривается как стратегия, направленная на поддержание утраченного иммунного ответа вследствие увеличения продолжительности жизни человека, поиск дополнительных возможностей управления инфекциями, вносящими вклад в развитие хронических неинфекционных заболеваний, например онкологической патологии, либо новыми инфекциями (COVID-19 и др.). Среди всего многообразия проблем, связанных с необходимостью постоянной напряженной работы в области разработки национального календаря прививок взрослого населения, особый интерес вызывает вакцинация от сезонного и эпидемического гриппа, пневмококковой инфекции и COVID-19. Поддержание адекватного коллективного иммунного ответа возможно только при достижении высоких целевых показателей проведения вакцинопрофилактики с использованием отработанных организационных, методических приемов и принципов иммунизации на международном и национальном уровнях.



