ВВЕДЕНИЕ
Диуретики играют ключевую роль в лечении артериальной гипертензии (АГ). Тиазидные (ТД) и тиазидоподобные диуретики (ТПД) реализовывают свое действие в дистальных канальцах нефрона, отличаются гетерогенностью и могут быть разделены на соединения, содержащие и не содержащие бензотиадиазиновое кольцо: к первым, в частности, относится ТД гидрохлоротиазид, ко вторым – ТПД хлорталидон и индапамид. ТПД применялись в большинстве исследований сердечно-сосудистых исходов, в которых были установлены преимущества лечения диуретиками. Применение ТД и ТПД снижает частоту кардиоваскулярных событий, что делает их препаратами первой линии в национальных и международных руководствах по лечению АГ. Они эффективны в качестве монотерапии и усиливают эффективность других классов антигипертензивных средств при лечении пациентов с АГ [1–7].
Диуретики включены в руководства по лечению АГ как один из равнозначных вариантов терапии первого ряда наряду с блокаторами кальциевых каналов (БКК), блокаторами ренин-ангиотензин-альдостероновой системы (РААС) – ингибиторами АПФ и блокаторами рецепторов ангиотензина II (БРА) [1–7]. В российских рекомендациях по АГ от 2020 г. в группу препаратов первого ряда вновь включены бета-адренобокаторы (ББ), показания для назначения которых остаются прежними (сочетание АГ с ишемической болезнью сердца, сердечной недостаточностью, нарушениями ритма сердца) [1].
При всем при этом ТД и ТПД остаются недостаточно назначаемыми средствами, несмотря на то что для многих пациентов эти препараты служат незаменимым компонентом лечения для достижения необходимого контроля артериального давления (АД). У практических врачей сохраняются опасения в отношении метаболических эффектов, которые могут быть связаны с применением диуретиков. Однако результаты исследований свидетельствуют, что риск клинически значимого изменения лабораторных показателей на фоне их приема очень низок и обычно не имеет клинического значения. Имеющиеся данные подтверждают снижение заболеваемости и смертности, преимущества контроля объема и натрийуреза, в частности, для снижения риска развития сердечной недостаточности, при приеме диуретиков.
Диуретики особенно эффективны у пациентов с сахарным диабетом (СД), пожилых людей, больных с перенесенным инсультом, сердечной недостаточностью (СН), изолированной систолической или резистентной АГ [1–7]. Существующие данные говорят о том, что конкретные ТД и ТПД следует рассматривать отдельно, поскольку они имеют разные профили эффективности и безопасности. В этом плане особое место в этой группе лекарственных средств занимает ТПД индапамид [8–11].
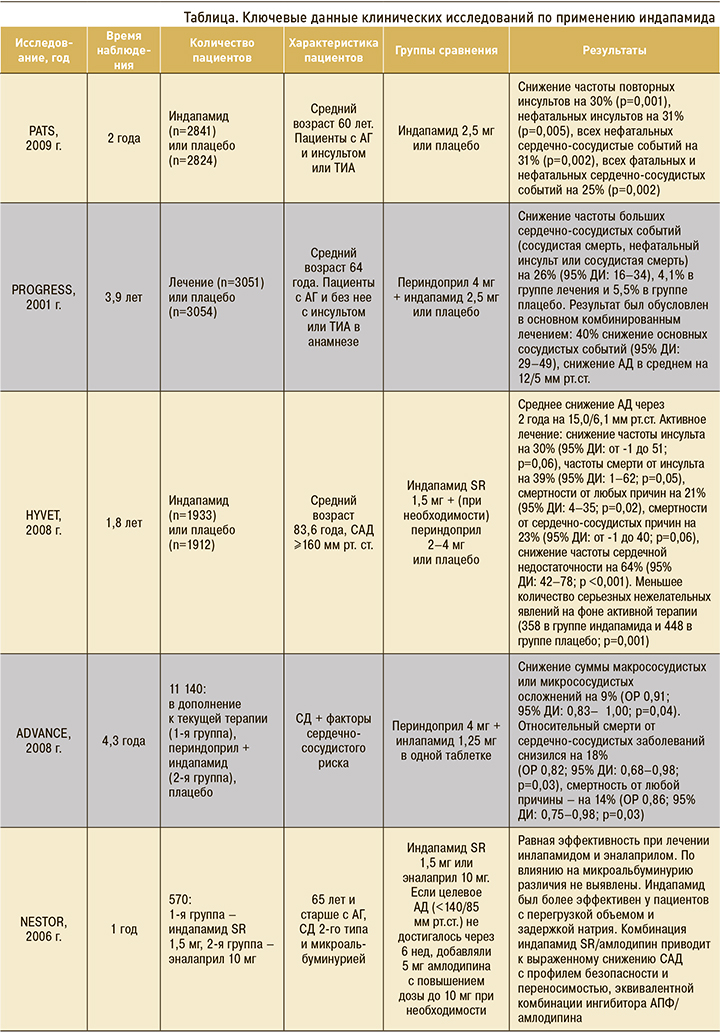
При выборе антигипертензивного препарата необходимо понимать его влияние на улучшение смертности от всех причин и сердечно-сосудистых исходов у различных категорий пациентов. Такое влияние может зависеть не только от наличия АГ, но и от степени кардиоваскулярного риска и коморбидности. Для оценки влияния индапамида на смертность от всех причин и сердечно-сосудистые исходы необходимо проанализировать полученные данные по применению этого лекарственного средства в качестве антигипертензивного препарата в ключевых международных исследованиях PATS, PROGRESS, HYVET, ADVANCE, NESTOR, PRIMUS, OPTIMAX, NATIVE [12–21].
РЕЗУЛЬТАТЫ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ С ИНДАПАМИДОМ
Рандомизированное, двойное слепое, плацебо-контролируемое исследование PATS (Post-stroke antihypertensive treatment study) изучало возможности антигипертензивной терапии в плане снижения риска фатального и нефатального инсульта у пациентов с перенесенными инсультом или транзиторной ишемической атакой (ТИА). В исследование было включено 5665 пациентов (2840 в группе индапамида, 28 825 – в группе плацебо). Средний возраст участников составил 60 лет, средний срок наблюдения – 2 года (максимально – до 45 мес). Через 2 года систолического АД (САД) в группе индапамида снизилось на 12,6±30,5 мм рт.ст., в группе плацебо – на 6,7±30,1 мм рт.ст. Для диастолического АД (ДАД) аналогичные показатели снижения равнялись 8,9±16,4 и 5,8±16,8 мм рт.ст. соответственно. Индапамид уменьшал частоту повторных инсультов на 30% (p=0,001), нефатальных инсультов – на 31% (p=0,005). Абсолютное снижение риска инсульта составило 40 случаев на 1000 участников (95% доверительный интервал (ДИ): 18–62). В группе индапамида все несмертельные сердечно-сосудистые конечные точки, включая инсульт, инфаркт миокарда и другие сердечно-сосудистые события, уменьшились на 31% (р=0,002). Активное лечение снижало все фатальные и нефатальные сердечно-сосудистые события на 25% (p=0,002) [12].
Целью исследования PROGRESS (Perindopril pROtection aGainst REcurrent Stroke Study ПРОГРЕСС) было определение эффектов режима снижения АД у пациентов с АГ и без нее с инсультом или ТИА в анамнезе. 6105 участников были случайным образом разделены на группы активного лечения периндоприлом (4 мг/сут) с добавлением индапамида по усмотрению лечащего врача (n=3051) или плацебо (n=3054). 58% пациентов в итоге получили комбинированную терапию. Первичной конечной точкой служила сумма фатального или нефатального инсульта. За 4 года наблюдения активное лечение снизило АД на 9/4 мм рт.ст. Инсульт произошел у 307 (10%) пациентов, получавших активное лечение, и у 420 (14%) в группе плацебо (снижение относительного риска (ОР) на 28%; 95% ДИ: 17–38; p <0,0001). Активное лечение также уменьшало риск крупных сердечно-сосудистых событий на 26% (95% ДИ: 16–34). Важным результатом исследования стало одинаковое снижение риска инсульта в подгруппах с АГ и без нее (p <0,01), причем такой результат был отмечен только у пациентов на терапии периндоприлом и индапамидом. Комбинированная терапия снижала АД на 12/5 мм рт.ст. и риск инсульта на 43% (95% ДИ: 30–54). Монотерапия периндоприлом снижала АД на 5/3 мм рт.ст. и не приводила к заметному уменьшению риска инсульта [13].
Известно, что АГ выступает важным фактором риска макрососудистых и микрососудистых осложнений у пациентов с сахарным диабетом (СД) 2-го типа. Частью исследования ADVANCE, изучавшего влияние интенсивного контроля уровня глюкозы на сосудистые исходы у пациентов с СД 2-го типа, являлась оценка влияния комбинации ингибитора АПФ и диуретика на сердечно-сосудистые события у пациентов с диабетом, независимо от исходного уровня АД или использования других антигипертензивных препаратов. 11 140 пациентов с СД 2-го типа были рандомизированы для лечения фиксированной комбинацией периндоприла и индапамида или плацебо в дополнение к текущей терапии. Первичная комбинированная точка включала смерть от сердечно-сосудистых заболеваний, нефатальный инсульт или нефатальный инфаркт миокарда, а также новое либо ухудшающееся почечное или диабетическое глазное заболевания. Анализ проводился и по каждому отдельному осложнению. В среднем через 4,3 года наблюдения 73% пациентов, которым было назначено активное лечение, и 74% пациентов группы контроля продолжали рандомизированное лечение. Среднее снижение САД в группе лечения составило 5,6/2,2 мм рт.ст. Уменьшение относительного риска крупного макрососудистого или микрососудистого события равнялось 9% (15,5% в группе активного лечения и 16,8% в группе плацебо; ОР 0,91; 95% ДИ: 0,83–1,00; р=0,04). Относительный риск смерти от сердечно-сосудистых заболеваний снизился на 18% (3,8% в группе активного лечения 4,6% в группе плацебо; ОР 0,82; 95% ДИ: 0,68–0,98; p=0,03), а смертность от любой причины – на 14% (7,3 и 8,5% соответственно; ОР 0,86; 95% ДИ: 0,75–0,98; р=0,03). При этом эффекты исследуемого лечения не зависели от исходного уровня АД или одновременного применения других видов лечения на исходном уровне [14].
Эффективность и безопасность лечения пациентов с АГ в возрасте 80 лет и старше всегда вызывала ряд вопросов. Высказывались предположения, что антигипертензивная терапия, несмотря на снижение риска инсульта, может увеличивать риск смерти. Важные данные в этом отношении были получены в исследовании HYVET (Treatment of Hypertension in Patients 80 Years of Age or Older). Группа лечения индапамидом (1933 пациента) и группа плацебо (n=1912) были хорошо сопоставимы (средний возраст 83,6 года, среднее АД 173,0/90,8 мм рт.ст.), 11,8% участников имели в анамнезе сердечно-сосудистые заболевания. Медиана наблюдения составила 1,8 года. Через 2 года среднее АД в группе активного лечения оказалось на 15,0/6,1 мм рт. ст. ниже, чем в группе плацебо. Лечение индапамидом привело к уменьшению частоты фатальных или нефатальных инсультов и смертности от инсульта на 30% (95% ДИ: 1–62; p=0,05), уровня смертности от любой причины – на 21% (95% ДИ: 4–35; p=0,02), смертности от сердечно-сосудистых причин – на 23% (95% ДИ: от -1 до 40; p=0,06), частоты развития сердечной недостаточности – на 64% (95% ДИ: 42–78; p <0,001) [16, 17]. При этом не было отмечено никаких существенных различий между группами активного лечения и плацебо с точки зрения изменений уровня калия в сыворотке по сравнению с исходным уровнем (- 0,02 ммоль/л в группе лечения и 0,03 ммоль/л в группе плацебо; p=0,09), мочевой кислоты (11,6 и 3,5 мкмоль/л; p=0,07), глюкозы (0,16 и 0,11 ммоль/л; p=0,56), креатинина (3,4 и 2,3 мкмоль/л; p=0,30). Количество зарегистрированных серьезных нежелательных явлений составило 448 в группе плацебо и 358 в группе активного лечения (p=0,001). Только пять из этих событий (три в группе плацебо и два в группе активного лечения) были классифицированы местными исследователями как возможно вызванные исследуемым препаратом [15].
В многоцентровом, контролируемом, двойном слепом, рандомизированном исследовании в двух параллельных группах NESTOR (Natrilix SR vs Enalapril in Hypertensive Type 2 Diabetics With Microalbuminuria) изучалось применение индапамида и эналаприла у пациентов в возрасте 65 лет и старше. В ходе него было рандомизировано 570 пациентов с АГ, СД 2-го типа и микроальбуминурией. Время наблюдения составило 1 год. Пациентам назначался индапамид SR 1,5 мг или эналаприла 10 мг. Если целевое АД <140/85 мм рт. ст. не достигалось через 6 нед, к терапии добавляли 5 мг амлодипина с повышением дозы до 10 мг при необходимости. Полученные данные показали равную эффективность при лечении индапамидом и эналаприлом. Снижение уровня натрия в плазме было значимым и независимым фактором, связанным со снижением систолического АД при применении индапамида 1,5 мг, но не эналаприла 10 мг; это позволяет предположить, что индапамид был более эффективен у пациентов с перегрузкой объемом и задержкой натрия. По влиянию на микроальбуминурию исследуемые препараты не различались. Частота гипокалиемии была выше при приеме индапамида, чем эналаприла (10,2 и 1,0% соответственно) [16, 17].
Важные данные в этом исследовании были получены при ретроспективном субанализе комбинированной терапии. Через 52 нед САД и ДАД снизились по сравнению с исходным уровнем на 26±13 и 14±9 мм рт.ст. в группе индапамида SR/амлодипина, включившей 135 человек, и на 21±14/11±9 мм рт.ст. в группе эналаприла/амлодипина, состоявшей из 156 пациентов (p=0,006 для ΔСАД). Лечение индапамидом SR/амлодипином характеризовалось хорошей переносимостью; лишь у нескольких пациентов наблюдались отеки. Как и ожидалось, при применении диуретиков в группе индапамида SR/амлодипина наблюдались небольшие изменения уровня мочевой кислоты. Изменения уровня глюкозы натощак, липидов, натрия, калия, клиренса креатинина были сходными между группами. Таким образом, комбинированное лечение индапамид SR/амлодипин вызывает выраженное снижение САД, при этом профиль его безопасности и переносимости эквивалентен комбинации ингибитора АПФ/амлодипина [18].
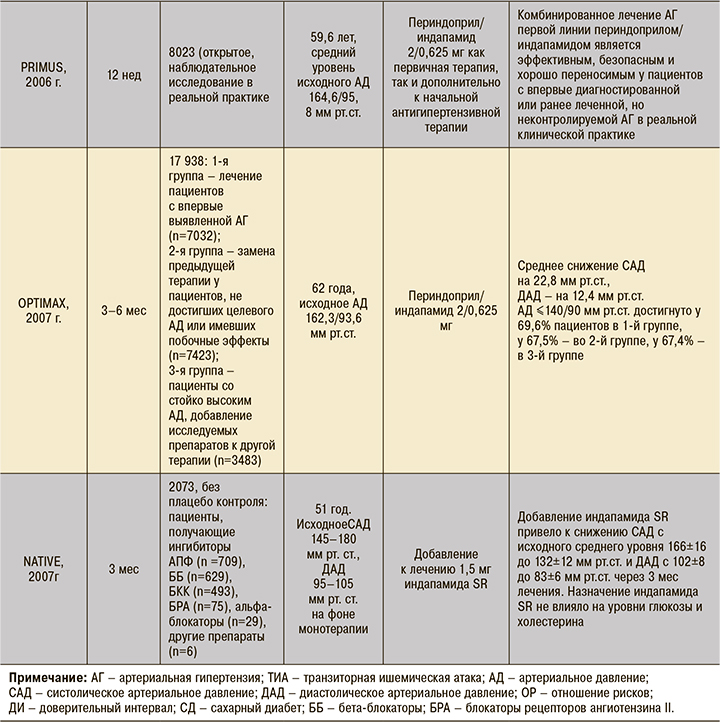
В открытое наблюдательное исследование PRIMUS (Efficacy and tolerability of the perindopril/indapamide combination therapy for hypertension), проведенное в Германии, вошли 8023 пациента, имевшие средний возраст 59,6 лет и средний уровень исходного АД 164,6/95,8 мм рт.ст. У 38% участников была впервые диагностированая АГ (среднее АД 166,1/97,2 мм рт.ст.), у 58% – неконтролируемая АГ, несмотря на проводимое ранее антигипертензивное лечение (среднее АД 163,5/94,9 мм рт.ст.). Предыдущее лечение состояло из ББ (49,5%), ингибиторов АПФ (36,4%), антагонистов кальция (29,3%), диуретиков (28,8%), БРА (7,1%) и других препаратов (8,1%). Лечение периндоприлом/индапамидом 2/0,625 мг значительно снижало САД (в среднем на 27,9 мм рт.ст.), ДАД (на 13,7 мм рт.ст.) и пульсовое давление (на 14,2 мм рт.ст.) по сравнению с их исходными уровнями (p <0,0001). 96% пациентов ответили на лечение, у 50% было достигнуто АД <140/90 мм рт. ст. Лечебная доза исследуемых препаратов была удвоена у 9,5% пациентов. Аналогичные результаты были получены при анализе различных подгрупп (пациенты с впервые выявленной АГ, пожилые, больные с изолированной систолической гипертензией, сопутствующими заболеваниями или поражением органов-мишеней, наличием дополнительных сердечно-сосудистых факторов риска). Наиболее частыми нежелательными явлениями (<1% пациентов) в исследовании были сухой кашель и тошнота. Полученные результаты подтвердили, что комбинированное лечение АГ периндоприлом/индапамидом является эффективным, безопасным и хорошо переносимым как при стартовой терапии АГ, так и в комбинированной терапии у пациентов с неконтролируемой АГ в реальной клинической практике [19].
Целью исследования OPTIMAX была оценка эффективности в повседневной клинической практике комбинации периндоприла/индапамида в фиксированных дозах, назначаемой в качестве начальной, заместительной или дополнительной антигипертензивной терапии. В это проспективное исследование было включено 17 938 пациентов, чей средний возраст равнялся 62 годам, а среднее АД – 162,3/93,6 мм рт. В 1-й группе проводилось лечение периндоприлом 2 мг/индапамидом 0,625 мг в течение 3–6 мес у пациентов с впервые выявленной АГ (n=7032). Во 2-й группе этими препаратами заменялась предшествующая терапия у больных, уже получавших лечение, но не достигших целевого АД или имевших побочные эффекты (n=7423). В 3-й группе периндоприл/индапамид добавляли к предшествующему лечению у пациентов со стойко высоким уровнем АД (n=3483). Целевым считалось АД 140/90 мм рт.ст. или ниже. В итоге при лечении периндоприлом/индапамидом целевое АД было достигнуто у 69,6% пациентов в 1-й группе («начальное лечение»), у 67,5% – во 2-й («замена других антигипертензивных препаратов») и у 67,4% – в 3-й («добавление к проводимой терапии»). Было зарегистрировано среднее снижение САД на 22,8 и ДАД на 12,4 мм рт.ст. Исследование подтвердило высокую эффективность комбинации периндоприл/индапамид в повседневной клинической практике [20].
Пакистанское исследование NATIVE (NATrilix SR use in combInation antihypertensiVe thErapy) охватило 2073 пациента с сохраняющейся АГ (САД 145–180 мм рт.ст., ДАД 95–105 мм рт. т.) на фоне монотерапии ингибитором АПФ (n=709), ББ (n=629), БКК (n=493), БРА (n=75), альфа-блокатором (n=29) или другим антигипертензивным препаратом (n=6). Добавление к лечению 1,5 мг индапамида SR привело к значительному снижению САД (с исходного среднего уровня 166±16 до 132±12 мм рт.ст.) и ДАД (с 102±8 до 83±6 мм рт.ст.) через 3 мес лечения. Назначение индапамида SR при этом не влияло на уровни глюкозы и холестерина [21].
Результаты приведенных выше исследований (табл.) продемонстрировали, что в различных популяциях пациентов длительное лечение индапамидом вызывало значительное снижение АД, достоверное уменьшение риска смертности от всех причин, смертности от сердечно-сосудистых заболеваний и риска фатального инсульта. Терапию индапамидом или комбинацией индапамида и ингибитора АПФ, индапамида и амлодипина следует рассматривать как терапию первого ряда для пациентов с АГ. Выбор конкретной комбинации и доз лекарственных средств должен проводиться с учетом исходного уровня АД, противопоказаний и переносимости лечения.
ВЫБОР СТАРТОВОЙ ТЕРАПИИ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ
Европейские (2018) и российские (2020) рекомендации по лечению АГ у взрослых предлагают в качестве стартовой терапии комбинацию ингибитора РААС и диуретика или БКК. Выбор между диуретиком и БКК остается на усмотрение врача [1–2].
В 2019 г. в журнале Lancet был опубликован масштабный метаанализ Suchard M. et al., включивший 4,9 млн пациентов, в котором изучалась оптимальная стартовая антигипертензивная монотерапия с применением ингибиторов АПФ, БРА, БКК и ТД/ТПД. Результаты показали сравнимую эффективность этих классов препаратов в большинстве клинических ситуаций. В то же время ТД/ ТПД имели лучшую, чем ингибиторы АПФ, первичную эффективность в снижении риска развития острого инфаркта миокарда (ОР 0,84; 95% ДИ: 0,75–0,95), инсульта (ОР 0,83; 95% ДИ: 0,74–0,95), госпитализаций по поводу сердечной недостаточности (ОР 0,83; 95% ДИ: 0,74–0,95) при первичном лечении АГ. С точки зрения профиля безопасности ТД/ ТПД также имели преимущества перед ингибиторами АПФ. Недигидропиридиновые БКК значительно уступали в этом плане другим четырем классам антигипертензивных средств [22].
Еще один метаанализ, выполненный Chen Y.J. et al. (2018), продемонстрировал отсутствие различий в смертности у пациентов с АГ при лечении ингибиторами АПФ, дигидропиридиновыми БКК, ТД/ТПД, ББ. При этом были отмечены различия в отношении некоторых исходов заболеваемости при приеме ТД/ТПД, которые в большей степени снижали риск сердечной недостаточности и инсульта, чем ингибиторы АПФ/БРА. БКК, в свою очередь, увеличивали риск развития сердечной недостаточности, но снижали вероятность инсульта по сравнению с ингибиторами РААС [23].
Пациентам, которые не достигли целевого АД на фоне моно- или комбинированной антигипертензивной терапии, не включавшей диуретики, рекомендуется назначение ТД/ТПД в составе комбинированного лечения в сочетании с БРА, ингибиторами АПФ, БКК. Следует помнить, что ТД/ ТПД характеризуются снижением антигипертензивной эффективности при скорости клубочковой фильтрации (СКФ) менее 45 мл/мин, а при СКФ менее 30 мл/мин становятся неэффективными. В этом случае в качестве альтернативы следует использовать петлевые диуретики [1–7].
ОСОБЕННОСТИ АНТИГИПЕРТЕНЗИВНОЙ ТЕРАПИИ У КОМОРБИДНЫХ И ПОЖИЛЫХ ПАЦИЕНТОВ 65 ЛЕТ И СТАРШЕ
Для пожилых пациентов с АГ характерна коморбидность. У них часто имеют место сопутствующие сердечно-сосудистые заболевания, почечная недостаточность, СД, что требует особого подхода в выборе лечения. Для пожилых больных характерен повышенный риск постуральной гипотонии, которая может усугубляться при проведении антигипертензивной терапии. В современных клинических рекомендациях отмечается важность проведения скрининга синдрома старческой астении, так как его наличие существенно влияет на тактику антигипертензивной терапии и уровень целевого АД [1–2]. У пациентов старческого возраста и больных со старческой астенией целесообразно начинать лечение АГ с монотерапии, используя любой из основных классов антигипертензивных препаратов [1–2]. В связи с этим отметим, что в исследовании HYVET на фоне лечения индапамидом была установлена не только хорошая его эффективность в лечении АГ у пациентов в возрасте 80 лет и старше, но также хорошая переносимость и метаболическая безопасность в виде отсутствия существенных изменений уровней калия, мочевой кислоты, глюкозы или креатинина в сыворотке крови [15].
Контроль и достижение целевого уровня АД у пациентов с перенесенным инсультом или ТИА является ключевым аспектом вторичной профилактики. Соответствующие рекомендации в значительной степени основаны на данных двух плацебо-контролируемых исследований, проведенных с участием пациентов с инсультом или ТИА в анамнезе, – PATS и PROGRESS [12, 13]. В них было выявлено значительное снижение частоты инсультов и серьезных сосудистых событий по сравнению с плацебо у пациентов, получавших лечение индапамидом (PATS), и комбинацией периндоприла и индапамида (PROGRESS).
Препаратами первой линии у пациентов с СД и хронической болезнью почек (ХБП) служат ингибиторы РААС. Больные с АГ и СД склонны к задержке жидкости и подвержены значительной опасности развития сердечной и почечной недостаточности. Диуретики позволяют снизить этот риск за счет контроля объема и натрийуреза [24]. Важность назначения диуретиков у этой категории пациентов отмечена в рекомендациях Американской диабетической ассоциации и Канадских рекомендациях по лечению АГ. Они в равной степени поддерживают назначение диуретиков и ингибиторов РААС, но отдают предпочтение первым при наличии протеинурии или микроальбуминурии [4, 25].
В исследовании NESTOR, изучавшем использование индапамида и эналаприла у пациентов с АГ, СД 2-го типа и микроальбуминурией, была установлена равная эффективность при лечении этими препаратами [16, 17].
ВЫБОР МЕЖДУ ИНДАПАМИДОМ, ХЛОРТАЛИДОНОМ И ГИДРОХЛОРОТИАЗИДОМ
Выраженность поражения органов-мишеней (ПОМ) и сердечно-сосудистая смертность в значительной степени связаны со снижением АД. Однако, при учете эффектов, обусловленных теми ПОМ, которые не связаны со снижением АД, начинают проявляться различия не только между разными группами антигипертензивных препаратов, но и между лекарствами, принадлежащими к одному терапевтическому классу. К примеру, при применении диуретиков маркеры почечной функции по-разному реагируют на лечение такими препаратами, как гидрохлоротиазид, хлорталидон и индапамид.
В исследовании Wan S. et al. (n=140) при сравнении терапии лозартан + индапамид (50 мг + 1,5 мг) с комбинацией лозартан/гидрохлоротиазид (50 мг + 12,5 мг) у больных АГ было выявлено улучшение соотношения альбумин/креатинин в моче, снижение уровней липокалина и связанных с желатиназой нейтрофилов, индекса резистентности почек по сравнению с исходным уровнем в обеих группах. Вместе с тем благоприятные изменения маркеров почечного повреждения и почечной гемодинамики, связанных с желатиназой нейтрофилов и индексом резистентности почек, были значительно выше в группе лозартана и индапамида [26].
В проспективном, рандомизированном, контролируемом исследовании Vinereanu D. et al. (n=56) пациентам с легкой и умеренной АГ и СД 2-го типа, имевшим нормальные показатели фракцией выброса левого желудочка, проводилось комбинированное лечение эналаприлом (10–40 мг) в комбинации с 1,5 мг индапамида или 25 мг гидрохлоротиазида. У участников выполнялась оценка эндотелиальной функции и биомаркеров исходно и через 6 мес. Было обнаружено, что индапамид положительно влияет на эндотелиальную функцию и функциональное состояние левого желудочка по сравнению с гидрохлоротиазидом [27]. В свою очередь, в рандомизированном контролируемом исследовании Senior R. et al. в 1993 г. (n=151) изучалось влияние 6-месячного лечения индапамидом в дозе 2,5 мг/сут на регресс гипертрофии левого желудочка у пациентов с АГ и ДАД в диапазоне 95–120 мм рт.ст. На фоне приема индапамида было отмечено достоверное снижение массы миокарда левого желудочка в сравнении с гидрохлоротиазидом 25 мг/сут [28].
Неоднородность диуретиков была установлена и в метаанализе Roush G. et al. в 2018 г. (12 исследований, n=1005), показавшем, что лечение хлорталидоном, индапамидом и калийсберегающими диуретиками, но не гидрохлоротиазидом, было связано со значительным снижением массы миокарда левого желудочка, по сравнению с ингибиторами РААС [10]. В целом результаты исследований свидетельствуют, что маркеры повреждения сердца также по-разному реагируют на разные варианты антигипертензивной терапии, и это может иметь существенное клиническое значение.
В метаанализе 2015 г. Liang W. et al. (21 исследование с поправкой на изменения АД и без таковой) было выявлено снижение риска сердечно-сосудистых событий и сердечной недостаточности, которое оказалось клинически значимым при приеме ТПД (индапамида, хлорталидона) независимо от поправки на АД [29]. Для ТД (хлоротиазида, гидрохлоротиазида, трихлорметиазида, бендрофлуметиазида, бендрофлуазида) уменьшение этого риска было значимым лишь в том случае, когда не проводилась поправка на снижение АД. Эти данные позволяют предположить, что снижение угрозы кардиоваскулярных событий и сердечной недостаточности, не зависящее от АД, происходит при применении ТПД, но не ТД [30].
В метаанализе Thomopoulos et al. 2015 г. подчеркивается, что индапамид и хлорталидон достоверно снижают частоту и сумму инсультов и ишемической болезни сердца (ИБС). Однако только данные по индапамиду, но не хлорталидону достигли значимости в отношении смертности от всех причин (ОР 0,86; 95% ДИ: 0,75–0,99), без поправки на АД [31]. В исследовании HYVET с индапамидом также было продемонстрировано снижение риска смерти на фоне приема инлапамида [15].
Результаты проведенного в Дании исследования указывают на возможность повышенного риска рака кожи при длительном лечении (>10 лет) гидрохлортиазида [32, 33]. Они поднимают важный вопрос о гетерогенности и интерпретации метаанализов, которые объединяют данные по различным препаратам группы ТД и ТПД.
В метаанализе Liang W. et al. (2017), включившем 5 исследований по сравнению индапамида с гидрохлоротиазидом и 5 исследований по сравнению хлорталидона с гидрохлоротиазидом, исследовалась эффективность снижения АД при применении отдельных ТД/ТПД. Полученные результаты продемонстрировали, что ТПД превосходят ТД в снижении АД: на фоне их приема САД в среднем снижалось на 5,59 мм рт.ст. (95% ДИ: от -5,69 до -5,49; p <0,001), ДА – на 1,98 мм рт.ст. (95% ДИ: от -3,29 до -0,66; p=0,003). При этом не наблюдалось увеличения частоты гипокалиемии, гипонатриемии, каких-либо изменений уровня глюкозы и общего холестерина. Добавим, что у 36–41% пациентов с АГ развивается гипертрофия левого желудочка, которая выступает независимым фактором риска сердечно-сосудистых событий и общей смертности. Согласно данным того же метаанализа, снижение массы миокарда левого желудочка под действием ТПД коррелирует с улучшением прогноза [9].
В метаанализе Roush G. et al. (2015), охватившем 14 рандомизированных исследований, сравнивались результаты применения гидрохлортиазида с индапамидом и хлорталидоном в отношении антигипертензивной активности или метаболических эффектов. Для справедливого сравнения доз диуретиков в каждой группе был назначен 1 из 3 уровней доз. Индапамид и хлорталидон снижали САД в большей степени, чем гидрохлоротиазид: первый препарат на 5,1 мм рт.ст. (95% ДИ: от -8,7 до -1,6; p=0,004), второй – на 3,6 мм рт.ст. (95% ДИ: от -7,3 до 0,0; p=0,052). Прямые сравнения продемонстрировали, что индапамид и хлорталидон более эффективны, чем гидрохлоротиазид, в традиционно назначаемых дозах и не вызывают серьезных неблагоприятных метаболических эффектов [8]. Более поздний метаанализ Roush G. et al. (2018), в который вошли 38 рандомизированных исследований, также был посвящен сравнительной эффективности ТПД (индапамида, хлорталидона) и ТД (гидрорхлоротиазида). ТПД в большей степени снижали гипертрофию левого желудочка в сравнении с ТД: индапамид – в среднем на 7,5% (ДИ: от -12,7 до -2,3; p=0,005); хлорталидон – на 8,2% (ДИ: от -14,7 до -1,6; p=0,015). Результаты продемонстрировали, что у пациентов с АГ ТПД уменьшают гипертрофию левого желудочка в большей степени, чем гидрохлоротиазид [10].
Следует подчеркнуть, что механизм действия индапамида имеет существенные отличия от других диуретиков. В этом отношении интересно исследование Lu M. et al., где изучалось влияние индапамида на нейротоксичность, вызванную амилоидом-β (белком, присутствующим в больших количествах в головном мозге пациентов с болезнью Альцгеймера и тесно связанным с патогенезом заболевания), и продукцию амилоида-β на клеточных моделях болезни Альцгеймера. Было обнаружено, что лечение индапамидом подавляет продукцию амилоида-β и значительно увеличивает жизнеспособность клеток в условиях его избытка. Кроме того, на фоне применения этого препарата увеличивалось время полужизни белка – предшественника амилоида [34].
Прямые сравнения индапамида и хлорталидона на сегодняшний день отсутствуют. Оба они обеспечивают полную 24-часовую антигипертензивную эффективность, поэтому выбор между ними должен основываться на известных дополнительных характеристиках препаратов. Существуют как минимум 3 фактора, которые могут повлиять на этот выбор, и все они дают основания для того, чтобы отдать предпочтение индапамиду.
1) Доступность и возможность применения различных доз. В реальной клинической практике в России хлорталидон встречается редко, преимущественно в комбинированных препаратах с азилсартана медоксомилом и атенололом в дозах 12,5 и 25 мг. Индапамид, в свою очередь, представлен как в препаратах обычного, так и замедленного действия и, кроме того, в широком диапазоне доз: в таблетках по 1,5 и 2,5 мг, а также в делимой на 4 части таблетке Индап® 2,5 мг (дозы 0,625; 1,25; 1,875 и 2,5 мг). Это позволяет легко осуществлять индивидуальный подбор дозы препарата.
2) Стоимость лечения. Если ориентировать на стандартную форму выпуска индапамида в дозе 2,5 мг (упаковка из 30 таблеток), то содержащие его монопрепараты, особенно генерические, в среднем имеют достаточно демократичную цену, что делает это лекарственное средство максимально доступным для всех разных категорий населения.
3) Метаболическая нейтральность. Применение индапамида не приводит к клинически значимым изменениям уровней натрия, калия, глюкозы, холестерина и мочевой кислоты в сыворотке крови [35].
ЗАКЛЮЧЕНИЕ
Диуретики являются ключевыми препаратами для лечения АГ с момента их появления в 1960- х гг. Их эффективность в предотвращении сердечно-сосудистых заболеваний и смертности подтверждена в многочисленных рандомизированных клинических исследованиях и метаанализах. Диуретики оказались более эффективными, чем другие классы препаратов, в профилактике развития сердечной недостаточности. Лекарственные средства, относящиеся к классу ТД/ТПД, имеют существенные отличия, подтверждающие необходимость дифференцированного подхода к выбору содержащих их препаратов в клинической практике. В целом соотношение долгосрочного риска и пользы у ТД менее благоприятно, чем у ТПД. Индапамид является препаратом выбора в ряду ТД и ТПД для стартовой моно- и комбинированной терапии широкого круга больных с АГ, включая пациентов с резистентной АГ, коморбидных пациентов и пациентов пожилого и старческого возраста. Имеющиеся данные говорят о дополнительной эффективности индапамида в комбинациях с ингибиторами АПФ, БРА и дигидропиридиновыми БКК.


