Семейная средиземноморская лихорадка (familial Mediterranean fever) или периодическая болезнь (ПБ) – это системное аутоиммунное генетически обусловленное заболевание с аутосомно-рецессивным типом наследования и определенной этнической предрасположенностью [1], которое проявляется приступами лихорадки, перитонита и плеврита, реже – артритом, поражением кожи, амилоидозом [2]. Встречается обычно в этнических группах, проживающих в среднеземноморском бассейне (армяне, евреи, турки, арабы), реже у жителей других регионов, в т.ч. кавказских народов. Примерно в половине случаев заболевание имеет доказанный семейный характер. Идентифицированный ген средиземноморской лихорадки (MEFV) расположен на коротком плече 16-й хромосомы (16р13.3), мутации его ответственны за развитие ПБ.
Наряду с «классическими» вариантами встречается множество редких и редчайших проявлений ПБ либо сомнительно причастных к ПБ, например, острый орхит, гломерулонефрит, хронический артрит с диагностическими критериями спондилоартрита [3], поражение верхних дыхательных путей (периодический ларингит), преходящая глухота, увеличение периферических (не относящихся к зоне воспаления) лимфатических узлов, периодическая сиалорея, поражение склер и конъюнктивы, а также ряд неврологических признаков [4].
Неврологические проявления ПБ обычно включают сильную головную боль как конституциональный компонент, сопровождающий приступ лихорадки, и несколько типов мышечной боли, рассматриваемых как формы васкулита [4]. Диапазон дополнительных неврологических расстройств при ПБ включает приступы эпилепсии [5], тромбоз венозного синуса [6], псевдоопухоль головного мозга [7], неврит глаза [8], осложнения системного васкулита со стороны ЦНС (пурпура Шенлейн–Геноха [9], узелковый полиартериит [10], болезнь Бехчета [11] и др. [12]), демиелинизирующие поражения и системный склероз [13–15], ишемический инсульт [16], возвратный асептический менингит [17, 18]. Описано несколько случаев ПБ с сильной головной болью и «менингизмом», головной болью на высоте приступа [19].
Проводится поиск взаимосвязи между видом мутации МЕFV и фенотипом ПБ [20].
Клинический пример
Больной П., 51 года, армянин, поступил на обследование в терапевтическое отделение Ставропольской краевой клинической больницы в марте 2015 г. с жалобами на общее недомогание, выраженную общую слабость, головную боль, появление болезненных красных пятен на голенях, небольшую потерю массы тела, субфебрильную температуру.
В апреле–мае 2014 г. появились покраснение глаз, больше правого, боль при движении в правом глазу, был диагностирован диффузный склерит, выявлена умеренная дисфункция стекловидного тела, факосклероз в обоих глазах. В августе 2014 г. температура поднялась до 39оС, появились боли в животе. Лечился по месту жительства, была выполнена диагностическая лапаротомия, обнаружено умеренное количество мутной без запаха жидкости с примесью фибрина в малом тазу и в левой подвздошной области, значительное увеличение и высокая плотность парааортальных лимфоузлов и узлов корня брыжейки тонкой кишки, увеличение плотной печени с поверхностью, покрытой «линейными тяжами». Диагностирован криптогенный серозно-фибринозный перитонит, брюшная полость была дренирована, послеоперационный период сопровождался длительной гипертермией. Заподозрена ПБ, образования на коже голеней были расценены как узловатая эритема. Выписан с рекомендацией приема глюкокортикостероидных препаратов, продолжал принимать метилпреднизолон 8–12 мг/ сут, несмотря на нормальную температуру, при этом сохранялись умеренная головная боль, общая слабость, периодически возникала эритема.
При поступлении состояние относительно удовлетворительное. Правильного телосложения, индекс массы тела 26 кг/м2. Пульс 80 в мин, артериальное давление 115/70 мм рт. ст. Над легкими коробочный оттенок перкуторного звука, ослабленное везикулярное дыхание. Тоны сердца значительно приглушены, ритмичные, систолический шум малой интенсивности на верхушке и в V точке. Печень выступает из-под реберного края на 2 см, плотная, безболезненная, селезенка не пальпируется. Кожа сухая, в области нижних конечностей множественные участки гиперпигментации округлой формы, диаметром от 0,5 до 2 см, некоторые из них слегка болезненные; по наружной поверхности левой стопы болезненный участок уплотнения (5×4 см) подкожной локализации с повышением местной температуры.
 Из анамнеза установлено, что с 14-летнего возраста страдает периодическими головными болями, возникающими 1 раз в 4–5 нед. Каждый болевой приступ продолжается 2–4 (в среднем 3) дня. Аналогичные приступы наблюдаются у отца и родного брата больного. Боли сильные, мучительные, сопровождаются тошнотой, рвотой; для их уменьшения иногда приходится перетягивать голову – от лба до затылка – мокрым полотенцем. Приступ болей в животе возник впервые, с этого времени приступообразность и выраженность головных болей значительно уменьшились.
Из анамнеза установлено, что с 14-летнего возраста страдает периодическими головными болями, возникающими 1 раз в 4–5 нед. Каждый болевой приступ продолжается 2–4 (в среднем 3) дня. Аналогичные приступы наблюдаются у отца и родного брата больного. Боли сильные, мучительные, сопровождаются тошнотой, рвотой; для их уменьшения иногда приходится перетягивать голову – от лба до затылка – мокрым полотенцем. Приступ болей в животе возник впервые, с этого времени приступообразность и выраженность головных болей значительно уменьшились.
В стационаре была осуществлена попытка отмены метилпреднизолона, после чего (на 3-й день) температура повысилась до 39оС (без озноба), усилились головная боль, слабость, появились мышечные боли. После однократного внутривенного введения метилпреднизолона температура нормализовалась, однако на 6-й день возникли сильная боль, сухость и першение в глотке, гиперсаливация, потеря (охриплость) голоса, непродуктивный кашель, общее недомогание, температура достигла 38оС. При осмотре слизистая оболочка полости носа, зева, задней стенки ротоглотки гиперемирована, слегка инфильтрирована, в полости носа серозно-слизистое отделяемое. Была заподозрена вирусная инфекция, назначен противовирусный препарат (осельтамивир) и введено 4 мг дексаметазона внутримышечно. На следующий день температура нормализовалась, головная боль, боль в горле, насморк прекратились, уменьшилась общая слабость.
Анализ крови: гемоглобин 120 г/л, эритроциты 4,3×1012/л, тромбоциты 147×109/л, лейкоциты 3,8×109/л, палочкоядерные нейтрофилы 4%, сегментоядерные нейтрофилы 70%, лимфоциты 20%, эозинофилы 1%, моноциты 5%, СОЭ 52 мм/ч. Глюкоза крови 5,5 ммоль/л, общий белок 64,5 г/л, альбумин 36 г/л, билирубин 7,4 мкмоль/л, креатинин 58 мкмоль/л, мочевина 6,2 ммоль/л, холестерин 2,76 ммоль/л, триглицериды 1,17 ммоль/л, липопротеиды низкой плотности 1,67 ммоль/л, липопротеиды высокой плотности 0,41 ммоль/л, коэффициент атерогенности 4,41, протромбиновый индекс 97%, фибриноген 5,39 г/л, активированное частичное тромбиновое время 35 с, щелочная фосфатаза 56 ед/л, креатинфосфокиназа 24 ед/л, аспартатаминотрансфераза 5,1 ед/л, аланинаминотрансфераза 15 ед/л, γ-глутамилтранспептидаза 26 ед/л, С-реактивный белок 124 мг/л. Содержание калия, натрия, ионизированного кальция в пределах нормы, уровень хлора 92 ммоль/л (снижен). Анализ мочи: относительная плотность 1,020, рН 6,5, белка и глюкозы нет, лейкоциты 1–2 в поле зрения, эпителий плоский – единичный.
Иммунологическое исследование: анти-НIV не обнаружены, НВsAg не обнаружен, анти-НСV обнаружены, РНК-НСV обнаружена, вирусная нагрузка 5,4×105 копий/мл, генотип 1b, ДНК-НВV не обнаружена. Индекс авидности IgG к цитомегаловирусу 0,63, ДНК цитомегаловируса в слюне и сыворотке крови не обнаружена. РНК Influenza virus A, virus B, virus A1H1N1 не обнаружена.
Электрокардиограмма: синусовый ритм, отклонение оси влево, блокада передней ветви левой ножки пучка Гиса, неполная блокада правой ножки пучка Гиса, нарушение реполяризации, более выраженное в верхушечно-боковой стенке левого желудочка. Допплер-эхокардиография: размеры лоцируемых структур сердца, магистральных сосудов и их взаимоотношения в пределах возрастной нормы, дисфункция трикуспидального клапана и клапана легочной артерии, фиброз створок митрального клапана с краевым уплотнением створок и подклапанных структур, гемодинамически незначимая митральная регургитация, пролабирование передней створки митрального клапана 1 степени, аномально расположенная хорда в полости левого желудочка, признаки склероза аорты, диффузных изменений в миокарде левого желудочка. Диастолическая дисфункция левого желудочка.
Рентгенография органов грудной полости: очаговых и инфильтративных изменений в легких не выявлено, атеросклероз грудного отдела аорты. Компьютерная томография органов грудной полости: эмфизема легких, диффузный пневмосклероз, признаки хронического бронхита, спаечный процесс в плевральных полостях. Мультиспиральная компьютерная томография брюшной полости с контрастированием: умеренная гепатомегалия, размеры селезенки 135×75×99 мм.
Ультразвуковое исследование органов брюшной полости: увеличение обеих долей печени – правой (182 мм) и левой (96 мм), структура диффузно-неоднородная; увеличение головки поджелудочной железы, повышенная ее эхогенность, диффузно-неоднородная структура с участками различной плотности; воротная вена 15 мм, селезеночная – 9 мм; селезенка 150×84 (157×85) мм. Дуплексное сканирование вен нижних конечностей: значимой патологии не выявлено, киста Бейкера типичной локализации левого коленного сустава.
Молекулярная диагностика ПБ: обнаружена одна мутация гена MEFV 16-й хромосомы (E148Q) в гетерозиготном состоянии (Центр медицинской генетики и первичной охраны здоровья, Ереван).
Заключение невролога: мигренозные головные боли, вестибуло-атактический синдром. Заключение окулиста: диффузный склерит обоих глаз.
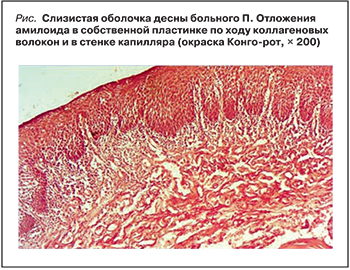
Наличие у больного гепатоспленомегалии, признаков диастолической дисфункции сердца послужило основанием для подозрения на амилоидоз, несмотря на отсутствие «классического» варианта ПБ. Проведено гистологическое исследование биоптатов десны и подкожно жировой клетчатки передней брюшной стенки: в обоих случаях установлено отложение фибриллярного компонента; при окраске Конго-рот и исследовании в поляризованном свете идентифицирован амилоид (рисунок).
Диагноз: Периодическая болезнь (семейная средиземноморская лихорадка) церебральный (мигренеподобный) и абдоминальный варианты с частыми мигренеподобными и единственным абдоминальным кризами, поражением глаз (склерит), кожи (рецидивирующая узловатая эритема, подкожные узлы – целлюлодермит), мышц (миалгия), верхних дыхательных путей (периодический ларингит). Системный амилоидоз. Цирроз печени С-вирусной этиологии (генотип 1b, виремия 5,4×105 копий/ мл), класс А по Чайлд–Пью в сочетании с амилоидозом (?) печени, портальная гипертензия компенсированная, минимальная биохимическая активность. Цитомегаловирусная инфекция в стадии латенции. Острая респираторная вирусная инфекция (?).
Проводилось лечение диклофенаком внутримышечно, метилпреднизолоном внутривенно, ранитидином, осельтамивир. Выписан с рекомендацией приема колхицином.
ОБСУЖДЕНИЕ
Интерес представленного клинического случая заключается в наличии у больного семейной средиземноморской лихорадки мигренеподобно-менингеальных приступов как единственного проявления болезни в течение многих лет (если не принимать во внимание клинически негативный спаечный процесс в плевральных полостях) с формированием осложнения в виде амилоидоза. Мигренеподобный вариант ПБ чаще всего расценивается как эквивалент классических приступов с благоприятным прогнозом, и развитие осложнения в случаях подобного изолированного течения болезни не имеет прецедента, т.к. клиника ПБ у 33-летнего мужчины с амилоидозом почек, развившимся на фоне многолетнего рецидивирующего асептического лимфоцитарного менингита, включала также рецидивы кожной сыпи и лихорадки [18]. Моносимптомное до определенного момента течение ПБ у пациента П. в виде периодически возникающих головных болей, безусловно, затруднило диагностику.
Смена «ведущего» варианта ПБ, причины которого неизвестны, произошла у нашего пациента после 40 лет болезни – фактически уже на этапе сформированного амилоидоза. Появлению нового, на этот раз классического, признака ПБ – абдоминального криза предшествовало (и сопутствовало ему) расширение клинической симптоматики, часть которой (склерит, миалгии, целлюлодермит) имеет отчетливый иммунный генез, а другая (транзиторная гиперсаливация, охриплость голоса, боль и першение в глотке) – возникла при попытке отмены глюкокортикостероидов и исчезла через несколько часов после возобновления их приема одновременно с прекращением лихорадки, что вполне согласуется с представлением об ангионевротическом отеке слизистых оболочек гортани и глотки [21]. Фактическое исчезновение приступообразных головных болей при появлении иного варианта ПБ, возможно, связано с появлением нового очага патологической активности в диэнцефальной области мозга [21] либо характеризует перенастройку иммунной системы с формированием новых мишеней для антителообразования, что при других аутоиммунных болезнях наблюдается редко и не в столь короткие сроки.
Перспективным направлением возможных исследований, которые в настоящее время активно проводятся, следует считать оценку взаимосвязи между фенотипом ПБ и некоторыми особенностями ее клинического течения, а также сроками развития осложнений [20, 22]. Присутствующая у нашего больного мутация E148Q, характеризуя доброкачественный полиморфизм [23], cоответствовала в целом «мягкому» фенотипу [20], хотя гетерозиготы, имеющие в т. ч. мутацию E148Q (E148Q/V726A), были склонны к увеличению риска развития амилоидоза [24–26], что отчасти согласуется с особенностями представленного клинического наблюдения – отсутствием до последнего времени лихорадочных и абдоминально-плевральных кризов и развитием амилоидоза.



