На сегодняшний день в Российской Федерации сохраняются высокие темпы роста заболеваемости сахарным диабетом (СД) 2 типа, наблюдается значительная распространенность артериальной гипертензии (АГ) (около 40% в популяции) без тенденции к ее снижению [1, 2]. Сочетание СД и АГ в десятки раз повышает риск развития кардиоваскулярных событий и терминальной хронической почечной недостаточности (ХПН) по сравнению с больными СД, не страдающими АГ [3].
К значимым предикторам ХПН относят падение скорости клубочковой фильтрации (СКФ), а также протеинурию и альбуминурию [4].
АГ при СД 2 типа является частью общего симптомокомплекса, в основе которого лежит инсулинорезистентность (ИР) [5]. ИР запускает системные и местные (органные и тканевые) вазоконстрикторные реакции и заканчивается развитием эндотелиальной дисфункции [6]. Для почек это означает усиление нарушения местного ренального кровообращения в результате возникновения дисбаланса между ведущими вазомодуляторами – NO и эндотелином-1 с преобладанием эффектов последнего [7]. Дисфункция эндотелия приводит к спазмированию артериол клубочков, нарушению трофики почки, почечного кровотока, микроциркуляции и клубочковой фильтрации, гипоксии и ишемии почечной паренхимы [8]. Ишемия и гипоксия ткани почек вследствие недиагностированной и некорригируемой ИР запускает компенсаторный каскад активации ренин-ангиотензин-альдостероновой системы, которая вносит свой вклад в прогрессирование функциональных и микроциркуляторных нарушений в почках [9].
 Таким образом, при выборе антигипертензивного препарата у больных АГ и СД 2 типа важно учитывать не только его способность эффективно снижать уровень артериального давления (АД), но и влияние на степень выраженности ИР и связанное с этим состояние почек как органов-мишеней. В доступной нам литературе мы не нашли публикаций, рассматривающих влияние комбинированной антигипертензивной терапии эналаприлом + индапамидом на функциональное состояние почек во взаимосвязи с оценкой ИР у больных АГ и СД 2 типа, что и обусловило актуальность проводимого нами исследования.
Таким образом, при выборе антигипертензивного препарата у больных АГ и СД 2 типа важно учитывать не только его способность эффективно снижать уровень артериального давления (АД), но и влияние на степень выраженности ИР и связанное с этим состояние почек как органов-мишеней. В доступной нам литературе мы не нашли публикаций, рассматривающих влияние комбинированной антигипертензивной терапии эналаприлом + индапамидом на функциональное состояние почек во взаимосвязи с оценкой ИР у больных АГ и СД 2 типа, что и обусловило актуальность проводимого нами исследования.
Цель исследования: оценить влияние 12-недельной комбинированной антигипертензивной терапии эналаприлом и индапамидом на функциональное состояние почек и ИР у больных АГ и СД 2 типа.
МАТЕРИАЛЫ И МЕТОДЫ
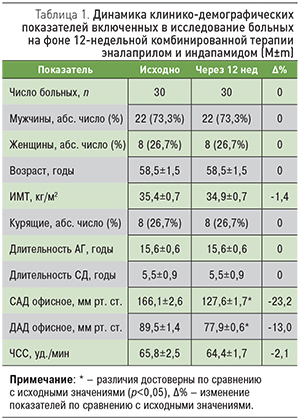
Работа выполнена в дизайне открытого проспективного неконтролируемого исследования, в которое были включены 30 больных АГ II–III стадии в сочетании с СД 2 типа в возрасте от 45 до 65 лет. Пациенты подписали форму информированного согласия на участие в исследовании. Клинико-демографическая характеристика больных представлена в табл. 1. У всех пациентов, принимавших антигипертензивные препараты до включения в исследование, не были достигнуты целевые значения АД – менее 140/85 мм рт. ст. [4]. За 5–7 дней до включения в исследование больным отменяли антигипертензивные препараты («отмывочный период»). Всем пациентам была назначена комбинированная антигипертензивная терапия эналаприлом в дозе 26,3±2,2 мг/сут и индапамидом в дозе 2,5±0 мг/ сут, продолжена гиполипидемическая терапия аторвастатином в дозе 16,3±0,9 мг/сут, а также комбинированная сахароснижающая терапия метформином по 1212,5±73,0 мг/сут и гликлазидом МВ по 81,3±6,3 мг/сут в течение 12 нед.
Физикальное обследование включало оценку общего состояния, клиническое измерение АД на обеих руках в положении пациента сидя по стандартной методике, антропометрию с расчетом индекса массы тела (ИМТ). Кроме того, у обследуемых подсчитывалась частота сердечных сокращений (ЧСС).
Функциональное состояние почек оценивали путем определения протеинурии по соотношению протеинурия/креатинин в утренней порции мочи (пирогаллоловым красным методом с помощью наборов реагентов для определения белка в моче «Юни-Тест-БМ», ООО «Эйлитон» (Россия), экскреции альбумина с мочой по соотношению альбумин/креатинин в утренней порции мочи (иммунотурбидиметрическим методом с помощью наборов «Микроальбумин-12/22», ОАО «Витал Девелопмент Корпорэйшн» (Россия) на биохимическом анализаторе Liasys (AMS, Италия), уровня ß2-микроглобулинов в моче (методом непрямого твердофазного иммуноферментного анализа – ELISA с использованием иммуноферментных наборов фирмы Orgentec (Германия), креатинина крови (методом Яффе при помощи колориметра фотоэлектрического концентрационного КФК-2-УХЛ 4.2 (Россия) и набора реактивов PLIVA-Lachema a.s. (Чехия) с расчетом СКФ по формуле CKD-EPI (Chronic Kidney Desease Epidemiology Collaboration) [10].
Уровень глюкозы в венозной крови натощак исследовали унифицированным колориметрическим глюкозооксидазным методом с помощью наборов «Lachema» (Чехия).
Уровень гликированного гемоглобина (HbA1c) определяли методом боратного аффинного анализа с помощью наборов NycoCard HbA1c (Axis-Shield, Норвегия) на NycoCard ридере II (Axis-Shield, Норвегия).
 Концентрацию базального инсулина определяли методом иммуноферментного анализа с помощью наборов DRG (США) на биохимическом анализаторе «Униплан» (Россия).
Концентрацию базального инсулина определяли методом иммуноферментного анализа с помощью наборов DRG (США) на биохимическом анализаторе «Униплан» (Россия).
ИР оценивали косвенными методами, представляющими собой математические модели в виде различных индексов, характеризующих чувствительность тканей к инсулину [11]. Применяли расчетный индекс HOMA-IR, отношение триглицеридов (ТГ) к холестерину липопротеидов высокой плотности (ХС ЛПВП) и метаболический индекс (МИ) с использованием показателей углеводного и липидного спектра [11].
На основании полученных результатов определяли наличие ИР при значении индекса HOMA-IR >2 у.е., индекса соотношения ТГ к ХС ЛПВП >1,37 у.е. и МИ ≥7 у.е. [11].
Статистическую обработку результатов проводили с использованием пакета статистических программ Microsoft Excel 2010. Применяли методы параметрической и непараметрической статистики. Данные представлены в виде M±m, где M – среднее значение, m – ошибка среднего. Достоверными считали различия при p<0,05.
Контроль безопасности терапии проводили путем регистрации пациентом в «Дневнике самоконтроля» нежелательных явлений в период лечения. Нежелательные лекарственные явления оценивали во время визитов с использованием метода открытого стандартного вопроса и мониторинга лабораторных и инструментальных показателей, которые могли бы свидетельствовать о развитии нежелательных лекарственных реакций.
Исследование проведено в соответствии с руководящими принципами закона «Об обращении лекарственных средств» № 61 от 12.04.2010 и принципами «Надлежащей клинической практики» (Good Clinical Practice).
Получено разрешение Регионального этического комитета на проведение клинического исследования (Протокол одобрения № 192-2013 от 11.03.2013).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
На фоне 12-недельной комбинированной терапии эналаприлом и индапамидом все больные достигли целевого уровня АД. Уровень офисного систолического АД (САД) снизился на 23,2% (p<0,05), а офисного диастолического АД (ДАД) – на 13,0% (p<0,05; табл. 1). Нежелательные явления за период наблюдения пациентов не зарегистрированы.
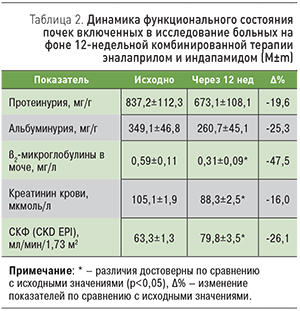
При анализе влияния комбинированной терапии эналаприлом и индапамидом на функциональное состояние почек выявлены достоверное уменьшение концентрации ß2-микроглобулинов в моче на 47,5% (0,31±0,09 против 0,59±0,11 мг/л исходно), а также статистически значимый рост СКФ на 26,1% (79,8±3,5 против 63,3±1,3 мл/мин/1,73 м2 исходно). На фоне 12-недельного лечения отмечено уменьшение альбуминурии и протеинурии на 25,3 и 19,6% соответственно, хотя различия не достигли статистической достоверности (табл. 2).
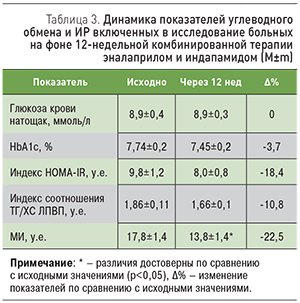 Комбинированная терапия эналаприлом и индапамидом не оказывала негативного влияния на показатели углеводного обмена в изучаемой группе пациентов: концентрация глюкозы крови натощак не изменилась, а уровень HbА1c снизился на 3,7% (табл. 3).
Комбинированная терапия эналаприлом и индапамидом не оказывала негативного влияния на показатели углеводного обмена в изучаемой группе пациентов: концентрация глюкозы крови натощак не изменилась, а уровень HbА1c снизился на 3,7% (табл. 3).
Через 12 нед лечения больных АГ и СД 2 типа отмечено уменьшение степени выраженности ИР: выявлено статистически значимое снижение МИ на 22,5% (13,8±1,4 против 17,8±1,4 у.е. исходно), а также положительное влияние на индекс HOMA-IR (∆%=-18,4) и индекс соотношения ТГ/ХС ЛПВП (∆%=-10,8).
Установлены достоверные корреляционные связи между функциональным состоянием почек и параметрами, характеризующими ИР: между индексом HOMA-IR, индексом соотношения ТГ/ХС ЛПВП, МИ и концентрацией креатинина сыворотки крови (r=+0,66, r=+0,29, r=+0,47 соответственно), индексом соотношения ТГ/ ХС ЛПВП, индексом HOMA-IR и уровнем ß2-микроглобулинов в моче (r=+0,52), индексом соотношения ТГ/ХС ЛПВП и протеинурией (r=+0,25), МИ и протеинурией (r=+0,25), индексом соотношения ТГ/ХС ЛПВП и альбуминурией (r=+0,25), МИ и альбуминурией (r=+0,25).
Таким образом, комбинация эналаприла и индапамида эффективно снижала уровень АД у больных АГ и СД 2 типа и хорошо переносилась пациентами.
Нормализация функционального состояния почек в изучаемой группе больных связана с дополняющими друг друга положительными эффектами ингибитора ангиотензинпревращающего фермента (иАПФ) эналаприла и тиазидоподобного диуретика индапамида, дополнительно обладающего вазодилатирующим действием [12]. Уменьшение уровней протеинурии и альбуминурии, вероятно, сопряжено с действием не только эналаприла, который снижает давление в капиллярах клубочков, но и индапамида, для которого доказано нефропротективное действие, сопоставимое с эффектом иАПФ [13].
Статистически значимое улучшение состояния проксимальных почечных канальцев (определяли по концентрации ß2-микроглобулинов в разовой порции мочи), возможно, обусловлено действием индапамида на кортикальный сегмент восходящей части петли Генле и на начальную часть проксимальных канальцев – препарат блокирует активность специального натриево-хлорного транспортера.
Достоверное увеличение СКФ, по-видимому, связано с влиянием эналаприла на эфферентные артериолы и прямым сосудорасширяющим действием индапамида. Этот нефропротективный эффект, на наш взгляд, является наиболее важным с точки зрения долгосрочного прогноза развития кардиоваскулярных событий и терминальной ХПН, т.к. СКФ характеризует не только клубочковую функцию, но и состояние нефрона в целом и является отражением сохранения массы действующих нефронов [14].
ЗАКЛЮЧЕНИЕ
Исследование подтверждает наличие тесных корреляционных взаимоотношений между ИР и поражением почек. Уменьшение степени выраженности ИР на фоне комбинированной терапии эналаприлом и индапамидом в течение 12 нед приводит к улучшению функционального состояния почек, что свидетельствует о возможности замедления прогрессирования АГ и СД 2 типа на фоне данной терапии.
Таким образом, применение нефиксированной комбинации эналаприла и индапамида в течение 12 нед является патогенетически обоснованным, безопасным и высокоэффективным у больных АГ и СД 2 типа.



