В индустриальных странах приблизительно 3/4 взрослого населения периодически страдают от боли в спине. При этом пик заболеваемости приходится на наиболее активный трудоспособный возраст (35–55 лет) [1].
На поликлиническом приеме пациенты с болью в спине составляют от 30 до 50% больных в зависимости от специализации врача. Боли в спине – одна из ведущих причин временной потери трудоспособности после острых респираторных заболеваний.
Острая боль в спине определяется как боль, локализованная в области позвоночного столба и длящаяся <6 нед. Это относительно доброкачественный симптомокомплекс. Быстрая редукция боли и возвращение к профессиональной деятельности наблюдается уже в течение первого месяца более чем у 80% больных, обращающихся за медицинской помощью [2]. В то же время катамнестические исследования в значительной степени опровергают тезис об исключительно благоприятном исходе боли в спине.
У небольшой части больных (10–17%) боль трансформируется в хроническую и может привести к инвалидизации, у значительной части пациентов боль меньшей интенсивности сохраняется длительное время, или же наблюдаются рецидивы эпизодов боли. Более чем у 1/3 пациентов боль в спине как минимум средней интенсивности продолжает персистировать в течение года после острого эпизода, причем приблизительно у каждого пятого пациента она значительно лимитирует обыденную активность [3]. В этом плане эффективное ведение пациента с острой болью в спине – хорошая гарантия против последующих обострений.
Диагностика: главное
Главная задача врача во время первичного осмотра – выявить пациентов, которые с высокой долей вероятности имеют серьезную патологию, требующую дальнейшего обследования и специфического лечения, например перелом тела позвонка, спинальный тумор, спинальную инфекцию. В связи с этим следует отметить, что среди пациентов, предъявляющих жалобу на боль в спине, 0,7% имеют спинальный тумор (первичный или метастатический), 4% – компрессионный перелом, 0,01% – спинальную инфекцию и 0,3% – анкилозирующий спондилит [4].
Все практические клинические рекомендации, базирующиеся на доказательной базе, предполагают использование системы «красных флажков» (симптомов опасности) для скрининга серьезных причин боли в спине (табл. 1). В первую очередь у практического врача должна быть настороженность в отношении неоплазмы.
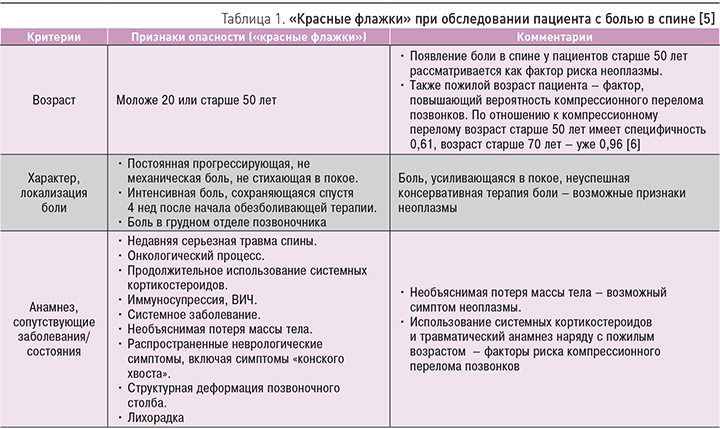
Отсутствие симптомов опасности после тщательного анализа позволяет исключить вторичный характер боли в спине. При выявлении таких признаков больному необходимо незамедлительное дополнительное обследование.
У молодых людей важно не пропустить анкилозирующий спондилит. Клиническими маркерами этого заболевания, помимо молодого возраста, служат утренняя скованность и альтернирующие боли в ягодичной области, усиление боли во второй половине ночи.
Следующий диагностический этап при боли в спине должен быть направлен на выявление корешковой боли. Боль, ассоциированная с радикулопатией, может приводить к стойкой утрате трудоспособности. Распространенность радикулопатии среди социально активной популяции людей значительно выше по сравнению с другими дегенеративными состояниями [7]. В течение года она возникает у 1–10% взрослого населения, а кумулятивная распространенность, отражающая вероятность заболевания в течение жизни, варьируется от 1,2 до 43%.
Ведение пациента с радикулярной болью требует определенных навыков, в отдельных случаях может потребоваться нейрохирургическое вмешательство. Поэтому пациент с подозрением на корешковую боль должен быть направлен на консультацию к неврологу.
Если боль иррадиирует в ногу ниже колена, то она с высокой долей вероятности вызвана компрессией волокон корешка. Поэтому для врача полезно стратифицировать пациентов с мышечно-скелетной болью в спине на группы: с иррадиацией боли в ногу и без нее. Этот момент важен не только для выявления возможной причины заболевания, но и потому, что боли с иррадиацией в конечность характеризуются большей тяжестью, тенденцией к хроническому течению и соответственно требуют более агрессивной терапии.
Основными причинами компрессии нервных корешков являются:
- грыжа межпозвонкового диска;
- остеофиты;
- гипертрофированная желтая связка;
- стеноз позвоночного канала.
Грыжи межпозвонковых дисков развиваются в континууме дегенеративного процесса в позвоночном столбе, который включает дистрофические и функциональные изменения в тканях опорно-двигательного аппарата (дугоотростчатые суставы, межпозвонковые диски, фасции, мышцы, сухожилия, связки) с возможным вовлечением смежных структур. Поэтому возникновению радикулярной боли, как правило, предшествуют эпизоды транзиторной мышечно-скелетной (неспецифической) боли.
Совокупность симптомов люмбальной радикулопатии может включать чувство онемения и слабости в зоне иннервации корешка, но более часто проявляется исключительно болью в ноге. Болевой синдром начинается остро или подостро. Пациенты описывают боль как стреляющую или пронизывающую. У некоторых она становится постоянной и имеет высокую интенсивнось. В дополнение к клинической оценке радикулярной боли могут быть использованы специальные опросники, например LANSS (табл. 2).

Чтобы определить, какой корешок страдает и какова степень его поражения, необходимо провести неврологическое обследование. Только по иррадиации боли судить об уровне поражения корешка нельзя. Только сочетание боли с гипестезией в соответствующем дерматоме может служить надежным маркером топирования радикулопатии.
Слабость мышц при дискогенных радикулопатиях обычно бывает легкой. Исключение – парализующий ишиас, характеризующийся выраженным парезом стопы. Развитие этого синдрома связывают с острой ишемией артерий, питающих корешки L5 или S1. Систематические обзоры диагностической ценности симптомов выпадения показали, что сенситивность сенсорного дефицита и рефлекторных нарушений составляет от 14 до 61% [8, 9], моторных симптомов (слабость) – от 27 до 62% [4, 5], симптомов натяжения – от 35 до 81% [10].
Таким образом, обследование пациента с подозрением на радикулярный болевой синдром должно включать оценку диапазона движений в поясничном отделе позвоночника, симптомов натяжения, неврологического дефицита (сенсорные, моторные, рефлекторные нарушения). Особое внимание следует уделять паттерну распространения парестезий или гипостезии, редукции дорсофлексии стопы и большого пальца, коленным и ахилловым рефлексам.
Оценка прогноза
После исключения специфических причин боли в спине и радикулярной боли следует оценить прогноз болевого синдрома. Более чем у 85% пациентов, испытывающих персистирующую боль в спине, невозможно установить конкретное заболевание или специфическое нарушение структур позвоночного столба. В настоящее время в отношении таких болевых феноменов принято использовать термин «неспецифические боли в спине».
Первичным источником такой боли могут служить различные структуры позвоночного столба и окружающих его тканей, например капсулы суставов, связки и фасции, межпозвонковый диск (болевые рецепторы обнаружены в наружной трети кольца), позвонки (ноцицепторы обнаружены в надкостнице и кровеносных сосудах), мышцы. Определить конкретный источник первичной боли в рутинной клинической практике довольно трудно. К счастью, современные подходы к эффективной терапии боли в спине не требуют специфического патанатомического диагноза. В то же время важно на ранних этапах идентифицировать возможные барьеры к редукции болевого синдрома. В первую очередь необходимо убедить пациента избегать иммобилизации и возобновить активность как можно скорее, в том числе возвращение к работе. Современные анальгетики позволяют в короткие сроки провести качественное обезболивание и активировать пациента уже на ранних этапах.
 Клинические и психосоциальные факторы, с большой вероятностью негативно влияющие на исход мышечно-скелетной боли в спине, а потому требующие минимизации в процессе ведения пациента, получили название симптомов «желтых флажков» (табл. 3).
Клинические и психосоциальные факторы, с большой вероятностью негативно влияющие на исход мышечно-скелетной боли в спине, а потому требующие минимизации в процессе ведения пациента, получили название симптомов «желтых флажков» (табл. 3).
В случае идентификации одного или нескольких из этих факторов необходимо обсудить с пациентом возможности когнитивно-поведенческой психотерапии. И хотя нет доказательств эффективности психотерапевтических методов воздействия на редукцию острой боли, высока вероятность того, что эти воздействия препятствуют хронизации болевого синдрома.
Продолжаются дебаты об уровне доказательности того, что среди работающей популяции населения профессиональная активность, связанная с физическим трудом, служит предпосылкой развития боли в спине [11]. Большинство экспертов признают значимость профессионального фактора в развитии этого заболевания. Следует отметить, что при рассмотрении этого фактора должны учитываться не только биомеханические, но и менее изученные специфические психосоциальные риски, обусловленные трудовой деятельностью [12]:
- интенсивная работа в условиях дефицита времени;
- монотонная работа;
- работа в условиях недостаточного управления производством;
- неудовлетворенность работой;
- отсутствие социальной поддержки на работе;
- профессиональные перегрузки;
- стрессовые события, связанные с профессиональной деятельностью.
В настоящее время среди экспертов по мышечно-скелетным болям достигнут консенсус в том, что риски, связанные с тяжелым физическим трудом, снижаются, тогда как роль профессиональных стрессовых факторов возрастает. В результате вероятность развития боли в спине, говоря условно, у «менеджера» и «грузчика» уравнивается.
Подходы к лечению
Цель лечения острой неспецифической боли в спине – редукция боли и профилактика последующих обострений. До начала терапии следует:
- оценить интенсивность боли по визуально-аналоговой шкале: слабая (≤3,4 балла), средняя (3,5–7,4), сильная (≥7,5) [1]. Подавляющее большинство пациентов, обращающихся за помощью к врачу, имеют боль средней интенсивности, и только у ≈10% отмечается сильная (трудно переносимая) боль;
- определить, нарушает ли боль двигательную активность;
- оценить потенциальную пользу лечения;
- оценить потенциальные риски, связанные с лечением;
- просчитать вероятность долгосрочной эффективности планируемого лечения.
В типичных случаях острая боль в спине благополучно разрешается с помощью консервативного лечения. Мучительная боль облегчается в течение нескольких дней, но остаточная незначительная боль может персистировать неделями. К сожалению, невозможно оценить индивидуальный прогноз болевого эпизода и ответ на терапию, основываясь на его инициальных характеристиках, включая даже инициальную тяжесть боли [13].
Общие принципы купирования болевых эпизодов
Основные терапевтические направления в период появления или усиления боли включают избегание как постельного режима, так и значительных физических нагрузок (в том числе профессиональных), поддержание «посильной» обычной активности. Обычная «посильная» (толерантная) нагрузка более эффективна, чем постельный режим, физиотерапия, физические упражнения. Однако для поддержания двигательной активности необходимо быстрое и качественное обезболивание пациента. Быстрая активизация способствует регрессу симптоматики и уменьшает риск хронизации боли. Пациент должен знать, что возвращение к нормальной активности должно начаться так скоро, как только это возможно. Ориентиром в наращивании двигательной активности служит интенсивность болевого синдрома. Расширение двигательных возможностей пациента не должно усугублять болевой синдром.
Препаратами первого выбора для купирования острой боли в спине служат нестероидные противовоспалительные препараты (НПВП). На протяжении последнего десятилетия было выполнено несколько широкомасштабных метаанализов, включая Кокрейновские обзоры, продемонстрировавших строгие доказательства (1а) превосходства НПВП над плацебо в контроле острой боли в спине по таким показателям, как снижение интенсивности болевого синдрома, восстановление функциональной активности, время полной редукции боли, потребность в дополнительной аналгезии [5].
Анализ сравнительной эффективности различных НПВП показал их эквивалентную эффективность, а также отсутствие различий в эффекте между парентеральным или пероральным приемом препарата при купировании боли в спине [5].
Бесспорным достоинством НПВП при купировании острой боли является быстрота их действия. Однократный пероральный прием НПВП редуцирует боль как минимум на 50% в течение 4–6 ч у одного из двух или трех пациентов (Индекс NNT – Number Needed to Treat равен 2 или 3). Обобщающие данные клинических исследований свидетельствуют, что при использовании НПВП средний уровень боли достоверно снижается по отношению к исходному на 3-й день лечения. У большинства больных острая боль полностью разрешается в течение 2–3 нед, и только незначительная часть пациентов нуждается в более продолжительном лечении.
Большинство клинически значимых побочных эффектов НПВП, в первую очередь НПВП-индуцированные гастропатии, связаны с блокированием фермента циклооксигеназы-1 (ЦОГ-1). Применение традиционных НПВП (неселективных ингибиторов ЦОГ-2) ассоциировано с повышением риска серьезных гастроинтестинальных осложнений по сравнению с плацебо при коротких и особенно длительных курсах применения (1а). Наиболее приемлемыми способами нивелирования гастроинтестинальной токсичности являются:
- применение низких доз и коротких курсов НПВП;
- параллельное использование гастропротекторов (ингибиторов протонной помпы);
- альтернативное применение селективных ингибиторов ЦОГ-2.
Возможно усиление анальгетического эффекта НПВП за счет адъювантного включения в терапию короткого курса миорелаксанта, например, при недостаточном ответе на НПВП или при исходно интенсивной боли.
Для воздействия на дистресс, связанный с персистирующей болью (более 6 нед), могут быть использованы антидепрессанты. Некоторые из них, в частности ингибиторы обратного захвата норадреналина, способны модулировать боль независимо от влияния на настроение [14].


