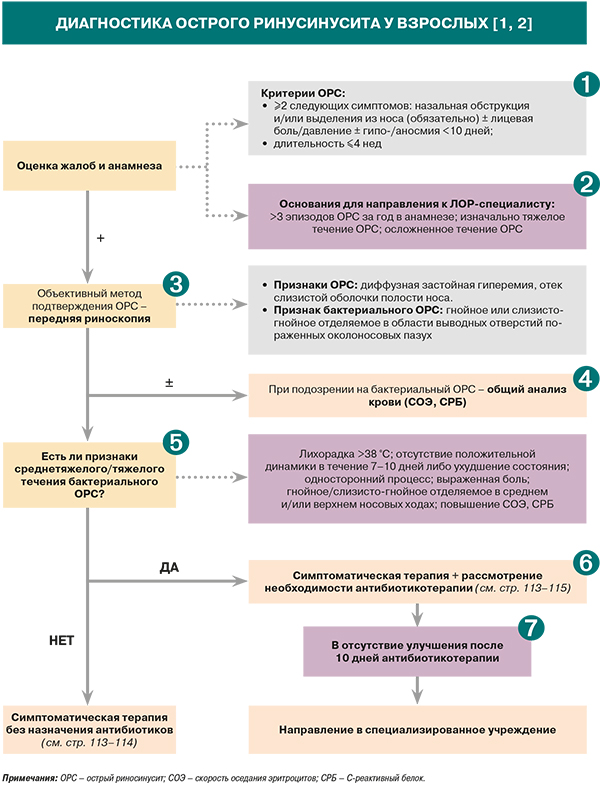
Диагностика
1.
• К основным симптомам ОРС относятся затруднение носового дыхания, выделения из носа и головная боль, к менее постоянным – снижение обоняния, заложенность ушей, повышение температуры тела, общее недомогание и кашель (последний более характерен для ОРС у детей) [1].
• Выделения при ОРС бывают слизистыми, гнойными и могут отходить при сморкании либо стекать по задней стенке глотки. Последнее более характерно для поражения клиновидной пазухи и задних отделов решетчатого лабиринта. Боль при ОРС, как правило, носит тупой, «ноющий» характер и может уменьшаться после применения назальных сосудосуживающих средств [1].
• При воспалении в верхнечелюстной и лобных пазухах боль локализуется в лице, области переносья и надбровья, при верхнечелюстном ОРС иррадиирует в верхние зубы на стороне поражения. Для воспаления клиновидной пазухи характерны боли в центре головы и в затылке («каскообразные» боли) [1].
• Симптоматика нетяжелых форм ОРС обычно ограничивается локальными проявлениями: затруднением носового дыхания, выделениями из носа слизистого, реже слизистогнойного характера, нарушением обоняния, нерезкими лицевыми болями в области лба либо в проекции верхнечелюстной пазухи. При этом признаки интоксикации отсутствуют или незначительно выражены, температура остается нормальной или субфебрильной. ОРС легкого течения имеет выраженную тенденцию к самостоятельному разрешению [1].
2.
Признаки тяжелого и осложненного ОРС отражены в таблице. Следует отметить, что степень тяжести заболевания в каждом конкретном случае определяется на основании субъективной оценки пациентом совокупности типичных симптомов по 10-сантиметровой визуально-аналоговой шкале (ВАШ), где полярные отметки (0 и 10 см) означают состояния «симптомы риносинусита совсем не беспокоят» и «симптомы мучительны настолько, насколько это можно представить». Обычно легкой (ВАШ 0–3) и среднетяжелой формам заболевания (ВАШ 4–7) соответствуют вирусный и поствирусный (затянувшийся сроком до 12 нед) ОРС, тогда как тяжелой форме (ВАШ 8–10) – бактериальный ОРС [1, 3, 4].

3.
• В случае воспаления верхнечелюстной и лобной пазух гнойное или слизисто-гнойное отделяемое при риноскопии можно увидеть в среднем носовом ходе, а в случае поражения клиновидной пазухи – в верхнем. Патологические изменения в среднем и верхнем носовых ходах лучше видны после анемизации слизистой оболочки, которая достигается аппликацией 0,1% раствора эпинефрина или распылением 0,1% раствора ксилометазолина/оксиметазолина. Патологический секрет может быть виден и в носоглотке или на задней стенке ротоглотки при задней риноскопии и фарингоскопии [1].
• Как отмечается в резолюции совета экспертов Российского общества ринологов «Актуализация клинических рекомендаций по острому риносинуситу и адаптация их к EPOS 2020» (далее – Резолюция), обзорная рентгенография околоносовых пазух как метод объективной диагностики нецелесообразна при вирусном, поствирусном (затянувшемся до 12 нед) и нетяжелом неосложненном бактериальном ОРС. Рентгенография может быть выполнена по решению ЛОР-специалиста при тяжелом и осложненном течении болезни, угрозе осложнений, а также при необходимости исключения латентно протекающего одонтогенного синусита, который манифестирует при присоединении риногенных факторов (причем в данной ситуации больше оправдано использование компьютерной томографии) [1, 2].
4.
Согласно Резолюции, врач первичного звена, наряду со знанием диагностических критериев ОРС и информированием пациента о схемах лечения (в том числе самостоятельного) заболевания, вправе назначить общий анализ крови при подозрении на бактериальный ОРС. В диагностических целях могут быть использованы такие лабораторные показатели, как лейкоцитоз, скорость оседания эритроцитов (СОЭ), уровень С-реактивного белка. В то же время отмечается, что ОРС может развиваться на фоне других заболеваний, в частности, известны случаи острого лейкоза, который впервые был обнаружен у больного ОРС с помощью анализа крови [2].
5.
• Критерии предположительно бактериального ОРС имеют важное значение, так как в дальнейшем служат основанием к назначению антибактериальной терапии. Основными диагностическими признаками в этой ситуации выступают клинико-анамнестические показатели, хотя следует помнить, что симптомы вирусного и бактериального ОРС в существенной степени дублируют друг друга, и это может затруднять дифференциальную диагностику [1, 5, 6]. В то же время такие объективные методы обследования, как рентгенография, компьютерная томография, культуральное исследование также мало помогают в данном случае [1].
• Бактериальный ОРС следует дифференцировать не только с вирусным ОРС, но и хроническим, грибковым и одонтогенным риносинуситом. Это позволяет сделать в первую очередь тщательный сбор анамнеза: для бактериального ОРС характерно одновременное поражение нескольких пазух (полисинусит), тогда как для грибкового и одонтогенного – изолированное поражение одной (обычно верхнечелюстной) пазухи [1].
6.
По данным EPOS (European position paper on rhinosinusitis and nasal polypis) 2020 г., в назначении антибиотиков на самом деле нуждается не более 2–5% больных, страдающих ОРС [2, 7]. В связи с этим в Резолюции оговаривается необходимость существенно сократить необоснованное назначение системной антибиотикотерапии в первую очередь при поствирусном (затянувшемся сроком до 12 нед) и нетяжелых формах бактериального ОРС [2, 8, 9]. Там же отмечается, что решение о необходимости назначения системной антибиотикотерапии по возможности должен принимать ЛОР-специалист на основании степени тяжести заболевания и угрозы развития осложнений [2].
7.
Эффективность эмпирической антимикробной терапии служит одним из вторичных дифференциальных признаков бактериального ОРС, вызванного типичными возбудителями (S. pneumoniae и Н. influenzae) [1].
Лечение
1.
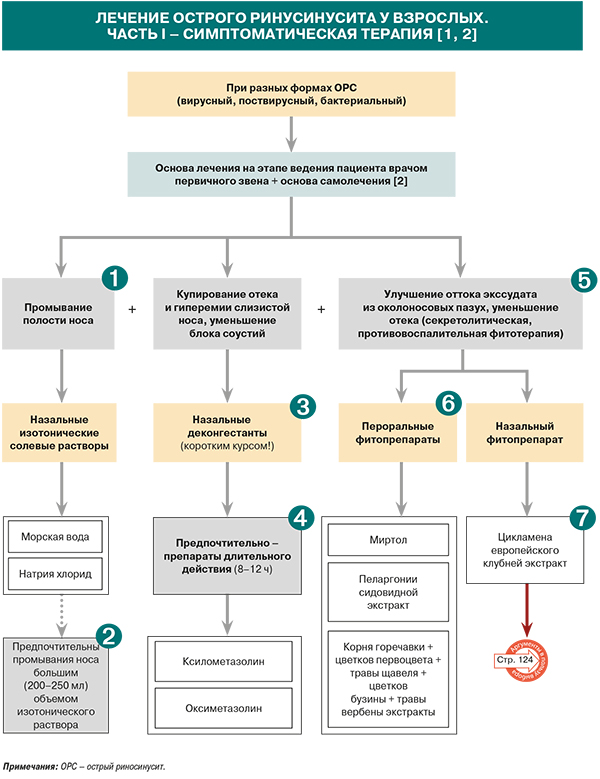
Промывание полости носа назальными солевыми растворами (ирригационная терапия, назальный душ) играет одну из ведущих ролей в лечении ОРС как вирусного, так и бактериального происхождения. В сочетании с системной или топической фитотерапией она позволяет сократить необходимость в назначении антибактериальных препаратов [2].
2.
Во всех контролируемых исследованиях эффективности иригационной терапии при ОРС применялось промывание полости носа большими (200–250 мл) объемами изотонического раствора [1, 10, 11]. Промывания малым объемом жидкости, аэрозолями разведенной морской воды не имеют доказательной базы. Они, безусловно, оказывают увлажняющий эффект, улучшают функционирование мерцательного эпителия, но не обеспечивают промывания глубоких отделов полости носа, структур остиомеатального комплекса и самих околоносовых пазух [1].
3.
Длительность применения назальных деконгестантов при ОРС во избежание развития медикаментозной зависимости не должна превышать 7–10 сут [1].
4.
Кроме ксилометазолина и оксиметазолина, на фармрынке России зарегистрированы и другие назальные сосудосуживающие средства, правда, с меньшей продолжительностью действия – трамазолин, нафазолин, фенилэфрин и др. [12].
Однако именно использование длительно действующих назальных деконгестантов при лечении ОРС уменьшает потребность в слишком частом применении препаратов и риск развития медикаментозной зависимости. Назальные деконгестанты следует назначать в виде дозированного аэрозоля/спрея, но не в форме капель, которые трудно точно дозировать [1].
5.
В резолюции совета экспертов Российского общества ринологов «Актуализация клинических рекомендаций по острому риносинуситу и адаптация их к EPOS 2020» отмечается, что фитопрепараты должны включаться в алгоритм терапии вирусного, поствирусного и бактериального ОРС [2].
6.
• В схеме указаны те системные фитопрепараты, которые присутствуют в России и при этом упоминаются в документе EPOS 2020 как средства, чья эффективность при ОРС подтверждена в контролируемых исследованиях (корень горечавки + цветки первоцвета и бузины + травы щавеля + вербены – при вирусном ОРС, пелларгония сидовидная и миртол – при поствирусном) [3, 13].
• Согласно клиническим рекомендациям Российского общества ринологов, у взрослых пациентов при ОРС режим приема комплексного фитопрепарата, содержащего экстракты корня горечавки + цветков первоцвета + травы щавеля + цветков бузины + травы вербены, следующий: по 2 драже или 50 капель 3 раза/сут курсом 7–14 дней [1].
7.
• Экстракт клубней цикламена европейского в форме дозированного назального аэрозоля – единственный топический фитопрепарат, упоминаемый в EPOS-2020 [2, 3]. Наряду с противоотечным действием, улучшением исхода патологического секрета из околоносовых пазух и эвакуации его в носоглотку, он усиливает микроциркуляцию крови в слизистой оболочке носа, а также стимулирует мукоцилиарный транспорт, оказывая отчетливый клинический эффект [1, 14, 15].
• Данные по экстракту цикламена европейского представлены двумя рандомизированными клиническими исследованиями у пациентов с затянувшимся/поствирусным ОРС: в одном – в виде монотерапии в сравнении с плацебо, а в другом – в комбинированной терапии с амоксициллином, где в группе сравнения пациенты получали только антибиотикотерапию. Назальная терапия цикламеном европейским позволила ускорить положительную динамику эндоскопической картины полости носа, а также уменьшить выраженность рентгенологических изменений в околоносовых пазухах и симптомов заболевания (особенно лицевой боли) [2, 13, 16].
• При неосложненном течении ОРС возможно применение экстракта цикламена европейского в качестве средства монотерапии под наблюдением врача, при бактериальном ОРС его следует назначать в комбинации с антибиотиками (в последнем случае сочетание фитопрепаратов с антибиотиками может ускорить выздоровление) [2, 17]. В то же время, учитывая опыт клинического применения препарата в России, он может использоваться при бактериальном ОРС и в тех ситуациях, когда системные противомикробные средства не показаны или противопоказаны [2].
• Режим применения назальной формы экстракта клубней цикламена европейского при ОРС у взрослых: по 1 дозе в каждую половину носа 1 раз/сут курсом 8 дней [1].
8.
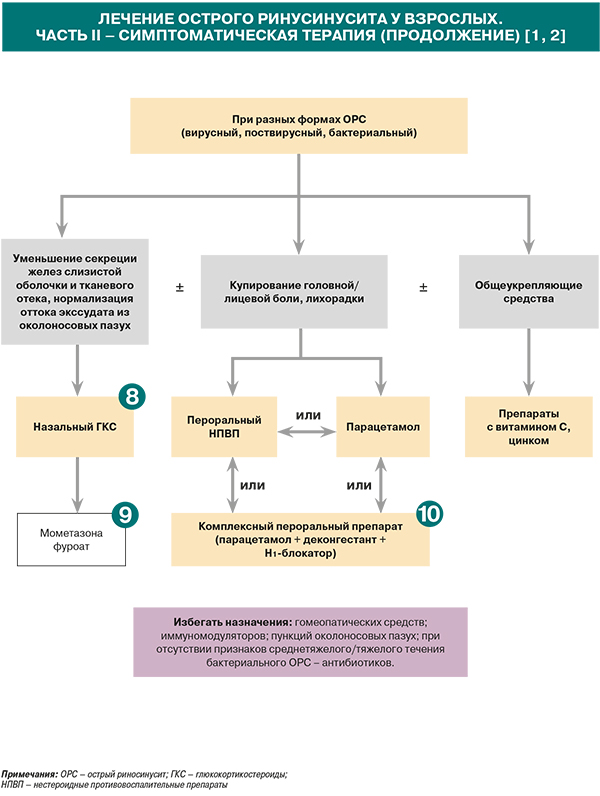
Ряд контролируемых исследований и систематический обзор убедительно продемонстрировал, что назальные глюкокортикостероиды (ГКС) могут с успехом применяться в качестве монотерапии при легких и среднетяжелых формах ОРС и как адъювантное средство при системном лечении антибиотиками (при среднетяжелой и тяжелой формах) [1, 18].
9.
• Рандомизированное мультицентровое исследование (n=981 пациент) продемонстрировало более высокую эффективность 15-дневного курса терапии мометазона фуроатом по сравнению со стандартным 10-дневным курсом лечения амоксициллином и плацебо. При этом суточная доза 400 мкг оказалась достоверно эффективнее, чем 200 мкг/сут [1, 19].
• В России, кроме мометазона фуроата, зарегистрированы и другие ГКС в форме назальных спреев. Но только назальные препараты мометазона имеют среди показаний в официальных инструкциях «острый риносинусит» [12].
• Режим применения спрея мометазона фуроата при ОРС у взрослых: по 100 мкг в каждую половину носа 2 раза/сут курсом 15 дней. При необходимости разовая доза может быть увеличена до 800 мкг/сут [1].
10.
Наличие в комплексных препаратах не только анальгетика, но также антиконгестивного и антигистаминного компонентов (примеры – парацетамол + фенилэфрин + фенирамин или парацетамол + фенилэфрин + хлорфенамин) может дополнительно способствовать устранению отека слизистой оболочки и восстановлению носового дыхания. Недостатком пероральных деконгестантов является риск развития системных побочных эффектов (со стороны центральной нервной и сердечнососудистой систем) [1].
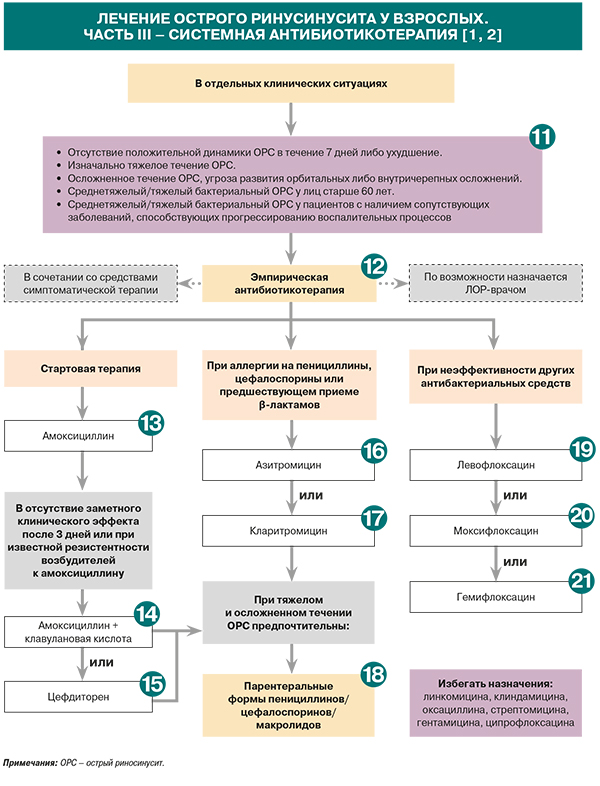
11.
• Признаки изначально тяжелого течения ОРС: лихорадка ≥39° C, головные и лицевые боли, гнойные выделения из носа, сохраняющиеся в течение 3–4 дней, выраженность симптомов по ВАШ ≥8 баллов [2].
• «Красные флажки», маркирующую угрозу развития орбитальных либо внутричерепных осложнений при ОРС, – нарастающие реактивные явления в мягких тканях орбиты и лица [2].
• К сопутствующим патологиям, способствующим прогрессированию воспалительных процессов при бактериальном ОРС, относятся сахарный диабет, хроническая обструктивная болезнь легких, гематологические, онкологические, аутоиммунные заболевания, иммунодефицитные состояния и др. [2].
12.
Ряд метаанализов последних лет продемонстрировал, что на 7–15-й день от начала заболевания ОРС у взрослых разрешается самостоятельно без назначения антибиотиков примерно в 86% случаев. Считают, что назначение антибиотика лишь незначительно (до 91%) повышает в те же сроки процент выздоровления, при этом оно связано с развитием известных побочных эффектов [1, 20]. Авторы метаанализов, обобщивших результаты всех рандомизированных контролируемых исследований эффективности антибиотикотерапии, констатируют, что «следует взвешивать ту небольшую выгоду, которую дает терапия антибиотиком при ОРС, и потенциальные побочные эффекты в отношении конкретного пациента и общества в целом» [20–24]. При выборе антибиотика для конкретного пациента нужно учитывать связанные с ним побочные эффекты: дисбактериоз, диарею, гепатотоксичность и др. [1].
13.
• С учетом российских данных об антибиотикорезистентности типичных патогенов (Н. influenzae и S. pneumoniae) препаратом первого выбора при бактериальном ОРС служит амоксициллин. Вместе с тем уже сейчас более 5% штаммов H. influenzae в России не чувствительны к незащищенным пенициллинам. Поэтому эффект эмпирической антибиотикотерапии должен мониторироваться; критерием ее эффективности является в первую очередь динамика основных симптомов ОРС (головной боли, выделений, заложенности носа) и общего состояния больного [1].
• Обзор литературы, посвященной переносимости антибиотиков, показал, что число пациентов, отметивших побочные эффекты лечения, составило 31% в группе, получавшей амоксициллин по сравнению с 22% в группе плацебо [1, 24].
• Режим применения амоксициллина при бактериальном ОРС у взрослых: внутрь по 500–1000 мг 3 раза/сут курсом 7–14 дней [1].
14.
• Режим применения амоксициллина/клавуланата при бактериальном ОРС у взрослых: внутрь по 625 (500 + 125) мг 3 раза/сут или по 1000 (875 + 125) мг 2 раза/сут курсом 7–14 дней [1].
• Согласно литературным данным, необходимость в отмене амоксициллина/клавуланата из-за развития побочных эффектов, возникала у 3,4% больных, получавших этот антибиотик, против 1% в группе плацебо [1, 24].
15.
Режим применения цефдиторена (цефалоспорин III поколения с высокой антипневмококковой активностью) при бактериальном ОРС у взрослых: внутрь по 400 мг 1 раз/сут или 200 мг 2 раза/сут курсом 7–14 дней [1].
16.
• Макролиды при бактериальном ОБС следует назначать при наличии в анамнезе анафилактических реакций на бета-лактамные препараты или подтвержденной аллергии на цефалоспорины II–III поколений [1]. Вероятность перекрестных аллергических реакций на цефалоспорины составляет 1,9 и 0,6% для II и III поколений соответственно [1, 25].
• Среди макролидных антибиотиков только кларитромицин и азитромицин действуют на H. influenza [1, 26]. По клинической эффективности и бактериологическому показателю эрадикации возбудителя при ОРС они не уступают бета-лактамам. К достоинствам макролидов можно отнести создание очень высоких тканевых концентраций в околоносовых пазухах, превышающие уровень препаратов в сыворотке крови. Способность макролидных антибиотиков действовать на внутриклеточно расположенные бактерии может сыграть важную роль при персистенции гемофильной палочки внутри клеток дыхательного эпителия и макрофагов [1].
• Азитромицин, наряду с левофлоксацином, относится противомикробным средствам, при приеме которых наиболее часто отмечают кардиотоксический эффект, способный вызывать тяжелые аритмии, особенно у пожилых людей и у пациентов, уже имеющих нарушения сердечного ритма [1, 27, 28].
• Режим применения азитромицина при бактериальном ОРС у взрослых: внутрь по 500 мг 1 раз/сут курсом 3–6 дней [1].
17.
• При терапии кларитромицином, в отличие от азитромицина, частота сердечнососудистых осложнений не выше, чем при лечении другими антибиотиками [1, 29].
• Режим применения кларитромицина при бактериальном ОРС у взрослых: внутрь по 250–500 мг 2 раза/сут («обычные» таблетки), 500 мг 1 раз/сут (таблетки с пролонгированным высвобождением курсом 10–14 дней [1].
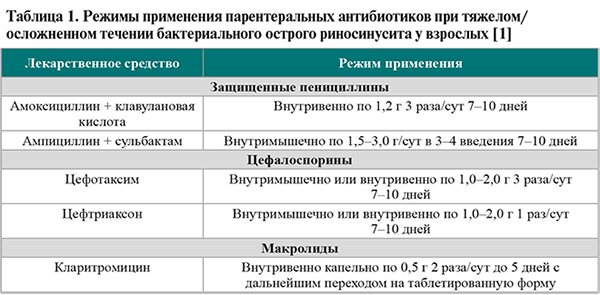
18.
Режимы применения парентеральных антибиотиков при тяжелом/осложненном течении бактериального ОРС у взрослых представлены в таблице 1.
19.
• Спектр антимикробного действия фторхинолонов III–IV поколений (левофлоксацин, моксифлоксацин, гемифлоксацин) адаптирован к возбудителям инфекций верхних дыхательных путей, и их калькулируемая бактериологическая эффективность приближается к 100%, что подтверждается и исследованиями, проведенными в России [1]. Вместе с тем в 2016 г. FDA выпустило предупреждение о том, неблагоприятные побочные явления, связанные с приемом фторхинолонов (тендинит, разрыв сухожилий, периферическая нейропатия, удлинение интервала QT, пируэтная тахикардия, myasthenia gravis, гиперчувствительность, отслойка сетчатки), в целом нивелируют их преимущества у пациентов с респираторными инфекциями, включая бактериальный ОРС. В связи с этим лечение фторхинолонами возможно только в тех клинических ситуациях, когда не остается других альтернатив антибактериальной терапии. Следует также помнить, что эти препараты нельзя использовать у лиц младше 18 лет [1].
• Режим применения левофлоксацина при бактериальном ОРС у взрослых: внутрь по 500–750 мг 1 раз/сут курсом 5–10 дней [1].
20.
Режим применения моксифлоксацина при бактериальном ОРС у взрослых: внутрь по 400 мг 1 раз/сут курсом 5–10 дней [1].
21.
• Режим применения гемифлоксацина при бактериальном ОРС у взрослых: внутрь по 320 мг 1 раз/сут курсом 5–10 дней [1].
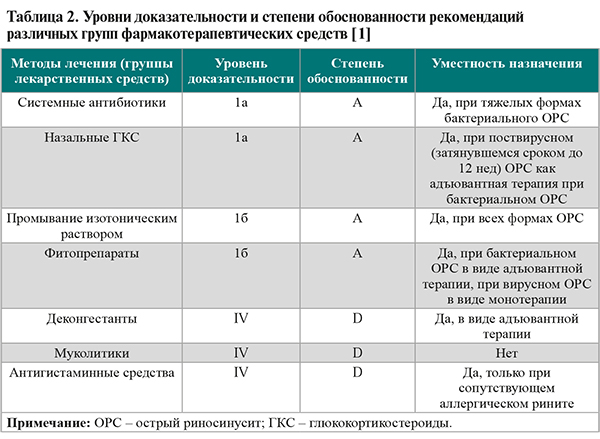
• Уровни доказательности и степени обоснованности рекомендаций по использованию различных методов лечения ОРС обобщены в таблице 2.