Артериальная гипертензия (АГ) остается одной из наиболее значимых медико-социальных проблем. Это связано как с широким распространением данного заболевания, так и с тем, что АГ является важнейшим фактором риска основных сердечно-сосудистых заболеваний (ССЗ), главным образом определяющих высокую смертность пациентов, – мозгового инсульта и инфаркта миокарда [1, 2].
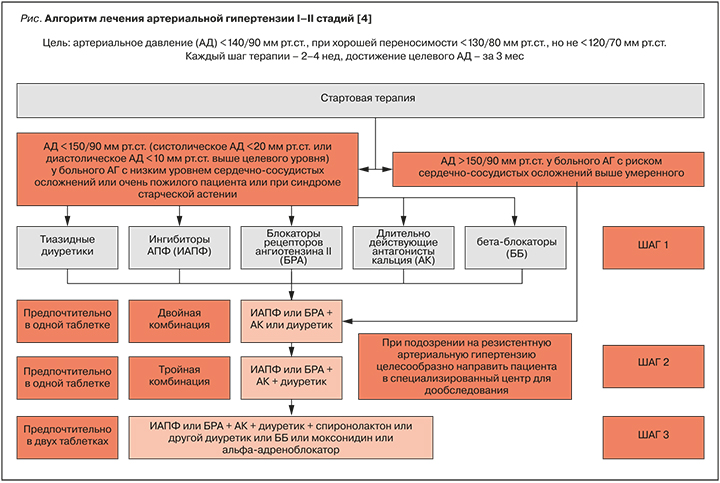
В рекомендациях Европейского общества кардиологов/Европейского общества артериальной гипертензии (ESC/ESH) 2018 г. [3] и Российских клинических рекомендациях 2020 г. [4] представлен алгоритм лечения АГ I–II стадий, который подходит для большинства больных с поражением органов мишеней (ПОМ), а также может быть использован при лечении пациентов с цереброваскулярной болезнью, сахарным диабетом (СД) или заболеваниями периферических артерий (рис.).
В соответствии с этим алгоритмом у пациентов с артериальным давлением (АД) >150/90 мм рт.ст. и риском сердечно-сосудистых осложнений (ССО) выше умеренного рекомендуется «двойная комбинация» антигипертензивных препаратов. Одним из составляющих этой комбинации служит блокатор ренин-ангиотензин-альдостероновой системы (РААС) – ингибитор ангиотензинпревращающего фермента (ИАПФ) или блокатор рецепторов к ангиотензину II (БРА).
В качестве второго компонента комбинированной терапии предлагается рассмотреть диуретик либо антагонист кальция (АК). Возможным вариантом решения этой дилеммы может быть выбор в пользу тиазидоподобного диуретика индапамида. Антигипертензивный эффект этого препарат обусловлен, с одной стороны, натрийуретическим действием, которое осуществляется в кортикальном сегменте петли Генле и проксимальном извитом канальце нефрона и соответственно позволяет устранить перегрузку сосудистой стенки натрием и уменьшить ее гиперреактивность к различным вазопрессорным агентам (норадреналину, ангиотензину II и др.). С другой стороны, индапамид обладает прямым сосудорасширяющим действием вследствие угнетения притока ионов кальция в гладкомышечные элементы сосудов, повышения синтеза простациклина в сосудистой стенке и простагландина Е2 (ПГЕ2) в почках, а также подавления синтеза эндотелийзависимого сосудосуживающего фактора [5, 6].
Периферическая вазодилатация проявляется у индапамида в большей степени, чем натрийуретический эффект, что отличает его от всех остальных тиазидных и тиазидоподобных диуретиков. Сосудорасширяющее действие препарата объясняют тем, что он является слабым антагонистом кальция [5–7]. Такой «двойной» механизм реализации антигипертензивного эффекта предопределяет более высокую эффективность и органопротекцию индапамида при АГ [7–9] и первоочередную возможность его применения в сочетании с блокатором РААС в рамках дилеммы «диуретик или АК» в составе комбинированной антигипертензивной терапии.
ДИУРЕТИКИ В ЛЕЧЕНИИ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ: АКТУАЛЬНЫЕ АСПЕКТЫ КЛИНИЧЕСКОЙ ЭФФЕКТИВНОСТИ И БЕЗОПАСНОСТИ
Применение диуретиков при АГ обосновано патогенетически, поскольку в механизмах повышения АД одну из центральных ролей играет увеличение объема циркулирующей крови и задержка во внутренней среде организма ионов натрия [10, 11]. Особое место тиазидные и тиазидоподобные диуретики, безусловно, занимают при АГ с низкой продукцией ренина, когда на первый план в ее развитии выходит объемзависимый патогенетический механизм, связанный с задержкой жидкости в организме. Такой вариант часто наблюдается у пациентов с метаболическим синдромом и СД, лиц пожилого возраста, мультиморбидных пациентов с сопутствующей хронической сердечной недостаточностью (ХПН) и/или хронической болезнью почек (ХБП) со скоростью клубочковой фильтрации ≥30 мл/мин/1,73 м2, а также у представителей негроидной расы [12].
В рекомендациях ESC/ESH 2018 г. [3] и Российских клинических рекомендациях 2020 г. [4] выбор диуретика для лечения АГ ограничен 3 препаратами: гидрохлоротиазидом (ГХТ), хлорталидоном и индапамидом. Тиазидные и тиазидоподобные диуретики на протяжении более полувека входят в число базовых лекарственных средств первой линии антигипертензивной терапии.
Релятивно их ренальным эффектам диуретики (тиазидные и тиазидоподобные) подразделяются на два поколения. Первое включает производные бензотиадиазина (ГХТ, бендрофлуметиазид, политиазид и др.) и хлорталидон, второе – производные квиназолинона (метолазон) и хлорбензамида (индапамид, ксипамид и др.) [13].
К настоящему моменту накоплена обширная доказательная база, основанная на результатах рандомизированных контролируемых исследований (РКИ) и проведенных метаанализах, свидетельствующая о позитивном влиянии диуретиков на прогноз, что проявляется в снижении риска развития сердечно-сосудистых и цереброваскулярных осложнений [14].
Часто в литературе, в том числе и в представленном на рисунке алгоритме, используются обобщенные понятия «тиазидные диуретики», или «диуретики». Однако в последнее время выявлены значимые различия в антигипертензивном эффекте и безопасности диуретических средств: например, в рекомендациях ESC/ESH 2018 г. [3] отмечается наличие более обширной доказательной базы у тиазидоподобных диуретиков с точки зрения их эффективности и прогностической значимости [15–17]. В связи с этим целесообразно четкое подразделение диуретиков на тиазидные и тиазидоподобные.
При этом следует отметить, что при сходном влиянии тиазидоподобных диуретиков на снижение цереброваскулярных событий/инсультов и общую смертность хлорталидон в большей степени повышает риск первичной ишемической болезни сердца (относительный риск (ОР)=2,0; 95% доверительный интервал (ДИ) 0,86–4,67) по сравнению с индапамидом (ОР=0,53; 95% ДИ 0,36–0,77) [17].
В метаанализе и систематическом обзоре турецких кардиологов отмечается, что нет исследований, свидетельствующих о положительном влиянии ГХТ на сердечно-сосудистые исходы, такие как инфаркт миокарда, почечная недостаточность, инсульт или смерть. Кроме этого, ГХТ в меньшей степени влияет на АД, таит высокий риск метаболических побочных явлений и может не иметь плейотропных эффектов. В результате оценка индапамида и хлорталидона как аналогов тиазидных диуретиков не может считаться точной [16]. В соответствии с рекомендациями британского Национального института здравоохранения (NICE) целесообразно рассматривать индапамид и хлорталидон в качестве диуретиков первого выбора, несмотря на сохраняющееся более частое применение ГХТ [18].
В метаанализе 19 РКИ с участием более 112 тыс. пациентов продемонстрировано, что именно прием тиазидоподобных диуретиков сопровождается значительным снижением риска сердечно-сосудистых заболеваний (ОР -0,78; p <0,001), инсульта (ОР -0,82; p=0,016) и сердечной недостаточности (ОР -0,57; p <0,001). В системном обзоре и метаанализе американских авторов, объединивших результаты 38 РКИ, наглядно продемонстрировано, что тиазидоподобные диуретики значимо (более чем в 2раза) превосходят ГХТ в снижении массы миокарда левого желудочка [19].
Тиазидоподобные диуретики имеют существенно больший период полувыведения по сравнению с тиазидами: если у ГХТ этот показатель находится в пределах 6–15 ч, то у индапамида – до 14–24 ч, у хлорталидона – 40–60 ч [17]. Длительность действия ГХТ варьирует, равняясь в среднем 16 ч, у индапамида она составляет ≥24 ч, у хлорталидона – 48–72 ч. В сравнительном исследовании низких доз ГХТ (12,5 мг) и хлорталидона (6,25 мг) на основе результатов суточного мониторирования АД сделан вывод, что ГХТ 12,5 мг проявляет антигипертензивный эффект преимущественно в дневное время и не влияет на уровень АД в ночные часы [20].
В систематическом обзоре и метаанализе, в который ученые из Колумбийского университета (США) включили 5 исследований с применением ГХТ в дозе 50 мг и 14 РКИ с использованием ГХТ в дозе 12,5–25 мг, было проведено сравнение контроля АД в течение 24 ч на фоне приема этого диуретика и других антигипертензивных препаратов (АГП). Полученные результаты позволяют говорить о явно недостаточном антигипертензивном эффекте ГХТ (как по систолическому, так и диастолическому АД) в сравнении с четырьмя другими базовыми классами АГП и поставить под сомнение целесообразность его назначения в качестве препарата первой линии для монотерапии АГ [10].
Еще одним актуальным вопросом является профиль лекарственной безопасности диуретиков. Так, в ряде метаанализов высказываются опасения, что терапия диуретиками может приводить к нарушениям электролитного баланса, негативным метаболическим эффектам – нарушениям липидного, пуринового и углеводного обмена, вплоть до повышения риска развития СД 2 типа [21, 22].
В метаанализе 60 РКИ из Кокрановского центрального регистра отмечено, что тиазидные диуретики снижают калий, повышают уровень мочевой кислоты и повышают общий холестерин и триглицериды [23]. Метаанализ сравнительных исследований ГХТ с индапамидом и хлорталидоном показал, что тиазидоподобные диуретики превосходят диуретики тиазидного типа в снижении АД без увеличения частоты гипокалиемии, гипонатриемии и любых изменений уровня глюкозы в крови и общего холестерина сыворотки [24].
В крупномасштабном сравнительном когортном исследовании [25] авторами были проанализированы эпизоды амбулаторного и стационарного лечения пациентов, впервые использовавших антигипертензивную монотерапию диуретиками в США за период 2001–2018 гг. Из 730 225 пациентов (средний возраст 51,5 года, 61,6% – женщины) 693 337 получали ГХТ и 36 918 – хлорталидон. Прием хлорталидона был связан со значительно более высоким риском гипокалиемии (ОР 2,72; 95% ДИ 2,38–3,12), гипонатриемии (ОР 1,31; 95% ДИ 1,16–1,47), острой почечной недостаточности (ОР 1,37; 95% ДИ 1,15–1,63), развитием хронического заболевания почек (ОР 1,24; 95% ДИ 1,09–1,42) и СД 2 типа (ОР 1,21; 95% ДИ 1,12–1,30), а также со значительно более низким риском диагностированного аномального увеличения веса (ОР 0,73; 95% ДИ 0,61–0,86). Исследователи подчеркивают, что прием хлорталидона сопряжен с более высоким риском почечных и электролитных нарушений. В описании активного вещества в инструкции к содержащим хлорталидон препаратам указывается на необходимость контроля картины периферической крови, электролитного состава крови, уровня мочевой кислоты и глюкозы в процессе лечения [26].
В другом обзоре говорится, что вероятность развития гипонатриемии, гипокалиемии и гиперурикемии, связанная с приемом ГХТ ниже, чем при использовании хлорталидона. В то же время терапия ГХТ была на ≥18% чаще сопровождалась побочными эффектами со стороны сердечно-сосудистой системы [27].
Во втором десятилетии нынешнего века при использовании ГХТ отмечено возможное развитие острой транзиторной миопии и острой закрытоугольной глаукомы [28, 29], а также значимое повышение угрозы развития немеланомного рака кожи (базальноклеточной карциномы и плоскоклеточной карциномы) [30, 31].
ИНДАПАМИД: АНТИГИПЕРТЕНЗИВНЫЙ ЭФФЕКТ, МЕТАБОЛИЧЕСКАЯ НЕЙТРАЛЬНОСТЬ И ОРГАНОПРОТЕКТИВНЫЕ СВОЙСТВА
С позиции доказательной медицины в качестве оптимального тиазидоподобного диуретика может рассматриваться индапамид; не случайно за 47 лет, прошедших со времени его синтеза, эффективность и безопасность этого препарата при АГ практически не подвергалась сомнению [7, 32].
Индапамид оказывает антигипертензивный эффект на протяжении всех суток как в дневное, так и ночное время, а также стабилизирует вариабельность АД, которая тесным образом ассоциирована с развитием сердечно-сосудистых осложнений и прогрессированием поражения органов-мишеней АГ [33]. Благодаря хорошо документированному позитивному влиянию на сердечно-сосудистые и почечные исходы, этот препарат представляет собой безопасный и ценный вариант лечения пациентов с высоким АД [34].
Метаанализ 9 РКИ с участием более 10 тыс. пациентов показал, что частота нежелательных реакций при использовании индапамида была сравнима с плацебо (ОР=0,97; 95% ДИ 0,76–1,22) [35].
Индапамид практически не оказывает влияния на метаболические процессы в организме: экскрецию калия, уровни глюкозы, холестерина и мочевой кислоты в крови. Метаболическая безопасность и высокая эффективность его применения в обычной (2,5 мг) и в ретардированной форме (1,5 мг), в том числе и у «проблемных» пациентов (с АГ и СД 2 типа, метаболическим синдромом, пожилых больных), подтверждена результатами международных и российских исследований ADVANCE, HYVET, NESTOR, PROGRESS, АРГУС-2, МИНОТАВР, ЭПИГРАФ и ряда других [36, 37].
В 6-месячном многоцентровом проспективном наблюдательном интервенционном открытом клиническом исследовании ACES с участием 9124 амбулаторных пациентов авторами отмечена метаболическая нейтральность индапамида, сходная с амлодипином и карведилолом [38].
В крупном рандомизированном исследовании PATS (Poststroke Antihypertensive Treatment Study,1998), включавшем 5665 больных с инсультом или преходящим нарушением мозгового кровообращения в анамнезе, изучался эффект индапамида (по 2,5 мг/сут) в сравнении с плацебо на риск развития повторного инсульта [39]. Наблюдение за больными продолжалось в среднем 3 года. В группе больных, леченных индапамидом, уровни АД были на 5/2 мм рт.ст. ниже, чем в контрольной группе, что сопровождалось снижением риска развития повторного инсульта на 29%. Это указывает на предотвращение 29 случаев инсульта в пересчете на 1000 леченых больных за 3 года при использовании индапамида. Польза от антигипертензивной терапии была одинаковой у больных с АГ и нормальным уровнем АД. Результаты исследования PATS послужили основанием для внесения в рекомендации еще одного показания к применению индапамида – вторичной профилактики инсультов. Сходные данные о снижении частоты повторных инсультов и других ССО у пациентов с цереброваскулярными заболеваниями получены китайскими исследователями [40].
В исследовании PROGRESS [41] достоверное уменьшение вероятности развития повторного инсульта на 43% было получено только в группе пациентов, принимавших индапамид по 2,5 мг в комбинации с периндоприлом, тогда как в группе монотерапии периндоприлом достоверного снижения риска инсульта не отмечалось. Кроме этого, у индапамида выявлена способность позитивно влиять на нейродегенеративные процессы: на фоне его применения происходит подавление продукции бета-амилоида [42] и улучшение структуры мозговых артериол с ослаблением процессов гипертрофического ремоделирования сосудистой стенки [43]. При этом данный эффект не связан непосредственно с антигипертензивным действием препарата.
Индапамид не оказывает неблагоприятного воздействия на толерантность к глюкозе у пациентов с АГ СД [44]. В одном из последних метаанализов установлено, что значительное снижение ССО при использовании тиазидоподобных диуретиков перевешивает возможный риск ухудшения контроля глюкозы при СД 2 типа и впервые возникшего диабета у лиц, ранее им не страдавших [45].
В экспериментальном исследовании индапамид предотвращал развитие фиброза миокарда у молодых спонтанно гипертензивных крыс, но при этом не оказывал влияния на соотношение коллагена типа I к типу III. Антифибротический эффект индапамида не связан с метаболизмом оксида азота [46].
Нефропротективный эффект индапамида [47] наиболее отчетливо продемонстрирован в комбинации с периндоприлом на всех стадиях хронической болезни почек (ХБП) у пациентов с АГ и СД [48, 49].
На основании результатов 26 РКИ индапамид рассматривается как оптимальный диуретик для применения у пациентов с нормолипидемией или гиперлипидемией, поскольку увеличивает уровень холестерина липопротеинов высокой плотности и при этом не повышает уровень холестерина липопротеинов низкой плотности [50].
Таким образом, индапамид, имеющий доказанные органопротективные свойства, оптимальный метаболический профиль среди диуретиков и благоприятно влияющий на прогноз в рамках сердечно-сосудистого континуума, занимает прочные позиции как в моно-, так и в комбинированной терапии АГ [7, 32, 51].
Препарат Индап® (PRO.MED.CS Praha a. s., Чехия) является единственным генериком индапамида с наличием объективных доказательств терапевтической эквивалентности по отношению к двум формам выпуска оригинального индапамида [52]. Успешный опыт использования препарата Индап® в России на протяжении 25 лет, результаты широкомасштабных проектов с длительным наблюдением пациентов, проведенных практически во всех регионах России и других странах, свидетельствуют о его метаболической нейтральности, наличии органопротективных свойств и высокой антигипертензивной эффективности, в том числе и у мультиморбидных больных с АГ и СД 2 типа или метаболическим синдромом, пациентов гериатрического профиля. Индап® может эффективно и безопасно применяться как в сочетании с липидснижающими и антигипергликемическими препаратами, так и в комбинации с другими антигипертензивными средствами [7, 32, 51, 53–55].
ФИКСИРОВАННЫЕ КОМБИНАЦИИ: ПЛЮСЫ И МИНУСЫ
В представленном алгоритме (см. рис.) отмечено, что «двойная комбинация» АГП «предпочтительнее в одной таблетке». Вместе с тем в российских клинических рекомендациях «Артериальная гипертензия у взрослых» (2020) [4] отмечается, что фиксированные комбинации (ФК), хоть и повышают пациентский комплаенс, но не всегда присутствуют в лекарственных формулярах ЛПУ и перечнях жизненно важных лекарственных препаратов. Еще один сравнительный недостаток ФК – достаточно ограниченный их набор, не способный полностью заменить произвольные сочетания монопрепаратов [56].
В нашей стране к наиболее часто назначаемым ФК относятся различные комбинации блокатора РААС (ИАПФ или БРА) с ГХТ. Однако применение ФК с ГХТ не исключает возможности развития при длительном приеме у пациентов гиперурикемии и гипокалиемии [57–61]. В реальной клинической практике нередко возникает ситуация, когда пациенту, получающему фиксированную комбинацию РААС и диуретика, для достижения целевого уровня АД может потребоваться повышение дозы ИАПФ или БРА; при этом в большинстве случаев нежелательно повышение дозы ГХТ, вызывающего метаболические расстройства.
Важное преимущество комбинации ИАПФ и индапамида заключается в ее метаболической нейтральности. На сегодняшний день на российском фармрынке представлены ФК индапамида с только тремя ИАПФ – эналаприлом, периндоприлом и лизиноприлом, а вот его ФК с БРА отсутствуют [62].
В связи с этим в определенных клинических ситуациях у свободных комбинаций АГП, в частности, содержащих в своем составе тиазидоподобный диуретик индапамид, есть определенные преимущества. Появление на российском фармрынке новой формы выпуска препарата Индап®, делимой на 4 равные части (со специальной риской) таблетки индапамида 2,5 мг, повышает удобство его применения, создает условия для увеличения приверженности пациентов к лечению, дает возможность врачу в условиях реальной клинической практики титровать индапамид в 4 разных дозах (0,625; 1,25; 1,875; 2,5 мг) и комбинировать его с другими АГП. Это способствует профилактике дозозависимых нежелательных реакций за счет постепенного индивидуализированного подбора минимально эффективной дозы индапамида, что особенно актуально для пациентов старших возрастных групп, больных с ИБС и гемодинамически значимыми стенозами брахиоцефальных артерий, перенесших инсульт или транзиторную ишемическую атаку.
В качестве иллюстрации того, как коррекция комбинированной терапии АГ с включением в ее схему индапамида может улучшить результаты лечения, приведем конкретный клинический пример.
ОПИСАНИЕ КЛИНИЧЕСКОГО ПРИМЕРА
У пациентки Д., 64 лет, на приеме участкового терапевта, к которому она обратилась по поводу обострения хронического холецистита, было отмечено повышение АД до 160/85 мм рт.ст.
Из анамнеза известно, что повышение АД впервые было зафиксировано 5 лет назад. Пациентке были назначены АГП, которые она не принимала. При сильной головной боли и повышении АД иногда вместе с анальгетиками применяет короткодействующие ИАПФ, однако после их приема отмечает неприятные ощущения в области губ и кончика языка. Живет с матерью 82 лет, страдавшей АГ в течение 30 лет и нуждающейся в постоянном уходе: «ничего не помнит», «не всегда узнает близких», «включает газ и забывает кастрюлю на плите». Отец пациентки умер в возрасте 48 лет от инфаркта. Последние 2 мес почти ежедневно измеряет АД: систолическое АД находится в пределах 150–170 мм рт.ст., ДАД – 85–90 мм рт.ст.
При осмотре общее состояние удовлетворительное, рост 164 см, вес 69 кг, индекс массы тела 25,6 кг/м2, имеется пастозность голеней. При дополнительном обследовании выявлена умеренная гипертрофия левого желудочка (ГЛЖ), толщина интима-медиа (ТИМ) – 0,9 мм, скорость клубочковой фильтрации (СКФ) – 92 мл/мин. Креатинин, глюкоза крови, липидный профиль, уровень калия и мочевой кислоты в норме.
Учитывая степень сердечно-сосудистого риска, пациентке в соответствии с алгоритмом лечения АГ I–II стадий (см. рис.) была назначена «двойная комбинация» АГП в виде ФК азилсартана медоксомил (по 40 мг) + хлорталидон (по 12,5 мг) 1 раз/сут утром, а также рекомендованы диета с ограничением поваренной соли, животных жиров и легкоусвояемых углеводов, ежедневные пешие прогулки.
Через 14 дней АД приблизилось к целевым значениям, было отмечено лишь 2 эпизода его повышения до 155/85 мм рт.ст. Спустя еще 14 дней при достижении целевых значений АД пациентка на приеме отметила снижение работоспособности, утомляемость, снижение настроения и сонливость в дневные часы, которой раньше не было. В течении последней недели у нее появились ощущения покалывания, жжения, мурашек по коже верхних конечностей.
При лабораторном исследовании уровень калия в сыворотке крови составил 3,1 ммоль/л, мочевой кислоты – 440 мкмоль/л.
Принимая во внимание выявленные электролитные изменения, которые могли быть обусловлены приемом хлорталидона в составе ФК, пациентке была проведена коррекция антигипертензивной терапии: к монопрепарату азилсартана медоксомила (по 40 мг) добавлен индапамид в дозе 1,875 мг (3/4 таблетки Индап®) однократно утром.
Через 10 дней пациентка на визите отметила улучшение общего самочувствия, еще через 2 нед – возвращение прежнего уровня работоспособности, повышение настроения, отсутствие сонливости в дневное время, исчезновение ощущения покалывания, жжения, мурашек по коже. При контрольном лабораторном исследовании уровень калия в сыворотке крови составил 3,7 ммоль/л, мочевой кислоты – 340 мкмоль/л.
АД достигло устойчивых целевых значений и сохранялось на этом уровне весь период наблюдения в течение 6 мес, кризовых повышений не было. Через полгода при обследовании было отмечено отсутствие увеличения ГЛЖ, ТИМ оставалась прежних размеров, в зонах визуализации не наблюдалось формирование атером, СКФ составила 92 мл/мин. Нежелательных явлений терапии не было.
НИТРЕНДИПИН: АНТИГИПЕРТЕНЗИВНЫЙ ЭФФЕКТ И ОРГАНОПРОТЕКТИВНЫЕ СВОЙСТВА
Согласно алгоритму лечения АГ, при недостижении целевого уровня АД на «двойной комбинации» АГП рекомендуется рассмотреть «тройную комбинацию»: ИАПФ или БРА + диуретик + АК.
В качестве возможного препарата выбора из группы АК в рамках указанной «тройной комбинации» обоснованный интерес вызывает дигидропиридиновый блокатор медленных кальциевых каналов нитрендипин, обладающий выраженными церебропротективным и нефропротективным эффектами, что особенно важно для мультиморбидных пациентов с АГ и СД.
Клиническая эффективность нитрендипина в исследовании SYST-EUR (Systolic Hypertension in Europe) [63, 64] проявлялась не только выраженным антигипертензивным действием, но и значительным уменьшением риска возникновения инсульта (42%) и других фатальных и нефатальных сердечно-сосудистых событий, в том числе снижением на 33% риска развития протеинурии и на 64% почечной дисфункции. Проведенный ретроспективный анализ результатов SYST-EUR наглядно продемонстрировал, что наиболее выраженное позитивное влияние на прогноз нитрендипин оказывал у пациентов с СД: у них было отмечено снижение риска смерти от сердечно-сосудистых заболеваний на 70% (p=0,001), инсульта – на 69% (p=0,02), всех сердечно-сосудистых событий – на 62% (p=0,002) [65].
В проведенном позднее исследовании SYST-CHINA (Systolic Hypertension in China) были получены близкие результаты. Так, 2 года лечения нитрендипином привели к достоверному снижению инсульта на 38%, смертности от инсульта – на 58%, сердечно-сосудистой смертности – на 39%, общей смертности – на 39% по сравнению с группой плацебо [66].
Таким образом, нитрендипин на сегодняшний день можно рассматривать как единственный блокатор медленных кальциевых каналов с доказанным церебропротективным действием. В исследовании SYST-EUR его применение у пациентов основной группы сокращало риск возникновения деменции на 55% (с 7,4 до 3,3 случаев на 1000 пациентов, 43 против 21 случая; р <0,001) в сравнении с терапией пациентов контрольной группы. Данные этого исследования позволяют предполагать, что антигипертензивная терапия с включением нитрендипина может положительно повлиять на развитие не только сосудистой, но и дегенеративной деменции [63, 67].
Возможность влияния нитрендипина на ЦНС подтверждается тем, что он проходит гематоэнцефалический барьер (ГЭБ) и снижает распад нейромедиаторных моноаминов, нейротрансмиттеров, дефицит которых особенно выражен при дегенеративной деменции [68]. Нитрендипин хорошо накапливается в отделах головного мозга, наиболее подверженных изменениям при болезни Альцгеймера, – коре, таламусе и гиппокампе [69].
Отметим, что нейропротективный эффект нитрендипина некорректно проецировать на другие дигидропиридиновые блокаторы медленных кальциевых каналов. В экспериментальном исследовании только нитрендипин и отчасти нилвадипин (препарат, отсутствующий в России) хорошо проникали через ГЭБ и способствовали снижению содержания бета-амилоида. При этом другие дигидропиридиновые АК (амлодипин и нифедипин) не влияли на уровень бета-амилоида или даже повышали его [70, 71].
Длительное время в России препараты нитрендипина отсутствовали. Затем на фармрынке появилась ФК нитрендипин (по 20 мг) + эналаприл (по 10 мг) [62], основанная на результатах исследования SYST-EUR. Однако в исследовании SYST-EUR у пациентов с изолированной систолической АГ базовый препарат нитрендипин применялся в широком диапазоне доз 10–40 мг, а при необходимости для достижения целевого уровня АД комбинировался с эналаприлом по 5–20 мг и/или ГХТ по 12,5–25 мг. В инструкции по применению это ФК указан режим дозирования – не более 1 таблетки/ сут. Соответственно у части пациентов применение только данной ФК не позволит достичь целевого уровня АД и потребует дополнительной терапии [56].
С 2016 г. на российском фармрынке присутствует единственный монопрепарат нитрендипина – Нитремед® (PRO.MED.CS Praha a. s., Чехия). Он выпускается в таблетках 10 и 20 мг, режим его дозирования устанавливается индивидуально. Суточная доза препарата составляет 10–40 мг в 1–2 приема [72].
Наличие в арсенале врачей препарата Нитремед® позволяет оптимизировать профилактику цереброваскулярной патологии на фоне АГ [73]. Перспективной в этом плане видится комбинированная терапия Нитремед® + Индап®, в том числе в период пандемии COVID-19 [74]. Среди важных достоинств этих препаратов, наряду с эффективностью в реальной клинической практике, можно отметить их экономическую доступность для широкого круга пациентов с АГ [55].
ЗАКЛЮЧЕНИЕ
Таким образом, при лечении пациентов АГ I–II стадий в соответствии с алгоритмом, представленным в рекомендациях ESC/ESH 2018 г. [3] и Российских клинических рекомендациях 2020 г. [4], на первом шаге терапии оптимальным решением дилеммы «диуретик или АК» в рамках «двойной комбинации» с блокатором РААС может рассматриваться индапамид, сочетающий свойства тиазидного диуретика и АК. На втором шаге терапии в рамках «тройной комбинации» оптимальным представляется добавление к блокатору РААС и индапамиду дигидропиридинового АК нитрендипина.


