Тактика ведения больных с продолжающимися симптомами COVID-19 (U08.9)
Продолжающиеся симптомы COVID-19 – это симптомы, продолжающиеся от 4 до 12 нед и не объясненные альтернативным диагнозом после протоколированного обследования (U08.9). Обобщенные данные основных исследований симптомов COVID-19 (длительностью >4, 8, 12 нед) отражены в таблице 1.
Вопросы, рекомендуемые для пациента, перенесшего острую фазу COVID-19 с персистирующими респираторными симптомами.
1. Должны ли все пациенты с персистирующими респираторными симптомами после COVID-19 проходить обследование легких, включая бодилетизмографию, измерение диффузионной способности легких и анализ газов крови?
Ответ: все пациенты с персистирующими респираторными симптомами после COVID-19 должны пройти обследование легких, включая плетизмографию, измерение диффузионной способности и анализ газов крови (убедительная рекомендация, достигнут консенсус).
2. Должны ли пациенты после COVID-19, у которых имеются интерстициальные изменения, после исключения активной инфекции, проходить лечение системными стероидами?
Ответ: возможно использование стероидов в качестве подхода к лечению, если, например, можно диагностировать организующую пневмонию или бронхиолит и исключить острую инфекцию. Поскольку в настоящее время не опубликовано ни одного рандомизированного контролируемого исследования (РКИ), это остается индивидуальным решением, если функция легких нарушена, и у пациента остаются симптомы.
3. Должны ли пациенты после COVID-19 с признаками легочного фиброза получать специфические антифибротические препараты?
Ответ: не ясно, должны ли пациенты после COVID-19, имеющие признаки легочного фиброза, получать конкретные антифибротические препараты. Хотя результатов РКИ, позволяющих однозначно ответить на этот вопрос, по-прежнему нет, в настоящее время проходят соответствующие исследования с нинтеданибом (NCT04619680, NCT04541680, NCT04338802) и пирфенидоном (NCT04607928, NCT04653831).
Наиболее часто регистрируемые респираторные симптомы:
- боль в грудной клетке: дыхательный дискомфорт (ограничение вдоха, ощущение тяжести в груди);
- одышка;
- кашель;
- отделение мокроты.
Анамнез:
- наличие в анамнезе подтвержденного или вероятного случая острого COVID-19;
- характер и тяжесть предыдущих и текущих симптомов;
- время появления и продолжительность симптомов с момента начала острого COVID-19;
- наличие хронических бронхолегочных заболеваний в анамнезе.
Физикальное обследование: необходимо оценить общее состояние больного, измерить температуру тела, провести аускультацию и перкуссию легких, измерить частоту дыхательных движений (ЧДД), определить SpO2.
Оценка одышки: при наличии у пациента одышки рекомендуется провести оценку одышки и толерантности к физической нагрузке по шкале Борга, тест с 3- или 6-минутной ходьбой (3МWT или 6MWT) либо 1-минутный тест «сесть–встать» (1STST) сообразно возможностям пациента.
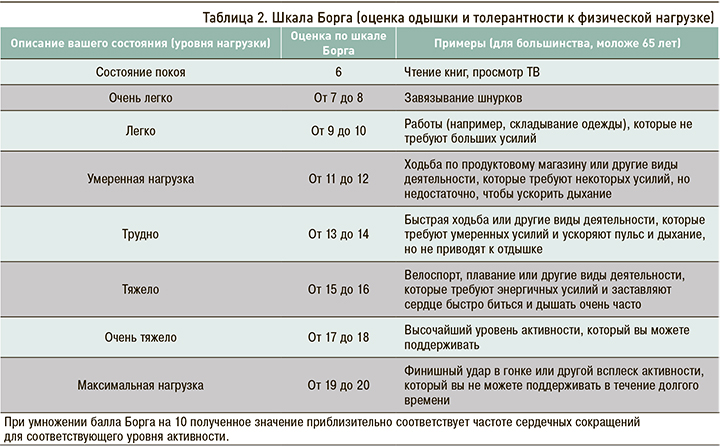
Шкала Борга – субъективный способ определения уровня нагрузки. Она разбита от 6 до 20 баллов (табл. 2) как ориентир по сердечному ритму: при умножении балла Борга на 10, полученное значение приблизительно соответствует частоте сердечных сокращений (ЧСС) для соответствующего уровня активности. Тест с 6-минутной ходьбой (6MWT) выполняется при 3- или 6-минутной ходьбе по внутреннему коридору в лечебном учреждении. При необходимости во время теста пациенту разрешается остановиться. До и после теста оцениваются ЧДД, SpO2 и ЧСС. При появлении неприятных ощущений в грудной клетке и/или снижении SpO2 до 88% тест прекращается.
1-минутный тест «сесть–встать» (1STST) проводится со стулом стандартной высоты (46 см) без подлокотников, установленным у стены. Пациент должен сидеть на стуле вертикально, колени и бедра должны быть согнуты под углом 90°, ступни поставлены на пол на ширине бедер, а руки положены на бедра и оставаться неподвижными. Пациента просят повторить вставание в вертикальном положении, а затем сесть в том же положении с индивидуальной скоростью (безопасной и удобной) как можно больше раз в течение 1 мин. Пациента необходимо проинструктировать не использовать руки в качестве опоры при вставании или сидении. Разрешается отдыхать в течение 1-минутного периода. Регистрируется количество повторов.
Модифицированная шкала Борга со шкалой от 0 до 10 баллов (табл. 3) используется для оценки одышки и утомляемости непосредственно до и после теста. Также проводится пульсоксиметрия, измерение ЧСС до и после теста с 6-минутной ходьбой либо 1-минутным тестом «сесть–встать». Уровень десатурации ≥4% считается клинически значимым для этого исследования.

Всем пациентам с продолжающимся симптоматическим COVID-19 рекомендуется проведение пульсоксиметрии с измерением SpO2 для выявления признаков дыхательной недостаточности (ДН).
Комментарии: пульсоксиметрия рекомендуется в качестве простого и надежного скринингового метода, позволяющего выявлять пациентов с ДН. Необходимо проводить измерение в динамике и записывать параметры сатурации не только в покое, но и при нагрузке (ходьба по комнате).
Всем пациентам с продолжающимся симптоматическим COVID-19 рекомендуется проведение исследование функции внешнего дыхания, бодиплетизмографии и определения диффузионной способности легких (DLCO).
Комментарии: наиболее частым функциональным нарушением респираторной системы после COVID-19 является нарушение DLco, что влияет на качество жизни пациентов, служит причиной одышки, слабости и утомляемости.
Лечение
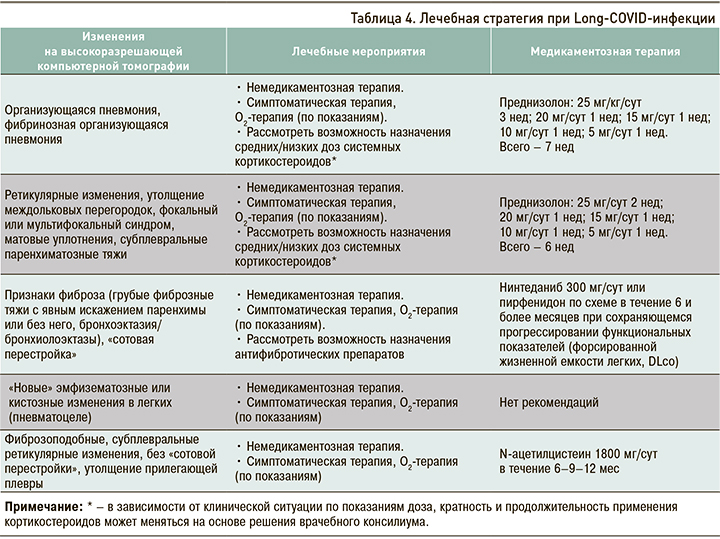
Лечебная стратегия при Long-COVID-инфекции отражена в таблице 4.
Респираторная поддержка: при снижении SpO2 менее 93% рекомендовано начало оксигенотерапии при помощи маски или назальных канюль с потоком кислорода 5–10 л в минуту до достижения показателя SpO2 >95%. Сочетание оксигенотерапии (стандартной или высокопоточной) с положением пациента лежа на животе в прон-позиции не менее 12–16 ч в сутки приводит к улучшению оксигенации.
Методы немедикаментозной терапии
1. Инспираторный тренинг: дыхательные упражнения при коронавирусном поражении легких вследствие повреждения альвеол для улучшения вентиляционной способности легких, улучшения механики дыхания, работы дыхательной мускулатуры.
2. Вибрационно-перкуссионная терапия: метод сочетает механическое воздействие высокочастотной вибрацией и компрессией на грудную клетку.
3. Интрапульмональная перкуссионная вентиляция.
4. Осцилляторные РЕР-тренажеры.
Комментарий: параметры использования респираторных тренажеров и устройств подробно изложены в следующих рекомендациях: Малявин А.Г., Адашева Т.В., Бабак С.Л. с соавт. Физиотерапия и кислородотерапия пациентов с дыхательными расстройствами и нарушением мукоцилиарного клиренса. Клинические рекомендации РНМОТ. Приложение к журналу «Терапия», 2019; 5: 1–152; Малявин А.Г., Адашева Т.В., Бабак С.Л., Губернаторова. Е.Е., Уварова О.В. Медицинская реабилитация больных, перенесших COVID-19 инфекцию. Методические рекомендации. Приложение к журналу «Терапия», 2020, №5: с. 1–48.
5. Индивидуальные рекомендации по питанию – персонифицированные:
- витамин С;
- витамин D;
- витаминно-минеральные комплексы;
- мультивитамины + омега-3 полиненасыщенные жирные кислоты;
- нутритивная поддержка;
- разработка индивидуальной диеты с учетом наличия сопутствующей патологии.
Симптоматическая терапия:
- противокашлевые препараты при непродуктивном кашле (у 80% больных – кашель непродуктивный);
- мукоактивные препараты при продуктивном кашле (у 8% пациентов наблюдается кашель с продукцией мокроты; как правило, это пациенты, перенесшие тяжелый COVID-19 с присоединением внутрибольничной бактериальной инфекции);
- бронхолитические средства при наличии обструктивных изменений.
Показания к длительной кислородотерапии в домашних условиях
1. Абсолютные: SрO2 ≤88% (задача: SpO2 >90%; титрование потока: при нагрузке + 1 л/мин, во время сна – + 1 л/мин).
2. Относительные:
- SрO2 89 % (при наличии особых условий: гематокрит (Ht) >55%, эритроцитоз, легочная гипертензия, сердечная недостаточность);
- SрO2 ≥90 % (нет показаний за исключением особых условий):
- десатурация при нагрузке;
- десатурация во время сна (титровать дозу во время сна: 8 ч – SpO2 >90%);
- болезнь легких с тяжелым диспноэ.
Комментарий: подробные показания к назначению длительной кислородотерапии и неинвазивной вентиляции изложены в публикации: Бабак С.Л., Горбунова М.В., Малявин А.Г. Алгоритм кислородотерапии и неинвазивной вентиляции легких у пациентов с COVID-19. Терапия. 2020; 5: 117–124.
В зависимости от клинической ситуации по показаниям доза, кратность и продолжительность применения кортикостероидов может меняться на основе решения врачебного консилиума.
По назначению антикоагулянтов, как парентеральных, так и пероральных, в постковидный период доказательной базы в настоящее время недостаточно. Однако в случае сохранения повышенных показателей D-димера, массивных изменений на компьютерной томографии, дыхательной недостаточности, требующей оксигенотерапии, целесообразно продолжить применение антикоагулянтов – низкомолекулярных гепаринов (подкожно), пероральных антикоагулянтов (апиксабана, ривароксабана) в профилактических дозах.
Кашель у пациентов с продолжающимся симптоматическим COVID-19, как-правило, непродуктивный. Для его купирования целесообразно назначение противокашлевых препаратов – бутамирата, леводропропизина.
Бутамирата цитрат (Синекод), являясь ненаркотическим противокашлевым препаратом центрального действия, избирательно действует на кашлевой центр, не подавляя дыхательный центр. Он не вызывает привыкания, может использоваться длительно без потери эффективности, разрешен к приему у пациентов с гипергликемией, не имеет межлекарственных взаимодействий.
Если у больного есть жалобы на продуктивный кашель (что, как правило, наблюдается у больных, перенесших тяжелое течение COVID-19 с присоединением нозокомиальной бактериальной инфекции), рекомендовано использование мукоактивных препаратов – амброксола, карбоцистеина, N-ацетилцистеина, эрдостеина. N-ацетилцистеин характеризуется комплексным действием – муколитическим, антиоксидантным и противовоспалительным. При необходимости назначения N-ацетилцистеина с антибиотиками, следует соблюдать интервал между назначениями препаратов не менее 2 ч.
Возможно также применение мукоактивных лекарственных средств комплексного действия на основе экстрактов лекарственных растений. Наиболее изученным препаратом такого рода является Бронхипрет, содержащий экстракты тимьяна, листьев плюща и корня первоцвета. Препарат обладает отхаркивающим, муколитическим, противовоспалительным, антибактериальным и противовирусным действием.
В условиях гипоксии определенную положительную роль могут сыграть препараты метаболического антиоксидантного действия. Полидигидроксифенилентиосульфонат натрия (Гипоксен®) – антигипоксантное и антиоксидантное средство. Препарат облегчает проникновение кислорода в клетки вследствие снижения сродства гемоглобина к O2 и восстанавливает нарушенные процессы образования энергии (АТФ) в митохондриях. Путем шунтирования 1-го и 2-го комплексов дыхательной цепи в митохондриях он поддерживает и повышает уровень тканевого дыхания и аэробных процессов, нивелирует негативные последствия гипоксии, способствует быстрому окислению накопленных восстановительных эквивалентов НАДФН2 и оптимизирует работу митохондрий, а также ингибирует свободно-радикальные процессы.
Включение препарата Гипоксен в терапию пациентов с пневмониями сокращает сроки выздоровления, ускоряет нормализацию показателей периферической крови, укорачивает продолжительность выявления влажных хрипов и одышки. Положительный эффект отмечен и у больных с острыми бронхитами, бронхиальной астмой, саркоидозом. Гипоксен повышает эффективность терапии у пациентов с хронической обструктивной болезнью легких (ХОБЛ) среднетяжелого и тяжелого течения. На фоне добавления Гипоксена к терапии установлена:
- положительная динамика в снижении выраженности десатурации (по пульсоксиметрии);
- положительная динамика к 6 мес терапии по индексу транзиторной одышки;
- положительная динамика, проявляющаяся в уменьшении выраженности одышки после выполнения нагрузки (по шкале Борга);
- увеличилась толерантность к физической нагрузке по 6-минутному шаговому тесту;
- положительная динамика в ответ на физическую нагрузку по кардиореспираторному тесту;
- улучшение качества жизни, связанного со здоровьем (по Респираторному вопроснику госпиталя Святого Георгия).
Этилметилгидроксипиридина малат (Этоксидол) – антиоксидантное средство, которое активирует супероксиддисмутазу и каталазу, ингибирует свободно-радикальные процессы, редуцирует оксидантный стресс, оказывает мембранопротекторное, антигипоксическое (повышает напряжение и уровень кислорода, восстанавливая активность синтеза макроэргического метаболита 2,3-дифосфоглицерата и увеличивая диссоциацию оксигемоглобина), антиишемическое (улучшает кровоток в зоне ишемии, ограничивает зону ишемического повреждения, уменьшает агрегацию тромбоцитов, улучшает реологические свойства крови и микроциркуляцию) действие, улучшает метаболизм (повышает уровень АТФ) в головном мозге, сердце и других органах, повышает устойчивость организма к стрессу, имеет ноотропное действие.
Благодаря антиоксидантному, антиишемическому и антигипоксическому действию, Этоксидол увеличивает метаболизм, уменьшает ишемические, гипоксические неврологические и сердечно-сосудистые нарушения, в том числе у пациентов с коронавирусной инфекцией.
Назначение Этоксидола при COVID-19 основано на блокаде образования метаболитов окислительного стресса, нейтрализации активных форм кислорода и повышении концентрации (нормализации) 2,3-дифосфоглицерата: он нормализует насыщенность крови кислородом, тем самым улучшает оксигенацию. Дополнительно препарат увеличивает концентрацию фоллистатина, способствуя ограничению воспалительного процесса в легких, снижая концентрацию и активность активина-А путем его связывания с фоллистатином и уменьшая концентрацию провоспалительных цитокинов (ИЛ-1β и ИЛ-6) и развитие «цитокинового шторма» и воспаления.
Препарат Цитофлавин (инозин + никотинамид + рибофлавин + янтарная кислота) за счет комплексного воздействия на метаболизм клетки усиливает интенсивность аэробного гликолиза, увеличивает устойчивость мембран клеток к ишемии. Обладая антиоксидантным и антигипоксантным действием, препарат оказывает положительное влияние на энергообразование в клетке, уменьшает продукцию свободных радикалов и восстанавливает активность ферментов антиоксидантной защиты, активирует окислительно-восстановительные ферменты дыхательной цепи митохондрий, ресинтез макроэргов, способствуя утилизации глюкозы и жирных кислот, что позволяет сделать вывод о целесообразности его использования при реабилитации пациентов с постковидным синдромом.
Цитофлавин может влиять на ключевое патофизиологическое звено полиорганной недостаточности при новой коронавирусной инфекции за счет того, что усиливает тканевое дыхание и восстанавливает митохондриальное звено энергетического обмена клетки.
Проведен анализ клинической практики применения лекарственных препаратов на основе сукцинатов у пациентов с тяжелым течением новой коронавирусной инфекции. Применение Цитофлавина позволяло положительно воздействовать на обратимые функциональные изменения ЦНС, что давало возможность активизировать пациента, повышало успех прекращения респираторной поддержки, ранней реабилитации и ускоряло выздоровление.
Для стимуляции мукозального иммунитета рекомендуется применение препарата ОМ-85 (Бронхо-Мунал). Помимо активации противоинфекционной защиты, он стимулирует Тreg-зависимые противовоспалительные механизмы. Применение ОМ-85 в комплексном лечении респираторной инфекции направлено на снижение риска вторичной бактериальной инфекции и потребности в антибиотиках. Также препарат используется с целью неспецифической профилактики респираторных инфекций и обострений хронических заболеваний дыхательных путей, индуцированных вирусами и бактериями. При COVID-19 ОМ-85 следует рекомендовать как средство профилактики рецидивирующих респираторных и вторичных бактериальных инфекций.
Особую проблему при Long-COVID-19 может представлять относительно редкое формирование в продуктивную фазу воспаления тонкостенных легочных кист вследствие ремоделирования ткани легких (рис. 1, 2). Как правило, они не требуют специального вмешательства, поскольку имеют тенденцию обратного развития и практически никогда не нагнаиваются.
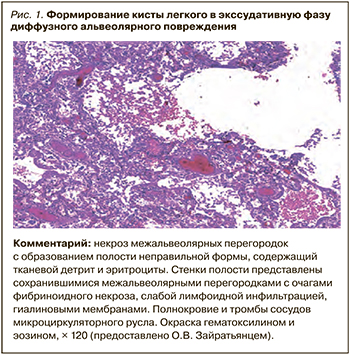
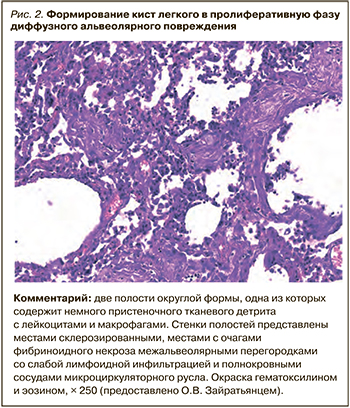
Тем не менее при субплевральном расположении кист нередко развиваются пневомторакс и пневмомедиастинум. Лечебная тактика в этом случае сводится к дренированию плевральной полости с целью формирования открытого пневмоторакса и спонтанного закрытия дефекта легочной ткани. В ряде случаев необходима активная аспирация из дренажа. Радикальное хирургическое вмешательство (торакоскопия, плевродез или диссекция кист) крайне ограничено и показано только при множественных рецидивах пневмоторакса и неэффективности консервативной терапии.
Пациентам с признаками функционального дефицита легких, в особенности при персистирующих респираторных симптомах и/или выраженных остаточных изменениях в легочной ткани, для улучшения показателей функции внешнего дыхания, физического состояния пациентов и клинической картины, в том числе для снижения выраженности легочной одышки, повышения уровня сатурации и толерантности к физической нагрузке, разрешения остаточных изменений в легких, рекомендуется назначение препарата Лонгидаза® (бовгиалуронидаза азоксимер) внутримышечно курсом 15 инъекций 1 раз в 5 дней. Согласно инструкции по медицинскому применению препарата, возможен общий курс до 25 введений: после первых 15 инъекций 1 раз в 5 дней следующие 10 инъекций проводятся в режиме 1 раз в 10 дней.
Лонгидаза® вызывает гидролиз гиалуроновой кислоты, снижая ее избыточное количество, затрудняющее газообмен, и оказывает антифиброзное действие. Препарат безопасен и хорошо переносится пациентами, что доказано в клинических исследованиях и в период пострегистрационного использования. Эффективность применения препарата у пациентов, перенесших COVID-19, показана в многоцентровом открытом проспективном исследовании DISSOLVE.
Для купирования выраженных симптомов заложенности носа или ринореи целесообразно применение назальных деконгестантов короткими курсами до 7 дней. Монопрепараты ксилометазолина и/или оксиметазолина (Отривин) позволяют уменьшить отек слизистой оболочки полости носа и восстановить проходимость воздушных путей в короткие сроки. Для устранения ринореи эффективна комбинация деконгестанта ксилометазолина с секретолитиком ипратропия бромидом (Отривин Комплекс).



