Диагностика
1
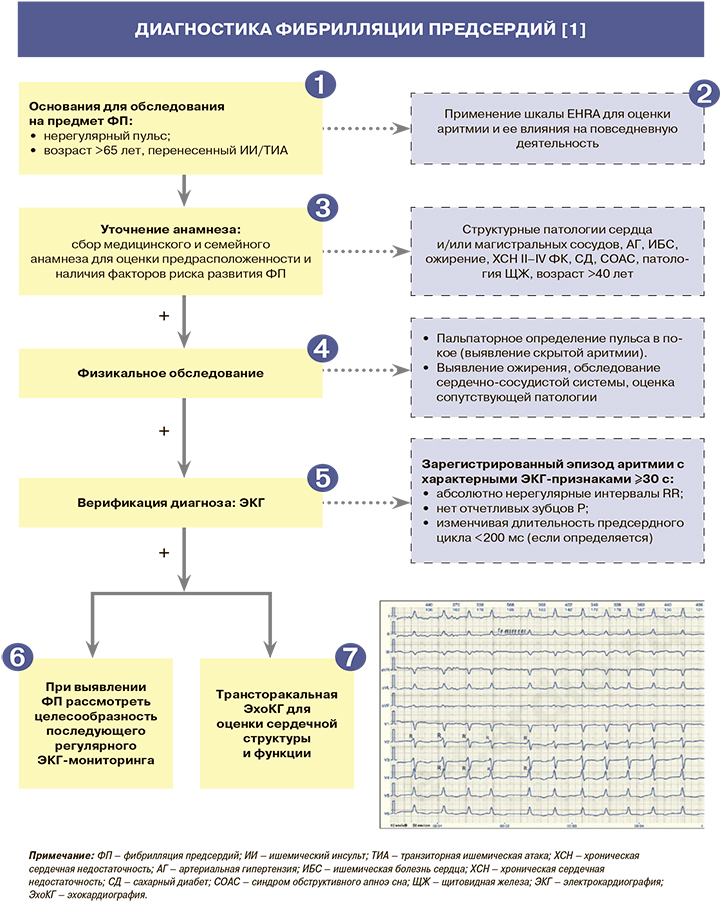
• Жалобы при фибрилляции предсердий (ФП) довольно нетипичны и могут встречаться при других наджелудочковых аритмиях и прочих патологиях сердечно-сосудистой системы. Наиболее частые из них: ощущения сердцебиения, одышки, тяжести в груди, нарушения сна, сонливости, слабости, психосоциальных расстройств.
У ряда пациентов отмечается полное отсутствие какой-либо симптоматики, и первым проявлением ФП могут быть ишемический инсульт (ИИ) или транзиторная ишемическая атака (ТИА) [1].
• Скрининг ФП рекомендован пациентам старше 65 лет (с использованием кратковременной записи ЭКГ либо пальпаторного исследования пульса или аускультации сердца): уровни достоверности доказательств согласно рекомендациям Европейского общества кардиологов (EОК) – IВ (уровень убедительности рекомендаций (УУР) – B, уровень достоверности доказательств УДД – 3) [1].
• Скрининг ФП рекомендуется пациентам с ТИА или ИИ (посредством регистрации кратковременной ЭКГ с последующим мониторированием ЭКГ в течение как минимум 72 ч): ЕОК – IВ (УУР – С, УДД – 4) [1].
2
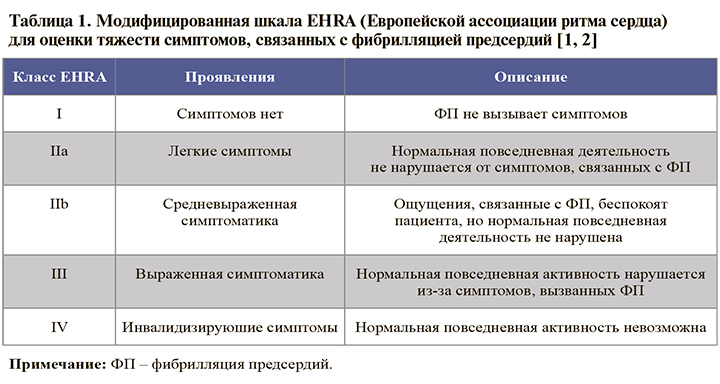
В клинической практике для оценки выраженности симптомов аритмии и ее влияния на повседневную деятельность рекомендуется использование модифицированной шкалы EHRA: EОК – IВ (УУР – С, УДД – 4) [1]. Применение этой шкалы (табл. 1) целесообразно для последующего назначения лечения, ориентированного на снижение симптоматики и длительного наблюдения за качеством жизни пациентов.
3
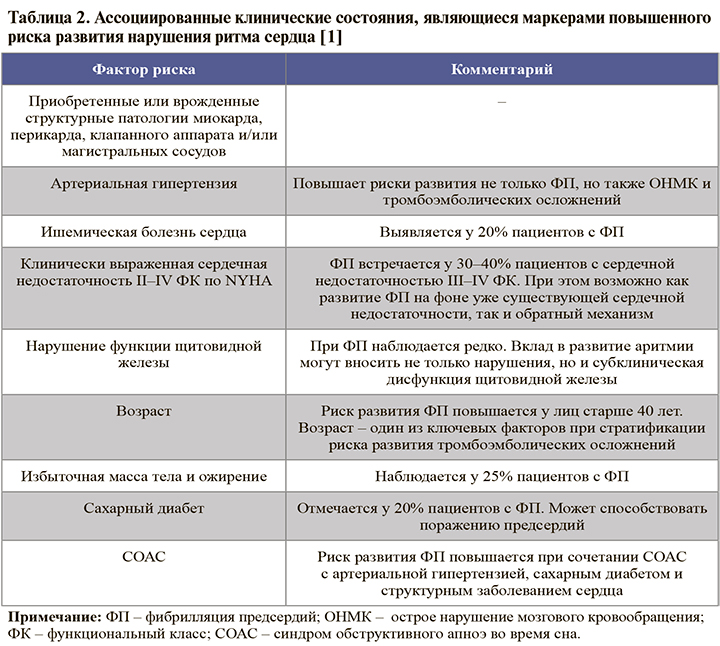
Рекомендуется собирать полный медицинский и семейный анамнез для оценки семейной предрасположенности и наличия факторов риска развития ФП: ЕОК – IC (УУР – C, УДД – 5) [1]. Информация о факторах риска заболевания отражена в таблице 2.
4
• Всем больным ФП рекомендуется пальпаторное определение пульса в покое для выявления скрытой аритмии: ЕОК – нет (УУР – С, УДД – 5) [1].
• У всех пациентов с ФП рекомендуется выполнение тщательного объективного обследования, определения антропометрических данных для выявления избыточной массы тела/ожирения, полное обследование сердечно-сосудистой системы и выявление сопутствующей патологии: ЕОК – нет (УУР – С, УДД – 5) [1].
5
• С целью подтверждения ФП всем пациентам с подозрением на ФП рекомендовано выполнение электрокардиографии (ЭКГ): ЕОК – IВ (УУР – C, УДД – 5) [1].
• Для установления диагноза ФП необходимо наличие зарегистрированного эпизода аритмии с характерными ЭКГ-признаками длительностью ≥30 с. Для ФП характерны [1]:
– абсолютно нерегулярные интервалы RR (не регистрируется при сочетании ФП и АВ-блокады III степени – синдроме Фредерика);
– отсутствие отчетливых зубцов Р на ЭКГ. В отдельных отведениях, обычно в V1, иногда определяется некоторая регулярная электрическая активность предсердий;
– длительность предсердного цикла (если определяется), т.е. интервала между двумя последовательными возбуждениями предсердий (F-волн), обычно изменчива и составляет менее 200 мс, что соответствует частоте предсердного ритма более 300/мин.
6
• При наличии жалоб на эпизоды неритмичного сердцебиения и при отсутствии документированных эпизодов ФП при записи ЭКГ рекомендуется выполнение суточного мониторирования по Холтеру для исключения коротких пароксизмов ФП: ЕОК – нет (УУР – С, УДД – 5) [1]. При наличии эпизода наджелудочковой тахикардии длительностью более 30 сек с характерными ЭКГ-признаками ФП пациентам должен быть выставлен соответствующий диагноз и приняты все надлежащие меры по профилактике повторных пароксизмов и тромбоэмболических осложнений.
• Пациентам на антиаритмической терапии для оценки безопасности и эффективности лечения рекомендуется регулярная ЭКГ в 12 отведениях: ЕОК – IC (УУР – С, УДД – 5) [1].
• Выполнение длительного мониторирования ЭКГ рекомендовано симптомным пациентам для оценки адекватности контроля частоты и уточнения взаимосвязи между приступами ФП и жалобами: ЕОК – IIaC (УУР – С, УДД – 5) [1].
• Для выявления бессимптомной ФП при криптогенном инсульте рекомендовано оценить возможность дополнительного мониторинга ЭКГ с применением неинвазивных мониторов или имплантируемых петлевых регистраторов: ЕОК – IIaВ (УУР – А, УДД – 2) [1].
7
Всем пациентам с ФП рекомендовано проведение трансторакальной эхокардиографии для оценки сердечной структуры и функции: ЕОК – IС (УУР – С, УДД – 5) [1].
Лечение
1
• Важнейшей проблемой для пациентов с ФП является высокий риск ИИ и системных тромбоэмболий, которые чаще всего имеют кардиоэмболическое происхождение, что связано с тромбообразованием в ушке, реже – в полости левого предсердия.
В структуре всех тромбоэмболических осложнений у пациентов с ФП более 90% приходится на ИИ. Среди ИИ наиболее плохой прогноз имеет кардиоэмболическая форма заболевания, что обусловлено высокой смертностью и развитием стойкой инвалидизации [1].
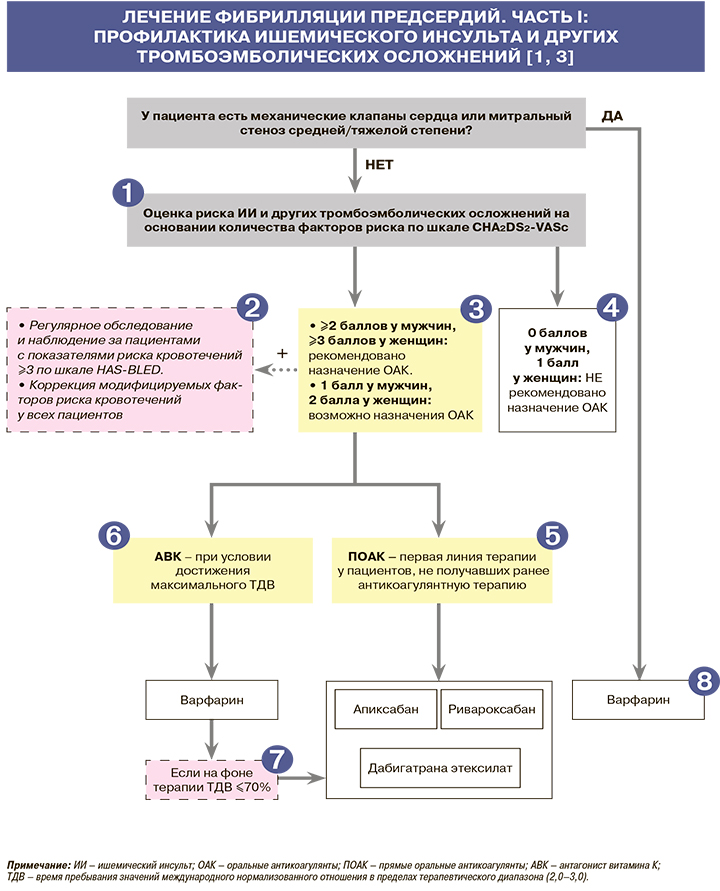
• Для оценки риска тромбоэмболических осложнений (ИИ, ТИА и системных тромбоэмболий) всем пациентам с ФП, не связанной с поражением клапанов сердца, рекомендовано использовать шкалу CHA2DS2-VASc (табл. 3): ЕОК – IA (УУР – B, УДД – 2) [1].

2
Всем пациентам перед назначением антитромботической терапии рекомендовано оценивать риск кровотечения, выявлять немодифицируемые и модифицируемые факторы риска кровотечения: ЕОК – IIaB (УУР – С, УДД – 5) [1].
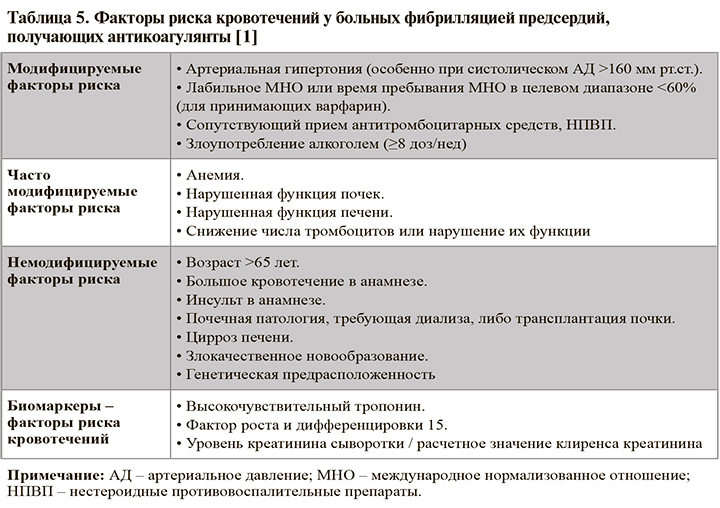
• Для оценки риска кровотечений предложено использовать несколько шкал, наибольшее распространение из них имеет шкала HAS-BLED (табл. 4). При этом расчетный высокий риск кровотечений не должен являться единственным ограничением к назначению антикоагулянтов. В первую очередь необходимо провести обследование пациента, направленное на выявление потенциальных источников кровотечений (табл. 5), и скорректировать модифицируемые факторы риска, а при наличии немодифицируемых факторов выбрать антикоагулянт, наиболее подходящий пациенту в соответствии с клиническими характеристиками (сопутствующие заболевания, риск инсульта, предпочтительный режим дозирования).

3
• Постоянный прием оральных антикоагулянтов (ОАК) с целью профилактики тромбоэмболических осложнений рекомендован мужчинам с суммой баллов по шкале CHA2DS2-VASc ≥2 и пациентам женского пола с суммой баллов по шкале CHA2DS2-VASc ≥3: ЕОК – IA (УУР – А, УДД – 2) [1].
• Назначение ОАК с целью профилактики ТЭО рекомендовано мужчинам с суммой баллов по CHA2DS2-VASc = 1 и женщинам с суммой баллов по CHA2DS2-VASc = 2 с учетом индивидуальных особенностей и предпочтений пациента: ЕОК – IIaB (УУР – B, УДД – 2) [1, 5].
• Основное преимущество ОАК, по данным рандомизированных клинических исследований, показано в первую очередь у пациентов с высоким риском тромбоэмболических осложнений (CHA2DS2-VASc ≥2 у мужчин и CHA2DS2-VASc ≥3 у женщин). Истинная частота инсульта и системных эмболий у пациентов мужского пола, имеющих 1 балл по CHA2DS2-VASc, и у женщин с 2 баллами по этой шкале значительно варьирует и составляет от 0,5 до 2,8% в год. Этот факт, наряду с оценкой индивидуального риска кровотечений, необходимо учитывать, принимая решение о назначении ОАК данной категории пациентов [1].
4
Не рекомендовано назначение антикоагулянтной терапии мужчинам и женщинам с фибрилляцией предсердий при отсутствии факторов риска тромбоэмболических осложнений: ЕОК – IIIB (УУР – С, УДД – 4) [1].
5
• Пациентам с неклапанной ФП, не получавшим ранее антикоагулянтную терапию, в качестве препаратов первой линии рекомендовано назначение прямых оральных антикоагулянтов (ПОАК) – апиксабана или дабигатрана этексилата или ривароксабана (при отсутствии противопоказаний к их назначению): ЕОК – IA (УУР–А, УДД – 1) [1]. НОАК, в отличие от антагонистов витамина K (варфарина), обладают предсказуемым эффектом (срок начала и пика действия) без необходимости регулярного мониторинга антикоагуляции [6].
• Рекомендовано назначать полную дозу ПОАК как обеспечивающую максимальную защиту от инсульта (за исключением специальных показаний): апиксабан по 5 мг 2 раза/сут, дабигатрана этексилат по 150 мг 2 раза/сут, ривароксабан по 20 мг 1 раз/сут: ЕОК – нет (УУР – А, УДД – 1) [1]. Специальные показания к приему пониженных доз ПОАК при ФП отражены в таблице 6.

6
• В случае назначения антагонистов витамина K (варфарина) рекомендовано достижение максимального времени пребывания значений международного нормализованного отношения (МНО) в пределах терапевтического диапазона (2,0–3,0), которое следует регулярно оценивать: ЕОК – IA (УУР – А, УДД – 2) [1].
• Во время подбора индивидуальной дозы варфарина необходимо контролировать значение МНО каждые 3–4 дня до получения двух последовательных близких его значений в пределах целевого диапазона. Это позволяет говорить о достижении терапевтического диапазона антикоагуляции. В дальнейшем контроль МНО необходимо осуществлять 1 раз в 4–6 нед. В случае развития чрезмерной гипокоагуляции, изменения дозы варфарина или назначения сопутствующей терапии, способной повлиять на уровень МНО, его значение необходимо определить через 4–5 дней для подтверждения пребывания в терапевтическом диапазоне.
• Необходимо стремиться к поддержанию МНО в целевом диапазоне 2,0–3,0 у всех (в том числе у пожилых) пациентов. Оптимальным считается время пребывания значений МНО в терапевтическом диапазоне ≥65%. Принятые ранее значения МНО 1,6–2,2 для пожилых пациентов в настоящее время считаются неоправданно низкими в связи с двукратным увеличением риска инсульта при МНО <2,0.
• К более низким значениям МНО в пределах целевого диапазона (2,0–2,5) следует стремиться при приеме варфарина в комбинации с ацетилсалициловой кислотой или клопидогрелом или при возобновлении терапии после кровотечения.
7
Если на фоне терапии варфарином значения МНО часто находятся за пределами целевого диапазона (время в терапевтическом диапазоне ≤70%), рекомендовано назначение ПОАК (если нет противопоказаний): ЕОК – IIaA (УУР А, УДД 1) [1]. Принципы смены антикоагулянта у пациентов, получающих варфарин (при необходимости), отражены в таблице 7.

8
• Пациентам с митральным стенозом умеренной или тяжелой степени либо с механическим искусственным клапаном сердца с целью профилактики тромбоэмболических осложнений рекомендованы только антагонисты витамина К (варфарин): ЕОК – IB (УУР – С, УДД – 4) [1].
• ПОАК не рекомендованы для профилактики тромбоэмболических осложнений пациентам с механическими клапанами сердца: ЕОК – IIIB (УУР – С, УДД – 4) [1].
• ПОАК не рекомендованы для профилактики тромбоэмболических осложнений пациентам с умеренным и тяжелым митральным стенозом: ЕОК – IIIC (УУР – А, УДД – 1) [1].
• В случае назначения варфарина пациентам с митральным стенозом умеренной или тяжелой степени терапевтический диапазон МНО составляет 2,0–3,0; у пациентов с механическим протезом клапана сердца целевое МНО определяется позицией и типом протеза. Длительность терапии варфарином у пациентов с ФП без ревматического поражения сердца после установки биопротеза составляет 3 мес, после чего допустимо назначение ПОАК [1].
• Рутинное сочетание ОАК c ингибиторами агрегации тромбоцитов повышает риск кровотечений, поэтому не рекомендовано пациентам с ФП при отсутствии дополнительных показаний: ЕОК – IIIB (УУР – А, УДД – 3) [1].
9
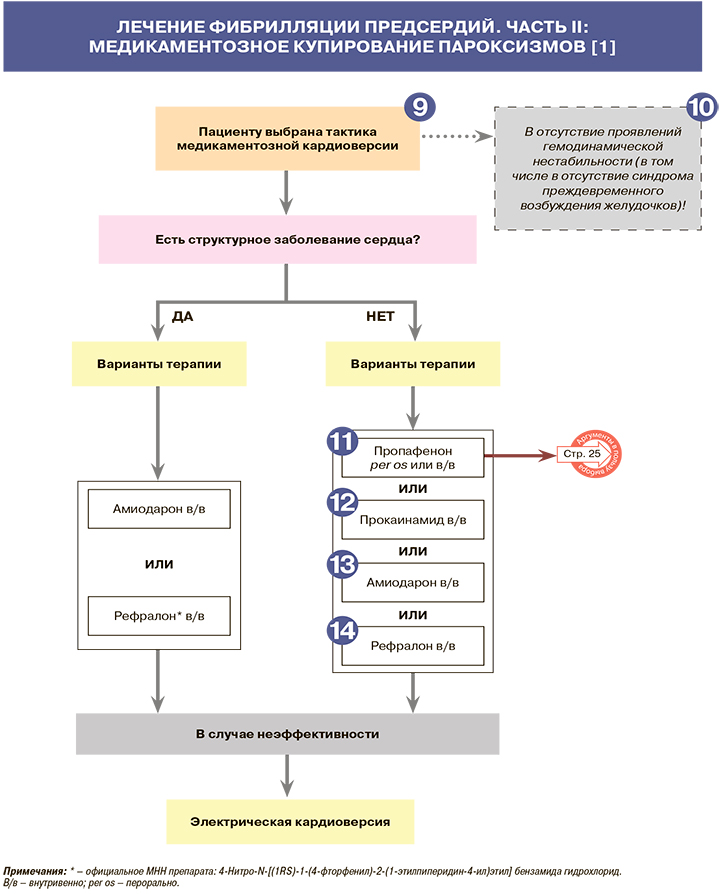
• Для планового восстановления ритма у пациентов с ФП рекомендуется применение медикаментозной или электрической кардиоверсии: ЕОК – IIaC (УУР – В, УДД – 3) [1]. Выбор способа восстановления ритма осуществляется с учетом клинической картины заболевания (длительности эпизода аритмии, приема антиаритмических препаратов, анамнестических сведений о предшествовавших безопасных и эффективных методах восстановления ритма, наличия органического поражения сердца), предпочтений врача и пациента. Лекарственные препараты, применяющиеся для восстановления синусового ритма, позволяют не только купировать ФП, но и предотвратить ранние рецидивы аритмии. Большинство из них (за исключением Рефралона) эффективны лишь при недавно развившихся эпизодах аритмии (длительностью менее 48 ч) [1].
• Целью антиаритмической терапии является уменьшение симптомов ФП, но не улучшение прогноза здоровья и жизни. Эффективная антиаритмическая терапия приводит к уменьшению, а не к полному исчезновению рецидивов ФП. Если один антиаритмический препарат (ААП) оказывается неэффективным, клинически приемлемый результат может быть достигнут при помощи другого препарата [1].
• Аритмогенные или экстракардиальные побочные эффекты ААП встречаются довольно часто. В первую очередь определять выбор ААП должна безопасность, а не эффективность должна [1].
• Пациентам, которым проводится медикаментозная кардиоверсия, рекомендовано непрерывное медицинское наблюдение и мониторирование ЭКГ во время введения препарата и после его завершения (в течение половины периода полувыведения) для обеспечения своевременного выявления возможного проаритмического действия (например, желудочковых тахиаритмий), брадикардий, остановки синусового узла или атриовентрикулярной блокады [1].
10
• При проявлениях гемодинамической нестабильности (в том числе наличии синдрома преждевременного возбуждения желудочков) пациентам с ФП рекомендована экстренная электрическая кардиоверсия: ЕОК – IB (УУР – С, УДД – 4) [1].
11
• Рекомендовано внутривенное введение пропафенона (ААП IC класса) для купирования ФП продолжительностью до 48 ч у пациентов, не имеющих противопоказаний к применению препарата: ЕОК – 1A (УУР – А, УДД – 2) [1, 7, 8]. Режим внутривенного введения препарата: 1,5–2 мг/кг в течение 10 мин. При отсутствии терапевтического эффекта ту же дозу можно ввести повторно через 90–120 мин через 1–2 ч; максимальная суточная доза – 560 мг [1].
• С целью восстановления синусового ритма пропафенон может быть рекомендован для однократного самостоятельного перорального приема в дозе 450–600 мг пациентам с редкими пароксизмами ФП, не принимающим поддерживающей антиаритмической терапии, без сопутствующего структурного заболевания сердца или ИБС при условии продолжительности аритмии менее 48 ч (режим «таблетка в кармане»): ЕОК – IIaB (УУР – С, УДД – 4) [1, 9–11].
• Не рекомендовано применение пропафенона для восстановления синусового ритма пациентам с ФП и структурным поражением сердца (постинфарктным кардиосклерозом, сниженной систолической функции левого желудочка (ЛЖ), фракцией выброса ЛЖ ≤40%, любыми проявлениями сердечной недостаточности, а также при гипертрофии миокарда ЛЖ, превышающей 14 мм по данным ЭхоКГ) в связи с высоким риском его аритмогенного действия у данной категории пациентов [1].
• Имеющаяся доказательная база подтверждает высокий уровень безопасности, эффективности и быстроты действия пропафенона при купировании пароксизмов ФП. Действие препарата характеризуется быстрым эффектом в течение 2–3 ч и отсутствием серьезных побочных реакций. Пероральная форма пропафенона менее эффективна по сравнению с внутривенной в первые 2 ч, но впоследствии обе они одинаково действенны. Частота восстановления ритма превышает 80% при назначении препарата в первые часы пароксизма. Наличие пероральной и внутривенной форм пропафенона дает возможность назначать его врачами амбулаторного звена, скорой медицинской помощи и стационара, а также применять препарат самостоятельно пациентом (режим «таблетка в кармане») [12].
12
• Рекомендовано внутривенное введение прокаинамида (ААП IА класса) для купирования ФП продолжительностью до 48 ч у пациентов, не имеющих противопоказаний к применению препарата: ЕОК – 1C (УУР – А, УДД – 2) [1]. Режим внутривенного введения препарата: 500–1000 мг однократно медленно (20–30 мг/мин) [1].
• Не рекомендовано применение прокаинамида пациентам с ФП и структурным поражением сердца в связи с высоким риском аритмогенного действия этого препарата [1].
13
• Рекомендовано внутривенное введение амиодарона (ААП III класса) для купирования ФП продолжительностью до 48 ч у пациентов, не имеющих противопоказаний к применению препарата: ЕОК – 1A (УУР – А, УДД – 1) [1]. Режим внутривенного введения препарата: 5–7 мг/кг в течение 1–2 ч, затем 50 мг/ч вплоть до максимальной дозы 1000–1200 мг в течение 24 ч [1].
• Амиодарон может быть использован в том числе у пациентов с ФП и структурным поражением сердца, включая тяжелую хроническую сердечную недостаточность с низкой фракцией выброса ЛЖ [1].
14
• Рекомендовано внутривенное введение Рефралона (ААП III класса) для купирования ФП любой продолжительности, в том числе персистирующей и длительно персистирующей форм аритмии, у пациентов, не имеющих противопоказаний к применению препарата: ЕОК – нет (УУР – А, УДД – 2) [1]. Препарат вводится в три этапа с повышением дозы 10 мкг/кг – 20 мкг/кг – 30 мкг/кг [1].
• Рефралон может быть использован в том числе как альтернатива плановой электрической кардиоверсии [1].
15
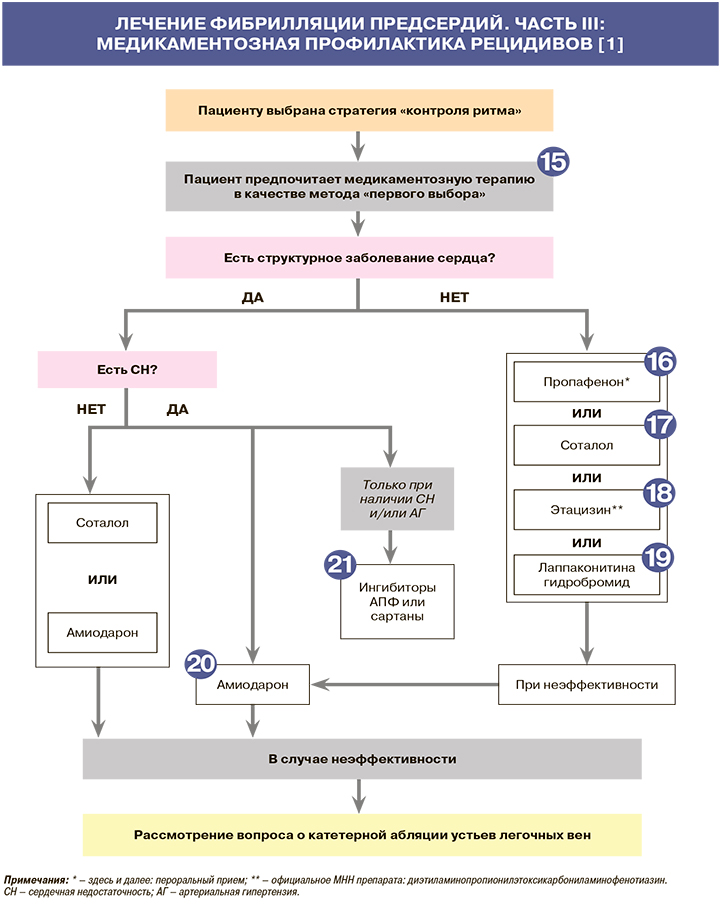
• Длительная медикаментозная антиаритмическая рекомендуется для контроля ритма у пациентов с симптоматичной рецидивирующей ФП, персистирущей формой ФП после кардиоверсии и у пациентов после абляции ФП в течение первых 3 мес или неопределенно долго (как составляющая часть гибридного подхода): ЕОК – IB (УУР – А, УДД – 2) [1]. При отсутствии симптомов (в том числе на фоне адекватного контроля частоты сердечных сокращений) больным обычно не следует назначать ААП. Выбор ААП для профилактики ФП рекомендуется производить с учетом наличия и тяжести органической патологии сердца, коморбидного фона пациента (наличие почечной, печеночной недостаточности), риска аритмогенного действия, спектра внесердечных нежелательных эффектов лекарственного препарата [1].
• До настоящего времени не существует доказательной базы в пользу того, что поддержание синусового ритма может улучшить жизненный прогноз у пациентов с ФП. По этой причине целью длительной медикаментозной антиаритмической терапии является сохранение синусового ритма для улучшения симптомов, ассоциированных с ФП. Назначение медикаментозной антиаритмической терапии примерно удваивает вероятность поддержания синусового ритма по сравнению с плацебо [1].
• Для более успешного поддержания синусового ритма, кроме назначения ААП, рекомендовано контролировать факторы риска сердечно-сосудистых осложнений (сердечная недостаточность, АГ, сахарный диабет, индекс массы тела и т.д.) и возможные провоцирующие факторы ФП – стресс, алкоголь, физические перегрузки, электролитные сдвиги, тиреотоксикоз: ЕОК – IIaB (УУР – А, УДД – 1) [1].
• Длительная антиаритмическая терапия не рекомендуется пациентам с интервалом QT >0,5 с (500 мс) или синусовой брадикардией менее 50 уд/мин в покое с эпизодами синоатриальной блокады 2–3 степени или атриовентрикулярной блокады 2–3 степени без предварительной имплантации электрокардиостимулятора [1].
16
• ААП IС класса – пропафенон и др. – рекомендованы для профилактики рецидивирующей симптоматической ФП у пациентов без структурного поражения сердца и сердечной недостаточности: ЕОК – IA (УУР – А, УДД – 1) [1]. В целях профилактики возможной трансформации ФП в трепетание предсердий (ТП) с высокой частотой проведения на желудочки рекомендуется комбинировать ААП IС класса с бетаадреноблокаторами [1].
• Режим приема пропафенона для поддержания синусового ритма: перорально 150 мг 3–4 раза/сут. Максимальная суточная доза – 900 мг в 3 приема. По данным многочисленных исследований и метаанализов, эффективность пропафенона при плановой антиаритмической терапии ФП составляет 50–70% [12].
• Необходимо соблюдать осторожность при назначении пропафенона больным с нарушением внутрижелудочковой проводимости, особенно с блокадой левой ножки пучка Гиса. Назначение пропафенона требует контроля за длительностью комплекса QRS на ЭКГ. Увеличение длительности комплекса QRS, по крайней мере на 25% по сравнению с исходным, указывает на риск развития проаритмического действия. В таких случаях следует снизить дозу или отменить препарат. Пропафенон способен вызывать трансформацию ФП в ТП [1].
17
• У пациентов без структурных заболеваний сердца профилактику рецидивов ФП рекомендовано начинать с бета-адреноблокаторов, особенно когда аритмия четко связана с психическим или физическим напряжением: ЕОК – IB (УУР – А, УДД – 2) [1].
ААП III класса, обладающим свойствами неселективного бета-адреноблокатора и рекомендованным в такой ситуации, является соталол; наиболее оправдано его применение у пациентов со стабильной ИБС: ЕОК – IA (УУР – А, УДД – 2) [1]. Также возможно его использования у пациентов со структурными заболеваниями сердца, но без тяжелого органического поражения сердца, без угнетения насосной функции и сердечной недостаточности. Режим приема соталола в рамках профилактики рецидивов ФП: 80–160 мг 2 раза/сут [1].
• По эффективности в профилактике рецидивов ФП соталол уступает амиодарону. Его прием сопряжен с риском возникновения желудочковой тахикардии torsades de pointes (1%). Проаритмическое действие препарата связано с удлинением интервала QT, что требует контроля за динамикой этого показателя на ЭКГ. Если интервал QT увеличивается до 500 мс и более, следует отменить соталол или снизить его дозу. Риск проаритмического действия более высок у женщин, пациентов с дисфункцией ЛЖ, сердечной недостаточностью, выраженной гипертрофией миокарда ЛЖ (толщина миокарда ЛЖ, превышающая 14 мм по данным ЭхоКГ), брадикардией, дисфункцией почек, гипокалиемией или гипомагниемией [1].
18
• Этацизин (ААП IC класса) применяется для сохранения синусового ритма при пароксизмальной ФП и персистирующей ФП после кардиоверсии. Режим приема препарата: 50 мг 2–3 раза/сут [1].
• Этацизин может быть использован для лечения пациентов у пациентов с АГ без гипертрофии ЛЖ (толщина миокарда ЛЖ <15 мм по данным ЭхоКГ), но не должен назначаться при ИБС, хронической сердечной недостаточности, АГ с гипертрофией ЛЖ в связи с риском проаритмического действия. Назначение препарата требует контроля длительности комплекса QRS и интервала PQ на ЭКГ. Увеличение длительности QRS на 25% и более требует отмены препарата или уменьшения его дозы. Препарат способен вызывать трансформацию ФП в ТП. Наиболее частые побочные действия этацизина – головокружение, головная боль, расстройства зрения [1].
19
• Лаппаконитина гидробромид (ААП IC класса) может быть использован при ФП у пациентов с АГ без выраженной (≤14 мм) гипертрофии миокарда ЛЖ, но не должен назначаться при ИБС, клинически значимой хронической сердечной недостаточности, АГ с выраженной гипертрофией ЛЖ (>14 мм) в связи с риском проаритмического действия. Он угнетает атриовентрикулярное и внутрижелудочковое проведение возбуждения, что требует контроля за длительностью интервала PQ и QRS. Как и другие ААП IC-класса, препарат способен вызвать трансформацию ФП в ТП. Наиболее частые его побочные эффекты – головокружение, головная боль, нарушение фиксации взора [1].
• Режим приема лаппаконитина гидробромида: 25–50 мг 3 раза/сут [1].
• Назначение ААП IC класса (пропафенон, этацизин, лаппаконитина гидробромид) не рекомендовано пациентам с признаками структурного поражения сердца, в том числе при наличии сердечной недостаточности, при снижении фракции выброса ЛЖ до 40% и менее, а также при гипертрофии миокарда (толщина стенок ЛЖ 15 мм и более по данным ЭхоКГ), так как препараты этой группы способны потенцировать возникновение жизнеугрожающих желудочковых аритмий: ЕОК – IIIA (УУР – А, УДД – 1) [1]. Также ААП IС класса не рекомендованы для применения у пациентов с ИБС: ЕОК – IIIA (УУР – А, УДД – 1) [1].
20
• Амиодарон (ААП III класса) рекомендуется для профилактики рецидивирующей симптоматической ФП у пациентов с сердечной недостаточностью: ЕОК – IB (УУР – А, УДД – 2). Пациентам без структурного поражения сердца, которым не противопоказаны другие ААП, назначение амиодарона рекомендовано только при их неэффективности: ЕОК – IIaC (УУР – А, УДД – 1) [1]. Пациентам с ИБС препарат назначается при неэффективности соталола: ЕОК – IIIA (УУР – А, УДД – 1). Режим приема амиодарона: 600 мг/сут на 4 нед, 400 мг/сут еще на 4 нед, затем по 200 мг/сут длительно [1].
• Амиодарон является самым эффективным препаратом для профилактики ФП.
В отличие от большинства других ААП, его можно назначать пациентам с органическим заболеванием сердца, включая сердечную недостаточность. Риск развития полиморфной желудочковой тахикардии типа torsades de pointes при лечении амиодароном ниже (0,5%), чем при применении других блокаторов калиевых каналов, что связано с блокадой нескольких видов ионных каналов. Однако в связи с наличием этого риска рекомендуется контролировать длительность интервала QT на ЭКГ. Удлинение этого интервала более чем на 500 мс требует снижения дозы или отмены амиодарона. Препарат вызывает различные внекардиальные побочные эффекты (щитовидная железа, печень, легкие, глаза), особенно при длительном применении, что делает обоснованным его назначение лишь при неэффективности или невозможности назначения других ААП. Из-за особенностей фармакокинетики препарата требуется длительный период насыщения [1].
• Всем пациентам перед назначением амиодарона рекомендуется рентгенологическое исследование легких и оценка уровня гормонов щитовидной железы (Т4 свободный, ТТГ). На фоне постоянной терапии этим ААП показано ежегодное рентгенологическое исследование легких, 1 раз в 6 мес – исследование функции внешнего дыхания, содержания Т4 свободного и ТТГ. С целью профилактики развития фотосенсибилизации при приеме амиодарона рекомендуется избегать пребывания на солнце или пользоваться специальными солнцезащитными средствами. Ежегодный осмотр окулиста необходим с целью выявления значительных отложений в роговице либо развития нарушений зрения [1].
• Пациентам, длительно получающим антиаритмическую терапию, рекомендовано периодическое прохождение обследования с проведением ЭКГ, ЭхоКГ, стресс-ЭхоКГ для подтверждения соответствия критериям безопасного выбора ААП: ЕОК – IIaC (УУР – B, УДД – 3) [1].
• Пациентам, длительно получающим антиаритмическую терапию, рекомендован регулярный контроль длительности интервалов PQ, QRS, QT и частоты сердечных сокращений с помощью ЭКГ и холтеровского мониторирования ЭКГ для оценки возможного риска проаритмического действия ААП и своевременного выявления клинически значимых нарушений проводимости и/или дисфункции синусового узла, обусловленных действием ААП: ЕОК – IB (УУР – С, УДД – 4) [1]. В начале лечения (первые 3 дня) рекомендован ежедневный контроль ЭКГ для обоснования адекватности выбора индивидуальной дозы препарата. При использовании амиодарона такой контроль рекомендовано проводить дополнительно через 1 и 4 нед. [1].
21
• Для профилактики ФП пациентам с сердечной недостаточностью и сниженной фракцией выброса ЛЖ рекомендовано назначение ингибиторов АПФ или антагонистов ангиотензина II: ЕОК – IIaA (УУР – B, УДД – 1) [1]. Также назначение этих препаратов рекомендовано с целью профилактики ФП пациентам с АГ, особенно при наличии гипертрофии ЛЖ: ЕОК – IIaB (УУР – А, УДД – 1) [1]. В то же время в отсутствие сердечной недостаточности и АГ ингибиторы АПФ или антагонисты ангиотензина II не рекомендуются для вторичной профилактики ФП не рекомендованы: ЕОК – IIIB (УУР – В, УДД – 1) [1].



