Диагностика

1
• Пост-COVID-синдром, включающий Long-COVID, – состояние, характеризующееся сохранением клинических симптомов более 4 нед с момента появления острых симптомов новой коронавирусной инфекции. К клиническим симптомам «длительного COVID» относятся утомляемость, одышка, усталость/слабость, снижение памяти, вегетативная дисфункция, головная боль, стойкая потеря обоняния или вкуса, кашель, депрессия, субфебрильная температура, учащенное сердцебиение, головокружение, мышечные боли и боли в суставах, боль в груди, нарушение памяти, нарушение глотания [1, 2].
• Другая составляющая постковидного синдрома – мультиорганные эффекты COVID-19, которые включают клинические проявления, относящиеся к сердечнососудистой, респираторной, почечной и нервно-психиатрической системам органов, хотя продолжительность этих мультиорганных системных эффектов неясна [1].
• Еще один возможный модус постковидных состояний – негативные последствия лечения/госпитализации COVID-19, к которым относится синдром после интенсивной терапии (PICS), приводящий к крайней слабости и посттравматическому стрессовому расстройству. Многие пациенты с этими осложнениями COVID-19 со временем выздоравливают [1].
• Возможные проявления постковидного синдрома со стороны различных систем и органов отражены в таблице 1.

2
• При наличии у пациента признаков одышки рекомендуется провести тест с 3или 6-минутной ходьбой (3МШТ или 6МШТ) либо 1-минутный тест «сесть–встать» (1STST) сообразно возможностям пациента. До и после теста для оценки одышки и утомляемости возможно использование модифицированной шкалы Борга. Также до и после теста выполняются пульсоксиметрия, измерение частоты сердечных сокращений. Клинически значимым считается уровень десатурации ≥4% [2].
• Проведение пульсоксиметрии с измерением SpO2 рекомендуется всем пациентам с продолжающимся симптоматическим COVID-19 для выявления признаков дыхательной недостаточности. Необходимо проводить измерение SpO2 в динамике и записывать параметры сатурации не только в покое, но и при нагрузке (ходьба по комнате). Сатурация артериальной крови кислородом <95%, нарастание одышки >22/мин или появление болей в грудной клетке – основание для направления пациента к кардиологу для исключения острой сердечно-сосудистой недостаточности [1, 2].
3
Объем лабораторных исследований у пациентов с подозрением на Long-COVID зависит от клинической картины [1]. Круг анализов, необходимых при наличии одышки, кашля, боли в груди, а также распространенных нереспираторных симптомах постковида, приведен в таблице 2.

4
Объем клинико-инструментальных исследований у пациентов с подозрением на Long-COVID при наличии одышки, кашля, боли в груди, а также при распространенных нереспираторных симптомах постковида суммирован в таблице 3.

5
Принципы принятия решений врачом амбулаторного этапа по результатам первичного осмотра пациентов, перенесших COVID-19, в таблице 4.

Лечение

1
• Пост-COVID-синдром можно рассматривать как мультисистемное расстройство, обычно проявляющееся респираторными, сердечно-сосудистыми, гематологическими и нейропсихиатрическими симптомами либо по отдельности, либо в сочетании. Таким образом, терапия должна быть индивидуальной и включать междисциплинарный подход, направленный на решение как клинических, так и психологических аспектов этого расстройства [1].
2
• В среднем у 40% пациентов после выписки из ковидного стационара сохраняется одышка на протяжении более 6 мес, а изменения на компьютерной томографии (КТ) легких продолжают обнаруживаться после острого периода инфекции у 76% лиц, госпитализированных в отделение реанимации и интенсивной терапии, еще в течение 6–12 мес [1, 3, 4]. Назначение ингаляционной терапии сурфактантом рекомендуется пациентам, перенесшим тяжелую COVID-19-пневмонию и выписанным из стационара с гипоксемией (т.е. нуждающимся в кислородотерапии в домашних условиях): УУР – С, УДД – 4 [1].
• Для ингаляции сурфактанта-БЛ могут быть использованы струйные небулайзеры или меш-небулайзеры; используют 2 ингаляции в сутки в дозе 75–150 мг сурфактанта-БЛ, обычно на протяжении 10–14 дней: УУР – С, УДД – 4 [1].
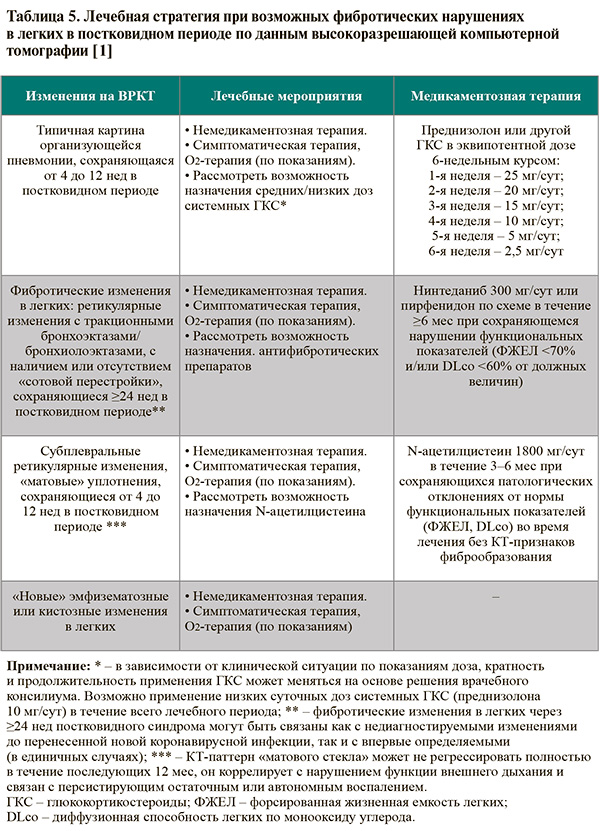
• Изменения на высокоразрешающей КТ, служащие показаниями для применения комплексной антифибротической терапии в постковидном периоде (УУР – С, УДД – 5), отражены в таблице 5.
• Методы немедикаментозной терапии фибротических нарушений при постковидном синдроме включают инспираторный тренинг, вибрационно-перкуссионную терапию, индивидуальные рекомендации по питанию [1].
• Критерии назначения антифибротических препаратов (нинтеданиб и пирфенидон), наряду с указанными в таблице 5 фиброзными изменениями в легких по данным ВРКТ (паттерн обычной интерстициальной пневмонии или вероятной обычной интерстициальной пневмонии), включают (УУР – С, УДД – 5) сохраняющиеся фиброзоподобные изменения в легких по данным ВРКТ в течение 6 мес от начала заболевания в сочетании с SpO2 ≤89% в покое или после теста с 6-минутной ходьбой и ФЖЕЛ <70% и/или DLco<60% от должных величин или в сочетании со снижением ФЖЕЛ ≥10% и/или DLco ≥15% в течение 3–6 мес в сравнении с исходными величинами, измеренными впервые в период от 4 до 12 нед от острых симптомов COVID-19. Также антифибротические препараты могут быть назначены при сохраняющихся фиброзоподобных изменениях в легких по данным ВРКТ в течение 6 мес от начала заболевания при отсутствии других известных причин развития фиброзирующих интерстициальных заболеваний легких [1].
• Группа антифибротических препаратов, используемых для лечения идиопатического легочного фиброза, представлена нинтеданибом и пирфенидоном [1]. У пациентов с остаточными COVID-ассоциированными поражениями легких рекомендуется назначение бовгиалуронидазы азоксимера [1, 5].
• У пациентов с постковидным синдромом при наличии показаний к длительной терапии антикоагулянтами и/или дезагрегантами (фибрилляция предсердий, тромбоз глубоких вен/тромбоэмболия легочной артерии в анамнезе ТГВ/ТЭЛА, протезы клапанов, тромбофилии, периферический атеросклероз, острое нарушение мозгового кровообращения в анамнезе, ишемическая болезнь сердца, острый коронарный синдром, стентирование в анамнезе) необходимо продолжить прием препаратов или инициировать терапию в соответствии с текущими рекомендациями. Следует также пересмотреть показания для пролонгации терапии. У пациентов с имеющимися сердечно-сосудистыми заболеваниями определяющие показания к приему ацетилсалициловой кислоты и других дезагрегантов – возможность продолжения их применения после перенесенного заболевания [1, 6].
• В отсутствие показаний к антитромботической терапии текущие рекомендации позволяют пролонгировать терапию антикоагулянтами до 45 дней после выписки в соответствии с рассчитанным тромботическим риском. В соответствии с текущими рекомендациями Минздрава продленную профилактику ТГВ (вплоть до 30–45 дней после выписки) следует проводить при сохраняющемся повышенном тромботическом риске у пациентов при наличии одного из следующих признаков: возраст старше 60 лет, госпитализация в ОРИТ, активное злокачественное новообразование, ТГВ/ТЭЛА в анамнезе, известная тромбофилия, сохраняющееся выраженное ограничение подвижности, концентрация Д-димера в крови, в ≥2 раза превышающая верхнюю границу нормы. Профилактику ТГВ нижних конечностей/ТЭЛА стоит рассматривать для больных со среднетяжелой формой COVID-19, которые лечатся дома и имеют высокий риск венозных тромбоэмболических осложнений, низкий риск кровотечений. Длительность применения антикоагулянтов при амбулаторном лечении COVID-19 не ясна и, по-видимому, может продолжаться вплоть до 30 сут в зависимости от динамики клинического состояния пациента и сроков восстановления двигательной активности [1, 6].
• Нет оснований для пролонгации применения антикоагулянтов более 30 дней для амбулаторных пациентов и более 45 дней после выписки из стационара с целью тромбопрофилактики без четких показаний. С точки зрения некоторых исследователей, анализ клинического статуса пациентов (гиперкоагуляционное состояние, повышение СРБ, Д-димера, фибриногена) позволяет не использовать унифицированную стратегию длительности применения антикоагулянтов после у пациентов с синдромом длительного COVID-19 [1, 7].
3
При Long-COVID возможно назначение противовирусных препаратов пациентам, у которых на протяжении нескольких месяцев сохраняется положительный результат полимеразной цепной реакции (ПЦР) на SARS-CoV-2 в назофарингеальных мазках. Альтернативный подход может быть связан с использованием в таких ситуациях иммуномодулирующих средств [1].
4
Рекомендовано использование противовирусного препарата прямого действия фавипиравира иммуносупрессивным пациентам с подтвержденной персистенцией вируса в течение длительного времени для прекращения репликации: УУР – A, УДД – 2 [1]. Применение этого лекарственного средства при Long-COVID-19 возможно в особых группах пациентов – с иммуносупрессивной коморбидностью: с онкологическими заболеваниями, после трансплантации солидных органов, у ВИЧинфицированных, с заболеваниями крови и др. Фавипиравир входит в международные клинические рекомендации по лечению и профилактике новой коронавирусной инфекции COVID-19. Представляется обоснованным его использование за пределами острого периода [1, 8, 9].
5
• Рекомендовано использование препарата с широким противовирусным действием риамиловира у пациентов с подтвержденной персистенцией вируса в течение длительного времени для прекращения его репликации: УУР – В, УДД – 2 [1]. Препарат обладает широким спектром противовирусной активности в отношении РНК-содержащих вирусов, в том числе SARS-CoV-2, подавляя синтез вирусных РНК и репликации геномных фрагментов. Риамиловир применяется внутрь независимо от приема пищи по 250 мг 3 раза/сут в течение 7 дней [1, 10–13].
• Эффективность и безопасность риамиловира в острый период COVID-19 и постковидный период подтверждена в целом ряде отечественных клинических исследований:
– в рамках ретроспективной обработки 108 законченных клинических случаев COVID-19 средней степени тяжести длительностью ≤3 сут за период 2020–2021 гг. пациенты были разделены на две группы: 1-я группа (n=53) дополнительно к стандартной терапии по решению врачебной комиссии получала риамиловир (off-label) в дозе 1250 мг/сут в течение 5 дней, 2-я группа (n=55) – комбинацию умифеновира с рибавирином (по 800 мг/сут) в течение 5 дней. Прием риамиловира для лечения пациентов с COVID-19 средней степени тяжести приводил к статистически значимому снижению длительности общеинфекционных синдромов, симптомов поражения респираторного тракта. Пациенты из основной группы статистически значимо быстрее достигали клинического выздоровления и санации от возбудителя по результатам диагностики с помощью метода амплификации нуклеиновых кислот [14];
– в обсервационном ретроспективном сравнительном исследовании оценивалось состояние 87 пациентов с COVID-19 различной степени тяжести через 3 мес после лечения этиотропными препаратами: 1-я группа (n=41) получала в острый период болезни риамиловир 250 мг 3 раза/сут в течение 7 сут, 2-я (n=46) – умифеновир 200 мг 4 раза/сут в течение 7 сут. В группе пациентов, получавших в острый период COVID-19 риамиловир, по сравнению группой умифеновира достоверно реже диагностировались синдром хронического системного воспаления (p <0,05), дисрегуляция клеточного звена иммунитета (p <0,001) в ранний постковидный период [15];
– в открытом исследовании 120 пациентов с клинико-эпидемиологическими проявлениями легкой коронавирусной инфекции и ее лабораторным (ПЦР) подтверждением оценивалась эффективность риамиловира при приеме по 250 мг 3 раза/сут в течение 7 дней в качестве монотерапии. Через 12 дней после начала терапии отрицательный ПЦР-тест на SARS-CoV-2 был зарегистрирован у 97,5% исследуемых, полное выздоровление – у 95,84%. У 97,5% переносимость препарата была хорошей, у 2,5% – удовлетворительной [11].
6
Рекомендовано использование препарата с широким противовирусным и иммуномодулирующим действием энисамия йодида у пациентов с подтвержденной персистенцией вируса в течение длительного времени для прекращения его репликации, а также коррекции иммунного статуса: УУР – В, УДД – 2 [1]. Препарат обладает противовирусной и иммуномодулирующей активностью (индукция синтеза интерферона). Рекомендованная схема назначения – по 500 мг 3 раза/сут курсом 5–7 дней [1, 16].
7
Рекомендовано использование препарата с широким противовирусным и иммуномодулирующим действием азоксимера бромида у пациентов с подтвержденной персистенцией вируса в течение длительного времени для прекращения его репликации, а также коррекции иммунного статуса: УУР – В, УДД – 2 [1]. Препарат обладает выраженной иммуномодулирующей (в том числе интерферонпродуцирующей) активностью, а также антитоксическими и антиоксидантными свойствами. В период репликации вируса применяется в комплексе со средствами этиотропной терапии, а в период реабилитации или с целью иммунопрофилактики респираторных инфекций, включая COVID-19, особенно при реабилитации вирусного поражения легких при SARS COV-2 инфекции, – в качестве монотерапии. Режимы применения: сублингвально – по 1 таблетке 2 раза/сут в течение 7 дней; инъекционно – в виде раствора внутривенно по 12 мг 1 раз/сут в течение 3 дней, затем внутримышечно через день пациентам с COVID-19 общим курсом 10 инъекций; интраназально или сублингвально – в виде раствора 6 мг/сут в 2–3 приема [1, 17–19].
8
Рекомендовано использование препарата с широким противовирусным и иммуномодулирующим действием имидазолилэтанамида пентандиовой кислоты у пациентов с подтвержденной персистенцией вируса в течение длительного времени для прекращения его репликации, а также коррекции иммунного статуса (УУР – С, УДД – 5) [1]. Препарат обладает комплексным действием – противовирусным, иммуномодулирующим (в том числе интерферонпродуцирующим) и противовоспалительным. Назначается внутрь по 90 мг 1 раз/сут в течение 5–7 дней [1, 20].
9
Рекомендовано использование препарата с широким противовирусным и иммуномодулирующим действием оксиэтиламмония метилфеноксиацетата у пациентов с подтвержденной персистенцией вируса в течение длительного времени для прекращения его репликации, а также коррекции иммунного статуса (УУР – С, УДД – 5) [1]. Препарат обладает иммуностимулирующими, антиоксидантными и адаптогенными свойствами. Повышает устойчивость организма к физическим нагрузкам, гипоксии, иммобилизационному стрессу, компенсирует когнитивные расстройства. Режим дозирования и длительность курса зависят от показаний [1, 21].



