В реабилитации и комплексном лечении пациентов с ишемической болезнью сердца (ИБС) наиболее актуальными являются 2 основные задачи: 1) улучшение прогноза; 2) уменьшение частоты и интенсивности приступов стенокардии, улучшение качества жизни (КЖ) [1, 2].
По данным отечественных и зарубежных обзоров, рациональное применение реабилитационных программ приводит к достоверному снижению смертности от всех причин на 20—25% и от сердечно-сосудистых заболеваний на 26—30% [2].
В последние годы структура методов кардиореабилитации расширяется за счет сочетанного применения (наряду с индивидуально дозированными физическими нагрузками) новых высокотехнологичных инструментальных методик. Одним из перспективных подходов является применение повторных многократных эпизодов адаптации к гипоксии — интервальные гипоксические тренировки (ИГТ). ИГТ — метод немедикаментозного лечения и профилактики хронических неинфекционных заболеваний, повышения физической работоспособности человека на основе многократной периодической стимуляции механизмов транспорта и утилизации кислорода путем дыхания газовыми смесями со сниженным содержанием кислорода.
Экспериментально и клинически доказано, что высокогорная адаптация или моделирование условий среднегорья в гипо- или нормобарическом вариантах, а также короткие повторяющиеся эпизоды нормобарической гипоксии с нормоксическими «паузами» активируют каскад прямых и перекрестных адаптационных эффектов, повышая устойчивость организма как к гипоксическим состояниям, так и другим стрессорам, патогенным факторам, посредством запуска гематологических (увеличение содержания эритропоэтина, гемоглобина, кислородной емкости крови) и негематологических (ангиогенез, активация гликолитической активности, утилизации липидов, систем антиоксидантной защиты, повышение буферной емкости мышц, их толерантности к повышению концентрации лактата, биоэнергетической эффективности митохондриальной дыхательной цепи, транспорта глюкозы в мышцах, хеморецепторной чувствительности, снижение симпатико-адреналовой реактивности и др.) механизмов [3—6].
Клинически значимые эффекты ИГТ во многом сходны с эффектами основного компонента «традиционных» программ кардиореабилитации — физических тренировок: повышение переносимости физических нагрузок (ПФН), улучшение сократительной функции миокарда, коронарной перфузии, снижение уровня фибриногена и агрегации тромбоцитов, позитивные изменения липидного состава плазмы крови, повышение чувствительности к инсулину, описанные как феномен ишемического прекондиционирования (чередование ишемии и последующей реперфузии), запускающего механизмы кардиопротекции и метаболической адаптации к умеренной ишемии, что актуально для пациентов со сниженным коронарным резервом [3, 7].
Поскольку при ИГТ воздействующим фактором является гипоксическая гипоксия с последующей реоксигенацией, то можно говорить об отсроченных эффектах повторяющегося, или хронического, гипоксического прекондиционирования, при котором происходит накопление веществ — триггеров множественных адаптивных сдвигов: опиоидов, норадреналина, аденозина, серотонина, ацетилхолина, ионов кальция, NO, цитокинов (интерлейкины 1B, 2), фактора некроза опухоли-α (ТNF-α), ядерного фактора κB (NF-κB), фактор, индуцируемый гипоксией (HIF-1α, HIF-2α), и др. [7]. Результатом такой активации являются открытие КАТФ-каналов сарколеммы и митохондрий кардиомиоцитов, стабилизация мембран, ослабление внутриклеточной кальциевой перегрузки, оптимизация синтеза АТФ, снижение сократимости миокарда и потребности его в энергии, уменьшение выраженности окислительного стресса, изменение метаболизма жирных кислот [8].
Установлено, что эффективность ИГТ можно повысить путем замещения нормоксических пауз (реоксигенации) подачей пациенту гипероксической газовой смеси — методом интервальных гипоксически-гипероксических тренировок (ИГГТ) [9]. В период создаваемой гипероксии происходит более выраженная, чем при нормоксической реоксигенации, индукция активных форм кислорода, необходимая для запуска каскада редокс-сигнального пути, что приводит к усиленному синтезу защитных внутриклеточных белковых молекул, главным образом, с антиоксидантной функцией (ферменты антиоксидантной защиты, железосвязывающие белки, белки теплового шока) [4, 9, 10]. В экспериментальных исследованиях продемонстрированы более выраженные мембран-стабилизирующие эффекты, существенное повышение стрессорной и гипоксической устойчивости миокарда и мозга, уровня антиоксидантной защиты, ПФН в результате проведения адаптации к ИГГТ по сравнению с ИГТ [9—14].
 Метод ИГГТ эмпирически обоснован на этапе санаторно-курортного лечения детей с бронхиальной астмой при сочетанном применении ИГТ и энтеральной оксигенотерапии (кислородные коктейли) [11], апробирован в пилотных исследованиях пациентов с метаболическим синдромом, ИБС, квалифицированных спортсменов с синдромом перетренированности [10, 12—14].
Метод ИГГТ эмпирически обоснован на этапе санаторно-курортного лечения детей с бронхиальной астмой при сочетанном применении ИГТ и энтеральной оксигенотерапии (кислородные коктейли) [11], апробирован в пилотных исследованиях пациентов с метаболическим синдромом, ИБС, квалифицированных спортсменов с синдромом перетренированности [10, 12—14].
Цель настоящего клинического плацебо-контролируемого исследования — комплексный анализ возможности применения и эффективности метода ИГГТ у больных ИБС, получающих оптимально подобранную медикаментозную терапию, на этапе поликлинического наблюдения, с особым вниманием к оценке динамики показателей ПФН и КЖ.
Материал и методы
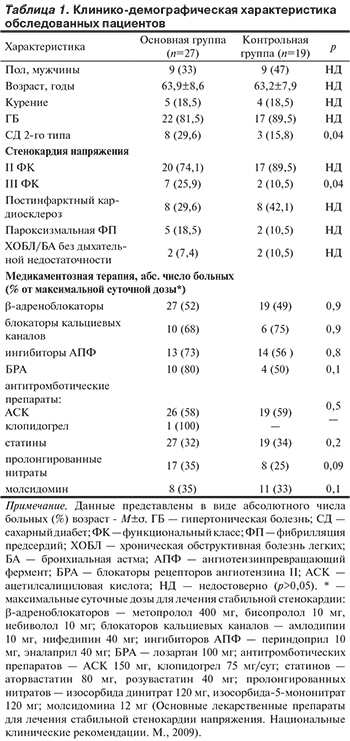
В исследование были включены 46 пациентов со стабильной стенокардией напряжения II и III функционального класса (ФК), среди которых 18 мужчин и 28 женщин в возрасте от 45 до 83 лет. Диагноз хронической ИБС и ФК устанавливали в соответствии с Национальными клиническими рекомендациями ВНОК (2009), согласно действующей классификации Канадской ассоциации кардиологов. Общая характеристика пациентов представлена в табл. 1.
Достоверные различия по клинико-демографическим признакам наблюдались по 2 характеристикам: в контрольной группе пациентов со стенокардией напряжения III ФК и с сахарным диабетом 2-го типа было несколько больше, чем в основной (р=0,04). Отбор пациентов в исследование осуществляли при условии наличия постоянной оптимально подобранной медикаментозной терапии, соответствующей национальным и европейским рекомендациям.
Достоверных различий по медикаментозной терапии среди пациентов группы ИГГТ и контрольной группы не наблюдалось. В группе ИГГТ на фоне лечения частота сердечных сокращений (ЧСС) в покое составляла 63±7 уд/мин, систолическое артериальное давление (АД) в покое — 125,8±20,2 мм рт.ст., диастолическое АД — 72,2±14,7 мм рт.ст., в группе контроля — 62±10 уд/мин, 125,8±21,2 мм рт.ст. и 76,4±8,6 мм рт.ст. соответственно.
Протокол исследований был сформирован в соответствии с положениями «Биоэтических правил проведения исследований на человеке» и одобрен биоэтической комиссией Университета, от всех пациентов до начала работы было получено письменное информированное согласие.
После исходного обследования пациенты случайным порядком были разделены на 2 группы в соотношении 1,5:1 — основная группа (n=27) и контрольная (n=19). Пациентам в основной группе проводили ИГГТ в течение 3 нед по 5 дней с перерывами 2 дня (15 тренировок) по одной процедуре в день. В исследовании использовали нормобарическую установку для получения гипоксических и гипероксических газовых смесей на основе обратной связи ReOxy Cardio (S.A. Aimediq, Luxembourg) [15].
Перед началом курса процедур определяли индивидуальную чувствительность пациентов к гипоксии путем проведения 10-минутного гипоксического теста (ГТ) — дыхание через маску газовой смесью с 12% содержанием О2, с ежеминутным мониторированием ЧСС и насыщения гемоглобина артериальной крови кислородом (SaO2).
При отпуске процедур ИГГТ длительность подачи газовой гипоксической (11—12% О2) и гипероксической (35% О2) смесей регулировали с учетом результатов ГТ по принципу биологической обратной связи автоматически на основе мониторирования индивидуальных значений SaO2 и ЧСС [15]. Длительность одной процедуры составляла 45—50 мин, каждого гипоксического периода — в среднем 4—6 мин, гипероксического периода — 1—2 мин в зависимости от скорости восстановления SaO2 у пациента. После каждой тренировки вносили отметку в дневник наблюдения, где указывали дату проведения процедуры, оценку пациентом переносимости процедуры, все возможные изменения состояния во время тренировки и в период между ними. До и после тренировки измеряли АД, ЧСС. После курса ИГГТ в течение 1 мес пациенты вели дневник самоконтроля, в котором указывали наличие загрудинных, головных болей, оценку общего самочувствия по шкале 1—5 баллов, прием препаратов, результаты измерения АД, ЧСС утром и вечером. Пациенты контрольной группы прошли курс плацебо-тренировок, имитирующих ИГГТ, получая через маску того же аппарата атмосферный воздух.
Всем пациентам проводили обследование до и после курса ИГГТ или плацебо-тренировок. В группе ИГГТ было выполнено дополнительное обследование через 1 мес после тренировок для оценки длительности сохранения эффектов, возникших в результате курса ИГГТ. В силу ограниченности ресурсов исследование отдаленных эффектов в контрольной группе не проводили.

Обследование включало опрос и осмотр пациента, регистрацию АД, ЧСС, электрокардиографию в покое, оценку ПФН путем проведения кардиопульмонального нагрузочного тестирования. Нагрузочное тестирование с газовым анализом проведено с применением комплекса CARDIOVIT CS-200, система с использованием беговой дорожки. Выбор протокола нагрузочного тестирования (BRUCE или M-BRUCE) осуществляли в соответствии с тяжестью патологии сердца, ПФН, наличием сопутствующей патологии, возрастом пациента [16]. Критерии прекращения нагрузочного теста соответствовали рекомендациям (цит. по [17]). КЖ больных до, после ИГГТ и через 1 мес изучено при помощи вопросника MOS 36-Item Short-Form Health Survey (SF-36). Использовали официальный русскоязычный аналог вопросника [18]. По результатам анкетирования проводили расчет 8 параметров: физической активности (ФА), роли физических проблем ограничении жизнедеятельности (РФ), боли, жизнеспособности (ЖС), социальной активности (СА), роли эмоциональных проблем в ограничении жизнедеятельности (РЭ), психического здоровья (ПЗ) и общего здоровья (ОЗ). Каждый показатель вычисляли в соответствии со шкалой от 0 до 100 баллов: чем ниже балл, тем хуже КЖ.
Дополнительно проводили тестирование пациентов с применением Сиэтловского опросника стенокардии (SAQ) [19] и Госпитального опросника тревоги и депрессии (HADS). Среди разработанных специализированных опросников для стенокардии SAQ считается наиболее чувствительным и воспроизводимым, удобным в использовании самостоятельным клиническим психодиагностическим инструментом [20, 21].
Статистический анализ данных проводили с помощью программы Statistica 6.0. При описании показателей, представленных в виде альтернативных переменных, приведены число наблюдений и доля пациентов (в процентах). Для описания показателей, представленных в виде количественных переменных, использовали среднее значение ± стандартное отклонение (М±s). Для оценки достоверности внутри- и межгрупповых различий показателей в динамике использовали одновыборочный критерий t, критерий Вилкоксона (для внутригрупповых сравнений) и критерий Манна—Уитни (для межгрупповых сравнений). Различия считали статистически значимыми при р<0,05.
Результаты
В табл. 2 отображена сравнительная характеристика параметров, отражающих ПФН у пациентов в группе ИГГТ и в группе контроля. После курса ИГГТ у пациентов отмечен статистически значимый прирост исходно сниженной по отношению к возрастным нормативам ПФН, что проявлялось в достоверном приросте времени физической нагрузки (протокол BRUCE), пикового потребления кислорода (р=0,03), его процентной доли от должных величин, а также потребления кислорода на уровне анаэробного порога (АП). После курса тренировок АП достоверно увеличился с 12,5 до 13,4 мл/кг/мин (р=0,002), а через 1 мес по их окончании — до 13,6 мл/кг/мин (р=0,0005). В группе плацебо-процедур достоверной динамики значений анализируемых показателей не отмечено.
Кроме того, в группе ИГГТ отмечалось снижение частоты возникновения ангинозных приступов во время повторных проведений нагрузочного теста на 50% сразу после процедур ИГГТ и на 75% через 1 мес после ИГГТ по сравнению с исходными значениями.
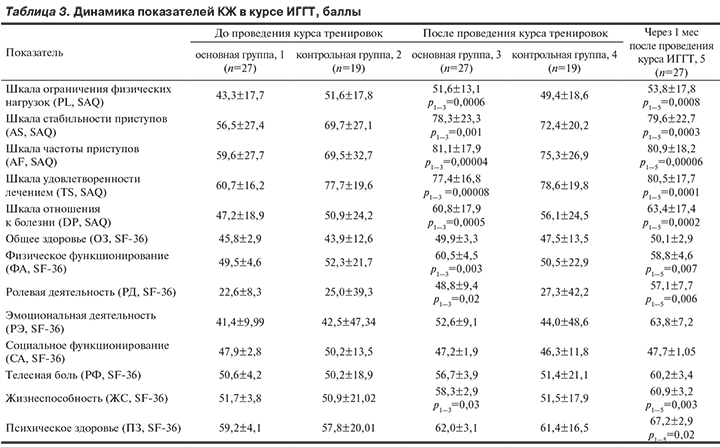
Повышение уровня ПФН у пациентов, прошедших курс ИГГТ, сопровождалось существенным улучшением субъективно оцениваемого КЖ по ряду шкал психодиагностических опросников (табл. 3). Так, по динамике показателей специфического Сиэтловского опросника стенокардии установлено статистически значимое улучшение по шкалам ограничения физических нагрузок (р=0,0006), стабильности приступов (р=0,001) и частоты приступов (р=0,00004). Отмеченные позитивные сдвиги сохранялись и через 1 мес после курса процедур. Важной представляется также позитивная динамика по шкалам психологического отношения к болезни (р=0,0005) и общей удовлетворенности лечением (р=0,00008). В группе пациентов, которым проводились плацебо-процедуры, достоверных изменений по шкалам теста SAQ не наблюдалось.
Достоверное улучшение в опытной группе было отмечено и при анализе данных опросника SF-36, причем позитивная динамика наблюдалась в оценках по шкалам, характеризующих физическую составляющую общей субъективной оценки здоровья: физическое функционирование, ролевая деятельность и жизнеспособность. Достигнутые субъективно оцениваемые улучшения состояния КЖ пациентов отмечались и через 1 мес после ИГГТ. По шкале «психическое здоровье» достоверный прирост показателя отмечен лишь через 1 мес после окончания курса ИГГТ — с 59,2±4,1 до 67,2±2,9 (р=0,02).
При анализе результатов применения опросника HADS в группе ИГГТ отмечалось достоверное снижение оценок по шкале «депрессия» после тренировок с 6,5±2,9 до 5,1±2,8 балла (р=0,02) и через 1 мес — до 4,9±2,5 балла (р=0,002). По шкале «тревога» в группе ИГГТ отмечалось достоверное снижение оценки с 8,6±2,3 до 6,2±3,1 балла (р=0,08) после тренировок и до 3,8±2,1 балла (р=0,02) через 1 мес. В группе контроля достоверных изменений оценок по шкалам опросников SAQ и HADS также не наблюдалось.
Полученные результаты позволили пересмотреть и провести анализ динамики клинической оценки ФК стенокардии напряжения у пациентов в группе ИГГТ. Отмечено сокращение числа пациентов с III ФК с 26 до 7% (такая динамика сохранялась через 1 мес после курса ИГГТ), прежде всего за счет перехода отдельных пациентов в I ФК. Однако выявленная динамика была нестабильной — через 1 мес после процедур число пациентов с I ФК сократилось. Стоит отметить, что в контрольной группе (пациенты аналогично получали оптимальную медикаментозную терапию) также отмечалось формирование группы пациентов с I ФК стенокардии (11%), однако число пациентов с III ФК в этой группе оставалось неизменным (11%).
Приобретенный опыт применения метода ИГГТ позволяет характеризовать метод как безопасный и хорошо переносимый пациентами. За время проведения плацебо- или гипоксических-гипероксических процедур (общее число ИГГТ составило 690), несмотря на существенную нагрузку — дыхание гипоксической смесью, что сопровождалось снижением индивидуальных значений SaO2 до 80—84%, — наблюдались единичные побочные эффекты, при которых не требовалось прекращение процедур. Умеренное чувство нехватки воздуха, учащенное сердцебиение либо легкое головокружение наблюдались у 5 (19%) больных в группе ИГГТ. Все побочные явления проходили к 4—5-й процедурам. Число пациентов, отметивших побочные явления, в сравниваемых группах статистически значимо не различалось. Большинство пациентов отмечали релаксирующее, сомногенное действие процедур ИГГТ, а периоды гипероксии были оценены ими как «освежающие», быстро снимающие некоторые неприятные ощущения и умеренно выраженную одышку в гипоксические фазы тренировки.
Обсуждение
Расширение средств реабилитации и вторичной профилактики, повышение КЖ пациентов с ИБС имеет большое медико-социальное значение. К числу таких перспективных технологий можно отнести методы адаптации к гипоксическим газовым смесям в различных режимах [3, 14]. Проведено несколько исследований, подтверждающих позитивные эффекты длительных гипоксических тренировок в интервальном режиме в повышении ПФН и коррекции факторов риска развития сердечно-сосудистых осложнений у кардиологических больных [10, 22], в частности у пациентов со стабильной стенокардией напряжения [3, 23]. Проведение ИГТ в режиме цикличного чередования периодов дозированной гипоксии и гипероксии является принципиально новой технологией повышения неспецифических адаптационных возможностей организма пациентов с ИБС.
В проведенном рандомизированном плацебо-контролируемом исследовании выявлено, что курс процедур ИГГТ на фоне оптимальной медикаментозной терапии статистически значимо повышает ПФН пациентов со стабильной стенокардией напряжения II—III ФК, что объективизировано проведением кардиопульмонального нагрузочного тестирования с газовым анализом (достоверно возросли значения пикового потребления кислорода, АП). Важно, что достигнутый результат сохранялся и через 1 мес после окончания курса ИГГТ, что ранее не было предметом специального анализа в сходных клинических исследованиях эффектов ИГТ [10].
Принципиально важным представляется одновременное улучшение практически у всех пациентов субъективного восприятия КЖ, что продемонстрировано в динамике оценок по шкалам специфического опросника стенокардии SAQ, а также по шкалам опросника SF-36, характеризующих субъективную оценку здоровья: «физическое функционирование», «ролевая деятельность» и «жизнеспособность». Показано [20, 21], что КЖ пациентов с ИБС существенно снижено, причем по мере увеличения ФК стенокардии физическое функционирование больных нарушается в большей степени, чем психологическое. В проведенном исследовании установлено, что после завершения курса ИГГТ у пациентов не только улучшается физическое функционирование (по опроснику SF-36), но и отмечается улучшение клинической картины заболевания, что выражается снижением ФК стенокардии, а также уменьшением количества ангинозных приступов и кратности приема нитратов короткого действия.
В качестве позитивного эффекта следует также отметить повышение после курса ИГГТ самооценок пациентов своего психологического состояния, а также удовлетворенности лечением, что можно рассматривать как повышение мотивации больных и их приверженности к рекомендуемому лечению.
Особое внимание в работе было уделено оценке безопасности применения технологии ИГГТ в лечении больных выбранной категории. Полученные результаты минимальных побочных эффектов при проведении процедур ИГГТ в целом подтверждают безопасность метода и более комфортную переносимость процедур по сравнению с традиционными протоколами гипоксически-нормоксического прекондиционирования, отмеченные в наших предыдущих работах [12, 13, 24]. Установленные нами и другими авторами оптимизирующие эффекты гипоксических тренировок в отношении модифицируемых факторов риска развития кардиометаболических нарушений открывают перспективы применения ИГГТ в качестве дополнительного метода лечения и реабилитации больных стабильной стенокардией напряжения.
Выводы
Получено клиническое подтверждение эффективности интервальных гипоксических-гипероксических тренировок у пациентов со стабильной стенокардией напряжения на фоне оптимальной медикаментозной терапии: применение курса интервальных гипоксических-гипероксических тренировок у пациентов с ишемической болезнью сердца повышает переносимость физических нагрузок, устойчивость к эпизодам гипоксии, а также сопровождается повышением качества жизни, снижением количества ангинозных приступов, сокращением кратности приема нитроглицерина.
Установлены безопасность и удовлетворительная переносимость процедур интервальных гипоксических-гипероксических тренировок с минимальными побочными эффектами в виде преходящих легкого головокружения, чувства нехватки воздуха, что не требовало прекращения проведения процедур. Таким образом, режим интервальных гипоксических-гипероксических тренировок хорошо переносится пациентами.
Ограничения исследования. В рамках исследования эффективности и безопасности метода ИГГТ по организационно-методическим соображениям не проведен сравнительный анализ эффектов ИГГТ и гипоксического прекондиционирования в режиме ИГТ, что потребовало бы обследования еще одной группы пациентов. Пациенты группы контроля получали плацебо-процедуры, дыша через маску прибора увлажненным атмосферным воздухом и не испытывая каких-либо затруднений, что потенциально могло ими не восприниматься как «медицинская процедура». Оптимальная медикаментозная терапия оценивалась со слов пациентов без проверки концентраций лекарственных средств в крови пациентов, что не позволяет исключить эффект повышения приверженности к проводимому лечению у пациентов в 2 группах пациентов.
Благодарности. Авторы выражают благодарность компании AiMediqS.A. (Люксембург) за предоставленный опытный образец прибора ReOxy для проведения гипоксических-гипероксических тренировок пациентов.
Информация о конфликте интересов/финансировании.
Конфликт интересов не заявляется.
Авторы подтверждают отсутствие спонсоров работы.
Аппарат Reoxy (производство «AIMediq S.A.», Люксембург) предоставлен компанией-производителем безвозмездно. Компания и ее представители не участвовали в дизайне исследования, сборе, анализе и интерпретации данных, в подготовке публикации.
Исследование выполнено при частичной поддержке Российского гуманитарного научного фонда, грант №17-06-00784 «Качество жизни пожилых больных с сердечно-сосудистой патологией: влияние процедур адаптации к интервальной гипоксии-гипероксии».



