Кардиопротекторные свойства магния обусловлены комплексным влиянием иона Mg2+ на состояние сердечно-сосудистой системы: воздействием на тонус сосудов (и, следовательно, регуляцию артериального давления — АД) [1]; ритм сердца — дефицит магния ассоциирован с аритмиями [2]; энергетический метаболизм сердца [3], тромбообразование и тромболизис [4], обмен жиров [5] и формирование атеросклеротических бляшек на сосудистой стенке [6, 7]. В статье подробно разобраны клинические аспекты применения в кардиологии как сульфата магния (внутривенно), так и пероральных форм магния в виде органических солей (оротат магния, цитрат магния, аспартат магния и др.), которые проиллюстрированы во многих доказательных исследованиях [8—10].
Важно помнить, что обеспеченность организма магнием достоверно ассоциирована с продолжительностью жизни. Например, в исследовании Nurses’ Health Study (n=88 375) дефицит магния был ассоциирован с повышенным риском внезапной сердечной смерти (ВСС, диагноз I46.1 по МКБ-10).
За 26 лет наблюдений зарегистрировано 505 случаев ВСС. Относительный риск ВСС был значительно ниже у женщин в квартили с самым высоким потреблением магния (>345 мг/сут) по сравнению с самым низким потреблением (<261 мг/сут) риск ВСС был снижен на 37% (относительный риск — ОР 0,63 при 95% доверительном интервале — ДИ от 0,44 до 0,91). Более высокие уровни магния в плазме крови также были достоверно ассоциированы со значительным снижением риска ВСС: по сравнению с квартилем пациенток с самыми низкими уровнями магния в плазме (менее 0,79 ммоль/л) у пациенток в квартиле с самыми высокими (более 0,88 ммоль/л) риск ВСС был снижен почти в 5 раз (ОР 0,23 при 95% ДИ от 0,09 до 0,60). При этом возрастание уровней магния в плазме на каждый 0,1 ммоль/л соответствовало снижению риска на 41% при 95% ДИ от 15 до 58% [11].
Экспериментальные и клинические исследования свидетельствовали о большой роли обеспеченности организма магнием для поддержания оптимального тонуса сосудов. В эксперименте диеты, обогащенные магнием (в том числе повышенное содержание магния в питьевой воде), нормализовали АД на минералокортикоид-солевых моделях артериальной гипертонии (АГ) [12] (в частности, за счет воздействия на активность эндотелина-1 [13, 14]) и нормализовали агрегацию тромбоцитов [15]. Пероральный прием магния в эксперименте снижает АД на моделях преэклампсии, вызванной длительной блокадой синтеза оксида азота [16].
В настоящей работе представлены результаты систематического анализа данных клинических исследований ролей магния в поддержании нормального, физиологического АД. Кроме того, последовательно рассматриваются взаимосвязь между уровнем магния и электролитным балансом, гипомагниемией и сосудистым тонусом, сопутствующими АГ заболеваниями, клинико-эпидемиологические данные по взаимосвязи гипомагниемии с риском развития сердечно-сосудистых заболеваний (ССЗ). Рассмотрены вопросы диагностики гипомагниемии, влияния магния на фармакодинамику антигипертензивных препаратов и результаты клинических работ по использованию пероральных форм магния в кардиологии для нормализации АД.
Магний, электролиты и микроэлементный баланс
С точки зрения молекулярной физиологии, ионы магния и кальция, натрия и калия являются электролитами фундаментального характера, посредством которых поддерживается электролитный баланс всего организма. Соотношения Na:K, Mg:Ca имеют фундаментальное значение для поддержания баланса всех макро- и микроэлементов. Магний имеет особое значение в поддержании уровней основных электролитов натрия и калия в диапазоне нормы. Пероральный прием магния предотвращает развитие алкогольной АГ за счет сокращения внутри-клеточной концентрации натрия, вызываемого активацией Mg-зависимых Na/K-насосов [17]. Проведенный нами ранее систематический анализ показал, что калийсберегающие свойства магния могут осуществляться посредством таких молекулярных компонентов, как АТФ-чувствительные выпрямительные калиевые каналы, Na/K-АТФазы и их регуляторный белок SIK1, транспортер SLC12A3 и WNK-киназы [18].
Исследование с участием 60 пациентов с острым инфарктом миокарда (ОИМ) и 100 лиц контрольной группы показало, что соотношения Са:Mg, K:Mg и Na:K у пациентов с ОИМ были значительно выше, чем в контроле (р<0,001). Анализ уровней электролитов как предикторов ОИМ методами машинного обучения позволил установить пороговые значения соотношений, оптимальные для наиболее точной диагностики, — Na:Mg (40,9), Са:Mg (3,4) и К:Mg (2,7) [19].
Терапия АГ в сочетании с железодефицитной анемией (ЖДА) представляет особую сложность. Поэтому определенный интерес вызывает взаимосвязь уровней магния с уровнями гемоглобина. Например, в группе 184 пациентов с АГ установлены корреляции более высоких уровней магния в плазме с более высокими уровнями гемоглобина (r=0,155; р=0,037), альбумина (r=0,180; р=0,018) и с более низким пульсовым АД (r=–0,156; p=0,035) [20]. В то же время в крупном проспективном исследовании COSM (n=36882; 45—79 лет) показано, что недостаточное потребление железа, причем именно в сочетании с недостаточным потреблением кальция, магния и цинка, соответствовало 3-кратному повышению риска развития ОИМ (ОР 3,0 при 95% ДИ от 1,43 до 5,82) [21].
Результаты этих исследований подтверждены в недавно проведенном скрининге магниевого статуса у россиян (n=2000; 18—90 лет). Наличие клинических признаков дефицита магния соответствовало 7-кратному повышению риска развития ЖДА, уровни магния плазмы крови менее 0,80 ммоль/л — 2-кратному риску (р=5,8·10–6), а уровни магния в эритроцитах менее 1,50 ммоль/л — 5-кратному повышению риска ЖДА [22].
 Взаимосвязь между ЖДА и дефицитом магния обусловлена, вероятно, алиментарным фактором. Например, низкое потребление зеленолистных растений характерно как для дефицита магния, так и для дефицита фолатов, необходимых для осуществления биологических функций железа. Низкое потребление зеленолистных растений также соответствует дефициту витамина С и биофлавоноидов (витамин Р), необходимых для усвоения железа из желудочно-кишечного тракта [23].
Взаимосвязь между ЖДА и дефицитом магния обусловлена, вероятно, алиментарным фактором. Например, низкое потребление зеленолистных растений характерно как для дефицита магния, так и для дефицита фолатов, необходимых для осуществления биологических функций железа. Низкое потребление зеленолистных растений также соответствует дефициту витамина С и биофлавоноидов (витамин Р), необходимых для усвоения железа из желудочно-кишечного тракта [23].
Магний оказывает позитивное влияние на гомеостаз ультрамикроэлемента рубидия. Рубидий является иммуномодулятором, и нарушения обмена рубидия ассоциированы с хроническим воспалением. Обмен рубидия связан с магнийзависимым транспортным белком Na/K-АТФазой, нарушения активности которого приводят к гипертонии и формированию катаракты. В эксперименте магнийдефицитная диета в течение 7 нед приводила к значительному снижению концентрации магния в сыворотке крови. При этом отмечено резкое снижение поглощения эритроцитами рубидия, что способствует возникновению рубидиевого дефицита в организме [24].
Гипомагниемия и сосудистый тонус: клинические исследования
Дефицит магния и ранняя АГ у подростков. Элементный статус подростков 15—18 лет (n=176) с высоким нормальным АД характеризуется снижением содержания магния и калия и накоплением натрия, токсичных и условно-токсичных микроэлементов. При этом у девушек чаще наблюдаются гипоэлементные состояния Mg, K, Zn, Cr, Mn, Br, As, Al при увеличении содержания Na, Sn, Sb; у юношей преобладают гиперэлементозы Na, Sn, Sb, Ba, P при снижении содержания K, Br, Cr. При АГ у юношей гипоэлементные состояния дополняются дефицитами магния, рубидия и цинка.
Дефицит магния при АГ у беременных. В сроке до 20 нед беременности изучен макро- и микроэлементный статус у 68 женщин (25 — с хронической АГ, 31 женщины с нормотензивной беременностью — контроль). Хроническая АГ определялась как повышение систолического АД (САД) более 140 мм рт.ст. и/или диастолического АД (ДАД) более 90 мм рт.ст., зарегистрированное до наступления беременности или в сроке до 20 нед гестации. Макро- и микроэлементный статус беременных с хронической формой АГ характеризуется недостаточностью магния и калия на фоне избытка натрия [25, 26].
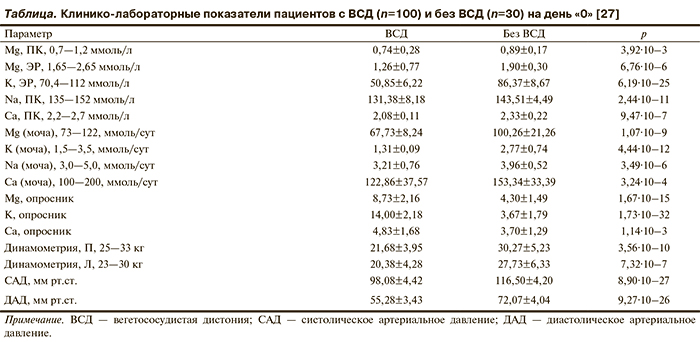
Дефицит магния и астения. В ходе исследования взаимосвязи пониженного АД и дефицита магния собраны данные по 145 антропометрическим и клинико-лабораторным параметрам для 130 участников (19±1 год, 119 девушек, 11 юношей), включая 100 пациентов с установленным диагнозом вегетососудистой дистонии (ВСД) (МКБ-10 — G.90.9). Для пациентов с ВСД были характерны выраженное снижение АД (САД 98,08±4,42 мм рт.ст., контроль, 116,50±4,20; р=8,90·10–27; ДАД 55,28±3,43 мм рт.ст., контроль — 72,07±4,04; р=9,27·10–26) на фоне повышения плотности β-адренорецепторов на эритроцитах («β-АРМ» >18, что соответствует симпатикотонии; р=1,04·10–4) [27].
Важно отметить, что пациенты с ВСД характеризовались систематическими нарушениями электролитного баланса: уровни 4 основных электролитов — Na+, K+, Ca2+, Mg2+ — в плазме крови, эритроцитах и в суточной моче у пациентов с ВСД были достоверно ниже, чем у здоровых участников (см. таблицу). Данным лабораторных исследований соответствовали результаты оценки клинической картины дефицита минералов: балльные оценки дефицита магния, калия и кальция были также достоверно выше у пациентов с ВСД. Недостаточность магния и калия коррелировала с астенической конституцией пациентов с ВСД, снижением мышечной силы и гипотонией [27].
Заболевания, сочетающиеся с АГ и диагнозом Е61.2 «Недостаточность магния». Результаты крупного скринингового обследования пациентов лечебных стационаров, поступивших в медицинские учреждения 7 регионов России (n=2000), свидетельствуют о высокой частоте сочетания сниженного уровня магния в крови и ряда заболеваний. В исследованной когорте пациентов установлено преобладание сочетанных состояний: среднее число диагнозов МКБ-10 на одного пациента составило 1,9±1,3 диагноза (при 95% ДИ от 1 до 6). Уровни магния были обратно пропорциональны числу диагнозов, т.е. более высокие уровни магния соответствовали более низкому числу сочетанных состояний у пациента. Уровень магния в плазме менее 0,80 ммоль/л ассоциирован со статистически значимым повышением риска развития многочисленных заболеваний и патологических состояний, в том числе судорог (R56.8), пароксизмальной тахикардии (I47.9), пролапса митрального клапана (I34.1), нестабильной стенокардии (I20.0), эссенциальной АГ (I10), избыточной массы тела (Е66.3), ожирения (Е66), инсулиннезависимого сахарного диабета (СД) с осложнениями (E11.7, E11.8) [22].
Важно отметить, что в ходе скрининга выявлено сочетание АГ (I10 «Эссенциальная первичная гипертония») с такими заболеваниями, как E11.7 «Инсулиннезависимый сахарный СД: с множественными осложнениями» (ОШ 3,89; р=2,3·10–5); Е66.3 «Избыточная масса тела» (ОШ 2,53; р=2,5·10–3); F43.0 «Острая реакция на стресс» (ОШ 2,79; р=4,6·10–4); I20.9 «Стенокардия неуточненная» (ОШ 5,76; р=1,3·10–15) и с уровнями магния в плазме крови менее 0,80 ммоль/л (ОШ 1,50; р=1,4·10–2) [22]. Заметим, что все перечисленные выше заболевания, в том числе АГ, сочетаются с диагнозом Е61.2 «Недостаточность магния».
Гипомагниемия и риск развития ССЗ: клинико-эпидемиологические данные
Более высокие уровни магния в суточной моче соответствует сниженному риску развития АГ. Среди участников исследования PREVEND (Prevention of Renal and Vascular End-stage Disease; n=5511; 28—75 лет) за 8 лет наблюдений у 1172 участников была зарегистрирована АГ (САД ≥140 мм рт.ст., ДАД ≥90 мм рт.ст. или прием антигипертензивных препаратов). При увеличении уровня магния в суточной моче на каждые 1 ммоль/л отмечено снижение риска развития АГ в среднем на 10% после поправок на возраст, пол, индекс массы тела, курение, употребление алкоголя, семейный анамнез [1] (рис. 1).
 Заметим, что цитируемые в данной работе исследования указывают на существование несомненной дозозависимой взаимосвязи между уровнями магния в плазме/сыворотке крови и риском развития ССЗ, в том числе АГ. Возникает вопрос, каким образом следует диагностировать гипомагниемию с практической точки зрения, т.е. при каком уровне магния в крови врачу следует «бить тревогу». Исследование, проведенное на основе базы данных ИМБД (База данных института микроэлементов), позволило систематически исследовать этот вопрос на основе данных для группы россиянок репродуктивного возраста (n=689; 20—45 лет) [28]. Анализ показал, что риск развития таких ССЗ, как АГ, гипотония, пролапс митрального клапана, пароксизмальная тахикардия и других, прогредиентно возрастает уже при снижении уровней магния в плазме крови менее 0,80 ммоль/л. При уровнях магния в плазме менее 0,70 ммоль/л риск развития рассматриваемых ССЗ достоверно возрастает в 2—5 раз, что указывает на необходимость использования порогового уровня не менее 0,80 ммоль/л для ранней диагностики гипомагниемии.
Заметим, что цитируемые в данной работе исследования указывают на существование несомненной дозозависимой взаимосвязи между уровнями магния в плазме/сыворотке крови и риском развития ССЗ, в том числе АГ. Возникает вопрос, каким образом следует диагностировать гипомагниемию с практической точки зрения, т.е. при каком уровне магния в крови врачу следует «бить тревогу». Исследование, проведенное на основе базы данных ИМБД (База данных института микроэлементов), позволило систематически исследовать этот вопрос на основе данных для группы россиянок репродуктивного возраста (n=689; 20—45 лет) [28]. Анализ показал, что риск развития таких ССЗ, как АГ, гипотония, пролапс митрального клапана, пароксизмальная тахикардия и других, прогредиентно возрастает уже при снижении уровней магния в плазме крови менее 0,80 ммоль/л. При уровнях магния в плазме менее 0,70 ммоль/л риск развития рассматриваемых ССЗ достоверно возрастает в 2—5 раз, что указывает на необходимость использования порогового уровня не менее 0,80 ммоль/л для ранней диагностики гипомагниемии.
Магний и фармакодинамика отдельных антигипертензивных препаратов
Содержание магния и кальция в скелетных мышцах у добровольцев (пациентов с АГ) является предиктором отклика на антигипертензивную терапию лизиноприлом и бендрофлуазидом. В группе 37 пациентов с АГ, получавших один из этих препаратов в течение 6 мес, исследовано содержание магния в биоптатах скелетных мышц до начала терапии. Соотношение между концентрациями магния и кальция в биоптатах мышц до лечения коррелировало с эффективностью терапии: более высокое соотношение Mg:Ca соответствовало более выраженной нормализации АД у пациентов (r=0,38; р<0,02) [29].
Пероральный прием препаратов магния пациентами, получавшими диуретики, нормализует уровни магния и калия в скелетных мышцах. В группе добровольцев (76 пациентов с АГ), получавших диуретики в течение 1—17 лет, уровни магния, калия и Na/K-насосов в скелетных мышцах были значительно ниже по сравнению контрольной группой (n=31). После приема препаратов магния в течение 6 мес уровни магния, калия и Na/K-насосов нормализованы у большинства пациентов [30].
Мета-анализ 9 рандомизированных исследований показал, что пероральный прием препаратов магния оптимизирует действие антигипертензивных препаратов. Длительный (6 мес и более) прием антигипертензивных средств в сочетании с препаратами магния (не менее 230 мг/сут) приводил к достоверному снижению АД. При использовании магния в дозах более 460 мг/сут эффект нормализации АД был максимален [31].
Пероральный прием препаратов органического магния способствует снижению АД при АГ в группе пациентов (n=92), получавших антигипертензивную терапию на начало исследования (ингибиторы ангиотензинпревращающего фермента, ингибиторы β-адренорецепторов, блокаторы кальциевых каналов, диуретики), в течение 6 мес и более. Дополнение курса лечения приемом препаратов магния (320 мг/сут, не менее 2 мес) было ассоциировано с дополнительным снижением САД на 15—20 мм рт.ст. и ДАД на и 5—9 мм рт.ст. в сторону нормы. Частота жалоб пациентов, в том числе на перебои, покалывание и боли в области сердца, нервозность, нарушение сна, раздражительность и плаксивость была достоверно снижена на фоне приема препаратов магния на основе органических солей [32].
Мета-анализ 7 рандомизированных исследований (n=135) показал, что пероральный прием магния способствует более выраженному снижению повышенного АД (САД 155 мм рт.ст.) у пациентов с АГ, принимающих антигипертензивные препараты (в среднем дополнительно на –19 мм рт.ст. при 95% ДИ от –14 до –22; р<0,0001) [33].
Клинические исследования пероральных форм магния в кардиологии: препараты магния per os и АГ
Пероральный прием препаратов магния эффективен для предотвращения повышенного АД во время беременности. Прием препаратов магния (300 мг/сут, цитрат магния) женщинами с первой беременностью, начиная с 25-й недели, был ассоциирован с более низким АД к 37-й неделе (72 мм рт.ст. — магний, 77 мм рт.ст. — контроль; р=0,031) [34].
Пероральный прием органической формы магния (магния аспартат гидрохлорид, 480 мг/сут Mg2+, 6 мес) также способствует снижению АД в группе женщин 35—77 лет (n=91) с умеренной АГ. При приеме аспартата магния ДАД достоверно снизилось в среднем на –3,4 мм рт.ст. (р=0,003) [35].
Пероральный прием препаратов органического магния снижает амбулаторное АД у пациентов с АГ. В группе 48 пациентов с неосложненной АГ 24 пациента принимали пироглутамат магния (600 мг/сут Mg2+, 12 нед) в дополнение к рекомендациям по изменению образа жизни, а 24 пациента вошли в контрольную группу. Прием магния соответствовал снижению среднесуточного САД (–5,6±2,7, контроль, –1,3±2,4 мм рт.ст.; р<0,001) и ДАД (–2,8±1,8, контроль, –1±1,2 мм рт.ст.; р=0,002) [36].
Мета-анализ 22 рандомизированных исследований (n=1173) показал, что прием пероральных препаратов магния (средняя доза 410 мг/сут при 95% ДИ от 120 до 973 мг/сут) ассоциирован с достоверным снижением САД на 3—4 мм рт. ст. и ДАД на 2—3 мм рт. ст., причем эффект усиливался при употреблении магния более 370 мг/сут [37].
Пероральный прием органических солей магния улучшает функцию сердечно-сосудистой системы у пожилых пациентов с СД. В исследовании 60 пациентов с СД старше 65 лет 30 человек принимали Mg-пироглутамат (368 мг/сут эл. магния), а 30 вошли в контрольную группу. Прием препарата магния привел к значительному улучшению поток-опосредованной дилатации (от 3,3±3,6 до 8,4±3,9%; р<0,05) по тесту с ацетилхолином [38].
Пероральный прием препарата магния снижает повышенное АД у пациентов с СД и АГ и в рамках другого рандомизированного двойного слепого плацебо-контролируемого исследования (n=82, 40—75 лет). Пациенты в группе «случай» принимали 450 мг/сут элементного магния (2,5 г/сут MgCl2) в течение 4 мес, в контрольной группе — только стандартную терапию. При приеме магния установлено достоверное снижение САД (–20,4±15,9 мм рт.ст., контроль, –4,7±12,7 мм рт.ст., р=0,03) и ДАД (–8,7±16,3, контроль, –1,2±12,6 мм рт.ст., р=0,02). Кроме того, прием магния способствовал нормализации липидного состава крови: повышались уровни липопротеинов высокой плотности в сторону середины интервала нормы (+0,1±0,6 ммоль/л, контроль, –0,1±0,7 ммоль/л, р=0,04) [39].
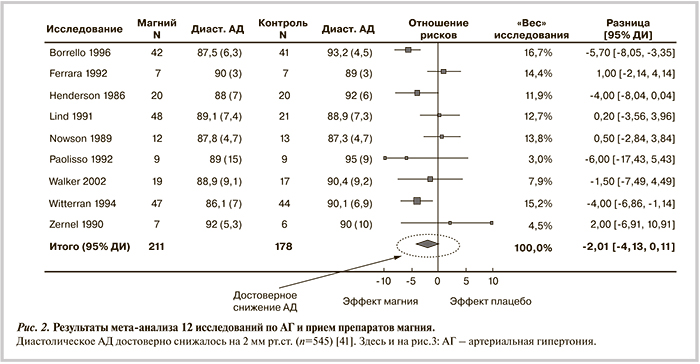
Эффективность включения препаратов магния per os в стандартные схемы лечения АГ подтверждена в ряде мета-анализов. Мета-анализ 12 рандомизированных исследований (n=545) показал эффективность перорального приема препаратов магния в течение 8—26 нед для контроля АГ у взрослых (САД >140 мм рт.ст. или ДАД >85 мм рт.ст.). По сравнению с плацебо прием препаратов магния приводил к статистически значимому снижению повышенного ДАД (в среднем на –2,2 мм рт. ст. при 95% ДИ от –3,4 до –0,9) [40] (рис. 2).
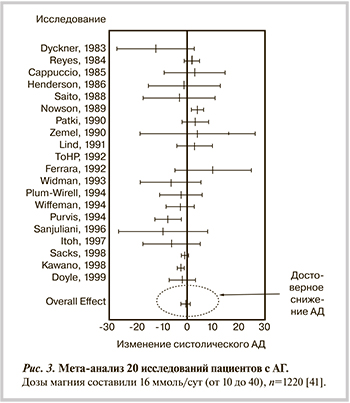
Мета-анализ 20 рандомизированных клинических исследований (n=1220) подтвердил эффективность воздействия препаратов магния per os в дозе 400 мг/сут (95% ДИ от 240 до 960 мг/сут) для снижения повышенного АД. Мета-анализ позволил установить дозозависимый эффект магния: при увеличении употребления магния на каждые 240 мг/сут САД снижалось в среднем на –4,3 мм рт.ст. (при 95% ДИ от –6,3 до –2,2 мм рт.ст.; р<0,001 ), ДАД — на –2,3 мм рт.ст. (при 95% ДИ от –4,9 до –0,1; р=0,08) [41] (рис. 3).
О кардиологическом использовании оротата магния
Фундаментальные исследования показали, что оротат магния является кардиопротектором in vitro и in vivo [42]. Исследования позволили установить комплексное воздействие оротата магния на функцию сердечно-сосудистой системы. Не только магний, но и оротовая кислота улучшают энергетический метаболизм миокарда, особенно после недавно перенесенного инфаркта. При этом в случае использования оротата магния также повышаются уровни «энергосодержащих» пуриновых и пиримидиновых фосфатов, а печенью стимулируется выпуск уридина в кровоток (что способствует восполнению истощенного при ишемии депо пиримидинов и пуринов в кардиомиоцитах). Оротат магния улучшает исход инфаркта миокарда, уменьшает тяжесть хронической дисфункции миокарда, повышает переносимость физической нагрузки у пациентов с ишемической болезнью сердца [43]. Результаты хемоинформационного анализа молекулы оротата магния показали, что оротат-анион оказывает выраженное кардиопротекторное действие [44].
В частности, оротат магния успешно используется в лечении АГ у беременных. В исследовании группы 150 беременных с АГ и дисплазией соединительной ткани (ДСТ) отмечено достоверное снижение выраженности симптоматики ДСТ, АГ, более благоприятное течение беременности и более частое успешное родоразрешение [45].
Длительный прием оротата магния (1500 мг/сут в течение 3 мес, по 2 курса в год в течение 15 лет) приводил к существенному улучшению состояния пациентов с пролапсом митрального клапана (n=31). Отмечено значительное сокращение среднего и максимального ритма сердца, числа эпизодов тахикардии, продолжительности интервалов QTc, пароксизмальных, наджелудочковых и желудочковых экстрасистол. Кроме того, выявлено достоверное снижение в сторону нормы повышенного САД и ДАД, снижение риска симпатикотонии в 2 раза и риска дисбаланса симпатической и парасимпатической частей вегетативной нервной системы в 5 раз [46].
Клинико-инструментальное обследование показало, что длительный прием оротата магния (50 мг/сут в течение 1-й недели, затем 25 мг/сут, в течение 4 мес) приводит к улучшению состояния подростков с такими формами ДСТ сердца, как пролапс митрального клапана и аномальные хорды сердца (chordae tendineae). Важно отметить, что в исследовании получено достоверное улучшение показателей гемодинамики, эхографии, ритма сердца и АД [47].
Заключение
Гипотензивный эффект внутривенного сульфата магния используется при оказании неотложной помощи пациентам с гипертоническими кризами и при артериальной гипертонии повсеместно и на протяжении десятков лет. Однако такой подход образно можно сравнить с тушением пожара. Прием органических солей магния per os часто упускается из вида и поэтому является неиспользуемым резервом антигипертензивной терапии. Мета-анализы показали, что прием органических солей магния per os (оротат магния, аспарагинат магния и др.) характеризуется самостоятельным антигипертензивным эффектом. Дополнение препаратами магния терапии β-адреноблокаторами и ингибиторами ангиотензинпревращающего фермента позволяет не только достичь более выраженного антигипертензивного действия этих препаратов, но и минимизировать их побочные эффекты (например, проаритмический и проатерогенный). В случае же сочетанного использования с диуретиками включение препаратов магния позволяет потенцировать и диуретический эффект, а также предотвращает развитие гипомагниемии вследствие усиленных потерь магния с мочой. Калийсберегающий эффект магния позволяет избежать такого опасного состояния, как гиперкалиемия, которая возникает при длительном использовании препаратов калия с ингибиторами ангиотензинпревращающего фермента или у пациентов с нарушениями функции почек.



