ВВЕДЕНИЕ
Среди ревматических заболеваний ревматоидный артрит (РА) – одна из наиболее изучаемых и дискуссионных тем. Это обусловлено широким распространением этой нозологии, значительной вариабельностью возраста пациентов, а также вероятностью быстрого прогрессирования заболевания при отсутствии или недостаточной эффективности терапии. Все эти факторы могут существенно влиять на качество жизни, физическое и психоэмоциональное состояние больных, в том числе вне зависимости от активности воспалительного процесса или патогенетической терапии [1, 2].
К числу таких факторов относятся коморбидные состояния, включая анемию – важный и недостаточно изученный аспект сопутствующей патологии при РА [3, 4]. Анемия может быть препятствующим фактором как для снижения активности заболевания, так и для применения некоторых препаратов [5, 6]. Это состояние, по данным литературы, встречается с частотой от 15 до 70% [4, 7, 8] и является самым распространенным гематологическим нарушением при РА [7].
Чаще всего анемию на фоне РА считают проявлением основного заболевания и рассматривают как анемию хронического воспаления (АХВ). В основе многофакторного патогенеза АХВ лежит хронически протекающее воспаление, выступающее ключевым фактором нарушений в цикле метаболизма железа. Кроме того, роль воспаления отмечена в нарушении выработки эритроидных предшественников, продукции эритропоэтина и длительности функционирования эритроцитов.
Как свидетельствуют исследования [5, 9], при РА часто наблюдается диссоциация между воспалительной активностью заболевания и тяжестью анемического синдрома, поскольку наряду с перераспределительным характером нарушения обмена железа, характерного для АХВ, большой процент анемий при РА обусловлен истинным дефицитом железа с развитием железодефицитной анемии (ЖДА). По этой причине долгое время анемия у пациентов с РА расценивалась как ЖДА из-за родства сопутствующих ей биохимических процессов с АХВ [4].
Однако клинической практикой подтверждено, что в случае больных РА данных в пользу высокой воспалительной активности при использовании стандартного набора биохимических тестов (показателей обмена железа) недостаточно для объективной оценки дефицита железа и, как следствие, дифференциальной диагностики ЖДА и АХВ [7–9]. Поэтому установление характера анемии у больных РА по-прежнему остается актуальной проблемой.
Частое необоснованное назначение препаратов железа при недифференцированной анемии на фоне РА определяет не только неэффективную терапию железом, но и назначение препаратов с риском развития осложнений («вторичная перегрузка железом»). В то же время длительная хроническая анемия с дефицитом железа (даже легкой степени) без должной терапии приводит к гипоксии тканей, что особенно опасно для пациентов с кардиологической патологией и хроническими заболеваниями почек [11, 12]. Наряду с этим доказано, что гипоксия тканей, являющаяся неизбежным следствием анемии, может способствовать нарушению процессов, связанных с делением, ростом и запрограммированной смертью клеток, а также с повышением синтеза коллагена и других компонентов фиброзного матрикса [5, 11]. Исследование крупной когорты больных РА с анемией показало, что повышение уровня гемоглобина на фоне проведенного лечения основного заболевания существенно повышает качество жизни и физическое состояние пациентов по сравнению с теми, у кого сохраняется сниженный уровень гемоглобина [13]. Поэтому разграничение АХВ и ЖДА имеет важное значение для клинической практики.
К сожалению, до настоящего времени в ревматологии не разработаны диагностические алгоритмы, позволяющие четко отделить истинную ЖДА от АХВ [6, 14]. За последнее десятилетие в связи с открытием системного регулятора обмена железа – гепсидина – был проведен ряд исследований [10, 15], которые позволяют предположить возможность использования этого биомаркера для диагностики характера анемии в случае иммуновоспалительных заболеваний, в частности РА [9, 16]. Установлено, что при коронавирусной инфекции COVID-19, лимфопролиферативных заболеваниях, новообразованиях уровень гепсидина значительно превышает нормальные значения. Однако у ряда пациентов наблюдается резкое понижение его содержания в сыворотке, что трактуется как проявление ЖДА [17, 18].
Цель исследования – разработать алгоритм с использованием гепсидина для дифференциальной диагностики АХВ от истинной ЖДА у больных с активным РА.
МАТЕРИАЛ И МЕТОДЫ
Исследование являлось проспективным. В анализ были включены 76 больных РА с высокой активностью воспалительного процесса по DAS28-СОЭ. Набор пациентов проводился последовательно, при поступлении на госпитализацию в ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой». Всего в исследовании приняли участие 66 женщин (86,8%) и 10 мужчин (13,2%).
Критерии включения в исследование: диагноз РА, соответствующий критериям EULAR 2010 г., возраст 18 лет и старше.
Критерии невключения: пациенты с мегалобластной и гемолитической анемиями, явными источниками кровопотери, новообразованиями, инфекционными заболеваниями, нарушениями функции почек и печени.
Из таблицы 1 видно, что средний возраст пациентов, отобранных в исследование, составил 48,9 ± 15,4 года, а средняя длительность РА – 61 мес. В большинстве случаев у больных диагностировалась поздняя клиническая стадия этого заболевания и его высокая воспалительная активность по DAS28 (63,2 и 73,7% соответственно). Преобладала позитивность по уровню ревматоидного фактора (РФ) и антител к циклическому цитрулинированному пептиду (АЦЦП). При рентгенологическом исследовании у участников чаще всего (51,3% случаев) определялась третья стадия РА. Системные проявления болезни выявлялись в 27,6% случаев.
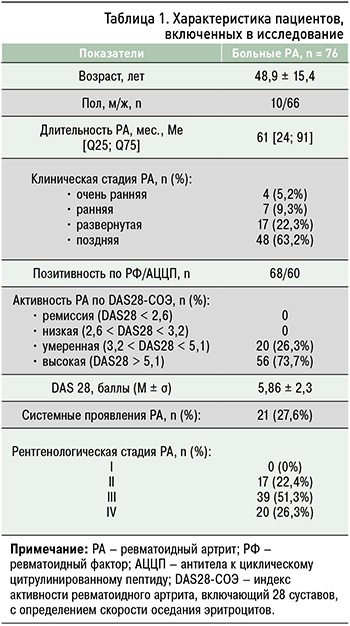
Исследование было проведено через локальный этический комитет ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой». Все пациенты подписали информированное согласие на участие в исследовании.
Пациентов разделили на две группы: основную, состоящую из 47 больных с анемией, и контрольную – 29 человек без анемии. Критерием анемии в соответствии с данными Всемирной организации здравоохранения (ВОЗ) считалось снижение уровня гемоглобина ниже 120 г/л для женщин и ниже 130 г/л для мужчин. Больные РА с анемией и без нее были сопоставимы по среднему возрасту (45,9 ± 13,1 и 48,6 ± 11,1 года соответственно) и длительности заболевания (р > 0,05).
Всем пациентам для оценки соответствия критериям включения/невключения были проведены общий и биохимический анализы крови. Также исследовались показатели метаболизма железа: сывороточное железо (СЖ), общая железосвязывающая способность сыворотки (ОЖСС), насыщение трансферрина железом (НТЖ), трансферрин и ферритин сыворотки (ФС). Исходя из цели исследования, у 76 пациентов определяли концентрацию гепсидина в сыворотке (набор The quantikine human immunoassy ELISA) и интерлейкина 6 (ИЛ-6). Уровень этого воспалительного цитокина измерялся методом иммуноферментного анализа с применением набора RayBio Human IL-6 ELISA.
Статистическая обработка данных выполнялась с применением программы Statistica, версия 10.0. Для анализа использовались среднее значение со стандартным отклонением (М ± σ) и медиана с интерквартильным интервалом Mе [Q25; Q75]. Сравнение групп проводилось с помощью t-критерия Стьюдента, а корреляционный анализ – методом Спирмена. Различия считались статистически значимыми при значении p < 0,05.
РЕЗУЛЬТАТЫ
В результате проведенного исследования установлено, что средние значения гепсидина (табл. 2) у больных РА, как с анемией, так и с нормальным уровнем гемоглобина, значимо не различались (85,8 ± 66,1 и 90,4 ± 37,9 пг/мл соответственно).
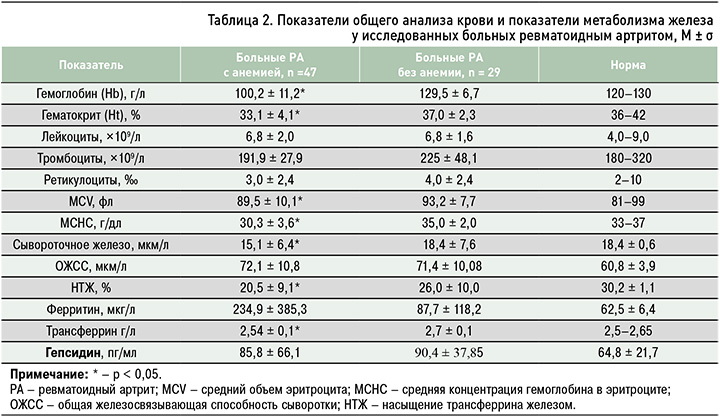
У пациентов с анемией наблюдались изменения в показателях обмена железа, что может быть важным фактором в развитии АХВ. Было обнаружено относительное снижение уровней гематокрита, СЖ, НТЖ и трансферрина в группе больных с анемией по сравнению с контролем. Значения этих показателей находились на нижней границе нормы, за исключением гематокрита. Уровень лейкоцитов, тромбоцитов, ретикулоцитов, объем клетки (MCV) и среднее содержание гемоглобина в эритроците оказались сопоставимы в обеих группах. Уровень исследуемого биомаркера – гепсидина – в основной и контрольной группах также не различался.
На первом этапе анализа для выделения истинной ЖДА у больных РА мы использовали двухступенчатый алгоритм с комплексной оценкой всех показателей метаболизма железа, разработанный в ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой» [9]. В соответствии с этим алгоритмом больные были разделены на две подгруппы. В первую подгруппу, с АХВ, вошли 27 человек, что составило 57,4% от всех пациентов с анемией. Вторую подгруппу (n = 20; 42,6%) составили участники с ЖДА.
На втором этапе изучались острофазовые показатели, уровень гепсидина (рис. 1) и показатели обмена железа (рис. 2) в указанных подгруппах. В первой подгруппе пациенты с АХВ имели достоверно более высокие средние значения гепсидина (120,3 ± 56,1 пг/мл) по сравнению с участниками без анемии (90,4 ± 37,9 пг/мл) и больными РА с ЖДА (см. рис. 1).
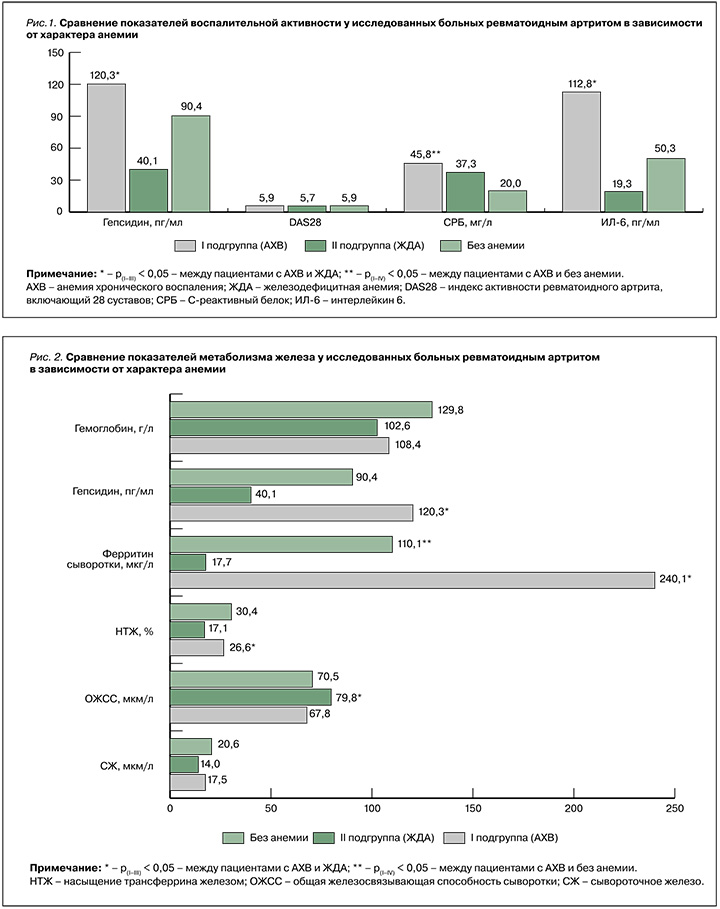
При изолированной АХВ отмечались более высокие значения DAS28, СРБ и ФС (см. рис. 2), отражающие высокую воспалительную активность болезни.
Учитывая патогенез АХВ, где основная роль отводится провоспалительным цитокинам, мы провели корреляционный анализ, который показал, что только при АХВ гепсидин коррелировал с уровнем ИЛ-6 (rил-6 = 0,8), тогда как у пациентов с ЖДА и больных без анемии (контрольная группа) такой взаимосвязи выявлено не было (rII = 0,3); (rIII = -0,18).
Стандартные биохимические показатели метаболизма железа, использующиеся в реальной клинической практике, позволили подтвердить, что оценка уровня гепсидина в сыворотке крови у больных с активным РА дает возможность дифференцировать истинную ЖДА и АХВ В. Как видно на рисунке 2, даже при активном воспалительном процессе во второй подгруппе больных (ЖДА) было обнаружено снижение насыщения трансферрина железа при повышенной ОЖСС и низком запасе железа, который определяется уровнем ФС. Все перечисленные изменения соответствовали общепринятым понятиям о классической ЖДА. При этом в первой подгруппе (с АХВ) уменьшение уровня гемоглобина сопровождалось нормальными уровнями СЖ, НТЖ, ОЖСС, трансферрина и высоким значениями ФС. На основании полученных данных мы предложили алгоритм дифференциальной диагностики анемии при РА (рис. 3).
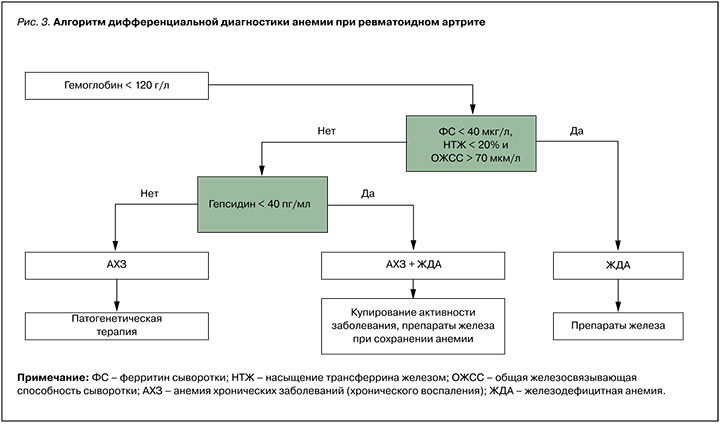
ОБСУЖДЕНИЕ
Железо – компонент, необходимый каждой клетке: хорошо известна его фундаментальная роль в транспорте кислорода посредством эритропоэза, оно является важной частью механизма производства энергии для эффективного функционирования всех структур организма [10, 18]. У пациентов с длительно существующим активным воспалительным процессом дефицит железа может быть особенно тяжелым; это способно усугубить течение основного хронического заболевания и привести к ускоренному клиническому ухудшению [11, 12, 19].
В клинической практике терапия пациентов с РА с высокой воспалительной активностью и анемией – сложная задача, поскольку почти в половине случаев анемия может иметь смешанный генез, объединяющий признаки АХВ и истинную ЖДА. Кроме того, клинические рекомендации и руководства по лечению разрабатываются для отдельных заболеваний и основаны на данных, полученных в ходе клинических испытаний, которые обычно исключают пациентов с сопутствующими заболеваниями, в том числе с ЖДА.
Согласно различным данным, истинный дефицит железа поражает 37–61% пациентов с хронической сердечной недостаточностью, 24–85% – с хронической болезнью почек и 13–90% – с воспалительными заболеваниями кишечника [5, 11, 20, 21]. По результатам нашего исследования установлено, что у больных РА с высокой воспалительной активностью и анемией истинная ЖДА диагностируется почти в половине случаев, что согласуется с данными литературы [4, 5].
Изученные в ходе исследования стандартные биохимические показатели обмена железа подтвердили сложность верификации истинной ЖДА у пациентов с высокой активностью РА. При анемии уровни СЖ находились на нижней границе нормы, но в то же время определялось достоверное повышение ОЖСС, отражающее степень «голодания» сыворотки и уменьшение насыщения железом трасферрина, что указывает на имеющийся истинный дефицит железа. Неслучайно при такой разнородности биохимических показателей обмена железа среди практикующих врачей существуют сомнения в вопросе дифференцировки больных РА с высокой воспалительной активностью по характеру анемии. Ситуацию осложняют схожесть симптомов анемии с клиническими признаками основного заболевания, недостаточно четко определенные диагностические критерии и лабораторные референсы ЖДА и АХВ, что и было продемонстрировано в нашем исследовании. Стоит отметить, что основной показатель, на который ориентируются при диагностике ЖДА, а именно уровень СЖ, находился в пределах нормальных значений в группах пациентов и с ЖДА, и с АХВ.
Как показано в этом исследовании, задачу диагностики ЖДА как элемента коморбидности при активном РА можно решить с помощью определения уровня сывороточного гепсидина. Повышенное содержание этого маркера было обнаружено только при АХВ, также у пациентов с указанной формой анемии отмечалась высокая воспалительная активность – повышение СРБ, ФС, а также ИЛ-6, что согласуется с данными других исследований [4, 15, 18, 20, 22].
Сывороточный уровень гепсидина может иметь практическую ценность не только для определения генеза анемии, но и прогнозирования ответа на пероральный прием препаратов железа. Более того, у пациентов с классической ЖДА показатели уровня гепсидина могут предсказывать неэффективность препаратов данной группы. В этом плане геспидин имеет лучшую прогностическую ценность по сравнению с СЖ и ФС [9, 18]. Определение его уровня может быть предложено как замена оценки показателей обмена железа, в том числе и ФС [15, 16, 18].
ЗАКЛЮЧЕНИЕ
Согласно результатам проведенного исследования, определение уровня сывороточного гепсидина может служить альтернативой измерению биохимических показателей обмена железа и использоваться в дифференциальной диагностике ЖДА и АХВ у больных РА с высокой активностью воспалительного процесса. У пациентов с РА и АХВ диагностируются значения гепсидина выше референсных, а при ЖДА – ниже.



