Гибридный подход является грудиносохраняющей малоинвазивной операцией на работающем сердце без применения искусственного кровообращения (ИК) с использованием техники ручного выполнения анастомоза между левой внутренней грудной артерией (ЛВГА) и передней нисходящей артерией (ПНА) через левопереднюю мини-торакотомию в сочетании с чрескожным коронарным вмешательством (ЧКВ) в других коронарных артериях (КА) для достижения полной функциональной реваскуляризации миокарда.
Исторически эта процедура была предложена для пациентов с высоким риском развития осложнений при традиционном коронарном шунтировании (КШ) через срединную стернотомию с ИК [1].
В последние годы гибридные операции вызывают все больший интерес при многососудистом поражении КА в связи с получением хороших результатов использования стентов с лекарственным покрытием, а также учитывая желание пациентов и кардиологов применять менее инвазивные методы лечения.
Несмотря на более чем 40-летний период интенсивных научных клинических исследований, существуют споры между кардиохирургами и интервенционными кардиологами относительно выбора наилучшего метода лечения пациентов с многососудистым поражением КА. Хирургическая реваскуляризация до сих пор связана с большим инвазивным вмешательством, риском развития геморрагических, неврологических, легочных, инфекционных и других осложнений, что особенно проявляется при лечении больных пожилого возраста. Использование стентов с лекарственным покрытием по сравнению с простыми металлическими стентами снижает частоту развития рестеноза. Риск развития рестеноза является довольно низким в широких КА с короткими неосложненными стенозами. При сложных атеросклеротических поражениях артерий все же наблюдается значительная частота развития рестеноза [2].
В исследовании SYNTAX у больных сахарным диабетом с трехсосудистым поражением КА частота рестеноза после установки нескольких стентов с лекарственным покрытием составила 14,2% за 12 мес [3]. В то же время при оценке результатов обычной послеоперационной ангиографии за 6—12 мес частота окклюзии аутовенозного шунта достигала 13—21% [4, 5]. Одинаковые ближайшие результаты проходимости стентов с лекарственным покрытием и венозных шунтов при коронарной реваскуляризации (не включающих ПНА) являются основой для гибридной операции в лечении больных с множественным поражением КА.
 В исследовании BARI [6] убедительно показано, что преимущество КШ в увеличении выживаемости больных связано с наличием функционирующего шунта ЛВГА-ПНА, а по результатам исследования SYNTAX при наличии изолированного проксимального поражения ПНА настоятельно рекомендуется проведение хирургической реваскуляризации (уровень доказательности I против II; см. таблицу).
В исследовании BARI [6] убедительно показано, что преимущество КШ в увеличении выживаемости больных связано с наличием функционирующего шунта ЛВГА-ПНА, а по результатам исследования SYNTAX при наличии изолированного проксимального поражения ПНА настоятельно рекомендуется проведение хирургической реваскуляризации (уровень доказательности I против II; см. таблицу).
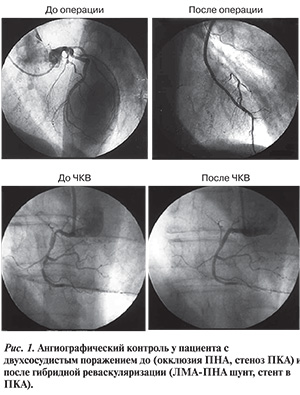
В то же время была разработана минимально-инвазивная хирургическая техника выполнения анастомоза ЛВГА-ПНА (MIDCAB — минимально-инвазивное прямое КШ), позволяющая избежать стернотомию, манипуляции на аорте, ИК и гарантировать тот же уровень качества шунта, как при стандартных коронарных операциях [7, 8]. Поэтому ЧКВ в сочетании с хирургической ЛВГА-ПНА (MIDCAB), так называемое гибридное, или интегрированное, вмешательство, имеет преимущества: стенты заменяют аутовенозные шунты, а шунт ЛВГА-ПНА выполняется с использованием малоинвазивной методики для уменьшения хирургической инвазивности и снижения частоты развития осложнений (рис. 1).
Гибридные операции пока не получили широкого распространения по ряду причин: недостаточное взаимодействие между кардиохиругами и интервенционными кардиологами; несовершенство в распределении времени и последовательности процедур; выполнение кардио-хирургической операции на фоне использования агрессивной антиагрегантной терапии; негативное отношение классического хирургического сообщества к минимально-инвазивным технологиям.
В результате этого стандартным подходом к хирургическому лечению больных с многососудистым поражением КА является стернотомия с выполнением анастомоза ЛВГА-ПНА и множественных аутовенозных шунтов в условиях ИК [9].
Однако интервенционные кардиологи, несмотря на недавние клинические рекомендации (2010), по-прежнему продолжают лечить больных с многососудистыми поражениями КА, устанавливая несколько стентов с лекарственным покрытием для снижения хирургического риска и для использования менее инвазивных методов лечения.
По этическим и научным соображениям существует доказанная необходимость убедить хирургов не выполнять лечение при многососудистом поражении КА только хирургическим путем, а также убедить интервенционных кардиологов обращаться к хирургии для проведения «идеальной» реваскуляризации ПНА.
Некоторые аспекты хирургической реваскуляризации
В исследовании SYNTAX убедительно показано, что КШ, выполненное с использованием срединной стернотомии и последующей полной реваскуляризацией, обеспечивает лучшие результаты по сравнению с ЧКВ с применением стентов, имеющих лекарственное покрытие, для пациентов с тяжелым многососудистым поражением КА [3].
По данным отчета STS, в США в 95% таких случаев производится шунтирование с использованием одной маммарной артерии и нескольких аутовенозных шунтов в условиях ИК с традиционной стратегией, применяющейся с 80-х годов прошлого века.
Несмотря на тенденцию к старению населения, нуждающегося в хирургических операциях, лишь единичные центры изменили тактику и стратегию выполнения оперативных вмешательств. Несколько методик хирургической реваскуляризации разработаны для того, чтобы избежать применения ИК, для выполнения малоинвазивного разреза грудной клетки или того и другого одновременно. С развитием технологий в целях уменьшения инвазивности шунтирования предложена операция OPCAB (Off Pump Coronary Artery Bypass) для достижения полной хирургической реваскуляризации через стернотомию без ИК, которая, казалось бы, вытеснила гибридный подход [10].
Лишь около 20% центров в США и Европе выполняют операцию OPCAB в повседневной практике. Однако ожидаемые преимущества не были достигнуты в полной степени из-за чрезгрудинного доступа, необходимости манипуляций на аорте и сложного доступа к заднебоковым ветвям, не гарантирующего высокое качество коронарного анастомоза по сравнению с традиционной операцией КШ [11]. Поэтому хирурги фактически осуществляют отбор пациентов для операции OPCAB, в большей степени основываясь на анатомии коронарных сосудов, а не на оценке факторов риска.
Кроме того, скорость развития окклюзии шунтов может зависеть от гемодинамически незначимых стенозов [12, 13], когда хирурги стремятся к полной анатомической реваскуляризации всех КА без оценки регионарного резерва кровотока.
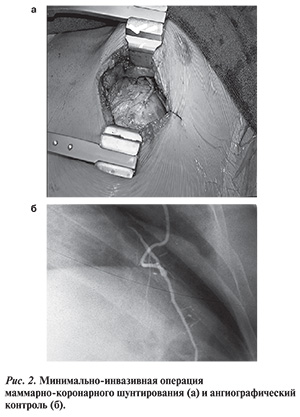
В связи с необходимостью выполнения стернотомии и кожных разрезов нижних конечностей для забора вен пациенты не понимают уменьшенной инвазивности операции OPCAB и предпочитают процедуры повторного стентирования. Парадокс современной хирургической реваскуляризации методом OPCAB состоит в том, что пациентам предлагается инвазивная процедура с применением субоптимальных аутовенозных шунтов [5, 14], схожих по эффективности со стентами с лекарственным покрытием. В то же время хорошие отдаленные результаты операции КШ в значительной степени связаны с качеством шунта ЛВГА-ПНА, отличающимся долговечностью [15], который может быть выполнен через щадящий доступ без разреза грудины и без остановки сердца (рис. 2) с тем же уровнем качества анастомоза, как и при ИК [11]. Обширные данные литературы подтверждают отличные ангиографические и клинические результаты операции MIDCAB [7, 8, 16, 17].
В дальнейшем, чтобы снизить объем манипуляций на грудной клетке, связанных с операцией MIDCAB, и уменьшить послеоперационный болевой синдром, стали применять торакоскопические и роботизированные методы выделения ЛВГА и наложения анастомоза ЛВГА-ПНА [18]. Эти технически более сложные операции освоены лишь немногими хирургами и пока не нашли широкого применения.
Следующий парадокс заключается в том, что с целью минимизации и так малоинвазивных операций ставится под угрозу качество анастомоза ЛВГА-ПНА (стенозы шунта ЛВГА-ПНА развиваются у 1% больных после операции OPCAB против 4,8% после эндоскопического выполнения анастомоза) [19].
 В настоящее время пациенты нуждаются в широком внедрении «золотого стандарта» коронарной реваскуляризации (шунта ЛВГА-ПНА) посредством малоинвазивного безопасного хирургического вмешательства, гарантирующего успешный результат.
В настоящее время пациенты нуждаются в широком внедрении «золотого стандарта» коронарной реваскуляризации (шунта ЛВГА-ПНА) посредством малоинвазивного безопасного хирургического вмешательства, гарантирующего успешный результат.
Одной из главных причин недостаточно широкого распространения гибридного подхода является то, что большинство кардиохирургов не освоили технику малоинвазивного КШ. Задачей является внедрение операции MIDCAB в каждый кардиохирургический центр.
Особенности применения стентов с лекарственным покрытием при многососудистых поражениях КА
Внедрение в клинику стентов с лекарственным покрытием привело к значительному снижению частоты рестеноза в сравнении со стентами без покрытия. Частота рестеноза была достаточно низкой в крупных сосудах с короткими неосложненными стенозами у пациентов, отобранных для клинических исследований.
Неполная реваскуляризация у пациентов, которым ЧКВ трудно или невозможно выполнить, в частности, при хронических окклюзиях, мелких, кальцинированных или извилистых сосудах, а также при продолжительных по длине атеросклеротических поражениях считается приемлемым подходом в кардиологической практике, когда правилом является последовательная, поэтапная и выжидательная стратегия.
Результаты исследования SYNTAX четко показали, что при многососудистом поражении КА и проксимальном поражении ПНА следует применять метод хирургической реваскуляризации, а не ЧКВ. В реальной жизни для лечения больных с проксимальными поражениями ПНА продолжают использовать ЧКВ со стентированием. При этом многие интервенционные кардиологи более осторожно подходят к комплексным сложным стенозам в связи с возможными правовыми последствиями.
Сочетанное использование ЧКВ и MIDCAB имеет преимущества оценки гемодинамически незначимых стенозов под контролем регионарного резерва кровотока, для которых реваскуляризация не имеет смысла [15].
Метод ЧКВ стал альтернативой для некоторых пациентов с поражением ствола левой КА, что получило отражение в изменениях рекомендаций кардиологов с III на IIb [20—22]. Ряд описательных исследований показал сопоставимые результаты кратко- и среднесрочной выживаемости после КШ и ЧКВ при стенозе ствола левой КА, за исключением более высокой частоты повторных реваскуляризаций у больных после ЧКВ [23, 24]. Относительно большой размер ствола левой КА делает этот сосуд привлекательным для ЧКВ в случае его локального стеноза. После выполнения операции MIDCAB стентирование левой главной КА становится более безопасным из-за функционирующего анастомоза ЛВГА-ПНА. Результаты гибридного подхода применительно к пациентам этой категории превосходят таковые при операции OPCAB [25].
Основное преимущество КШ в повышении выживаемости больных ишемической болезнью сердца объясняется наличием анастомоза ЛВГА-ПНА [15]. Гибридная реваскуляризация представляет минимально-инвазивную альтернативную стратегию, которая сочетает в себе высокую долговечность шунта ЛВГА-ПНА и малоинвазивные ЧКВ стентами с лекарственным покрытием для лечения поражений других артерий. Традиционный хирургический скептический взгляд по поводу частоты повторных реваскуляризаций при использовании ЧКВ должен быть пересмотрен в гибридной концепции. Кандидаты на гибридные операции имеют меньшую, чем при многососудистом ЧКВ, необходимость в повторных реваскуляризациях.
Таким образом, комбинация положительных качеств двух методов обеспечивает преимущества выживаемости, обусловленные созданием шунта ЛВГА-ПНА, и минимальную инвазивность ЧКВ.
Отбор пациентов и стратегии гибридной коронарной реваскуляризации
Отбор пациентов для гибридной коронарной реваскуляризации требует тесного сотрудничества кардиохирургов и интервенционных кардиологов. Например, при оценке анатомических особенностей коронарного русла в плане возможности выполнения ЧКВ и минимально-инвазивной ЛВГА-ПНА операции. Так, малый калибр или протяженный интрамиокардиальный сегмент ПНА могут стать противопоказанием к операции.
Идеальный кандидат на гибридную реваскуляризацию должен иметь подходящую ЛВГА для операции MIDCAB в случае проксимального поражения огибающей и правой коронарных артерий.
Абсолютными или относительными критериями исключения пациентов при отборе на гибридную реваскуляризацию являются стеноз левой подключичной артерии, известное повреждение левой маммарной артерии, внутримиокардиальное расположение ПНА, сопутствующее поражение клапанов, обусловливающее необходимость хирургической коррекции, выраженное ожирение, спайки в перикарде и плевральной полости, анатомически сложные (окклюзии, угловые, бифуркационные, кальцинированные поражения) для стентирования сужения КА и случаи рестеноза.
Порой сложный выбор оптимальной последовательности выполнения процедур (MIDCAB и ЧКВ), а также использование комбинированной антиагрегантной терапии у хирургических больных являются факторами, ограничивающими широкое распространение гибридного подхода. Поэтому мы должны вновь констатировать необходимость тесного сотрудничества между кардиохирургом и интервенционным кардиологом в выборе тактики лечения для получения оптимальных результатов. В большинстве случаев требуется индивидуальная стратегия, и попытка шаблонного подхода может увести в сторону и стать причиной нежелательных последствий.
Есть 3 варианта очередности выполнения гибридной реваскуляризации, каждый со своими потенциальными преимуществами и недостатками [26]: ЧКВ перед MIDCAB имеет преимущества минимизации риска ишемии во время MIDCAB, сохраняя традиционное КШ в качестве запасного варианта при неудачном или субоптимальном результате ЧКВ, и также является возможной стратегией после первичного ЧКВ, не связанного с ПНА. К недостаткам можно отнести отсутствие раннего ангиографического контроля ЛВГА-ПНА, возможную повышенную кровоточивость, так как MIDCAB осуществляется на фоне двухкомпонентной антитромбоцитарной терапии, риск тромбоза стента с прекращением применения антитромбоцитарных ингибиторов.
 MIDCAB перед ЧКВ имеет преимущества нивелирования агрессивной непрерывной антиагрегантной терапии после ЧКВ, выполнения обычной ангиографии ЛВГА-ПНА. ЧКВ при сложных стенозах высокого риска защищено функционирующим ЛВГА-ПНА шунтом. Недостатком является то, что операция MIDCAB осуществляется при остающихся стенозах в других КА, и в случае неудачного ЧКВ применять обычное КШ для исправления ситуации нежелательно. Кроме того, удваивается количество процедур коронарографии (до шунтирования и после).
MIDCAB перед ЧКВ имеет преимущества нивелирования агрессивной непрерывной антиагрегантной терапии после ЧКВ, выполнения обычной ангиографии ЛВГА-ПНА. ЧКВ при сложных стенозах высокого риска защищено функционирующим ЛВГА-ПНА шунтом. Недостатком является то, что операция MIDCAB осуществляется при остающихся стенозах в других КА, и в случае неудачного ЧКВ применять обычное КШ для исправления ситуации нежелательно. Кроме того, удваивается количество процедур коронарографии (до шунтирования и после).
Одновременное проведение MIDCAB и ЧКВ позволяет сразу осуществлять ангиографический контроль шунта ЛВГА-ПНА и ЧКВ при сложных стенозах КА высокого риска, достигая полной реваскуляризации за одну операцию. К недостаткам можно отнести возможный риск кровотечения при двухкомпонентной антитромбоцитарной терапии, применяемой сразу после операции, организационные хирургические, экономические и логистические аспекты [9, 27]. Мы считаем, что одновременное выполнение гибридной операции является более привлекательным для пациентов с психологической точки зрения, но требует специальной организации и оснащения, доступных не в каждом центре. Концепция, подразумевающая, что для гибридной реваскуляризации требуется «гибридный люкс», вводит в заблуждение и может стать еще одним препятствием для распространения метода.
На практике пациентам с многососудистым коронарным поражением и нестабильной стенокардией на фоне критического стеноза правой или огибающей КА сначала выполняют ЧКВ. Когда ПНА рассматривается как основная причина ишемии, последовательность действий меняется в обратном порядке, и сначала выполняется шунтирование. Первостепенное значение имеют взаимопонимание и тесное взаимодействие между интервенционными кардиологами и кардиохирургами.
Наконец, краткий комментарий о затратах. В настоящее время общая стоимость гибридной реваскуляризации, вероятно, превышает стоимость КШ в большинстве центров. Однако так как гибридный подход снижает частоту развития послеоперационных осложнений и по результатам сравним с обычной операцией OPCAB без ИК [9], пациенты возвращаются к работе и нормальной деятельности быстрее. Поэтому реальные затраты должны быть тщательно проанализированы. Выполнение большего числа процедур, дальнейшая интеграция и координация протоколов обеспечат клиническую эффективность и снизят экономические затраты.
Заключение
За последнее десятилетие операция MIDCAB стала хорошо изученным малоинвазивным вмешательством и может считаться одним из стандартных методов реваскуляризации, доступным для пациентов с ишемической болезнью сердца.
Больные ишемической болезнью сердца стали старше и, как правило, относятся к группе повышенного риска. Индивидуальный подход к реваскуляризации должен стать нормой в отношении каждого из них с возможностью свободного выбора из существующего арсенала вмешательств: традиционного коронарного шунтирования с использованием искусственного кровообращения, операций OPCAB, MIDCAB, стентирования и гибридной реваскуляризации.
После тщательной оценки коронарной анатомии и клинического состояния пациента кардиологическая группа специалистов (хирурги и интервенционные кардиологи) должна определить оптимальный для него метод реваскуляризации, максимально увеличивающий качество и продолжительность предстоящей жизни с наименьшим риском вмешательства.



