Частота фибрилляции предсердий (ФП) при ишемической болезни сердца (ИБС) достигает 34,5% [1]. При этом мало данных о результатах ее лечения у пациентов данной категории. В литературе встречается немного работ [2—7] по указанной проблеме, однако они основаны на небольших неоднородных группах пациентов без рандомизации и не дают полного представления об эффективности лечения данной тяжелой категории больных. Кроме того, предшествующие исследования, касающиеся операции Maze и различных ее модификаций, были в основном направлены на изучение смертности, заболеваемости, необходимости имплантации электрокардиостимулятора и восстановление транспортной функции предсердия после операции. Однако еще одним важным аспектом оценки результата операции служит выявление и оценка рецидивов ФП после аблации. Наиболее часто для этих целей используются более доступные способы, такие как плановые оценки стандартных электрокардиограмм (ЭКГ), холтеровское мониторирование (ХМ) ЭКГ (24 ч или 7 дней), приборы, активируемые пациентом, или автоматические и наружные регистрирующие устройства. Однако более информативным является непрерывный мониторинг ЭКГ, который может быть постоянным и длительным (2 года или более) с использованием имплантируемых устройств. При этом, несмотря на бесспорные преимущества имплантируемых устройств и их высокую диагностическую ценность при распознавании рецидивов ФП или трепетания предсердий (ТП), данные устройства довольно редко используются в клинической практике. Большинство авторов [8—11] продолжают использовать более привычные способы оценки эффекта операции и выявления рецидивов ФП, такие как стандартная ЭКГ, ХМ ЭКГ. В отечественной литературе совсем мало данных, посвященных этому вопросу [12—17].

Поэтому было проведено проспективное рандомизированное исследование, одной из целей которого была оценка эффективности радиочастотной абляции (РЧА) источника ФП у больных ИБС во время операции коронарного шунтирования (КШ) и оценка отсутствия ФП/ТП в отдаленном периоде на основе данных имплантируемых устройств мониторирования ритма.
Материал и методы
Обследование и лечение больных в рамках проспективного рандомизированного исследования проводили на базе центра хирургии аорты, коронарных и периферических артерий ФГУ «ННИИПК им. акад. Е.Н. Мешалкина» с марта 2007 г. по июнь 2012 г.
В исследование были включены пациенты, страдающие персистирующей ФП и ИБС с показаниями к аортокоронарному шунтированию. Согласно рекомендациям ACC/AHA/ESC (2012), под персистирующей формой ФП понимают эпизод ФП, не купирующийся самостоятельно, требующий медикаментозного лечения или выполнения электрической кардиоверсии продолжительностью обычно более 7 дней [18].
Всего в исследование были включены 95 пациентов: 74 (78%) мужчины и 21 (22%) женщина. Средний возраст пациентов составил 62,8±8,8 года. Пациенты методом случайной выборки были разделены на 3 группы: в 1-ю группу включен 31 пациент (24 мужчины и 7 женщин, средний возраст 64±7 лет), которым выполнялась радиочастотная изоляция устьев легочных вен с использованием системы Cardioblate и биполярного электрода Cardioblate BP; во 2-ю группу включены 30 пациентов (25 мужчин и 5 женщин, средний возраст 62,1±7,1 года), которым выполнялась радиочастотная модифицированная процедура mini Maze с использованием системы Cardioblate и биполярного электрода Cardioblate BP; в 3-ю группу (контрольную) включены 34 пациента (25 мужчин и 9 женщин, средний возраст 63,5±7 лет), которым выполнялась только операция КШ без устранения ФП.
У пациентов 1-й группы средняя длительность аритмии составила 63,9±84,1 мес (от 2 до 240 мес), причем у 2 пациентов имелись указания на перенесенные ранее эпизоды нарушения мозгового кровообращения. Во 2-й группе длительность аритмии колебалась от 4 до 480 мес, что в среднем составило 74,9±86,9 мес. Случаи нарушения мозгового кровообращения в анамнезе имелись у 3 пациентов. В контрольной группе пациенты с персистирующей формой ФП страдали аритмией до операции в среднем 44,8±82,9 мес (от 5 до 300 мес). Данные, подтверждающие нарушение мозгового кровообращения, получены у 8 пациентов. Больные основной и контрольной групп были сопоставимы по большинству клинико-демографических показателей, влияющих на прогноз и течение заболевания, но различались по длительности анамнеза аритмии до операции (р=0,03).
При анализе коронарограмм трехсосудистое поражение коронарного русла выявлено у 46 (48,4%) пациентов, двухсосудистое — у 33 (34,7%), поражение одного сосуда — у 14 (14,7%). Сравнительная характеристика больных в исследуемых группах представлена в табл. 1.
Техника операции. Для РЧА источника аритмии у всех пациентов использовали систему Cardioblate 6800 и соответствующий биполярный электрод. После выполнения срединной стернотомии подключали аппарат искусственного кровообращения по стандартной схеме. Затем, в соответствии с рандомизацией, выполняли соответствующую процедуру: радиочастотную изоляцию устьев легочных вен или радиочастотную модифицированную процедуру mini Maze, либо изолированное КШ.
Радиочастотная изоляция устьев легочных вен включала нанесение абляционной линии на устья легочных вен единым коллектором. Бранши электрода подводили сначала под правые легочные вены, выполняли абляцию с постоянным орошением изотоническим раствором натрия хлорида со скоростью 5 мл/мин до достижения трансмурального эффекта, регистрируемого системой. Затем электрод перекладывали по направлению к стенке предсердия на расстояние 2—3 мм от первой аблационной линии и выполняли повторную абляцию также до достижения трансмурального эффекта. Затем сердце выворачивали на хирурга и аналогичным образом выполняли абляцию левых легочных вен [13]. Наносили две абляционные линии. После этого выполняли этап КШ в изолированном виде или в сочетании с каким-либо другим вмешательством по показаниям.
 Модифицированная радиочастотная процедура mini Maze включала изоляцию устьев легочных вен единым коллектором, резекцию ушка левого предсердия, а также создание абляционных линий к левым верхней и нижней легочным венам и фиброзному кольцу митрального клапана [13]. Первым этапом выполняли изоляцию правых и левых легочных вен, как описано ранее. Затем отсекали ушко левого предсердия, бранши электрода заводили через отсеченное ушко по направлению к верхней и нижней левым легочным венам, выполняли абляцию до достижения трансмурального эффекта. После этого электрод устанавливали через отсеченное ушко по направлению к фиброзному кольцу митрального клапана под пальпаторным контролем хирурга, а затем по направлению к правым легочным венам по крыше левого предсердия. Наносили одну аблационную линию до трансмурального эффекта. Электрод извлекали, основание отсеченного ушка ушивали двурядным непрерывным швом монофиламентной нитью 4/0. Затем выполняли необходимое вмешательство на коронарных артериях.
Модифицированная радиочастотная процедура mini Maze включала изоляцию устьев легочных вен единым коллектором, резекцию ушка левого предсердия, а также создание абляционных линий к левым верхней и нижней легочным венам и фиброзному кольцу митрального клапана [13]. Первым этапом выполняли изоляцию правых и левых легочных вен, как описано ранее. Затем отсекали ушко левого предсердия, бранши электрода заводили через отсеченное ушко по направлению к верхней и нижней левым легочным венам, выполняли абляцию до достижения трансмурального эффекта. После этого электрод устанавливали через отсеченное ушко по направлению к фиброзному кольцу митрального клапана под пальпаторным контролем хирурга, а затем по направлению к правым легочным венам по крыше левого предсердия. Наносили одну аблационную линию до трансмурального эффекта. Электрод извлекали, основание отсеченного ушка ушивали двурядным непрерывным швом монофиламентной нитью 4/0. Затем выполняли необходимое вмешательство на коронарных артериях.
Для непрерывного длительного мониторинга ЭКГ в отдаленном послеоперационном периоде мы использовали имплантируемые устройства Reveal XT (рис 1, см. цветную вклейку). Данная система была имплантирована 53 пациентам (в 1-й группе — 21, во 2-й группе — 25, в 3-й группе — 7).
Техника имплантации устройства Reveal XT. Имплантацию данной системы осуществляли во время операции КШ одновременно с наложением второго ряда швов на подкожную жировую клетчатку (рис. 2, см. цветную вклейку). Выполняли разрез кожи протяженностью 2—3 см. В подкожно-жировой клетчатке формировали «карман» для датчика несколько меньших размеров по сравнению с аппаратом. Датчик помещали в ложе, ориентация которого такова, что полимерная часть направлена краниально, длинная ось датчика ориентирована под углом 45° к центральной линии тела пациента, параллельно электрической оси сердца. После этого выполняли послойное ушивание раны рассасывающейся нитью 3/0. В послеоперационном периоде на 4—7-е сут в зависимости от тяжести состояния пациента осуществляли активацию аппарата. В дальнейшем через 3, 6, 12 и 24 мес после операции проводили «опрос аппарата» (считывание зарегистрированных данных) и оптимизацию его работы.
Результаты
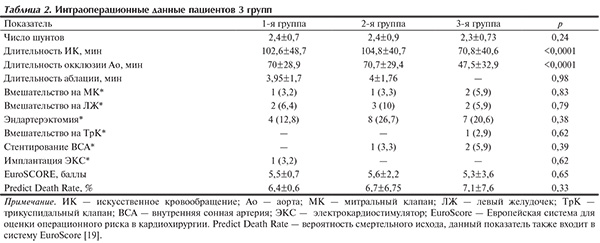
Операции КШ в сочетании с различными вариантами абляции ФП проходили в стандартном режиме без технических сложностей. Интраоперационные данные пациентов трех групп представлены в табл. 2.
Достоверные различия получены только по длительности искусственного кровообращения и длительности окклюзии аорты в группах, в которых выполнялась абляция ФП, и группе изолированного КШ. В раннем послеоперационном периоде все пациенты после выполнения абляции субстрата ФП получали антиаритмическую и антикоагулянтную терапию.
Средняя длительность пребывания пациентов в палате интенсивной терапии составила в 1-й группе 55,6±54,8 ч, во 2-й — 57,7±11,3 ч, в контрольной группе — 75,8±69,2 ч, при этом достоверных различий по продолжительности пребывания в палате реанимации не получено. При анализе длительности нахождения пациентов на искусственной вентиляции легких (ИВЛ) также достоверных различий не получено как между двумя основными группами, так и при сравнении с контрольной группой. В 1-й группе пациенты находились на ИВЛ в среднем 673,5±83,9 мин во 2-й — 674,5±84,8 мин, в контрольной — 484,2±186 мин.
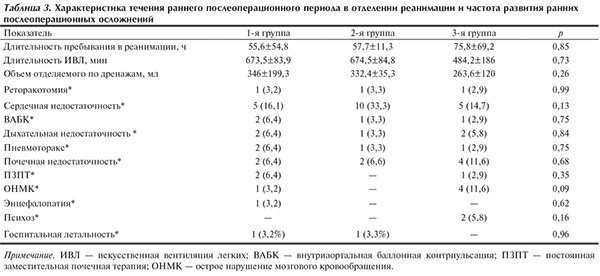
Анализ данных течения раннего послеоперационного периода в палате интенсивной терапии и реанимации представлен в табл. 3.
Не наблюдалось различий между основными и контрольной группами как по характеру послеоперационного течения, так и частоте развития осложнений в раннем послеоперационном периоде, достоверных различий не получено и при межгрупповом парном сравнении. Случаи смерти в стационаре отмечены в 1-й и 2-й группах (по одному), смерть не была связана с процедурами аблации, а была обусловлена исходной тяжестью состояния умерших. Пациент из 1-й группы умер от сепсиса вследствие тяжелого медиастинита на фоне сахарного диабета и тяжелой почечной недостаточности. Пациент из 2-й группы умер от фибрилляции желудочков на фоне сердечной недостаточности (фракция выброса ЛЖ 32%).
При выписке синусовый ритм регистрировался у всех пациентов из 1-й и контрольной групп, при этом у одного из пациентов в каждой из этих групп регистрировался ритм электрокардиостимулятора, который был планово имплантирован во время операции. Во 2-й группе у одного пациента на момент выписки имелась ФП, остальные были выписаны с синусовым ритмом. Из нарушений ритма сердца, возникших после операции, у 3 пациентов 1-й группы зарегистрировано ТП, во 2-й и контрольной группах пароксизмов ТП не отмечалось.
Отсутствие ФП. Для оценки ритма сердца мы использовали ЭКГ, ХМ ЭКГ и имплантируемые устройства Reveal XT.
Данная система имплантирована 53 пациентам (в 1-й группе — 21, во 2-й группе — 25, в 3-й группе — 7).
При оценке результатов операции и отсутствия аритмии «слепым» периодом мы считали 3 мес. В течение «слепого» периода пациенты контрольной группы получали назначенную при выписке антиаритмическую и антикоагулянтную терапию.
Оценка отсутствия ФП проводили по методу Каплана—Майера, согласно международным рекомендациям, по которым рецидив ФП расценивался как любой приступ предсердной тахиаритмии, продолжающийся более 30 с и возникший через 3 мес после хирургического лечения [19].
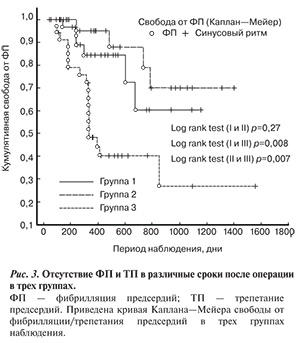
При анализе ритма сердца в отдаленные сроки после операции использовали данные подкожного монитора Reveal и ХМ ЭКГ. По данным отчетов, полученных при опросе монитора Reveal и результатам ХМ ЭКГ, в 1-й группе синусовый ритм имелся у 26 (86,7%) из 30 обследованных пациентов. Во 2-й группе через 1 год после операции синусовый ритм имелся у 28 (96,5%) из 29 наблюдавшихся пациентов. В контрольной группе через 1 год наблюдения только у 18 (53%) из 34 пациентов имелся синусовый ритм. Ко второму году наблюдения ФП и ТП в 1-й группе отсутствовали у 26 (80%) из 30 пациентов, во 2-й группе — у 86,2%, в 3-й группе — у 44,1% (рис. 3).
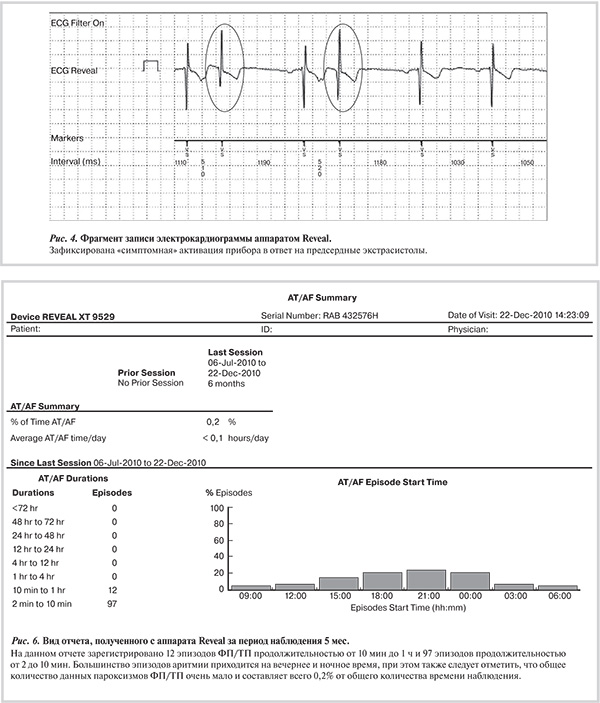
При анализе данных, полученных при использовании аппарата Reveal, получены интересные результаты. Так, у некоторых пациентов регистрируются «симптомные» активации прибора. Это означает, что пациент активирует систему в момент ощущения им перебоев или дискомфорта в области сердца. Учитывая характерный аритмический анамнез у данных пациентов, можно было бы предположить, что в этот момент у пациента возникает ФП или ТП, однако при анализе записей ЭКГ в памяти аппарата нередко регистрируются экстрасистолы (рис. 4) или даже обычный синусовый ритм. Приводим пример многократных «симптомных» активаций аппарата у пациента со стабильным синусовым ритмом (рис. 5, см. цветную вклейку).
Подробное изучение данных отчетов, несмотря на наличие жалоб пациентов на перебои в работе сердца, позволяют адекватно корректировать антиаритмическую терапию, а также отменять антиаритмические и антикоагулянтные препараты. Все это позволяет минимизировать нежелательные побочные эффекты и возможные осложнения приема препаратов указанных групп. Это особенно актуально именно для пациентов с ИБС, так как большинство из них принимают антикоагулянты именно по причине ФП.
Другим важным аспектом оценки эффективности операции абляции субстрата ФП является выявление и регистрация пароксизмальных (ФП и ТП) и бессимптомных аритмий, которые могут быть разными по продолжительности (от нескольких с до нескольких ч) и возникают не каждый день. В данной работе у 7 (24%) пациентов (3 из 1-й группы, 2 — из 2-й и 2 — из 3-й группы) отмечались бессимптомные аритмии, которые были выявлены, по данным непрерывного мониторирования ритма сердца. Такие пароксизмы практически не удается зарегистрировать при обычном суточном мониторировании ЭКГ, в то время как пациенты в большинстве случаев нуждаются в приеме антиаритмических и антикоагулянтных препаратов. В то же время корректное использование имплантируемых приборов мониторирования ритма позволяет выявлять и фиксировать подобные аритмии и своевременно контролировать их и корректировать терапию. Ниже приводим пример информационных отчетов с аппарата Reveal с пароксизмами ФП (рис. 6) .
Обсуждение
С учетом всей информации, полученной при применении данных приборов, которые позволяют регистрировать даже единичные редкие и бессимптомные пароксизмы, складывается впечатление о низкой эффективности исследуемых процедур абляции. Однако это впечатление обманчиво. Полученные в нашем исследовании данные соотносятся с результатами большинства ведущих мировых клиник, занимающихся проблемой хирургии ФП. Большинство указанных клиник для оценки эффективности операции используют суточное или 7-дневное мониторирование ЭКГ, при этом зачастую данные способы мониторирования не позволяют зарегистрировать бóльшее число эпизодов, тем более, если они возникают неежедневно. Кроме того, данные способы мониторирования обладают значительно меньшей чувствительностью и специфичностью в отношении выявления пароксизмов ФП. Так, данные, записанные при 7-дневном или суточном мониторировании в сочетании с записями во время «симптомной» активации, способны документировать приблизительно 70% рецидивов ФП, при этом их ожидаемая прогностическая ценность отрицательного результата отсутствия ФП колеблется между 25 и 40% [20, 21]. В последние годы стал доступным длительный подкожный имплантируемый монитор для осуществления непрерывного отслеживания ФП, который основан на анализе интервалов RR в течение более 2 лет [16, 22]. Данные типы приборов непрерывного мониторинга ЭКГ могут быть использованы для оценки результатов операции аблации субстрата ФП [17]. При этом устройство Reveal обладает 96% специфичностью и 92% чувствительностью в отношении регистрации ФП, что доказано в проведенном исследовании [16]. Следует отметить, что несмотря на явные и бесспорные преимущества данных имплантируемых устройств в отношении оценки отсутствия ФП и высокий уровень развития медицины в Европе и США, в мировой литературе встречается лишь небольшое число работ, в которых дана объективная оценка эффекта операции по устранению ФП, основанная на анализе данных имплантируемых устройств [16]. В России эта проблема стоит еще острее. Лишь единичные центры в России [12—17] используют данные устройства для выявления рецидивов ФП и оценки эффекта операции по ее устранению. Тем не менее наличие рецидивов ФП, их частота и продолжительность, а также клиническая переносимость ФП/ТП пациентом являются ключевыми в определении дальнейшей тактики лечения. Необходимо принять решение о необходимости назначения антиаритмической и антикоагулянтной терапии, а в некоторых случаях и о проведении инвазивного электрофизиологического исследования и катетерной процедуры. Имплантируемые устройства являются просто незаменимыми в этих вопросах. Данные, полученные при применении Reveal, позволяют адекватно корректировать антиаритмическую терапию, а также отменять антиаритмические и антикоагулянтные препараты. Следует еще раз отметить, что в отдаленном периоде наблюдения стоит более внимательно подходить к оценке эффекта операции. Для этих целей необходимо использовать современные способы непрерывного длительного мониторирования ритма, которыми являются имплантируемые устройства (Reveal XT). Это позволит корректно оценивать эффект операции, выявлять ее проаритмогенные эффекты, а в некоторых случаях своевременно направлять пациента на повторное вмешательство.



