ВВЕДЕНИЕ
Оптимизация прогноза пациентов с клиническими формами атеросклероза – одна из наиболее актуальных медико-социальных задач ввиду широкой распространенности данной проблемы и ее тяжелых последствий. Применяемые для этой цели шкалы стратификации риска основаны на материале масштабных проспективных исследований, таких как EUROASPIRE, SMART, REACH [1]. Для пациентов с острым инфарктом миокарда валидированы шкалы GRACE, TIMI [2]. Одним из перспективных направлений кардиологии в вопросах стратификации сердечно-сосудистого риска следует считать привлечение перспективных биомаркеров, к которым в настоящее время относится параметр аутофлуоресценции кожи (АФК) [3]. Метод АФК основан на регистрации флуоресценции, вызванной локальным воздействием на кожу слабым облучением ультрафиолетового диапазона. Интенсивность флуоресценции пропорциональна накопленным в верхних слоях кожи конечным продуктам гликирования (КПГ).
КПГ являются неоднородной группой поперечно-сшитых молекул, образующихся в результате процессов неэнзимной связи белков, жиров с сахарами [4]. Их накопление обусловлено старением и такими заболеваниями, как атеросклероз, хроническая болезнь почек (ХБП), сахарный диабет 2-го типа (СД 2). К фундаментальным механизмам сосудистого поражения с участием КПГ относятся [5]:
- изменение белков экстрацеллюлярного матрикса – коллагена и эластина с утратой эластичности аорты;
- взаимодействие КПГ со специфическими рецепторами на поверхности клеток с последующим выбросом воспалительных интерлейкинов, стимуляцией процессов перекисного окисления в клетках сосудистого эндотелия и гладкомышечных клетках.
Параметр АФК не подвержен быстрым изменениям и отражает кумулятивный эффект процессов перекисного окисления и гликирования, в том числе в жизненно важных органах, что нашло отражение в понятии «метаболическая память».
Цель работы – определить взаимосвязь параметра АФК с основными показателями клинического статуса, биохимическими и инструментальными данными сердечно-сосудистого ремоделирования, а также создать модель прогноза для больных заболеваниями периферических артерий (ЗПА) с последующей ее валидизацией применительно к пациентам с ишемической болезнью сердца (ИБС).
МАТЕРИАЛ И МЕТОДЫ
В соответствии с целью работы были выделены две основные группы из контингента мужчин, госпитализированных в ГБУЗ «Самарская областная клиническая больница им. В.Д. Середавина»: 1-я – 31 пациент с ИБС, экстренно поступивший в стационар с диагнозом острого коронарного синдрома (ОКС), 2-я – 122 больных с ЗПА из отделения сосудистой хирургии. Возраст исследуемых составил от 42 до 78 лет.
Критериями включения для 1-й основной группы служили достоверные инструментальные признаки ИБС, выявленные у 31 пациента, подвергнутого коронарографии. У 10 человек ИБС клинически манифестировала острым инфарктом миокарда левого желудочка (ИМ) без зубца Q (диагноз был подтвержден повышением тропонина Т), у 21 – нестабильной стенокардией. ИМ в анамнезе имелся у 12 больных. Процедуру стентирования в период госпитализации или ранее перенесли 25 пациентов.
Критериями включения для 2-й основной группы были клинические признаки периферического атеросклероза как минимум в одном артериальном бассейне.
От всех включенных в исследование пациентов получено информированное согласие на участие в нем.
Основные критерии исключения: хроническая сердечная недостаточность (ХСН) 2б стадии и выше, ХБП 4-й стадии и выше, тяжелые острые и хронические сопутствующие заболевания, деменция, невозможность самообслуживания.
Проспективное исследование проводилось в сроки от 515 до 1043 дней (в среднем 736 дней). Информация была получена методом телефонного опроса пациента или члена его семьи у 139 участников – у 27 из 31 в группе ИБС и у 112 из 122 в группе ЗПА. Анализировались госпитализации, их причины, в том числе проведенные операции, даты госпитализаций, используемые лекарственные препараты.
Группа контроля в нашем исследовании состояла их 35 практически здоровых мужчин в возрасте от 42 до 68 лет без клинических признаков атеросклероза [6]. При этом 15 из них имели диагноз гипертонической болезни, причем у 7 человек заболевание было диагностировано во 2-й стадии. Эта группа была выделена из участников диспансерного осмотра, в соответствии с требованиями которого определялись общий холестерин и глюкоза крови, статус курения и индекс массы тела, а также осуществлялась стратификация сердечно-сосудистого риска по шкале SCORE.
Клиническая характеристика участников представлена в таблицах 1, 2. Протокол исследования получил одобрение этического комитета ФГБОУ ВО «Самарский государственный медицинский университет» Минздрава России.
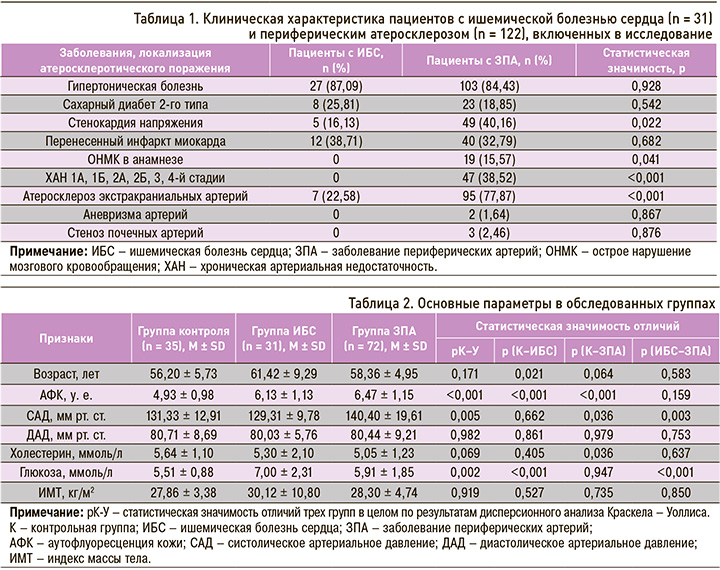
У пациентов в основных группах исследования были изучены клинические, антропометрические, биохимические, инструментальные параметры сонных артерий сердца методами ультразвукового исследования [6]. Параметр АФК определялся с помощью оригинального прибора (ридера), разработанного коллективом кафедры лазерных и биотехнических систем (заведующий – д. ф.-м. н., профессор В.П. Захаров) ФГАОУ ВО «Самарский национальный исследовательский университет им. академика С.П. Королева» [7]. После аппликации внутренней поверхности предплечья на панель прибора в течение 2 мин. производилось воздействие слабым потоком излучения с длиной волны 365 нм и происходило считывание показателей аутофлуоресценции. Параметр АФК рассчитывался как среднее арифметическое по данным трех последовательных измерений.
Основное назначение группы контроля в нашем исследовании сводилось к оценке в ней АФК в сопоставлении с аналогичным параметром среди пациентов с ИБС и ЗПА. Поскольку участники контрольной группы в целом были моложе пациентов группы ЗПА, из последней были выделены сопоставимые по возрасту 72 пациента (см. табл. 2).
Статистический анализ данных выполнялся в среде пакета SPSS 25.0 (IBM Corporation, Armonk, NewYork, USA, лицензия № 5725-А54). Для сравнения групп применялись критерий Манна – Уитни и однофакторный дисперсионный анализ Краскела – Уоллиса. Для номинальных признаков использовался Хи-квадрат (χ2) Пирсона. Описательные статистики представлены в виде среднего и стандартного отклонения (M ± SD) либо медианы и квартилей (Me (Q1–Q3). Исследование взаимосвязей проводилось с помощью корреляционного анализа Спирмена. Для оценки воздействия различных факторов на риск госпитализаций в связи с сердечно-сосудистыми событиями применяли логистическую регрессию и регрессию Кокса, строили ROC-кривые и кривые Каплана – Мейера, которые сравнивали по лог-ранговому тесту. По результатам построения регрессионных моделей в тексте работы приведены отношения шансов (ОШ), относительные риски (ОР) и их 95% доверительные интервалы (ДИ). Результаты считались статистически значимыми при р < 0,05 [6].
РЕЗУЛЬТАТЫ
Необходимо отметить значительную распространенность в обеих основных группах исследования гипертонической болезни, а также двух форм хронического коронарного синдрома – стабильной стенокардии и перенесенного инфаркта миокарда (см. табл. 1). Среди проявлений ЗПА превалировали стенозы экстракраниальных артерий и признаки хронической артериальной недостаточности (ХАН) нижних конечностей. В целом в группе ЗПА оперативной реваскуляризации артерий нижних конечностей было подвергнуто 9% пациентов, коронарных – 11,4%, каротидных – 5,7%.
Следует обратить внимание на существенно меньшую величину АФК в группе контроля, где значение этого параметра коррелировало с возрастом (r = 0,33, p = 0,02), концентрацией общего холестерина (r = 0,40, p = 0,01), результатами оценки по шкале риска SCORE (r = 0,36, p = 0,02). В основной группе связь АФК с возрастом не выявлялась.
Для учета основных клинических параметров и событий, сопряженных с негативным прогнозом сердечно-сосудистых исходов по данным литературы [1], мы использовали суммарный показатель, выраженный в баллах. ХАН 2а стадии соответствовала 1 баллу, 2б стадии – 2 баллам, 3–4-й стадии – 3 баллам, перенесенный инфаркт миокарда – 1 баллу, СД 2 – 1 баллу, инсульт в анамнезе – 1 баллу, стенокардия – 1 баллу, каротидный стеноз более 50% – 1 баллу, ХБП 3-й стадии и выше – 1 баллу, возраст 55–65 лет – 1 баллу, старше 65 лет – 2 баллам. Среднее значение балльной оценки в группе ИБС составило 4,93 ± 1,17 в диапазоне 3–11 баллов, в группе ЗПА – 7,57 ± 1,85 в диапазоне от 4 до 14 баллов (р < 0,001).
В группе ИБС параметр АФК прямо коррелировал с индексом коронарных стенозов SYNTAX (r = 0,4, p = 0,03). Среди пациентов с ЗПА его значения положительно и достоверно коррелировали с баллами по шкале клинико-прогностических признаков (r = 0,36, p < 0,001) и общим холестерином (r = 0,21, p = 0,03). Отрицательные корреляции величины АФК наблюдались с концентрацией гемоглобина (r = -0,2, p = 0,038) и гематокрита (r = -0,25, p = 0,008). Из качественных признаков АФК обнаруживала связь с наличием ХАН (r = 0,23, p = 0,013) и перенесенных операций на артериях нижних конечностей (r = 0,3, p = 0,002).
В обеих основных группах были исследованы параметры общего анализа крови, биохимические показатели: тропонин, общая креатинфосфокиназа и ее МВ-фракция, общий холестерин и его фракции, триглицериды, аминотрансферазы, креатинин, мочевина, расчетная скорость клубочковой фильтрации. Достоверные изменения были выявлены только в отношении уровня аспартатаминотрансферазы (АСТ), который в группе ИБС составил 35,40 (23,45–59,75), а в группе ЗПА – 22,10 (15,50–32,00) ед./л (р < 0,001), что, очевидно, отражает большую выраженность системной воспалительной реакции у пациентов с ИБС.
Из эхокардиографических параметров в основных группах были изучены конечно-диастолический размер левого желудочка (ЛЖ) и его конечно-систолический размер, диастолические параметры толщины межжелудочковой перегородки и задней стенки ЛЖ, фракция укорочения его диаметра, индекс массы миокарда и фракция выброса ЛЖ, диаметр левого предсердия, скорость трансмитрального потока в раннюю диастолу и систолу предсердий, пиковые скорости движения кольца митрального клапана в систолу, в раннюю диастолу и в фазу систолы предсердий. Указанные параметры в группах не отличались, свидетельствуя о высокой распространенности гипертрофии ЛЖ с сохраненной фракцией выброса при умеренных диастолических нарушениях по данным допплерографии трансмитрального потока и тканевой допплерографии латеральной части фиброзного кольца митрального клапана.
Сведения о лекарственных средствах, постоянно используемых включенными в исследование пациентами, были получены нами методом опроса с помощью анкеты, в которой требовалось самостоятельно указать такие препараты. Блокаторы ренин-ангиотензин-альдостероновой системы суммарно принимали только в 55% больных, что было явно недостаточно, учитывая хотя бы распространенность среди них АГ на уровне 90%. Впрочем, антигипертензивный эффект мог быть достигнут и селективными брадикардическими β-блокаторами, которые получали 48% пациентов. Очевидно, что столь частое назначение препаратов этой группы было связано с перенесенным ИМ и сопутствующей ИБС. Следует отметить достоверно более низкую частоту приема статинов в группе ЗПА – 50 против 100% в группе ИБС, что подтверждает неоднократные наблюдения низкой комплаентности к этой группе препаратов в реальной клинической практике. Из дезагрегантов 76% пациентов использовали ацетилсалициловую кислоту, еще 12% – другие препараты данного класса, а также пероральные антикоагулянты. Частота применения клопидогрела была в несколько раз выше в группе ИБС, нежели в группе ЗПА – 22 против 5%, что объясняется большей распространенностью двойной антиагрегантной стратегии среди первой когорты больных. Тем не менее ни одна из перечисленных групп препаратов не была достоверно связана с частотой госпитализации по сердечно-сосудистым причинам.
За время наблюдения в группе ЗПА случилось 7 летальных исходов, не менее чем одна госпитализация по сердечно-сосудистым причинам произошла у 42 (37,5%) пациентов. Наиболее частыми были госпитализации с целью консервативного лечения при обострении ХАН – у 12 (12%) пациентов. Потребность в проведении аортокоронарного шунтирования (АКШ) была реализована у 11 (10%), в стентировании коронарных артерий – у 6 (5,3%) больных. Необходимость в других операциях возникала реже: бифуркационное аорто-бедренное шунтирование было выполнено 2 (2%), ампутации – 3 (3%), стентирование почечных артерий – 3 (3%) пациентам. Инсульты перенесли 2 (2%) больных.
В группе ИБС по крайней мере одна госпитализация имела место у 16 (59%) человек; среди них повторной госпитализации подверглись 6 участников исследования. Основным поводом для госпитализаций служило выполнение оперативного лечения – у 12 пациентов. Операция АКШ была проведена 7 (26%) из этих больных, чрескожное коронарное вмешательство – 4 (15%), еще 1 пациент подвергся бифуркационному аорто-бедренному шунтированию. В течение всего периода наблюдения летальных исходов группе ИБС не произошло, при этом было зарегистрировано 2 инфаркта миокарда.
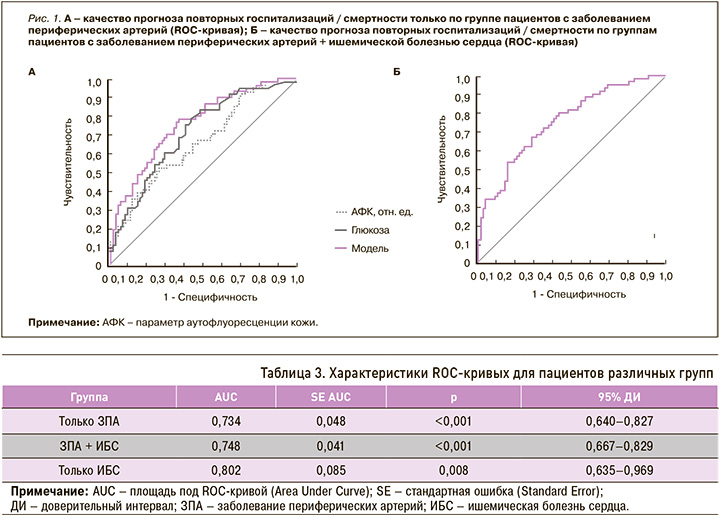
Применение метода множественной логистической регрессии позволило определить, что в группе ЗПА факт госпитализации или летальности был связан с АФК (ОШ 1,71; 95% ДИ: 1,20–2,45; p = 0,003) и уровнем глюкозы плазмы крови (ОШ 1,23; 95% ДИ: 1,004–1,51; p = 0,046). Качество прогнозирования модели было следующим (рис. 1а): чувствительность 71%, специфичность 68% при пороговой вероятности 0,4, площадь под ROC-кривой (AUC) – 0,76 (95% ДИ: 0,64–0,97; р = 0,008).
Исходя из данной модели, вероятность риска прогнозируемых событий может быть рассчитана по формуле:
Р = exp (0,538 × АФК + 0,208 × Глюкоза - 5,104) / (1 + exp (0,538 × АФК + 0,208 × Глюкоза - 5,104).
Помимо множественной логистической регрессии, для группы ЗПА была построена множественная регрессия Кокса. При этом виде моделирования учитываются не только неблагоприятные события, но и время до их наступления. В модель Кокса, наряду с АФК и гликемией, вошел параметр функционального класса (ФК) ХСН. В результате были получены следующие значения ОР: для АФК (в у. е.) – 1,34 (95% ДИ: 1,05–1,71; р = 0,018), для уровня глюкозы плазмы крови (в ммоль/л) – 1,13 (95% ДИ: 1,02–1,25; р = 0,016), для ХСН (2 ФК против 0–1 ФК) – 2,93 (95% ДИ: 1,35–6,38; р = 0,007). Однако у регрессии Кокса есть недостаток: она позволяет вычислить риски относительно некоторого базового риска, который нам неизвестен, но не вероятность прогноза. Поэтому дальнейшее исследование устойчивости построенной модели проводили только по логистической регрессии.
Тестирование логистической регрессионной модели было выполнено на группе пациентов с ИБС. По найденным коэффициентам логит-регрессии были рассчитаны вероятности неблагоприятных событий в иной группе больных и сделано сопоставление прогнозов с реально наблюдаемыми исходами. В тестовой выборке (больные ОКС) площадь под ROC-кривой оказалась сопоставимой с таковой для обучающей группы ЗПА (табл. 3). При пороговой вероятности в 0,35 чувствительность прогноза составила 86%, а специфичность – 61%.
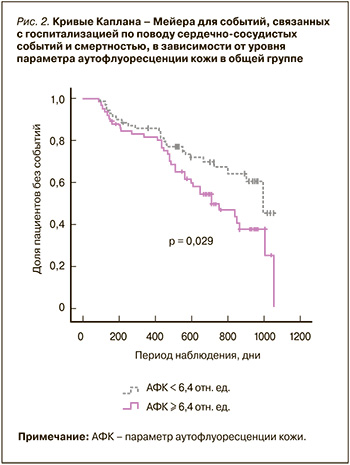
Кривые Каплана – Мейера, которые учитывают события, связанные с госпитализацией по поводу сердечно-сосудистых событий и смертностью, а также время до их наступления, были достоверно менее благоприятны для повышения АФК более 6,4 отн. ед. (медианы дожития: 1000 и 716 сут.) (рис. 2), гликемии натощак (медианы дожития: 1054 и 716 сут.), наличия функционального класса ХСН выше 1-го класса (медианы дожития: 1000 и 510 сут.).
ОБСУЖДЕНИЕ
Приведенное исследование методологически было разбито на две части. Первая представлена как кросс-секционное исследование, задача которого – сопоставить значения параметра АФК в группах и установить его взаимосвязи с известными факторами сердечно-сосудистого риска. Зависимость АФК от возраста, обнаруженная в группе контроля, является фундаментальной для популяции первичной кардиоваскулярной профилактики и многократно подтверждена предыдущими исследованиями [8, 9]. В группе ЗПА и ИБС такая корреляция не прослеживается, поскольку накопление КПГ больше зависит от активности патологического процесса, чем от возраста, но при этом сохраняется прямая связь АФК с общим холестерином крови, выявленная в контрольной группе. Существенное значение имеют корреляции АФК с индексом коронарных стенозов, баллами клинико-прогностической оценки, тяжести ХАН, фактом ранее проведенных операций по поводу сердечно-сосудистых заболеваний. Эти данные согласуются с концепцией атеросклеротической трансформации артерий, в основе которой лежат процессы воспаления, в том числе опосредованные перекисным окислением липидов, а также метаболические нарушения – гликемия и сопутствующее ей гликирование структурных белков и энзимов [5]. Так, увеличение параметра АФК связано со степенью выраженности атеросклероза (от субклинической до клинически манифестных форм) [10]. Авторы подчеркивают, что ассоциация АФК с объективными признаками увеличенной жесткости центральной аорты [11] и поражения коронарных и каротидных артерий существенна и лишь частично опосредована обычными факторами риска [12]. В большом популяционном исследовании когорты Rotterdam Study была установлена связь АФК с количеством бляшек сонных артерий, кальциевым коронарным счетом и фактом перенесенного ИМ [13].
Вторая, проспективная часть исследования, впервые проведенного в России, предоставляет весомые доказательства клинической ценности АФК, определяемой ее способностью служить независимым фактором прогноза. В качестве конечной точки был выбран кумулятивный показатель – сумма смертельных событий и главных сердечно-сосудистых событий, требующих госпитализации. В модели прогноза группы ЗПА, кроме АФК, независимыми параметрами выступали уровень гликемии и функциональные классы ХСН. Доказано, что гликемические нарушения в категориях пациентов с предиабетом и СД 2 – существенные факторы прогноза независимо от той или иной клинической формы атеросклероза [14]. В отношении ХСН накоплен обширный материал, который свидетельствует о крайне негативном прогнозе для жизни этого осложнения, сопоставимом с прогнозом при онкологической патологии [15]. В целом наши результаты хорошо согласуются с фактами, установленными в недавнем систематическом анализе Cavero-Redondo I. et al., в который вошли 10 проспективных исследований. У 4109 пациентов с высоким кардиоваскулярным риском параметр АФК предсказывал кумулятивную и сердечно-сосудистую смертность у пациентов с кардиологическими заболеваниями, в том числе в сочетании с СД и ХБП [16].
Поражение сосудистого русла атеросклерозом характеризуется системностью, но вместе с тем оно распределено неравномерно, с локальными участками, склонными к дестабилизации. Именно события, связанные с атеротромбозом в зоне нестабильной бляшки, определяют прогноз пациента, но далеко не всегда существование и локализация таких бляшек могут быть установлены до индексного события. Наличие субклинических нестабильных зон поражения артерий снижает точность прогностических подходов, основанных на учете клинической информации. Процесс ускоренного образования КПГ, отображаемый АФК, – часть общей воспалительной активности, которая рассматривается как ключевой фактор атерогенеза. Важными преимуществами метода АФК следует считать неинвазивность, удобство для пациента и полное отсутствие зависимости от оператора.
Полученные данные в сочетании с накопленным международным опытом исследований дают основания оценивать АФК как интегральный маркер атерогенеза. Закономерности, учтенные в модели, разработанной для пациентов с ЗПА, могут быть распространены и на пациентов с ИБС, что хорошо проиллюстрировано в объединенной группе исследования. Таким образом, АФК целесообразно рассматривать как биомаркер в широком спектре кардиоваскулярной патологии, вплоть до мультифокальных форм атеросклероза и случаев коморбидности, включающей СД и ХБП.
ЗАКЛЮЧЕНИЕ
1. В группе пациентов без клинических проявлений атеросклероза параметр АФК связан с возрастом, величиной систолического артериального давления, уровнем холестерина и балльной оценкой по шкале SCORE.
2. Параметр АФК существенно увеличен у пациентов с ИБС и клиническими проявлениями периферического атеросклероза, без достоверных отличий между ними. Это подтверждает концепцию долговременных метаболических изменений тканей под действием процессов, ассоциированных с атеросклерозом.
3. Значения параметра АФК прямо пропорциональны баллам по шкале клинико-прогностических признаков, индексу коронарных стенозов, тяжести ХАН. Также они выше у тех, кто был прооперирован по поводу сердечно-сосудистых заболеваний.
4. Параметр АФК имеет прогностическую ценность как предиктор общей смертности и сердечно-сосудистых событий, требующих госпитализации у пациентов с ЗПА, а также в общей группе с включением пациентов, перенесших ОКС.



