Нарушение функционирования центральной и вегетативной нервной системы (ВНС) наряду с наследственностью и эндокринно-метаболическим дисбалансом является важным фактором развития эссенциальной артериальной гипертонии (АГ). Основную роль в развитии и прогрессировании АГ играет активация нейрогормонов [1—3].
В основном это симпатико-адреналовая система (САС) и ее эффекторы (норадреналин и адреналин), ренин-ангиотензин-альдостероновая система (РААС) и ее эффекторы (ангиотензин II и альдостерон), а также система натрийуретических пептидов. Хроническая гиперактивация нейрогормонов сопровождается развитием и прогрессированием систолической и диастолической дисфункции левого желудочка (ЛЖ) при АГ.
В настоящее время существуют 3 основных метода изучения состояния САС и РААС: определение уровня катехоламинов в плазме крови, определение чувствительности барорецепторов и изучение вариабельности ритма сердца (ВРС). Среди этих методов наиболее эффективным и неинвазивным является определение ВРС.
В последние годы значительный интерес представляет подход к лечению АГ, основанный на представлениях о механизмах нейрогормональной регуляции. Благодаря анализу ВРС можно легко, высокоинформативно и надежно подобрать рациональную медикаментозную терапию больным различными сердечно-сосудистыми заболеваниями, в том числе с эссенциальной АГ, в последующем оценить эффективность проведенной терапии.
Исследования влияния нейрогуморальных модуляторов из группы ингибиторов ангиотензинпревращающего фермента (АПФ) на ВРС проводились с применением препаратов первого и второго поколений. Причем у исследователей нет единого мнения по поводу влияния ингибиторов АПФ на ВРС. Ряд авторов сообщили о положительных изменениях вегетативной регуляции ритма сердца при лечении препаратами этих групп. Так, выявлено статистически значимое увеличение парасимпатических и уменьшение симпатических составляющих на фоне лечения эналаприлом, рамиприлом и лизиноприлом [4—7]. Другие авторы отмечают, что ингибиторы АПФ не влияют на ВРС [8—10]. В исследовании M. Campelo и соавт. [11] у больных АГ 1—2-й степени при лечении атенололом и цилазаприлом отмечено выраженное уменьшение симпатической активности лишь при лечении атенололом. A. Bliqe и соавт. [8] также не обнаружили достоверных изменений ВРС у больных АГ 1—2-й степени при лечении фозиноприлом. Имеются сведения о том, что у пациентов с АГ в возрасте моложе 40 лет при условно нормальных значениях ВРС эффективная терапия лизиноприлом не изменяла ее или снижала в процессе неэффективной терапии, у пациентов старше 40 лет эффективная антигипертензивная терапия улучшала ВРС, а неэффективная — не влияла на нее [9].
В связи с изложенным мы поставили перед собой цель оптимизировать фармакотерапию у больных АГ с исходной симпатикотонией препаратами из группы нейрогуморальных модуляторов на основании данных о ВРС при лечении в течение 1 и 6 мес.
Материал и методы
В исследование были включены 315 больных АГ 1—3-й степени в соответствии с Американскими рекомендациями 2003 г. и рекомендациями Европейского общества по гипертонии (ESH)/Европейского общества кардиологов (ESC) 2007 г. У 104 (33%) больных диагностирована АГ 1-й, у 106 (33,7%) — 2-й и у 105 (33,3%) — АГ 3-й степени. Группу контроля составили 43 практически здоровых добровольца (25 мужчин и 18 женщин, средний возраст 36,7±0,9 года), сопоставимых с больными по полу и возрасту.
Для установления диагноза проводили тщательное общеклиническое обследование больных с использованием следующих лабораторных и инструментальных методов исследования — общий анализ крови и мочи, биохимическое исследование крови (калий, глюкоза натощак, креатинин, липидограмма), электрокардиография, эхокардиография, рентгенография грудной клетки, при необходимости — осмотр глазного дна, ультразвуковое исследование органов брюшной полости.
Критерии исключения: симптоматическая АГ и другие заболевания, способные изменять ВРС: сахарный диабет, нестабильная стенокардия, стабильная стенокардия напряжения III—IV функционального класса (ФК) по Канадской классификации, инфаркт миокарда, хроническая сердечная недостаточность III—IV ФК по классификации Нью-Йоркской ассоциации сердца с фракцией выброса ЛЖ менее 40%, устойчивая желудочковая экстрасистолия, атриовентрикулярные блокады, мерцательная аритмия, синдром слабости синусного узла, тяжелые хронические заболевания легких с признаками дыхательной недостаточности.
Для оценки деятельности ВНС использовали также индекс Кердо (ИК), который вычислялся по формуле: ИК=100×(1-ДАД/пульс), где ДАД — диастолическое артериальное давление. ИК>0 свидетельствовал о преобладании возбуждающих симпатических влияний в деятельности сердца, ИК<0 — о преобладании тормозных влияний, если ИК был равен 0 — о функциональном равновесии.
Для определения чувствительности барорецепторов, а также анализа степени нарушения симпатического (С-ВНС) или парасимпатического звена ВНС регуляции у больных АГ использовали активную ортостатическую пробу (АОП).
Интерпретацию результатов АОП осуществляли по коэффициенту 30:15 (К30/15) — отношение минимального значения интервала RR на электрокардиограмме (ЭКГ) в момент 15-го удара от начала подъема из горизонтального положения к самому длинному интервалу RR, обычно в момент 30-го удара. Низкий К30/15 указывал на недостаточную парасимпатическую активность. Реакция на АОП разделялась на нормальную (К30/15 от 1,25 до 1,75), сниженную (К30/15 от 1,0 до 1,25), высокую или избыточную (К30/15 более 1,75), пародоксальную (К30/15 менее 1,0).
Для изучения ВСР у больных АГ использовали метод мониторирования ЭКГ по Холтеру при помощи неинвазивной системы EСGproHolter (Германия). Методика анализа ВСР соответствовала Стандартам измерений, физиологических интерпретаций и клинического использования, выработанным рабочей группой Европейского общества кардиологов и Северо-Американского общества по стимуляции и электрофизиологии (1996) [12].
Подход к фармакотерапии. За 5 дней до начала настоящего исследования больным отменяли предшествующую антигипертензивную терапию («очистительный период», период вымывания). Только определенным пациентам с АГ 2-й и 3-й степени был рекомендован пероральный прием нифедипина в случаях развития гипертонических кризов.
Наш подход к фармакотерапии заключался в необходимости выделения индивидуальных клинико-патогенетических вариантов АГ на основании данных о регуляции ВНС, полученных путем анализа ВРС.
Для изучения влияния нейрогуморальных модуляторов на ВНС из обследованных 315 пациентов 51 больному (32 мужчины и 19 женщин, среди которых АГ 1-й степени наблюдалась у 7, 2-й — у 29 и 3-й — у 15) с симпатикотонией покоя (ИК=12,7±0,7) и избыточной активацией симпатических влияний при проведении АОП (К30/15=1,03±0,2) назначили ингибитор АПФ лизиноприл (диротон, «Гедеон Рихтер», Венгрия) в сочетании с индапамидом (арифон, «Сервье», Франция) в начальной дозе 2,5 мг. Титрование дозы лизиноприла (5—10 мг, в среднем 9,7±0,13 мг) проводили через каждые 2 нед до снижения артериального давления (АД) до целевого уровня (140/90 мм рт.ст.) или оптимального снижения АД на 10—20% от первоначального уровня в течение 1 мес. Лечения 23 больных, у которых удалось снизить АД до целевых уровней в течение 1 мес, продолжили препаратами в индивидуально подобранных дозах в течение 6 мес. При этом 28 пациентам с недостаточным снижением АД до целевого уровня за 1 мес к лечению добавили бисопролол (конкор, Merck, Германия ) с титрованием дозы от 5 до 10 мг (в среднем 7,7±0,31 мг) через каждые 2 нед до достижения целевого уровня АД. Повторные исследования ВРС проводили через 1 и 6 мес исследования.
Статистическую обработку данных исследования проводили с помощью пакета программ Statistica 6,0 фирмы StatSoft.Inc (США).
Вычислены средние значения полученных выборок (M), их стандартные ошибки (m), минимальные (min) и максимальные (max) значения, а также определены частоты появления исследуемых качественных признаков. Для оценки различий количественных показателей использовали параметрический t-критерий Стьюдента, непараметрический U-критерий Манна—Уитни и критерий Вилкоксона. Различия считали статистически значимыми при p<0,05.
Результаты
Средние уровни систолического АД (САД) и ДАД у больных до лечения составляли 170,2±4,4/106,1±0,9 мм рт.ст.
К концу 1 мес лечения средние уровни АД снизились до 149,7±3,3/93,2±1,8 мм рт.ст. Среди нежелательных проявлений при применении комбинации лизиноприла и индапамида у 2 больных наблюдался сухой кашель, у 4 — головная боль. Эти побочные эффекты были невыраженными и не потребовали прекращения лечения.
Учитывая эффективность и безопасность терапии с применением комбинации лизиноприл+индапамид пациентов с исходной симпатикотонией, 23 больным, которым удалось снизить АД до целевых уровней (с 168,7±3,8/101,2±1,8 до 140,6±4,1/81,1±0,9 мм рт.ст.) без проявлений побочных эффектов лекарств продолжили лечение препаратами в индивидуально подобранной дозировке на протяжении 6 мес, контролируя эффективность лечения каждые 4 нед. Через 6 мес лечения САД и ДАД у этих больных снизились до 131,8±3,3/79,4±1,2 мм рт.ст., из нежелательных проявлений у 1 пациента развился сухой кашель, у 3 — головокружение на фоне гипотонии.
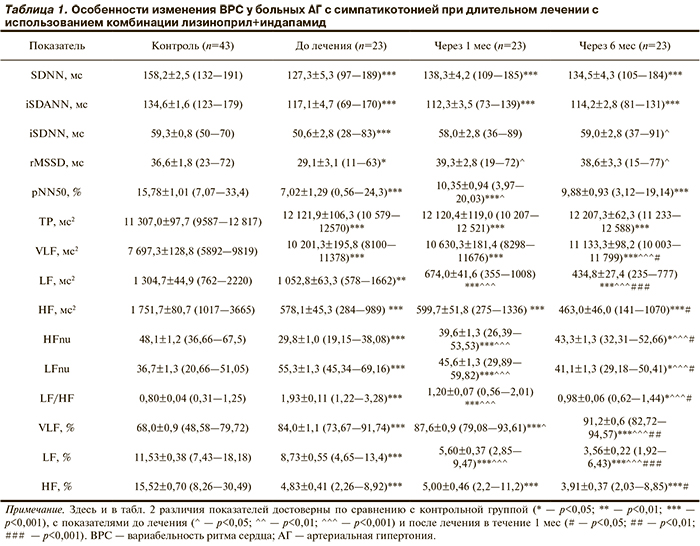
Изменения параметров ВРС у пациентов с исходной симпатикотонией при длительной 6-месячной терапии с использованием комбинации лизиноприла и индапамида в сопоставлении с контролем и с данными до и после 1-месячного лечения отражены в табл. 1. Рассматривая в первую очередь временные параметры ВРС, мы установили, что тенденция к подъему показателей ВРС за счет уменьшения симпатических и усиления парасимпатических воздействий на ритм сердца, появившаяся спустя 1 мес лечения, сохранялась и к окончанию 6 мес. В сопоставлении с показателями до лечения через 1 мес терапии значения SDNN возросли на 8,7%, а через 6 мес — на 5,7%. Как до, так и после лечения значения SDNN оставались значительно ниже, чем в контрольной группе: на 19,6, 12,7 и 15,1% соответственно (p<0,001). Изменения величин симпатической составляющей временнóго анализа — iSDANN — у пациентов с исходно повышенной активностью С-ВНС характеризовались тенденцией к уменьшению его значений через 1 и 6 мес на 4,2 и 2,6% соответственно по сравнению с результатами до лечения. Причем значения iSDANN и до, и после 1- и 6-месячного лечения оказывались значительно меньше — на 13,1%, 16,6 и 15,2% соответственно (p<0,001), чем у здоровых добровольцев.
Величины парасимпатических составляющих временнóго анализа, в частности iSDNN и rMSSD, у пациентов с исходной симпатикотонией через 6 мес лечения характеризовались достоверным увеличением на 16,7 и 33,6% соответственно (p<0,05) по сравнению с таковыми до лечения.
Итак, особенности изменения показателей ВРС во временнóм диапазоне у пациентов с исходно повышенной активностью СНС, выявленные спустя 1 мес лечения комбинацией лизиноприл+индапамид и характеризующиеся улучшением параметров ВРС на фоне значительного возрастания парасимпатических влияний и невыраженного снижения активности С-ВНС на ритм сердца, сохранялись и через 6 мес лечения.
Особенности изменения показателей ВРС в спектральной области у пациентов с исходной симпатикотонией характеризовались достоверным усилением активности гуморальных систем лишь к завершению 6 мес лечения, что нашло отражение в достоверном увеличении величин очень низкочастотного компонента в абсолютных единицах (VLF) и в процентном отношении (VLF%) на 9,2 и 8,6% соответственно (p<0,001) спустя 6 мес терапии, в сопоставлении с параметрами до лечения на 44,6 и 35 соответственно (p<0,001) — с контрольной группой и на 4,7% (p<0,05) и 4,1% (p<0,01) — с месячным лечением. При этом, если спустя 1 мес терапии доля очень низкочастотного компонента спектра возрастала с 84 до 87,6% (p<0,05), то через 6 мес лечения лизиноприлом и индапамидом увеличивалась до 91,2% (p<0,001). Следовательно, выраженная активация гуморально-метаболических систем у пациентов с исходно повышенной активностью С-ВНС при лечении лизиноприла в комбинации с индапамидом происходит лишь при длительном лечении указанными лекарствами.
Особенности изменения спектральных параметров симпатической активности у пациентов с исходно повышенной активностью С-ВНС при длительном лечении лизиноприлом и индапамидом характеризовались достоверным уменьшением величин низкочастотного компонента в абсолютных (LF), нормализованных (LFnu) единицах и в процентном отношении (LF%) через 6 мес лечения на 58,7, 26,7 и 58,2% соответственно (p<0,001) в сопоставлении с данными до лечения и на 35,5% (p<0,001), 10,1% (p<0,05) и 37,4% (p<0,001) по сравнению с данными месячного лечения.
Изменения спектральных параметров парасимпатической активности при длительном 6-месячном лечении лизиноприлом в комбинации с индапамидом больных АГ с исходной симпатикотонией характеризовались незначительной тенденцией к уменьшению величин высоких частот в абсолютных единицах (HF) и в процентном отношении (HF%) через 6 мес. Однако на фоне длительного лечения наблюдалось увеличение значений высокочастотного компонента в (HFnu) на 45% (p<0,001) по сравнению с показателями до лечения и на 9,3% (p<0,05) — по сравнению с данными месячной терапии. Величины HFnu через 6 мес лечения возросли настолько, что на 10,1% (p<0,05) отличались от показателей группы контроля.
Итак, длительное 6-месячное лечение лизиноприлом и индапамидом пациентов с АГ и исходной симпатикотонией не ухудшает периферическую парасимпатическую активность, способствуя выраженной относительной парасимпатикотонии.
Значительное устранение проявлений относительной симпатикотонии у больных при длительном 6-месячном лечении подтверждалось достоверным уменьшением индекса LF/HF на 49,1% (p<0,001) по сравнению с параметрами до лечения и на 18,3% (p<0,05) — с данными месячной терапии.
Таким образом, при длительном 6-месячном лечении пациентов с исходной симпатикотонией лизиноприлом в комбинации с индапамидом уменьшается периферическая симпатическая активность, устраняются признаки относительной симпатикотонии на фоне значительного усиления активности РААС и развития относительной парасимпатикотонии.
В результате месячного лечения пациентов с исходно повышенной активностью С-ВНС у 28 из них САД и ДАД не снизились до целевого уровня (в среднем с 172,4±3,1/109,1±2,1 до 159,1±3,9/96,7±1,8 мм рт.ст.). Из побочных эффектов у 2 пациентов наблюдался сухой кашель, у 4 — головная боль. Для увеличения эффективности лечения с применением комбинации лизиноприл+индапамид этим 28 пациентам спустя 1 мес добавили третий препарат из группы селективных β-адреноблокаторов — бисопролол (конкор, Merck, Германия ) с титрованием дозы от 5 до 10 мг (в среднем 7,7±0,31 мг) каждые 2 нед. до снижения АД до целевых уровней. Через 6 мес лечения этими препаратами достигнуто снижение АД до 135,2±3,6/86,4±1,8 мм рт.ст.
Из побочных эффектов у 3 пациентов наблюдался сухой кашель, который не стал причиной для отмены лечения.
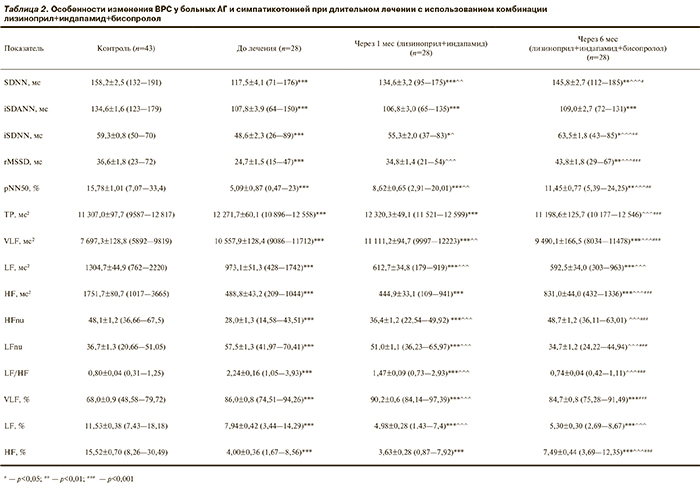
Особенности изменения параметров ВРС во временнóм и частотном диапазонах при длительной 6-месячной комбинированной терапии (лизиноприл+индапамид+бисо-пролол) в сопоставлении с контролем и с результатами до и после месячного лечения с применением комбинации лизиноприл+индапамид отражены в табл. 2.
У пациентов с исходно повышенной активностью С-ВНС, у которых уровни САД и ДАД через 1 мес лечения лизиноприлом в комбинации с индапамидом не снижались до целевых, прослеживалось выраженное уменьшение SDNN (на 26,7%; p<0,001) за счет снижения как симпатических — iSDANN (на 19,9%; p<0,001), так и парасимпатических — iSDNN, rMSSD и pNN50 на (18,1, 33,4 и 67,8% соответственно; p<0,001) составляющих временнóго анализа по сравнению с таковыми в контрольной группе.
По сравнению с результатами до лечения спустя 1 мес терапии лизиноприлом и индапамидом достоверно увеличились значения SDNN (на 14,6%; p<0,01) в основном за счет увеличения парасимпатических параметров — iSDNN (на 13,6%; p<0,05), rMSSD (на 41,8%; p<0,001) и pNN50 (на 69,3%; p<0,01).
Изменение значений временнóго параметра симпатического составляющего — iSDANN — было недостоверным. Следовательно, несмотря на отсутствие должного снижения АД на фоне месячного лечения лизиноприлом и индапамидом у 28 больных с исходной повышенной активностью С-ВНС, у этих пациентов наблюдалось значительное улучшение показателей ВРС во временнóм диапазоне в основном за счет достоверного усиления активности парасимпатической нервной системы (ПСНС) на ритм сердца.
 Добавление бисопролола к терапии лизиноприлом и индапамидом помимо должного снижения АД приводило к достоверному улучшению показателей ВРС во временнóй области. Через 6 мес применения трехкомпонентной терапии значительно возрастали величины SDNN — на 24,0% (p<0,001) по сравнению с данными до лечения и на 8,4% (p<0,05) по сравнению с показателями через 1 мес терапии. Величины парасимпатических составляющих временнóго анализа — iSDNN, rMSSD и pNN50 — также достоверно возрастали при длительной трехкомпонентной комбинированной терапии, а изменения временнóго параметра симпатической активности — iSDANN — даже после 6 мес лечения оставались невыраженными.
Добавление бисопролола к терапии лизиноприлом и индапамидом помимо должного снижения АД приводило к достоверному улучшению показателей ВРС во временнóй области. Через 6 мес применения трехкомпонентной терапии значительно возрастали величины SDNN — на 24,0% (p<0,001) по сравнению с данными до лечения и на 8,4% (p<0,05) по сравнению с показателями через 1 мес терапии. Величины парасимпатических составляющих временнóго анализа — iSDNN, rMSSD и pNN50 — также достоверно возрастали при длительной трехкомпонентной комбинированной терапии, а изменения временнóго параметра симпатической активности — iSDANN — даже после 6 мес лечения оставались невыраженными.
Итак, добавление бисопролола к комбинации лизиноприл+индапамид помимо должного снижения АД приводит к значительному улучшению параметров ВРС во временнóм диапазоне в основном за счет усиления активности ПСНС на ритм сердца.
Особенности изменения данных ВРС в спектральном диапазоне у 28 пациентов с исходно повышенной активностью С-ВНС, у которых не наблюдалось должного снижения АД на фоне месячного лечения лизиноприлом в комбинации с индапамидом, характеризовались в первую очередь достоверным усилением нейрогуморальных воздействий на ритм сердца в виде возрастания величин очень низкочастотного компонента как в абсолютных единицах (VLF), так и в процентном отношении (VLF%) на 5,3% (p<0,01) и 4,9% (p<0,001) соответственно в конце 1-го месяца лечения по сравнению с показателями до лечения и на 44,4 и 32,6% соответственно (p<0,001) — по сравнению с контролем. Следовательно, причиной неэффективности терапии у этих пациентов может быть чрезмерная стимуляция гуморальных систем, прежде всего, вследствие избыточного накопления ренина при лечении лизиноприлом и индапамидом. Поэтому добавление третьего препарата из категории нейрогуморальных модуляторов – бисопролола – приводило к должному снижению АД на фоне достоверного уменьшения активности РААС. Так, величины VLF и VLF% после эффективной длительной 6-месячной терапии с применением комбинации лизиноприл+индапамид+бисопролол достоверно уменьшились на 14,5 и 6,2% (p<0,001) по сравнению с таковыми после месячного лечения лизиноприлом и индапамидом. В сопоставлении с параметрами до терапии величины VLF через 6 мес лечения достоверно уменьшились на 10,1% (p<0,001). При этом, если до лечения доля нейрогуморальных воздействий на ритм сердца (VLF%) составляла 86%, спустя 1 мес лечения — увеличилась до 90,2% (p<0,001), то через 6 мес — вновь уменьшилась до 84,7% (p<0,001).
Итак, при значительной активации гуморальных систем на фоне терапии лизиноприлом и индапамидом добавление бисопролола наряду с эффективным снижением АД приводит к нормализации влияний РААС на ритм сердца.
Особенности изменения симпатических составляющих спектрального анализа при длительной трехкомпонентной терапии у пациентов с исходно повышенной активностью С-ВНС характеризовались достоверным уменьшением низкочастотного параметра в абсолютных (LF), нормализованных (LFnu) единицах и в процентном отношении (LF%) через 6 мес лечения на 39,1%, 39,7 и 33,3% соответственно (p<0,001) по сравнению с данными до лечения. Уже через 1 мес лечения лизиноприлом в комбинации с индапамидом наблюдалось достоверное уменьшение указанных показателей на 37,1%, 11,4 и 37,4% соответственно (p<0,001) в сопоставлении с параметрами до лечения.
Величины низкочастотного компонента спектра в нормализованных (LFnu) единицах через 6 мес лечения уменьшились настолько, что достоверно не отличались от значений в группе контроля. Причем по сравнению с месячным лечением через 6 мес терапии значения LFnu достоверно снизились на 31,9% (p<0,001). Следовательно, добавление бисопролола к комбинации лизиноприл+индапамид у пациентов с исходно повышенной активностью С-ВНС обеспечивает дополнительный симпатолитический эффект за счет как уменьшения периферической симпатической активации, так и значительного снижения признаков относительной симпатикотонии.
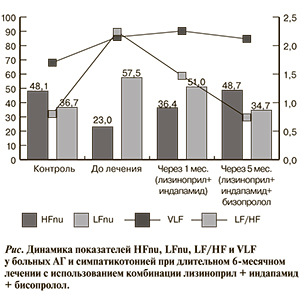
Изменения парасимпатических составляющих спектрального анализа на фоне месячного лечения лизиноприлом и индапамидом 28 пациентов с АГ и исходно повышенной активностью С-ВНС характеризовались недостоверными изменениями значений спектра высоких частот в абсолютных единицах (HF) и в процентном отношении (HF%) в сопоставлении с параметрами до лечения. Однако прослеживалось значительное увеличение показателя HFnu через 1 мес лечения — на 30,2% (p<0,001). Следовательно, так же как и в предыдущей группе из 23 пациентов с достаточным снижением АД при лечении лизиноприлом и индапамидом, у данных пациентов лечение этими же препаратами приводило к развитию относительной парасимпатикотонии без изменения активности ПСНС на периферии (см. рисунок).
Добавление к терапии лизиноприлом и индапамидом третьего препарата бисопролола привело к достоверному возрастанию величин парасимпатических составляющих спектрального анализа через 6 мес лечения в абсолютных единицах (HF), нормализованных единицах (HFnu) и в процентном отношении (HF) (см. рисунок).
Итак, добавление бисопролола к комбинации лизиноприл+индапамид у пациентов с АГ и исходно повышенной активностью С-ВНС обеспечивает развитие стойкой парасимпатикотонии на фоне достоверного усиления периферических парасимпатических воздействий.
Способность бисопролола при добавлении к комбинации лизиноприл+индапамид у пациентов с исходной симпатикотонией значительно снижать признаки относительной симпатикотонии при длительном лечении подтверждается достоверным уменьшением индекса LF/HF через 6 мес применения трехкомпонентной комбинации на 67,1% (p<0,001) в сопоставлении с параметрами до лечения и на 49,7% (p<0,001) — месячного лечения лизиноприлом и индапамидом. Уже к концу месячного лечения величины этого параметра уменьшались на 34,6% (p<0,001) по сравнению с показателями до лечения. Индекс LF/HF через 6 мес лечения уменьшился настолько, что достоверно не отличался от результатов группы контроля (см. рисунок).
Таким образом, при лечении пациентов с АГ с исходной симпатикотонией лизиноприлом в комбинации с индапамидом недостаточная эффективность терапии может быть объяснена чрезмерной стимуляцией гуморальных систем вследствие избыточного накопления ренина. Добавление бисопролола к терапии способствует дополнительному снижению АД за счет нормализации нейрогуморальных воздействий на ритм сердца и дополнительного развития симпатолитического и парасимпатикотонического эффектов.
Обсуждение
Изучению влияния ингибиторов АПФ на ВРС посвящены многочисленные публикации [4—11]. Однако у исследователей нет единого мнения по поводу влияния ингибиторов АПФ на ВРС. Так, одни авторы сообщают о положительных изменениях вегетативной регуляции ритма сердца при лечении препаратами этой группы за счет значимого усиления парасимпатического и ослабления симпатического тонуса [4—7, 13]. Другие исследователи отмечают, что ингибиторы АПФ не оказывают существенного влияния на ВРС [8—11]. Ряд авторов указывают на снижение удельного веса колебаний очень низкой частоты, ответственных за гуморально-метаболические влияния на ритм сердца, при лечении лизиноприлом, другие отмечают повышение гуморальной активности на фоне терапии этим препаратом.
В нашем исследовании изменения временных параметров ВРС на фоне месячной терапии лизиноприлом в комбинации с индапамидом заключались в улучшении ВРС за счет незначительного снижения симпатических и достоверного усиления вагусных влияний на ритм сердца.
Изменения спектральных показателей ВРС характеризовались уменьшением симпатического тонуса с устранением признаков относительной симпатикотонии. Вместе с тем наблюдалась тенденция к возрастанию гуморальной активности на фоне развития относительной парасимпатикотонии.
Улучшения временных параметров ВРС, выявленные через 1 мес терапии препаратами, сохранялись и к концу 6 мес лечения.
Особенности изменения спектральных параметров ВРС при длительном 6-месячном лечении пациентов с исходной симпатикотонией лизиноприлом и индапамидом, как и при месячной терапии, характеризовались уменьшением симпатической активности с устранением признаков относительной симпатикотонии на фоне развития относительной парасимпатикотонии. Однако значительное усиление активности гуморальных систем происходило лишь через 6 мес терапии, что, вероятно, было связано с так называемым феноменом ускользания эффекта ингибиторов АПФ, длительное применение которых вызывает компенсаторное повышение концентрации ренина в крови и других компонентов РААС, находящихся в начальной части ее каскада. Аналогичные данные получены и в других исследованиях [14—16].
К попыткам преодоления указанного феномена относится использование комбинации ингибитора АПФ и β-адреноблокатора, подавляющего синтез ренина. Известно, что при ятрогенном, спровоцированном приемом ингибиторов АПФ росте плазменной активности ренина, наблюдается дальнейшая активация РААС, обусловливающая утрату контроля АД [17—21]. Этим, наверное, и объяснялась недостаточная гипотензивная эффективность комбинации лизиноприл+индапамид у 28 пациентов с АГ, к лечению которых через 1 мес терапии добавили третий препарат из группы селективных β-адреноблокаторов — бисопролол. При этом через 6 мес терапии с использованием трехкомпонентной комбинации было достигнуто эффективное снижение АД до 135,2±3,6/ 85,4±1,9 мм рт.ст. без выраженных побочных эффектов препаратов.
Эффективность сочетанного применения ингибиторов АПФ и β-адреноблокаторов демонстрировалась в многоцентровых исследованиях (ALLHAT, COPERNICUS) [22]. Данная комбинация не только усиливала контроль активности основных прессорных систем, включая РААС, но и эффективно влияла на клиническое состояние, параметры гемодинамики, ремоделирование и сократительную функцию ЛЖ, индексы суточной ВРС у больных АГ и другими сердечно-сосудистыми заболеваниями [17, 20, 21].
В нашем исследовании добавление бисопролола к комбинации лизиноприл+индапамид помимо эффективного снижения АД до целевых значений приводило к значительному улучшению временных параметров ВРС, в основном за счет усиления активности ПСНС.
Изменения спектральных параметров ВРС при добавлении к лечению бисопролола характеризовались нормализацией гуморально-метаболической активности на фоне дополнительного развития симпатолитического и парасимпатотонического эффектов.
Таким образом, полученные данные о сочетанном применении ингибитора АПФ с β-адреноблокаторами дают основание применять многоуровневую блокаду РААС с целью обеспечения более эффективного контроля активности нейрогуморальных систем у больных АГ с исходной симпатикотонией.



