Радиочастотная катетерная абляция (РЧА) субстрата постоянной формы фибрилляции предсердий (ФП) — наиболее эффективный метод лечения больных этой аритмией [1, 2]. Накопилось значительное количество данных о клинических результатах РЧА у пациентов этой категории, которые свидетельствуют о возможности поддержания синусового ритма (СР) у 60—80% пациентов в отдаленном периоде после интервенционного лечения [1—4].
В настоящее время в клинической практике используется преимущественно комбинированная методика РЧА, включающая остиальную радиочастотную (РЧ) изоляцию устьев легочных вен (ЛВ), нанесение линейных РЧ-повреждений в левом предсердии (ЛП), а также абляцию в области регистрации фрагментированных электрограмм в ЛП и в коронарном синусе (КС).
В 2005 г. группа M. Haissaguerre для данной методики предложила использовать термин пошаговой абляции и продемонстрировала, что ее использование приводит к организации цикла ФП, трансформации ее в предсердную тахикардию и/или трепетание предсердий (ТП) с последующим восстановлением СР у 87% пациентов без проведения электроимпульсной терапии (ЭИТ) [5—8].
В 2006 г. H. Oral и соавт. опубликовали результаты РЧА у пациентов с постоянной формой ФП. Из 77 пациентов, которым проводилось интервенционное лечение, СР восстанавливался на фоне проведения РЧА только у 16%, а методом наружной ЭИТ после РЧА в ЛП — у 84%. Устойчивый СР сохранялся в 74% случаев в течение 204±82 дней наблюдения [3, 9, 10].
Таким образом, полученные данные свидетельствуют о том, что унифицированный методический подход к РЧА субстрата постоянной ФП в настоящее время отсутствует. Существующее научное обоснование тактики РЧА у больных постоянной ФП в сочетании с ЭИТ или без него и антиаритмической терапией (ААТ) не в полной мере объясняет эффект от проведения интервенционного вмешательства и не удовлетворяет требованиям времени. Во многом это может быть связано с тем, что патогенез различных форм ФП нельзя считать полностью изученным.
Нам представляется, что автоволновые процессы 6-волнового re-entry в двумерной активной среде, полученные с использованием методики сканирования и с учетом геометрии предсердий, могут являться приемлемой математической моделью постоянной формы ФП [11—13]. Последующее проведение абляционного форматирования (АФ) с помощью создания невозбудимых линий в данной среде, имитирующих лечебные РЧ-воздействия, возможно, позволит определиться с оптимальным методическим подходом к проведению РЧА, и в конечном итоге приблизиться к унификации методики абляции в клинической практике.
Цель исследования — сравнить теоретические возможности элиминации постоянной ФП (на модели 6-волнового re-entry) в условиях математического моделирования АФ и последующей электрической кардиоверсии и сопоставить полученные данные с результатами электрофизиологического исследования (ЭФИ), РЧА и динамического клинического наблюдения за пациентами с постоянной формой ФП.
Материал и методы
Клинический этап. В настоящее исследование были включены 20 пациентов (6 женщин), средний возраст 51,4±13,6 года с постоянной формой ФП (см. таблицу). Диагноз постоянной формы ФП устанавливали на основании критериев, предложенных в рекомендациях Российского кардиологического общества по диагностике и лечению ФП (2013). Более того, обязательным условием включения в исследование было указание в анамнезе на эпизод неэффективной наружной электрической кардиоверсии и/или успешной ЭИТ с поддержанием устойчивого СР не более 7 сут, несмотря на проводимую ААТ [14].
 Предоперационная подготовка осуществлялась в соответствии c Консенсусом EHRA/АСС от 2012 г. и заключалась в назначении непрямых антикоагулянтов и антиаритмических препаратов как минимум за 4 нед до интервенционного вмешательства.
Предоперационная подготовка осуществлялась в соответствии c Консенсусом EHRA/АСС от 2012 г. и заключалась в назначении непрямых антикоагулянтов и антиаритмических препаратов как минимум за 4 нед до интервенционного вмешательства.
После подписания информированного согласия пациентам выполняли процедуру эндокардиального ЭФИ и РЧА ФП с использованием электрофизиологической системы и системы нефлюороскопического картирования.
В ходе процедуры пунктировали правую и левую бедренные вены, левую подключичную вену, по Сельдингеру устанавливали интродьюсеры через которые 10- и 4-полюсный диагностические электроды проводили в КС и область верхушки правого желудочка (RVA).
После верификации отсутствия тромбов в ушке ЛП методом внутрисердечной эхокардиографии выполняли пункцию межпредсердной перегородки (под рентгеноскопическим и внутрисердечным ультразвуковым контролем), через трансептальный интродьюсер картирующий электрод вводили в полость ЛП и осуществляли его трехмерную реконструкцию.
Следующим этапом проводили РЧ-воздействия вокруг устьев ЛВ (циркулярная изоляция), которые дополняли линейными РЧ-воздействиями в области свода (между устьями верхних левой и правой ЛВ), митрального перешейка (между устьем левой нижней ЛВ и кольцом митрального клапана), а также в области задней стенки ЛП (рис. 1, см. цв. вклейку).
До начала проведения РЧА на электродных парах катетера, установленного в КС, измеряли не менее 10 интервалов цикла ФП, вычисляли их среднее значение.
После проведения РЧА в митральном перешейке и по периметру левой нижней ЛВ на электродных парах катетера, установленного в КС, измеряли не менее 10 интервалов цикла ФП, вычисляли среднее значение (рис. 2, см. цв. вклейку).
Следующее измерение 10 циклов ФП на электродных парах электрода, установленного в КС, проводили после РЧ-воздействий по периметру левой верхней ЛВ и правых ЛВ (см. рис. 2). Заключительное измерение 10 циклов ФП на электродных парах электрода, установленного в КС, проводили после нанесения линейных РЧ-аппликаций по своду и линейно по задней стенке ЛП (см. рис. 2).
Во всех случаях после завершения РЧА с целью восстановления СР с использованием дефибриллятора выполняли наружную ЭИТ согласно методике, представленной в отечественных рекомендациях по оказанию анестезиологического пособия [15].
В раннем послеоперационном периоде пациенты в течение 24 ч получали гепарин под контролем активированного частичного тромбопластинового времени с последующим возобновлением терапии непрямыми антикоагулянтами и антиаритмическими препаратами.
После проведения РЧА в течение 3—6 мес все пациенты продолжали принимать антиаритмические препараты и антикоагулянты под контролем международного нормализованного отношения с последующим принятием решения лечащим врачом о целесообразности их отмены.
Клиническое наблюдение заключалось в оценке жалоб пациента, проведении физического обследования, регистрации 12 отведений электрокардиограммы и ее холтеровского мониторирования через 3, 6 и 12 мес после выполнения РЧА.
В случае появления предсердных аритмий и/или ФП в раннем или позднем послеоперационном периоде пациентам выполняли медикаментозную и/или электрическую кардиоверсию. При стойкой тенденции к рецидивам аритмического синдрома пациентам проводили повторную операцию эндоЭФИ и РЧА.
Математическое моделирование ФП и РЧА ФП. На первом этапе в ходе вычислительного эксперимента реализовали заданный автоволновой процесс возбудимой ткани ЛП и производили моделирование ФП с использованием уравнения Фитцхью—Нагумо, что позволяло учитывать электрическую неоднородность предсердий (устья ЛВ) [16].
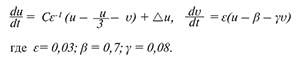
Выбор использованной математической модели был основан на создании модели 6-волнового re-entry, в которой направление вращения re-entry определялось базовыми свойствами синхронизации вращения круговых волн [11—13].
В различных областях предсердий создавались re-entry с различными частотами. Это свойство достигалось за счет фрагментации ЛП на неоднородные области. Скорость распространения электрического возбуждения в предсердиях, использовавшаяся в расчетах, составляла 50 см/с. Для вычисления характеристик автоволновых процессов в двумерной математической модели предсердий использовали специально разработанный нами метод сканирования, позволяющий производить эффективные подсчеты в случае сложных границ области и ее гетерогенности [11—13]. С этой целью использовали сеточную схему метода прямых в сочетании с методом сканирования в программной среде MATLAB7, что позволило эффективно исследовать автоволновые процессы при наличии сложных границ области и ее гетерогенности [11—13]. Метод сканирования позволил оперативно моделировать геометрию исследуемой области с учетом наличия устьев 4 ЛВ и границ среды.
Для графического представления автоволн электрического возбуждения красным цветом отображалась область нарастания электрического возбуждения, желтым — область спадания, бирюзовым — область медленного нарастания, относящаяся к фазе рефрактерности возбуждения, зеленым — отсутствие возбуждения (рис. 3, см. цв. вклейку).
На втором этапе с помощью процедуры, реализуемой с использованием метода сканирования, производили абляционное форматирование, моделирующее линейные и циркулярные РЧ-воздействия, наносимые в ходе проведения интервенционной процедуры (рис. 4, см. цв. вклейку).
Для моделирования заключительного этапа РЧА — кардиоверсии, проводили вычислительный эксперимент, соответст-вующий наружной кардиоверсии. Математическая модель кардиоверсии представляет собой дополнительное слагаемое в первом уравнении Фитцхью—Нагумо [16]. Амплитуда дополнительного слагаемого имеет значение U=0,4, время действия дополнительного слагаемого T=50 мс. После истечения этого времени дополнительное слагаемое из уравнения удаляется.
Результаты
Клинический этап. В ходе проведения эндоЭФИ до начала РЧ-воздействия в ЛП исходная средняя длительность цикла ФП у 20 пациентов, измеренная на электродных парах электрода, позиционированного в КС, составляла 156±47 мс (от 108±26 до 194±12 мс).
После проведения РЧА в митральном перешейке и по периметру левой нижней ЛВ эта величина составляла 169±47 мс (от 109±21 до 220±16 мс). При этом «организация» или увеличение средней длительности цикла ФП наблюдалось у 10 (50%) из 20 оперированных пациентов.
Последующие РЧ-воздействия по периметру левой верхней ЛВ и правых ЛВ привели к дальнейшему увеличению длительности цикла ФП у 12 (60%) пациентов. Средняя длительность цикла ФП на электродных парах электрода, позиционированного в КС, составляла 191±47 мс (от 108±13 до 230±16 мс).
Нанесение линейных РЧ-аппликаций по своду и линейно по задней стенке ЛП привело к увеличению средней длительности цикла ФП до 210±22 мс (от 111±24 до 260±19 мс), которое наблюдалось у 16 (80%) из 20 пациентов (рис. 5, см. цв. вклейку)
Ни в одном из случаев мы не наблюдали восстановления СР на фоне проведения РЧ-аппликаций. Заключительным этапом процедуры с целью восстановления СР выполняли наружную ЭИТ, которая эффективно купировала ФП.
На рис. 6 (см. цв. вклейку) представлен клинический пример «организации» цикла ФП и последующее восстановление СР методом наружной электрической кардиоверсии в ходе проведения процедуры РЧА у пациента (мужчина, 56 лет, с длительностью анамнеза постоянной ФП около 3 лет), включенного в данное исследование.
В остром периоде (первые 3 мес после проведения РЧА) отмечалось 14 рецидивов аритмического синдрома (ФП и/или атипичного ТП) у 8 (40%) пациентов, при этом в 7 случаях потребовалось проведение наружной электрической кардиоверсии, а 7 случаев были купированы с помощью дополнительных доз базового антиаритмического препарата (рис. 7, см. цв. вклейку).
Через 12 мес после РЧА устойчивый СР сохранялся у 15 (75%) пациентов, из них 11 (55%) прекратили ААТ, а 4 (20%) продолжали ААТ, 4 (20%) пациента перенесли повторные РЧА по поводу атипичного ТП и/или ФП. У 5 пациентов через 12 мес сохранялась ФП и/или атипичное ТП, несмотря на повторные РЧА и неоднократные попытки кардиоверсии (см. рис. 7).
Этап математического моделирования. После создания модели 6-волнового re-entry методом сканирования в программной среде MATLAB с помощью сеточной схемы проводилось АФ, моделирующее линейные и циркулярные РЧ-воздействия, соответствующие наносимым в ходе проведения интервенционной процедуры в клинике. Предложенный вариант АФ позволил трансформировать 6-волновое re-entry в 4-волновое (рис. 8, см. цв. вклейку). Затем проводилось моделирование ЭИТ-кардиоверсии, в результате которой происходили купирование «остаточного» 4-волнового e-entry, восстановление СР и не было отмечено возобновления 4-волнового re-entry в последующем (рис. 9, см. цв. вклейку). Установлено также, что при моделировании ЭИТ на фоне 6-волнового re-entry отмечалось незамедлительное возрождение ФП в полном объеме (рис. 10, см. цв. вклейку).
Обсуждение
Моделирование механизмов постоянной формы ФП. Существующие представления о природе возникновения и поддержания постоянной формы ФП связывают, в том числе с механизмами многоволнового re-entry по типу спиральных волн, которые возникают в результате ремоделирования активной среды предсердий, сопровождающегося повышенной возбудимостью, уменьшением длительности рефрактерного периода, гетерогенностью миокарда предсердий. В нашем исследовании нам удалось создать устойчивую модель 6-волнового re-entry на основании использования метода сканирования и фрагментировать ЛП на неоднородные по геометрии участки. Данная математическая модель может рассматриваться как одна из возможных моделей постоянной формы ФП.
Моделирование РЧА постоянной формы ФП. Существующие в клинической практике методики РЧА субстрата постоянной формы ФП подразумевают использование агрессивного подхода, заключающегося в проведении абляции триггеров ФП как связанных, так и несвязанных с устьями ЛВ, нанесение РЧ-апликаций в области регистрации фрагментированных электрограмм в предсердиях, а также нанесении линейных воздействий с целью формирования компартментов в миокарде предсердий [5—8, 17]. Последовательная реализация данной тактики, как правило, приводит к развитию так называемой организации цикла ФП в результате уменьшения (выключения) некоторой площади миокарда предсердий, являющейся субстратом аритмии. Электрофизиологическим проявлением данной «организации» служат увеличение длительности цикла ФП и трансформация ФП в конечном итоге в ТП и/или предсердную тахикардию. Следует понимать, что каждый последующий шаг в этой методике увеличивает длительность операции и экспозиции РЧ-воздействий, а, следовательно, может повышать риск развития осложнений, связанных с развитием перфорации предсердий, формированием пищеводно-предсердной фистулы, сужением ЛВ, развитием постабляционных аритмий и/или stiff-синдрома.
В частности, в работах группы M. Haissaguerre и соавт., использовавших «пошаговый подход» к РЧА субстрата постоянной формы ФП, длительность РЧА составляла 60—120 мин [5].
При альтернативном (с использованием электрической кардиоверсии) подходе к РЧА постоянной формы ФП общая длительность РЧА составляла от 37±11 [3] до 44±13 мин [4].
При многоволновом re-entry существенное значение приобретает РЧА такого вида, при котором минимальные размеры «областей-островков» возбудимой ткани становятся меньше минимального диаметра (D) области, при котором возникновение re-entry невозможно, т.е. в математическом варианте:
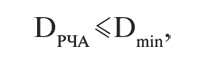
где DРЧА — диаметр ограниченной области РЧА, Dmin — минимальный диаметр области, при котором появление re-entry невозможно.
Проведение АФ, выполненного нами в ходе математического эксперимента и соответствующего методике РЧА в клинической практике, позволило достичь подобных условий.
Это подтверждалось трансформацией 6-волнового re-entry в 4-волновое. Клиническим электрофизиологическим эквивалентом данного трансформирования являлось увеличение длительности цикла ФП в ЛП, верифицированное нами у 80% пациентов.
Сопоставление клинических результатов электрической кардиоверсии с данными математического моделирования. Полученные нами результаты математического моделирования ЭИТ 6-волнового re-entry свидетельствуют о том, сохранение начальных электрофизиологических условий в ЛП не приводит к прекращению ФП. В то же время моделирование ЭИТ для 4-волнового re-entry, возникшего в результате проведенного АФ, эффективно прерывало ФП.
В связи с этим заслуживают внимание данные H. Oral и соавт., которые показали, что у пациентов с постоянной ФП через 2 мес наблюдения после проведения ЭИТ рецидив аритмического синдрома наблюдался в 97% случаев, тогда как у пациентов, которым выполнялась РЧА с последующей ЭИТ, устойчивый СР сохранялся в 74% случаев в течение 204±82 дней динамического наблюдения. Данные, полученные нами в этом исследовании, а также опубликованные нами ранее оптимистичны в отношении долгосрочного (на протяжении 5 лет) поддержания СР у 66 пациентов, перенесших РЧА по поводу постоянной ФП, у которых СР в конечном итоге был восстановлен методом ЭИТ [4]. Более того, через 5 лет клинического наблюдения у пациентов, перенесших РЧА, не было отмечено ни одного случая инфаркта миокарда или ишемического инсульта. При этом в контрольной группе (медикаментозный контроль частоты сердечных сокращений) было зарегистрировано 5 случаев инфаркта миокарда (р=0,006) и 6 случаев инсульта (р=0,001) [4].
Таким образом, экстраполяция результатов математического эксперимента на клинические результаты интервенционного лечения у больных этой категории может являться подтверждением того, что линейная РЧА в ЛП приводит к уменьшению количества циклов re-entry, большей организации ФП, повышает эффективность ЭИТ и отдаленную эффективность поддержания СР.
Результаты, полученные на математическом этапе нашего исследования, свидетельствуют о том, что восстановление СР на фоне выполнения РЧ-воздействий, не является обязательной конечной точкой интервенционной процедуры, а наружная ЭИТ может рассматриваться как правомочный заключительный этап в комплексе с РЧА ФП. Это важный факт, который аргументировано обосновывает возможность уменьшения как длительности абляционной процедуры, так и времени РЧ-воздействий, что не может не иметь значения в отношении безопасности интервенционного вмешательства. Кроме того, увеличение длительности цикла ФП, регистрируемой с референтного катетера, установленного в КС, может использоваться как маркер, непосредственным образом определяющий длительность процедуры и ее конечные точки. Последнее утверждение косвенно подтверждается данными многофакторного анализа, выполненного в 2009 г., который показал, что предикторами положительного клинического результата РЧА ФП являются длительность эпизода ФП менее 2 лет и исходная длительность цикла ФП в ушке ЛП более 161 мс [5]. В этом же исследовании обращало на себя внимание и то, что восстановление СР на фоне РЧА не относилось к предикторам положительного отдаленного результата.
Более того, увеличение агрессивности РЧА может сопровождаться увеличением риска развития тяжелых, в том числе угрожающих жизни, осложнений, а также частоты возникновения постабляционных «ятрогенных» аритмий, при которых в дальнейшем требуется проведение повторных эндокардиальных вмешательств [1, 18].
Заключение
Абляционное форматирование, выполненное на математической модели 6-волнового re-entry и имитирующее циркулярную и линейную радиочастотную абляцию субстрата постоянной формы фибрилляции предсердий является возможным и приводит к трансформации 6-волнового re-entry в 4-волновое. Последующее математическое моделирование электрической кардиоверсии свидетельствуют об устранении 4-волнового re-entry и невозможности устранении 6-волнового.
По результатам клинико-математического моделирования, электрическая кардиоверсия может рассматриваться как заключительный этап в комплексном лечении больных с постоянной формой фибрилляции предсердий.
Результаты, полученные в ходе математического моделирования, соответствуют данным, полученным в ходе выполнения радиочастотной абляции пациентам с постоянной формой фибрилляции предсердий и последующего клинического наблюдения в течение года после операции.
Исследование выполнено при финансовой поддержке РФФИ в рамках научного проекта № 13-02-01307 а.



