Определение. Трепетание предсердий (ТП) — правильный, регулярный, скоординированный предсердный ритм, обусловленный механизмом macrore-entry и превышающий частотной характеристикой предсердную или внутрипредсердную тахикардию (более 200—250 в минуту).
Эпидемиология. ТП — одно из наиболее часто встречающихся нарушений ритма сердца, на его долю приходится около 10% всех пароксизмальных наджелудочковых тахиаритмий [1—5]. По данным исследования MESA (Marshfield Epidemiologic Study Area), в США распространенность ТП составляет 88 на 100000 населения, при этом ежегодно в мире выявляется 200 тыс. новых случаев аритмий данного вида [6]. Заболеваемость ТП в 2—5 раз выше у мужчин и, подобно заболеваемости фибрилляцией предсердий (ФП), увеличивается с возрастом [2, 6, 7]. В большинстве случаев ТП встречается у лиц со структурной патологией миокарда [1, 5, 6]. Основными причинами развития ТП являются различные формы ишемической болезни сердца (ИБС); кроме того, данный вид аритмии часто встречается в группе пациентов, перенесших хирургическое вмешательство на открытом сердце [1]. К другим наиболее частым причинам возникновения ТП относятся хронические заболевания легких, тиреотоксикоз, перикардиты, ревматизм (особенно у лиц с митральным стенозом) [1, 5].
Этиология ТП. По данным J. Granada и соавт., выполнившими тщательный анализ этиологических факторов развития ТП у 58 000 пациентов с суправентикулярной тахикардией, которые принимали участие в исследовании MESA, основными этиологическими факторами ТП являются ИБС, ревматизм, артериальная гипертензия, хроническое или острое легочное сердце, гипертиреоз, врожденные и приобретенные пороки сердца, дисфункция синусного узла (синдром тахи-бради) [5].
Данные клинического обследования 254 прооперированных нами пациентов за период с 1999 г. свидетельствуют о том, что наиболее частой причиной как пароксизмальной (87%), так и хронической (81%) форм типичного ТП является ИБС. Оставшиеся случаи приходились на долю постмиокардитического кардиосклероза и идиопатического вариантов течения типичного ТП (табл. 1) [1, 8].
Таблица 1. Причины развития типичного ТП*
Примечание. * — по данным Рентгенохирургического центра интервенционной кардиологии ГВКГ им. Н.Н. Бурденко. ТП — трепетание предсердий; ИБС — ишемическая болезнь сердца; ФК — функциональный класс; АКШ — аортокоронарное шунтирование.
Классификация и патогенез. В настоящее время общепризнано, что в основе ТП лежит механизм macrore-entry. Выделяют типичное и атипичное ТП (табл. 2).
Таблица 2. Классификация ТП (модифицированная классификация M. Sheinman, 2001)*
Примечание. * — классификация представлена в модификации авторов (2008); ТП — трепетание предсердий; ЛП — левое предсердие; ЛВ — легочные вены; МПП — межпредсердная перегородка; КС — коронарный синус.
Типичное ТП обусловлено правопредсердной циркуляцией волны возбуждения вокруг кольца трехстворчатого клапана (рис. 1). Круг re-entry ограничен так называемыми пределами латеральных границ ТП: сзади, сверху и снизу — анатомическими препятствиями (верхняя и нижняя полая вена), сзади септально-евстахиевым клапаном/евстахиевой складкой) и сзади в латеральной части — функциональным барьером проведения (область терминальной кристы), кпереди — периметром трехстворчатого клапана1.
Рис. 1. Типичное трепетание предсердий.
А — цикл ТП, вид на предсердия спереди. Черными стрелками обозначены пространственно-временны`е характеристики распространения волны ТП по периметру трехстворчатого клапана «против часовой стрелки» и далее в область левого предсердия по структурам, близким к коронарному синусу (КС); Б — трехмерная реконструкция правого предсердия того же цикла ТП с помощью нефлюороскопической системы эндокардиального картирования, направление фронта возбуждения показано стрелками; В — ЭКГ в 12 отведениях (скорость регистрации 50 мм/с) во время типичного ТП с циркуляцией фронта деполяризации «против часовой стрелки». Обращают внимание отрицательная «пилообразная» геометрия волн ТП в нижних стандартных (показано стрелками) и усиленных отведениях и положительная направленность волн ТП в отведении V1; Г — ЭКГ в 12 отведениях (скорость регистрации 50 мм/с) во время типичного ТП с циркуляцией фронта деполяризации «по часовой стрелке». Обращает внимание положительная «пилообразная» геометрия волн ТП в нижних стандартных (показано стрелками) и усиленных отведениях. ТП — трепетание предсердий; НПВ — нижняя полая вена; ВПВ — верхняя полая вена; ТК — терминальная криста; ЕС — евстахиева складка; ЛВ — легочные вены; НП — нижний (кавотрикуспидальный) перешеек (область между НПВ и периметром трикуспидального клапана); ЕК — евстахиев клапан; ЭКГ — электрокардиограмма.
В зависимости от направления волны возбуждения в предсердиях выделяют две разновидности типичного ТП:
— ТП с активацией межпредсердной перегородки (МПП) в каудокраниальном направлении, а латеральных отделов правого предсердий (ПП) — в краниокаудальном, т.е. с циркуляцией волны возбуждения вокруг трехстворчатого клапана против хода часовой стрелки (counterclockwise — CCW) при рассмотрении цикла циркуляции со стороны верхушки сердца. Данный тип петли macrore-entry выявляется у 90% больных с ТП, в том числе у пациентов, перенесших операцию на открытом сердце (см. рис. 1, А—В) [1, 9, 10];
— ТП с противоположной активацией структур ПП, т.е. циркуляцией волны возбуждения по часовой стрелке (clockwise — CW) (см. рис. 1, Г) [1, 9, 10].
Главным отличительным признаком типичного ТП является истмус-зависимость, т.е. возможность его купирования при радиочастотном воздействии или сверхчастой стимуляции в области нижнего (кавотрикуспидального) перешейка (НП), так как последний представляет собой наиболее уязвимое звено тахикардитического цикла (см. рис. 1, А).
Истмус-зависимыми, помимо типичного ТП (CCW- и CW-ТП), являются и некоторые варианты ТП, ранее трактуемые в рамках атипичных, такие как двухволновое, нижнепетлевое и внутриперешеечное2 ТП (рис. 2, см. цветную вклейку) [1, 11—13].
Для двухволнового ТП характерно формирование 2 волн деполяризации в ПП, циркулирующих друг за другом вокруг кольца трехстворчатого клапана в одном направлении, в результате чего происходит ускорение ТП. При этом геометрия предсердной активации на поверхностной электрокардиограмме (ЭКГ) не претерпевает существенных изменений. Данный вид аритмии, вероятно, имеет незначительное клиническое значение, так как сохраняется непродолжительный период времени (до 11 комплексов), трансформируясь в последующем в типичное ТП, реже в ФП [1, 11—13]. Нижнепетлевое ТП характеризуется прорывом волны возбуждения через терминальную кристу на разных ее участках с формированием круга re-entry вокруг устья нижней полой вены (рис. 2, В, см. цветную вклейку). При внутриперешеечном ТП волна возбуждения циркулирует в самом НП по периметру коронарного синуса (см. рис. 2, А, см. цветную вклейку) [1, 14].
К истмус-независимым ТП относятся верхнепетлевое, множественноцикловое и левопредсердные ТП. Эти разновидности аритмии встречаются гораздо реже истмус-зависимых ТП (см. рис. 2, см. цветную вклейку) [1, 12—15].
При верхнепетлевом ТП волна деполяризации, прорываясь через ТК, формирует круг re-entry в области свода ПП по периметру верхней полой вены (ВПВ), при этом нижние отделы ПП не вовлечены в цикл ТП (см. рис. 2, Б, см. цветную вклейку). Множественно-цикловое ТП характеризуется одновременным сосуществованием разнонаправленных нескольких циклов активации в ПП вследствие возможности множественных прорывов волн возбуждения через терминальную кристу (см. рис. 2, Г, см. цветную вклейку) [1, 13]. При левопредсердном ТП в большинстве случаев циркуляция волн возбуждения включает в себя формирование петель re-entry вокруг «электрически немого пространства», по периметру митрального клапана, а также вокруг одной или нескольких легочных вен (рис. 3, см. цветную вклейку). Однако у некоторых пациентов круги re-entry могут быть более сложными, с чередованием реализации волны деполяризации по 2 или 3 петлям, а в некоторых случаях и с циркуляцией волны деполяризации по контуру цифры 8 [1, 15].
Отдельно выделяют левопредсердное ТП, которое, как правило, обусловлено ятрогенными причинами (хирургические вмешательства на сердце, а также процедура радиочастотной абляции — РЧА при ФП). Цикл re-entry может поддерживаться по периметру митрального клапана [15], «электрически немого пространства» в задней стенке левого предсердия (ЛП) [16] или в ушке ЛП [17], а также вокруг устьев легочных вен или мембранозной части МПП [16—18] (см. рис. 3, см. цветную вклейку).
Клинические проявления ТП. Обычно пациенты с ТП предъявляют жалобы на внезапно возникшие ощущения сердцебиения, одышку, общую слабость, плохую переносимость физических нагрузок или боли в грудной клетке (табл. 3). Однако возможны и более тяжелые клинические проявления — синкопэ, пресинкопэ, головокружение, гипотензия и даже остановка сердца, обусловленные высокой частотой сокращения желудочков и угрозой трансформации в желудочковую тахикардию и фибрилляцию желудочков. Патофизиологической основой данной симптоматики являются снижение ударного выброса, системного артериального давления и уменьшение коронарного кровотока, которое, как правило, обратно пропорционально частоте сердечных сокращений. По некоторым данным, снижение коронарного кровотока может достигать 60% при возрастающей на фоне тахисистолии потребности миокарда в кислороде. Вследствие рецидивирования или даже хронизации выраженных гемодинамических расстройств выше означенного характера развивается диастолическая, а в дальнейшем — систолическая дисфункция сердца с последующей дилатацией его полостей, приводящая к структурному ремоделированию миокарда и сердечной недостаточности [1]. Риск развития тромбоэмболических осложнений, как паутина, окутывает весь этот патогенетический каскад. Тем не менее следует заметить, что частота развтия эмболических осложнений у пациентов с ТП в 2 раза ниже, чем у пациентов с ФП [1, 3].
Таблица 3. Клинические проявления типичного ТП*

Примечание. * — по данным Рентгенохирургического центра интервенционной кардиологии ГВКГ им. Н.Н. Бурденко.
Диагностика типичного ТП. Комплекс клинико-лабораторно-инструментальных исследований должен быть направлен на исключение/подтверждение структурной патологии миокарда. Всем больным проводят элекрокардиографию в 12 отведениях, трансторакальную эхокардиографию, по показаниям — коронарографию и вентрикулографию.
Дифференциальный диагноз ТП необходимо проводить со всем спектром суправентрикулярных тахикардий, к которым относятся атриовентрикулярная (АВ) узловая реципрокная тахикардия, АВ-реципрокная тахикардия при синдроме Вольфа—Паркинсона—Уайта, ФП, предсердные и внутрипредсердные тахикардии, постоянно-рецидивирующая тахикардия из области АВ-соединения. Ключевым моментом диагностики ТП является тщательный анализ поверхностной ЭКГ в 12 отведениях, который на ранних этапах обследования позволит клиницисту судить о типичности или атипичности ТП, что будет определять тактику лечения больного.
Электрокардиографическая диагностика. ЭКГ типичного ТП с циркуляцией волны возбуждения «против хода часовой стрелки» (CCW) характеризуется отрицательными волнами F в отведениях II, III, avF, отражающими синхронную активацию МПП снизу вверх, и положительными волнами трепетания в отведении V1. Нисходящее колено волн F в нижних стандартных и усиленных отведениях имеет большую длину (более пологое) по сравнению с восходящим (более крутым). Важным моментом является заметно меньшая амплитуда положительных (+) комплексов предсердной электрической активности в V1, проецирующихся на восходящую фазу волн ТП в отведении avF (см. рис. 1, В, Г) [1, 9, 10].
Типичное ТП с циркуляцией волны деполяризации «по ходу часовой стрелки» (CW), электрокардиографически характеризующееся положительной направленностью волн трепетания в нижних стандартных и усиленных отведениях и сопоставимыми по амплитуде с отрицательными волнами F в отведении V1 (cм. рис. 1, Г) [1, 9, 10].
Электрокардиографическая характеристика нижнепетлевого ТП будет зависеть от уровня проведения через пограничную борозду. Она будет варьировать от ЭКГ, идентичной типичному ТП/CWW, с незначительным уменьшением амплитуды положительной фазы волны трепетания в нижних отведениях и волны F в отведении V1 из-за интерференции встречных фронтов деполяризации в области свода ПП (при прорыве волны ТП в области каудальной части терминальной кристы) до ЭКГ, характерной для типичного ТП/CW вследствие активации МПП в краниокаудальном направлении (при прорыве в области краниальной части терминальной кристы) [1, 11—15].
При верхнепетлевом ТП геометрия предсердной активации на поверхностной ЭКГ аналогична типичному ТП с циркуляцией импульса по часовой стрелке (см. рис. 1, Г).
Эндокардиальное электрофизиологическое исследование (эндоЭФИ). ЭндоЭФИ выполняется пациентам с ТП, которым планируется одномоментное выполнение РЧА по поводу клинической аритмии. Обязательным условием является полная отмена антиаритмических препаратов (ААП) за 6 периодов полувыведения до операции.
Основная цель эндоЭФИ — верификация и картирование цикла ТП и выполнение дифференциальной диагностики с другими суправентрикулярными аритмиями. Для проведения картирования цикла типичного ТП широкое применение получил многополюсной катетер HALO (нимб) с коротким межэлектродным расстоянием (около 2 мм), который выставляется по периметру трехстворчатого клапана в пределах латеральных границ ТП. Установка этой системы кпереди от терминальной кристы позволяет проследить геометрию внутрипредсердной активации при ТП. Регистрирующие биполярную электрограмму 10—20 пар этого катетера позволяют выявлять четкую иерархию внутрипредсердной активации. При типичном ТП эта геометрия распространения волны деполяризации иллюстрирует направление циркуляции импульса либо по ходу часовой стрелки (CW), либо против хода часовой стрелки (CCW) по периметру кольца трикуспидального клапана. Полезной может быть и регистрация внутрисердечных электрограмм из области коронарного синуса, которые будут отражать особенности левопредсердной активации при ТП.
В настоящее время в клинической электрофизиологии получили распространение методики верификации цикла ТП с использованием внутрисердечной эхокардиографии, систем бесконтактного многоканального картирования и трехмерного электромагнитного нефлюороскопического картирования, которые позволяют воспроизводить трехмерную структуру предсердий и верифицировать круг re-entry в них [19—22]. Применение этих систем особенно оправдано при атипичных формах ТП (рис. 4) [22].
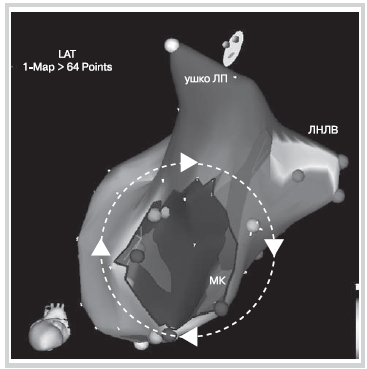
Рис. 4. Трехмерная реконструкция ЛП на фоне атипичного (левопредсердного) ТП с циркуляцией импульса по периметру МК «по часовой стрелке». Распространение фронта деполяризации показано стрелками.
МК — митральный клапан; ЛНЛВ — левая нижняя легочная вена, ЛП — левое предсердие.
Лечение. Неотложная терапия ТП. Пациентам с выраженными гемодинамически значимыми проявлениями ТП, такими как синкопэ, пресинкопэ, гипотензия, стенокардия, нарастание сердечной недостаточности показана экстренная синхронизированная кардиоверсия. Успешного восстановления синусового ритма, как правило, можно добиться разрядом 100 Дж [1, 3, 23, 24].
В отечественной практике для восстановлении синусового ритма у пациентов с типичным ТП широкое распространение получила методика чреспищеводной электрокардиостимуляции, эффективность которой колеблется от 55 до 100% и в среднем составляет 82% [1, 3, 25].
В том случае, если у пациента имеется минимальная гемодинамическая значимость клинической симптоматики ТП, первым этапом целесообразно назначение лекарственных средств, замедляющих АВ-проведение и обеспечивающих контроль частоты сердечных сокращений с последующим проведением плановой электрической или фармакологической кардиоверсии. Для этой цели чаще всего назначают препараты, относящиеся к группе недигидропиридиновых блокаторов кальциевых каналов (верапамил и дилтиазем), или β-адреноблокаторы. По данным рандомизированных исследований, дилтиазем или атенолол в стандартных терапевтических дозах эффективно контролируют частоту активации желудочков на фоне типичного ТП у большинства больных уже через 30 мин после приема внутрь [1—3]. Что касается таких препаратов, как кордарон [26] или сердечные гликозиды, то в ряде исследований было показано, что достижение нормосистолии при их внутривенном введении возможно в среднем через 4—6 ч [1—3, 26]. Получены многообещающие данные об эффективности использования нового отечественного ААП III класса нибентана для купирования пароксизмов ТП [27].
Вторым этапом является восстановление синусового ритма методом электрической и/или фармакологической кардиоверсии. Наиболее эффективны дофетилид и ибутилид [3, 28]. Их эффективность при внутривенном введении достигает 76% и значительно превосходит эффективность пропафенона, новокаинамида, верапамила, купирующая эффективность которых составляет соответственно 40, 14 и 5%. Тем не менее следует помнить, что применение дофетилида сопряжено с риском развития веретенообразной желудочковой тахикардии, вероятность возникновения которой составляет 6% [28].
ААП IС класса эффективны в отношении удлинения цикла ТП, что может привести к возникновению АВ-проведения 1:1, сопровождается увеличением частоты сокращения желудочков на фоне ТП и в конечном итоге может ухудшить клиническое состояние больного [1—3].
Постоянная антиаритмическая терапия. Постоянная фармакологическая профилактическая терапия при ТП обычно является эмпирической, эффективность ее определяется методом проб и ошибок. Традиционно рекомендуется двухкомпонентная терапия с применением как препарата, эффективно блокирующего проведение в АВ-соединении, так и мембранно-активного средства. Как правило, существующие данные об эффективности препаратов I класса у пациентов с ТП были получены в рандомизированных исследованиях по оценке их эффективности у больных, страдающих ФП и/или ТП. При этом отдельная группа пациентов с ТП не всегда выделялась. Установлено, что применение флекаинида обеспечивало эффективное поддержание синусового ритма у пациентов с ТП в 50% случаев в течение 6 мес наблюдения. Следует отметить, что во всех случаях, помимо препаратов I класса, пациенты принимали β-адреноблокаторы или блокаторы кальциевых каналов [3].
Препараты III класса сочетают в себе черты ААП всех классов и поэтому назначение лекарственных средств, блокирующих АВ-проведение, в этом случае необязательно [3, 26]. По данным нескольких рандомизированных плацебо-контролируемых исследований, наиболее эффективным препаратом для ААТ при хронической ТП является дофетилид [3]. При его применении в максимальных терапевтических дозах эффективный контроль за синусовым ритмом в течение 1 года наблюдения обеспечивался в 73% случаев [3].
Что касается постоянной ААП при ТП, проводимой кордароном или соталололом, то данные, полученные в нескольких рандомизированных исследованиях при использовании этих препаратов, свидетельствуют о том, что их эффективность существенно не отличается от результатов, полученных при оценке эффективности постоянной ААП этими препаратами у больных с ФП, и составляет 63 и 40% соответственно при длительности лечения 1 год [3].
Антикоагулянтная терапия. В настоящее время не существует рандомизированных исследований, результаты которых убедительно свидетельствуют о необходимости антикоагулянтной терапии у пациентов с ТП. Установлено, что риск развития эмболических осложнений после электрической кардиоверсии у пациентов с ТП составляет 2,2%, в то время как у пациентов с ФП вероятность развития эмболических событий составляет от 5 до 7%. Тем не менее, согласно современным отечественным и зарубежным руководствам по лечению больных с суправентрикулярными тахикардиями, пациентам с верифицированным ТП, длительность которого превышает 48 ч, рекомендуется назначение адекватной антикоагулянтной терапии (варфарин) в течение 4 нед перед проведением электрической или медикаментозной кардиоверсии, несмотря на то что вероятность развития эмболических осложнений у пациентов этой категории в 2—3 раза ниже, чем у больных с ФП [3, 24].
Катетерная РЧА у пациентов с типичным ТП. Согласно существующим в настоящее время отечественным и зарубежным рекомендациям по постоянной терапии типичного ТП, катетерная РЧА НП является методом выбора, который позволяет пациенту полностью избавиться от необходимости приема антиаритмических препаратов (табл. 4) [1, 3, 24]. Отношение к данной методике как к определяющей при лечении пациентов с типичным ТП основано на данных единственного рандомизированного исследования, проведенного группой A. Natale. В нем проводилось сравнение фармакологического и интервенционного подходов к лечению ТП, заключавшегося в выполнении РЧА нижнего перешейка. В этом исследовании принимал участие 61 пациент с пароксизмальной формой типичного ТП. У 31 пациента выполнялась РЧА нижнего перешейка и полностью прекращалась проводимая ранее ААТ, а у 30 больных проводилась ААТ. Через 12 мес наблюдения рецидивы типичного ТП возникали у 64% пациентов, получавших ААТ, и только у 20% больных, которым проводилась РЧА при ТП [29].
Таблица 4. Рекомендации по постоянной терапии типичного ТП (Рекомендации Всероссийского научного общества специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции, 2005)
Примечание. ТП — трепетание предсердий; ФП — фибрилляция предсердий; РЧА — радиочастотная абляция; ААП — антиаритмические препараты. *Класс I — условия, для которых имеются доказательства и/или единодушие экспертов о пользе и эффективности метода лечения. Класс II — условия, для которых имеются противоречивые свидетельства и/или расхождение мнений экспертов относительно пользы и эффективности метода лечения. Класс IIa — преобладают доказательства или мнения в пользу эффективности и метода лечения. Класс IIb — польза и эффективность метода лечения менее обоснованы доказательствами и мнением экспертов. Класс III — условия, для которых имеются доказательства и/или общее согласие о том, что данная диагностическая процедура или метод лечения не являются полезными и эффективными, а в некоторых случаях могут приносить вред. Доказательность считается наивысшей (класс А) при наличии данных большого количества рандомизированных клинических исследований, средней (класс В) при ограниченном количестве рандомизированных и нерандомизированных исследований или данных публикаций в медицинской литературе. Низший класс (С) относится к рекомендациям, основанием для которых служило мнение экспертов.
Согласно данным нашего исследования, в котором принимали участие 254 пациента, оперированных по поводу типичного ТП, в отдаленном периоде наблюдения, в среднем составившем 36±14 мес (от 1 года до 8 лет), эффективность первичной процедуры РЧА достигала 87%. Рецидивы типичного ТП наблюдались в первые 1,8±1,0 мес (от 1 до 4 мес) после первой процедуры РЧА у 13% пациентов. Проведение повторной сессии РЧА позволяло достичь абсолютных показателей эффективности (100%) в лечении этого вида нарушений ритма на протяжении одного года наблюдения после интервенционного вмешательства [1, 8]. Современные данные ведущих аритмологических центров свидетельствуют о том, что эффективность РЧА при типичном ТП колеблется от 90 до 100% в течение 3 лет наблюдения [30, 31].
Типичное ТП часто сопровождается наличием ФП. В исследовании, проведенном в 1998 г. H. Paydak и соавт., было установлено, что после проведения РЧА при типичном ТП через 20 мес клинического наблюдения ФП наблюдалась у 25% пациентов. Авторы установили, что статистически значимыми и независимыми предикторами появления ФП после РЧА при типичном ТП являлись указания в анамнезе на ранее переносимые эпизоды ФП и умерено выраженное снижение фракции выброса левого желудочка (<50%) [32].
Следует обратить внимание (см. табл. 4), что практически при всех возможных вариантах клинического течения типичного ТП методом выбора является РЧА (класс I или IIa). Противопоказаниями к проведению РЧА служат ТП, трактуемое в рамках нестабильного течения ИБС, электролитных нарушений, тиреотоксикоза, воспалительных процессов в миокарде, а также отказ пациента от интервенционного лечения и предпочтение им ААТ [1, 3, 24].
Методика проведения РЧА. Первоначально конечной точкой процедуры РЧА при ТП являлось прекращение аритмии в момент приложения энергии в зоне НП. Однако при последующем наблюдении за этой категорией пациентов выявлено, что в этом случае доля рецидивов ТП после процедуры РЧА достигала всего лишь 30—40%. Внедрение в клиническую практику методики орошаемой (ирригационной) РЧА значительно уменьшило частоту рецидивирования типичного ТП после первичной процедуры. Использование орошаемых электродов позволяет избежать появления барьера из коагулированных белковых молекул в интерфейсе электрод—ткань, возникающего при применении неирригационных электродов, и лимитирующего глубину повреждения в нижнем перешейке [9, 33]. По нашим данным, физические характеристики радиочастотных воздействий ирригационным электродом(со скоростью орошения 10 мл/мин) в НП должны быть следующими: средняя мощность 36,2±3,2 Вт, средняя температура 40,0±2,2 °С, общая продолжительность воздействий 18,2±4,5 мин [1, 33].
Клинические исследования показали, что свидетельством эффективного воздействия являются создание полной двунаправленной блокады проведения волны деполяризации через НП и обязательная ее верификация в ходе процедуры контрольного эндоЭФИ [1, 9, 34].
Традиционно верификация двунаправленного блока в НП осуществляется непрямым (косвенным) методом на основании изменения геометрии внутрипредсердной активации в пределах латеральных границ ТП. При этом осуществляется стимуляция из области нижнелатеральных отделов ПП и верифицируется «обходная активация» септальных отделов через латеральные отделы ПП снизу вверх и далее через свод ПП к перегородке — сверху вниз по направлению к НП. Противоположная направленность блока верифицируется при стимуляции из области устья КС и на основании констатации «обходной активации» перешейка через перегородку снизу вверх в направлении свода ПП и далее по латеральным отделам ПП сверху вниз (рис. 5, А) [1, 33].
Рис. 5. Верификация блока проведения в нижнем перешейке на основании непрямых критериев.
Схематично изображено ПП, периметр которого — периметр трехстворчатого клапана и его структуры: устье нижней полой вены (НПВ), устье верхней полой вены (ВПВ), устье коронарного синуса (КС), евстахиева складка и евстахиев клапан, терминальная криста (ТК). Показано положение HALO-катетера (Н1—Н6), стимулирующей пары ( ). направление распространения волны деполяризации (указано стрелками). А — активация структур ПП при наличии полного блока проведения в нижнем перешейке; Б — активация структур ПП при сохраненном медленном проведении через нижний истмус (зигзагообразная линия).
При неполном блоке проведения в НП, т.е. при прорыве стимуляционного импульса через нижний истмус, происходит слияние фронтов деполяризации в области латеральных отделов ПП (рис. 5, Б).
Решающим фактором в данном методе является регистрация множественных отведений из области латеральных границ ТП, при этом обычно используется многополюсной катетер HALO с коротким межэлектродным расстоянием (около 2 мм), который выставляется по периметру трехстворчатого клапана. Однако непрямой (косвенный) метод верификации блока проведения в НП не позволяет исключить неполного блока проведения, так как не предусматривает возможности его оценки непосредственно в зоне НП [1, 34]. Данный факт может служить объяснением причины рецидивирования типичного ТП в послеоперационном периоде.
В 1998 г. D. Shah и соавт. предложили методику верификации блока перешейка на основании прямых (непосредственных) критериев, регистрируемых собственно из зоны радиочастотного воздействия [1, 34]. Методика позволила снизить частоту рецидивирования ТП до 5% за период годичного наблюдения [1, 34].
Опыт использования разработанной и применяемой в нашей клинике методики, сочетающей в себе верификацию двунаправленной блокады проведения в НП на основании как прямых, так и непрямых критериев, позволяет нам утверждать, что после первичной процедуры РЧА при типичном ТП эффективность лечения составляет 87% за 8-летний период клинического наблюдения за этими пациентами. После повторных операций у пациентов с рецидивом типичного ТП эффективность этого метода может достигать 100%. Что касается антиаритмической терапии, то ни один из известных нам препаратов не обладает сопоставимой по эффективности с РЧА антиаритмической активностью в отношении типичного ТП на протяжении столь длительного периода наблюдения [1, 29, 35].
РЧА при типичном ТП характеризуется крайне низким риском развития операционных осложнений [1, 3, 10, 33, 34]. Описаны единичные случаи окклюзии правой коронарной артерии при радиочастотном воздействии в НП, при которых потребовались экстренные интервенционные вмешательства [10].
Заключение
Трепетание предсердий представляет собой аритмию, в основе которой в большинстве случаев лежит структурная патология сердца, обусловливающая изменение электрофизиологических характеристик миокарда предсердий и создание условий для возникновения re-entry в правом предсердии.
Под типичностью трепетания предсердий подразумевается истмус-зависимость, а именно, определяющая роль нижнего (каво-трикуспидального) перешейка в поддержании и прерывании цикла re-entry при ТП.
Доказанная высокая эффективность и безопасность радиочастотной катетерной абляции делает этот метод определяющим при лечении больных с типичным трепетанием предсердий.



