Типичное трепетание предсердий (ТП) по распространенности занимает второе место среди тахиаритмий после фибрилляции предсердий (ФП). Для восстановления синусового ритма (СР) при ТП применяют антиаритмические препараты (ААП), электроимпульсную терапию, электрокардиостимуляцию и катетерную аблацию [1, 2]. Устранение ТП с помощью фармакологических препаратов — более сложная задача, чем лечение ФП, и связано это с тем, что ФП вызывается несколькими волнами microre-entry, a для ТП характерно macrore-entry [3]. При ТП эффективность применения в ранние сроки возникновения аритмии ААП внутривенно не превышает 20—30%, а при длительных эпизодах — неэффективна. Оптимальным является применение чреспищеводной электрокардиостимуляции (ЧП-ЭКС), эффективность которой достигает 75—95%. Электрическую стимуляцию предсердий осуществляют с частотой, превышающей частоту тахикардии, с целью проникновения волны стимуляции в круг rе-еntry и создания условий для его прерывания [4, 5].
В основе патофизиологии ТП лежит правильная предсердная цепь циркуляции возбуждения. Эта цепь включает электрический импульс возбуждения и готовый к проведению участок миокарда предсердия.
ААП IА класса уменьшают скорость проведения в цепи re-entry и в целом сокращают период возбудимости. ААП IС класса замедляют проведение импульса и, таким образом, увеличивают длину цикла тахикардии. И напротив, ААП III класса (амиодарон) увеличивают период рефрактерности и могут купировать ТП, так как импульс наталкивается на рефрактерную ткань. Электрическая стимуляция предсердий может купировать ТП при создании функционального блока в одном из направлений круга rе-еntry. Кроме того, эффективность электростимуляции может быть увеличена при использовании антиаритмической терапии (ААТ), которая облегчает создание зоны абсолютной рефрактерности [3, 5].
Цель работы — оценить эффективность электростимуляционной кардиоверсии при типичном ТП неклапанного генеза в зависимости от длины кардиоцикла.
Материал и методы
 С целью восстановления СР при типичном ТП неклапанного генеза проведено 225 ЧП-ЭКС у 208 (92,4%) мужчин и 17 (7,6%) женщин в возрасте 34—80 лет (в среднем 59,3±0,6 года).
С целью восстановления СР при типичном ТП неклапанного генеза проведено 225 ЧП-ЭКС у 208 (92,4%) мужчин и 17 (7,6%) женщин в возрасте 34—80 лет (в среднем 59,3±0,6 года).
ТП выявлено у 161 (71,6%) больных на фоне ИБС, в том числе постинфарктного кардиосклероза — у 10 (4,4%), стабильной стенокардии — у 17 (7,6%) и у 64 (28,4%) пациентов на фоне постмиокардитического кардиосклероза. Сопутствующую артериальную гипертензию наблюдали у 157 (69,8%) больных, в том числе с острыми нарушениями мозгового кровообращения и транзиторными ишемическими атаками в анамнезе — у 2 (0,9%). Кардиохирургические вмешательства перенесли 11 (4,9%) больных (аортокоронарное шунтирование — 3, стентирование коронарных артерий — 8). Хроническую сердечную недостаточность (СН) I стадии, по классификации Н.Д. Стражеско и В.Х. Василенко, диагностировали у 183 (81,3%) больных, IIА стадии — у 19 (8,4%).
У 35 (15,6%) обследованных не выявлено признаков СН, поскольку аритмия не ограничивала выполнение физических нагрузок.
Выявлена сопутствующая патология: сахарный диабет — у 9 (4%), различные заболевания щитовидной железы без нарушения ее функции — у 12 (5,3%) и хронические заболевания легких — у 39 (17,3%).
У 28 (12,4%) пациентов пароксизм аритмии зарегистрирован впервые. При проведении обследования на фоне СР выявлены нарушения проводящей системы сердца (ПСС): синдром слабости синусного узла (СССУ) — у 3 (1,3%) больных, дисфункция синусного узла (СУ) — у 14 (6,2%), нарушение атриовентрикулярного (АВ-) проведения органического генеза — у 7 (3,1%) и функционального — у 14 (6,2%). Анамнез аритмии составлял от 10 сут до 16 лет (в среднем 7,1 года), продолжительность существующего эпизода — от 1 до 343 сут (в среднем 25,3 сут).
В исследование не включали больных ревматизмом, врожденными и приобретенными клапанными пороками, острым миокардитом, острым коронарным синдромом, СН выше IIА стадии, тяжелыми нарушениями функции печени и почек, а также пациентов с зафиксированной в анамнезе ФП или получающих какую-либо ААТ.
Перед восстановлением ритма всем больным проводили лечение основного заболевания, коррекцию артериального давления, компенсацию СН, а также антикоагулянтную терапию в соответствии с существующими современными рекомендациями. У всех больных попытки медикаментозной кардиоверсии были неэффективными.
Перед плановой кардиоверсией всем больным выполняли трансторакальную эхокардиографию по общепринятому протоколу на ультразвуковой системе Sonoline-Omnia («Siemens», Германия) для оценки структурно-функционального состояния миокарда предсердий и желудочков, а также исключения клапанных пороков сердца.
ЧП-ЭКС осуществляли с помощью временного электрокардиостимулятора Cordelectro-04 (Литва), диагностическими электродами ПЭДМ-6 и ПЭДМ-9 (Украина); регистрацию электрокардиограммы (ЭКГ) проводили на электрокардиографе Mingograf-82 («Siemens-Elema», Швеция). Положение электрода определяли по монополярной чреспищеводной электрограмме (ЧПЭГ). Оптимальным считали такое положение, когда от дистального полюса электрода регистрировали двухфазные зубцы А максимальной амплитуды. Эффективность навязывания ритма на предсердия контролировали по ЭКГ. Электростимуляцию начинали с частоты, на 25—35% превышающей кардиоцикл ТП, и в последующем ее повышали до восстановления СР или перевода в стойкую ФП. Сила тока составляла 15—30 мА, продолжительность импульса — 10 мс, продолжительность залпа — 1—5 с, межполюсные интервалы 10—20 мм. При стабильном ритмовождении предсердий и сохранении ТП электростимуляцию повторяли через несколько секунд в том же режиме, а в отсутствие эффекта повышали частоту электростимуляции. Количество повторных залпов электростимуляции не ограничивали. При сохранении ФП в течение 15—20 мин внутривенно вводили прокаинамид в дозах до 2000 мг.
При первой процедуре не удалось восстановить СР у 15 (6,7%) пациентов. Из них у 3 (1,3%) человек с постстимуляционной ФП ритм восстановлен медикаментозно, а у 11 (4,9%) — ФП в течение суток трансформировалась в ТП и ритм восстановлен повторной ЧП-ЭКС. У 1 (0,4%) пациента СР восстановить не удалось, и он был выписан с постоянной формой ФП в связи с тяжестью основного заболевания и неэффективностью ААТ.
Статистическую обработку полученных данных проводили с помощью пакетов прикладных программ Microsoft Excel 2003. Качественные показатели представлены в виде абсолютных и относительных частот (n, %). Различия количественных показателей между группами оценивали с помощью t-критерия Стьюдента. Данные представлены в виде среднего значения и ошибки (M±m). Различия считали статистически значимыми при p<0,05.
Результаты и обсуждение
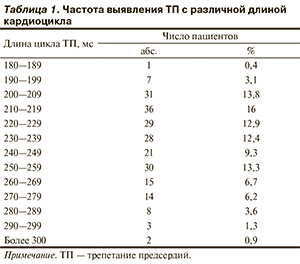
По данным нашего исследования, наиболее часто встречается ТП с длиной цикла 200—259 мс (соответствует 230—300 уд/мин) (табл. 1). Для оценки эффективности ЧП-ЭКС при восстановлении СР в зависимости от частотных характеристик предсердий все больные были разделены на 3 группы: у пациентов 1-й группы (n=75) длина кардиоцикла была менее 220 мс, 2-й группы (n=108) — 220—259 мс и 3-й группы (n=42) — 260 мс и более.
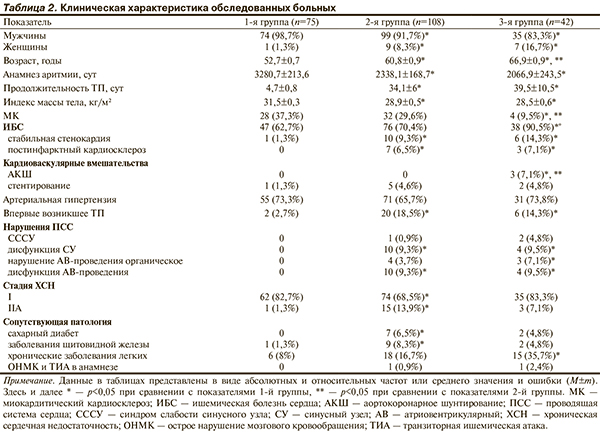
Большинство обследованных составили мужчины, во 2-й и 3-й группах женщин было больше, чем в 1-й группе (табл. 2). Выявлена достоверная прямая зависимость между длиной цикла тахикардии и возрастом пациента, прогрессированием ИБС, нарушениями ПСС, хроническими заболеваниями легких. У пациентов 1-й группы отмечали наиболее продолжительный анамнез аритмии, достоверно реже фиксировали впервые возникшие пароксизмы, а существующий эпизод был непродолжительным (менее 7 сут), отсутствовали нарушения ПСС, СН, сопутствующие патологии. Однако в 1-й группе преобладали пациенты с ожирением. Клиническая характеристика больных 2-й и 3-й групп была сопоставима, за исключением достоверных различий по возрасту и частоте выявления ИБС. Следует отметить, что у пациентов 2-й группы достоверно чаще регистрировали СН IIА по сравнению с таковым показателем у больных 1-й группы.
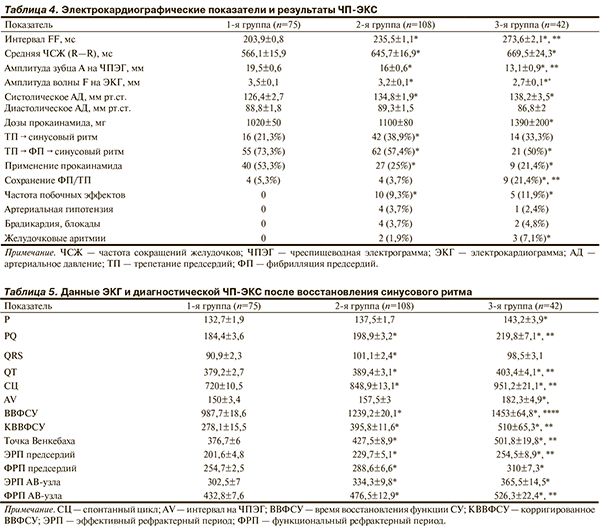
Отмечено достоверное снижение эффективности ЧП-ЭКС (как первичных, так и в целом) у больных 3-й группы, что обусловлено возрастным электрофизиологическим ремоделированием с формированием устойчивости петли rе-еntry на фоне фиброзных изменений миокарда предсердий и ПСС (табл. 3). Влияние возраста пациента на электрофизиологические характеристики миокарда и ПСС отмечено также и в работах других авторов [6]. Этот факт подтверждают и данные нашего исследования: у пациентов 3-й группы отмечены более низкие амплитуды волны F на ЭКГ и зубца А на ЧПЭГ, а также достоверно большие дозы, применяемого во время процедуры прокаинамида (табл. 4). Несмотря на это полученные данные свидетельствуют о высокой эффективности применения метода кардиоверсии при типичном ТП, позволяющего восстановить СР более чем у 92% пациентов, независимо от частоты предсердного ритма у больных с длительными эпизодами аритмии (более 30 сут), причем без предварительной антиаритмической подготовки.
Снижение амплитуд волны F на ЭКГ и зубца А на ЧПЭГ обусловлено процессами электрофизиологического ремоделирования на фоне возрастных фиброзных и склеротических изменений миокарда, проявляющихся снижением электрической активности кардиомиоцитов предсердий и ухудшением проводимости по проводящей системе предсердий [7, 8].
Выявленная прямая зависимость между длиной цикла ТП и дозами применяемого прокаинамида также связана с устойчивостью субстрата аритмии. Следует обратить особое внимание на довольно высокую частоту применения прокаинамида (53,3%), а также достоверно более низкие эффективные дозы и полное отсутствие побочных эффектов, что, безусловно, обусловлено малой продолжительностью пароксизма, более молодым возрастом пациентов и отсутствием органической патологии сердца.
 Жизнеугрожающих состояний при проведении электростимуляций не возникало. Реакции и побочные эффекты, такие как значимые брадиаритмии, блокады и артериальная гипотензия, а также желудочковые аритмии (частая желудочковая экстрасистолия по типу бигеминии, парная, пробежки нестойкой желудочковой тахикардии) достоверно чаще возникали у больных 3-й группы.
Жизнеугрожающих состояний при проведении электростимуляций не возникало. Реакции и побочные эффекты, такие как значимые брадиаритмии, блокады и артериальная гипотензия, а также желудочковые аритмии (частая желудочковая экстрасистолия по типу бигеминии, парная, пробежки нестойкой желудочковой тахикардии) достоверно чаще возникали у больных 3-й группы.
Многочисленные исследования показали возрастное снижение вариабельности ритма сердца, предрасполагающее к появлению опасных для жизни аритмий [5]. Кроме того, основное действие ААП направлено на снижение возбудимости и замедление проведения, которое и так нарушено у больных старших возрастных групп, чем и объясняется повышение частоты проаритмогенных эффектов.
После восстановления СР всем больным проведена диагностическая ЧП-ЭКС для выявления нарушений в ПСС и определения тактики дальнейшей ААТ (табл. 5).
В зависимости от длины цикла ТП, у пациентов всех групп отмечается достоверная динамика всех ЭКГ и электрофизиологических показателей, отражающая снижение функциональных возможностей СУ и АВ соединения, увеличение рефрактерных периодов предсердий и АВ узла. Максимальные значения этих показателей зафиксированы у пациентов 3-й группы. Подобную зависимость этих показателей от возраста отмечают и другие авторы [8].
В исследованиях доказано, что потенциалы покоя предсердий у лиц пожилого возраста значительно снижены по сравнению с потенциалами покоя в нормально сокращающихся предсердиях. Гипополяризация предполагает уменьшение скорости проведения, так как снижаются амплитуда и скорость нарастания положительной части потенциала действия. Более того, в частично деполяризованных клетках увеличивается рефрактерный период и задерживается процесс реполяризации в связи со значительной задержкой движения быстрых и медленных ионных токов, направленных внутрь клетки. Эта постреполяризационная рефрактерность приводит к пространственной дисперсии рефрактерных периодов (неоднородности эффективного рефрактерного периода между клетками предсердий). Как редуцированная скорость проведения, так и увеличенная дисперсия рефрактерности предрасполагают к re-entry [9, 10].
Предполагается, что фиброз также играет важную роль в возникновении электрофизиологической неоднородности миокарда предсердий. С возрастом в предсердиях разрастаются коллагеновые волокна, что приводит к прогрессирующей потере связей между параллельно ориентированными предсердными волокнами. Фиброз может вызывать не только замедленное проведение, но и дисперсию рефрактерности предсердий, которая увеличивается с возрастом [11—13]. Следовательно, наблюдают неоднородность восстановления возбудимости или функциональной рефрактерности предсердий в целом. Анизотропное проведение всегда неоднородно, но с возрастом становится более выраженным. На электрофизиологические свойства предсердий значительно влияет автономная нервная система — симпатическая и парасимпатическая. Эти влияния на различные участки предсердий также неоднородны [2]. Следовательно, предсердия имеют анатомическую, электрофизиологическую и нейрогенную неоднородность, усиливающуюся с возрастом, что в свою очередь может способствовать возникновению аритмий.
Повышенный симпатический или парасимпатический тонус также играет важную роль в возникновении аритмии. В экспериментах на животных показано, что парасимпатическая стимуляция укорачивает рефрактерные периоды предсердий, способствуя возникновению и поддержанию ФП/ТП, а вагусная денервация предсердий предотвращает запуск аритмии. Так, у большинства больных с изолированным ТП не выявляют органической кардиальной патологии, а вагусное влияние носит доминирующий характер.
Таким образом, полученные результаты свидетельствуют о существенном достоверном снижении функции автоматизма, проводимости и увеличении рефрактерности миокарда предсердий у больных старших возрастных категорий. Кроме того, выявленная возрастная динамика интервала QT может предрасполагать к возникновению у таких больных проаритмогенных эффектов ААП.
Следовательно, у больных с длиной цикла ТП до 220 мс, по-видимому, будет более целесообразным проведение предварительной антиаритмической подготовки. В то же время у больных с длиной цикла больше 260 мс такая подготовка будет только повышать риск возникновения побочных эффектов и осложнений при проведении электростимуляции, поэтому ААП будет логично применять после стимуляционной трансформации ТП в ФП, используя при этом препараты с коротким периодом полувыведения (ААП I класса по классификации Vaughan Williams).
По данным литературы, для купирования пароксизма применение ААП имеет низкую эффективность, а проведение электрокардиостимуляции — высокую [1, 4].
В нашем исследовании при длительных (более 30 сут) пароксизмах медикаментозная кардиоверсия была неэффективна, в том числе внутривенное применение прокаинамида. Однако его дозированное использование после стимуляционно спровоцированной ФП является более эффективным и безопасным, чем предварительная антиаритмическая подготовка препаратами с продолжительным периодом полувыведения. Следует также отметить, что при возрастном электрофизиологическом ремоделировании миокарда значительно возрастает риск возникновения проаритмогенных побочных эффектов ААП, и тем более их комбинаций.
Таким образом, ЧПЭКС является эффективным методом кардиоверсии при длительных эпизодах изолированной аритмии, независимо от длины цикла ТП без предварительной ААТ. В то же время проведение электростимуляций с учетом частотных характеристик предсердий поможет не только повысить результаты метода, но и избежать осложнений процедуры, а также побочного действия ААП.
Выводы
Наиболее часто регистрируют трепетание предсердий с длиной кардиоцикла 200—259 мс.
Чреспищеводная электростимуляция является эффективным методом кардиоверсии, позволяющим восстановить синусовый ритм у 92—100% больных с длительным (более 30 сут) эпизодом типичного трепетания предсердий независимо от длины кардиоцикла, без предварительной антиаритмической терапии.
Выявлена достоверная прямая зависимость между длиной цикла трепетания предсердий и возрастом пациента, прогрессированием ИБС, нарушениями проводящей системы сердца, хроническими заболеваниями легких и, вследствие этого, достоверным снижением эффективности электростимуляционной кардиоверсии.
При длине цикла тахикардии менее 220 мс достоверно чаще применяли прокаинамид, в связи с чем у таких больных целесообразно проведение предварительной антиаритмической подготовки перед электрокардиостимуляцией. В то же время у пациентов с длиной кардиоцикла более 260 мс такая тактика повышает риск развития проаритмий, поэтому применение антиритмических препаратов будет эффективнее и безопаснее после электростимуляционной трансформации трепетания в фибрилляцию предсердий, используя при этом препараты с коротким периодом полувыведения (I класс по классификации Vaughan Williams).