Фибрилляция предсердий (ФП) и трепетание предсердий (ТП) — самые частые предсердные тахикардии. Так, распространенность ФП составляет 1—2% популяции, в то время как это число для ТП составляет 0,3%. Распространенность аритмий увеличивается с возрастом и составляет 5—15% для ФП и 587/100 000 для ТП среди больных старше 80 лет [1, 2]. Возникновение и распространенность признаков тромбообразования и выраженной дисфункции ушка левого предсердия (УЛП) у больных с ФП интенсивно исследуется, однако данная проблема у больных с ТП недостаточно изучена. Типичное ТП представляет собой правильный, регулярный, скоординированный предсердный ритм, обусловленный истмус-зависимым механизмом макро-re-entry и превышающий частотной характеристикой предсердную тахикардию (более 200—250 уд/мин) [3]. При этом ФП имеет совершенно иные характеристики: нерегулярный ритм с частотой активации предсердий более 300 в минуту. В основе данной аритмии лежат фокальная триггерная активность, микро-re-entry и хаотичное распространение независимых друг от друга элементарных волн возбуждения с локализацией источников аритмии прежде всего в мышечных муфтах легочных вен и левом предсердии [1]. Различия в электрофизиологических механизмах аритмий ведут и к разным гемодинамическим следствиям. Так, при ФП потеря координированных сокращений предсердий, сокращения предсердий при закрытых предсердно-желудочковых клапанах, высокая частота и нерегулярность сокращений сердца, снижение миокардиального кровотока приводят к развитию кардиомиопатии предсердий и желудочков. Только потеря координированной работы предсердий приводит к снижению сердечного выброса на 5—15% [1]. Основным же фактором, который влияет на гемодинамическую нестабильность при ТП, является высокая частота предсердных сокращений с развитием систолической дисфункции и сердечной недостаточности [1, 3].
Целью данной работы были определение частоты признаков тромбообразования у больных с типичным ТП и выявление клинических и эхокардиографических факторов, которые позволили бы прогнозировать образование тромбов у больных с ТП.

Материал и методы
В исследование включили 406 пациентов: 299 с персистирующей и постоянной формой ФП и 107 — с персистирующей формой ТП. Всем больным при поступлении в стационар проводили общее клиническое исследование, которое, кроме всего прочего, предполагало анализ международного нормализованного отношения (МНО). Всем больным проводили трансторакальную и чреспищеводную эхокардиографию на ультразвуковых аппаратах Toshiba applio XG и Phillips HD 11 XE с использованием мультиплановых чреспищеводных датчиков 5 МГц и 2—7 МГц. Во время исследования выполняли двухмерное сканирование УЛП с регистрацией в двух взаимно перпендикулярных плоскостях: поперечной и продольной. Оценивали среднюю скорость изгнания из УЛП (ССУЛП), степень феномена спонтанного эхоконтрастирования (ФСК) и наличие тромбов в УЛП. Для измерения скорости опорожнения УЛП использовали импульсно-волновую допплерографию с размещением контрольного объема в устье УЛП. Тромбом считали умеренно- или гиперэхогенное образование различной плотности, формы, размеров и подвижности, которое определялось в полости УЛП больше чем в одной проекции на протяжении всего сердечного цикла. Конечный диастолический (КДО) и конечный систолический (КСО) объемы левого желудочка (ЛЖ) рассчитывали из двух- и четырехкамерной верхушечной позиции при трансторакальной эхокардиографии по формуле Симпсона. Фракцию выброса (ФВ) ЛЖ рассчитывали по общепринятой формуле. Систолическую функцию ЛЖ дополнительно оценивали с помощью двух показателей тканевой допплерографии в импульсном режиме: систолической волны Sе — на латеральном сегменте кольца митрального клапана и St (см/с) на латеральном сегменте трехстворчатого клапана. Объемные показатели левого и правого предсердий также рассчитывали из верхушечного доступа по формуле Симпсона. Для оценки диастолической функции миокарда использовали импульсную допплерографию: измеряли показатели пиковой скорости ранней диастолической волны трансмитрального тока Е (см/с), длительность периода изоволюмической релаксации, времени замедления волны Е. Путем тканевой допплерографии в импульсном режиме проводили измерение ранней диастолической волны Еm (см/с) на латеральном сегменте кольца митрального клапана и комбинированного показателя Е/Еm. Для оценки функции клапанного аппарата использовали двухмерный режим, непрерывно-волновую и цветовую допплерографию.
Средний возраст больных составил 59,3 года, ССУЛП 37,02 см/с, средняя ФВ ЛЖ 52%, а средняя оценка по шкале CHA2DS2-VASC 1,86 балла. Основным диагнозом были ишемическая болезнь сердца (89%), миокардиофиброз (8%), метаболическая кардиомиопатия (2%), гипертрофическая кардиомиопатия (0,7%). Артериальная гипертензия регистрировалась в 84% случаев. Первый эпизод аритмии определялся в 37,8% случаев. На момент исследования средний уровень МНО был ниже рекомендованного, а уровень ≥2 был достигнут только у 16,3% больных. Среди больных с ТП только 4,1% на момент исследования принимали новые пероральные антикоагулянты, в то время как остальные больные принимали антагонисты витамина К, но уровень МНО у них был значительно меньше 2. Уровень МНО <2 не ассоциировался с наличием признаков тромбообразования: феноменом спонтанного эхоконтрастирования 3—4+ (χ2 Пирсона 0,6; р=0,43) и тромбом в УЛП (χ2 Пирсона 0,3; р=0,57). В то же время признаки тромбообразования ассоциировались со средней скоростью изгнания из УЛП <25 см/с, с уровнем достоверности р<0,0001 как для ФСК 3—4+, так и для тромба в УЛП.
Статистическую обработку данных проводили с помощью стандартного пакета программ Excel и Statistica 8.0. Для всех выборок оценивали соответствия эмпирических распределений нормальному закону (распределение Гаусса) по критериям Колмогорова—Смирнова. Для количественных показателей первичная статистическая обработка включала расчет среднеарифметического значения, ошибки среднеарифметического значения, среднеквадратичного отклонения. Достоверность различий оценивали по уровню значимости p. Взаимосвязь между количественными переменными рассчитывали при помощи парного коэффициента корреляции Пирсона, а для ранговых переменных использовали ранговый коэффициент корреляции Спирмена. Для номинальных переменных взаимосвязь рассчитывали по таблицам сопряженности при помощи критерия χ2 Пирсона.
Результаты
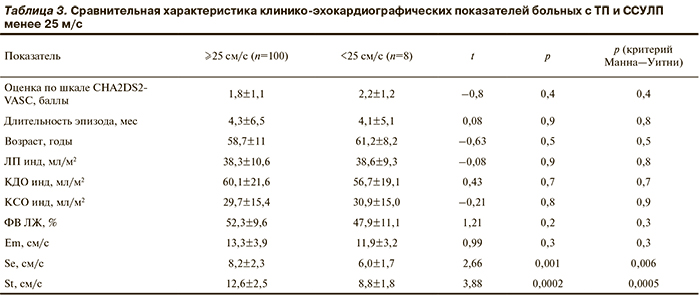
Группы больных с ФП и ТП не различались по длительности эпизода аритмии, суммарной оценке по шкале CHA2DS2-VASC, возрасту, выраженности митральной регургитации, признакам систолической и диастолической функции ЛЖ и систолической функции правого желудочка (табл. 1). Однако больные ТП достоверно отличались более высокой (в 1,7 раза) ССУЛП и меньшим объемом левого (на 11%) и правого предсердий и более высокой частотой желудочковых сокращений (на 10,7%). Следует также отметить, что среди больных с ТП у 27% имелась ФВ ЛЖ <45%, а среди больных с ФП — у 19% (табл.2).
Затем была проанализирована частота выявления ФСК разной степени у обследованных больных. Как представлено на рис. 1, у больных с ТП чаще обнаруживался ФСК 0—1+, в то время как у пациентов с ФП суммарно более частой находкой было обнаружение ФСК 2, 3, 4+. Причем выраженный ФСК в группе больных ФП был обнаружен в 9,6%, а у больных с ТП только в 1,8% случаев, т.е. более чем в 5 раз чаще. Корреляция между наличием умеренного и выраженного ФСК и ФП была достоверной (р<0,0001, ранговый показатель Спирмена –0,35).
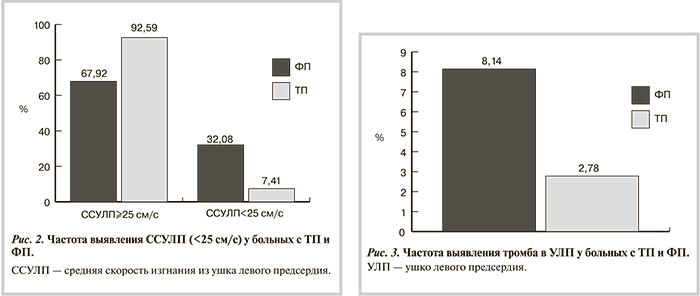
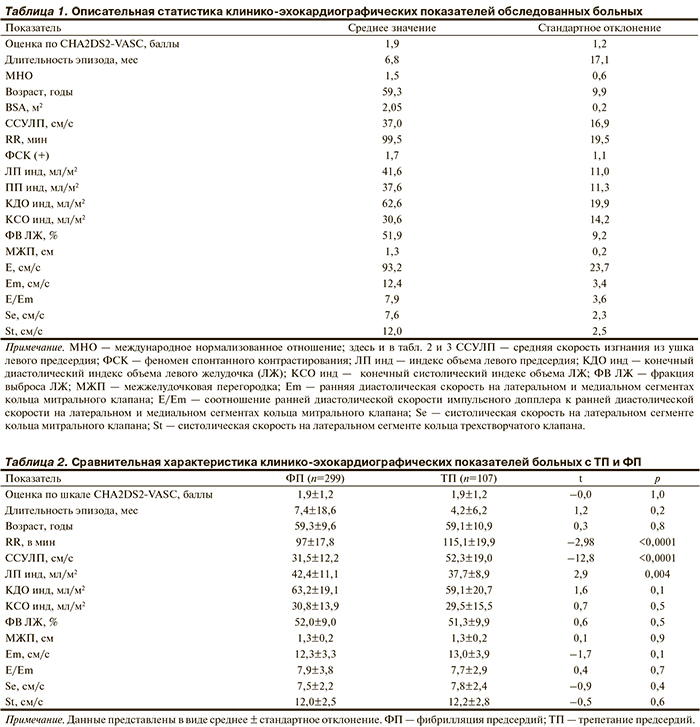
У больных с ТП также гораздо реже (р<0,0001) обнаруживаются признаки дисфункции УЛП (р<0,0001; рис. 2) и тромб в УЛП (р<0,038; рис. 3).
ССУЛП достоверно коррелировала с обнаружением тромба в УЛП у больных с ТП (χ2 Пирсона 15,6; р<0,0001). Для выявления основных факторов, которые лежали в основе дисфункции УЛП у больных с ТП, пациенты были разделены на 2 группы: с ССУЛП ≥25 и с ССУЛП <25 см/с. Результаты, представленные в табл. 3, демонстрируют, что эти группы больных различались по показателям систолической функции ЛЖ: Se (см/с) и St (см/с). Таким образом, было выявлено, что группа ТП со сниженной ССУЛП отличалась признаками систолической дисфункции, которая также согласно данным литературы является одним из определяющих механизмов развития дисфункции УЛП у больных с ФП [4].
В дальнейшем было обнаружено, что у больных с ТП достоверно чаще образуются тромбы в полости ЛЖ (у первичных больных без инфаркта миокарда в анамнезе, средний возраст 52,7 года). Это может объясняться более частым развитием кардиомиопатии вследствие длительной тахикардии у данной группы больных. Таким образом, тромбы в полостях сердца были обнаружены у 5,9% больных с ТП и у 8,5% больных с ФП.
Затем были рассчитаны основные корреляции признаков тромбообразования у больных с ТП и систолической дисфункцией ЛЖ, что представлено в табл. 3.
Согласно представленным в табл. 3 данным, у больных с типичным ТП ФВ ЛЖ <35% и показатель Se <6 см/с с равной степенью достоверности прогнозируют обнаружение тромбов в ЛЖ. Однако ФВ ЛЖ <35% была наиболее взаимосвязана с обнаружением ФСК 4+, в то же время систолическая скорость на латеральном сегменте кольца митрального клапана <6 см/с наиболее достоверно прогнозировала ССУЛП и обнаружение тромба в УЛП. Это может быть связано с тем, что показатель Se измеряется вблизи УЛП.
Обсуждение
Данные о тромбообразовании у больных с ТП ограничены. В частности, в современных рекомендациях по ведению больных с ФП отмечено, что риск развития инсульта у больных с ТП изучался ретроспективно с участием большого числа пожилых больных и подобен риску у больных с ФП [1]. Мы не нашли данных литературы о частоте обнаружения тромбов в ЛЖ у больных с ТП. Касательно признаков тромбообразования в предсердиях у больных с ТП полученные нами результаты совпадают с данными литературы о частоте тромбообразования в предсердиях у больных с ТП. В крупной работе по данной тематике, в которой обследованы 202 больных с ТП, H. Schmidt и соавт. обнаружили тромбы в УЛП только у 2 (1%) больных, признаки тромбообразования выявлены у 15 (7,4%) больных. Независимыми предикторами выраженного ФСК в левом предсердии у больных с ТП оказались низкая систолическая функция ЛЖ <40%, сахарный диабет и артериальная гипертензия [5]. В другом исследовании, которое включало только 50 пациентов с ТП, тромбы были обнаружены в 2% наблюдений против 24% у больных с ФП [6]. В небольшом исследовании W. Irani и соавт. среди 47 больных с ТП тромбы в левом предсердии были обнаружены у 11% [7]. В еще одном небольшом исследовании с участием 28 больных с ТП выраженный ФСК и снижение скоростных показателей в УЛП были обнаружены в 14% случаев, в то время как при ФП — в 28% [8]. Таким образом, по результатам различных исследований, частота обнаружения тромба в предсердиях у больных с ТП составляет от 1 до 11% [7].
Полученные в данной работе результаты продемонстрировали более частое обнаружение тромба и сладжа в УЛП у больных с ФП. Однако частота выявления признаков тромбоза у больных с ТП и ФП различалась недостоверно за счет более частого обнаружения тромбов в ЛЖ у больных с ТП. Можно предполагать, что более частое обнаружение тромбов в ЛЖ у больных с ТП связано с более частым развитием кардиомиопатии, обусловленной длительной тахисистолией [9].
Выводы
По сравнению с больными с фибрилляцией предсердий у больных с трепетанием предсердий реже развиваются признаки выраженной дисфункции ушка левого предсердия и выраженный феномен спонтанного эхоконтрастирования, однако достоверно чаще обнаруживаются тромбы в полости левого желудочка.
Систолическая дисфункция левого желудочка является основным фактором, который приводит к появлению признаков тромбообразования у больных с трепетанием предсердий.
Больные с трепетанием предсердий и систолической дисфункцией левого желудочка (систолическая скорость на латеральном сегменте кольца митрального клапана <6 см/с, фракция выброса <35%) относятся к категории лиц с высоким риском развития эмболических осложнений.



