АКТУАЛЬНОСТЬ
По данным Международной федерации диабета (International Diabetics Federation, IDF), в 2021 г. около 537 млн человек в мире страдали сахарным диабетом (СД), что свидетельствует о наличии этой патологии у каждого десятого взрослого человека. К 2045 г. ожидается увеличение количества таких пациентов до 783 млн [1].
В российском Федеральном регистре пациентов с CД на 11 ноября 2023 г. было зарегистрировано 5 038 116 случаев заболевания, из которых 92,3% (n=4 650 211) приходилось на долю СД 2-го типа. Важно отметить, что в течение последнего года в нашей стране было выявлено 212 392 новых случаев СД 2-го типа [2]. Ситуация с высокой встречаемостью этой патологии осложняется тем, что СД 2-го типа рассматривается как одна из ведущих причин смертности взрослого населения. К примеру, в 2021 г. в результате СД умерло около 6,7 млн человек [3].
Результаты отечественного крупномасштабного эпидемиологического кросс-секционного исследования NATION также свидетельствуют не только о высокой встречаемости СД 2-го типа (около 5,9 млн человек) в возрастной когорте 20–79 лет, но и о достаточной распространенности предиабета (19,3%, или около 20,7 млн случаев) [4].
В российском одномоментном популяционном исследовании с участием 1174 человек (в том числе 424 мужчин) гипергликемия натощак была обнаружена у 22% обследованных – у каждого четвертого мужчины и каждой пятой женщины (р=0,045); для предиабета аналогичные показатели гендерной распространенности составили 17,2 и 11,9% соответственно (р=0,013) [5].
В соответствии с информацией, представленной на сайте IDF, количество человек в возрасте от 20 до 79 лет с нарушенной толерантностью к глюкозе достигает 541 млн, и все они рассматриваются в качестве группы риска развития СД 2-го типа в ближайшие годы [3]. По прогнозам, к 2040 г. практически 8% населения планеты будут страдать предиабетом [6].
Таким образом, раннее выявление нарушений углеводного обмена необходимо для предупреждения развития СД и его осложнений, а также разработки соответствующих мероприятий по замедлению прогрессирования предиабета.
КРИТЕРИИ ДИАГНОСТИКИ ПРЕДИАБЕТА
Предиабет представляет собой раннее расстройство углеводного обмена – нарушение гликемии натощак и толерантности к глюкозе, приводящее к снижению утилизации глюкозы в тканях организма. Как правило, эти изменения бессимптомны, сопровождаются инсулинорезистентностью, нарушением функции β-клеток поджелудочной железы и диагностируются с помощью глюкозо-толерантного теста. Иными словами, предиабет – это раннее нарушение углеводного обмена, не соответствующее критериям СД. Критерии его диагностики отражены в таблице [7].
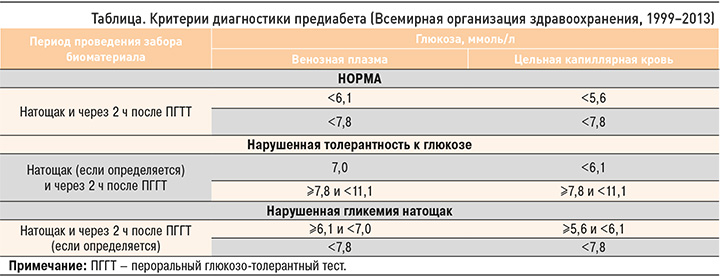
Несмотря на существующие общепринятые критерии, диагностика предиабета представляет собой сложную задачу, поскольку между ведущими мировыми экспертами нет единого мнения о пороговых значениях этого состояния. Так, Всемирной организацией здравоохранения (ВОЗ) и Американской диабетической ассоциацией (American Diabetes Association, ADA) взяты за ориентир разные значения глюкозы для определения нарушения гликемии натощак: 6,1–6,9 ммоль/л (100–125 мг/дл) и 5,6–6,9 ммоль/л (100–125 мг/дл) соответственно.
Международный комитет экспертов (International Expert Committee, IEC) и эксперты ADA предлагают также использовать для ранней диагностики нарушения углеводного обмена уровень гликированного гемоглобина (HbA1c): 6,0–6,4% (42–47 ммоль/ моль) и 5,7–6,4% (39–47 ммоль/моль) соответственно [8, 9].
В России, Великобритании и Канаде на сегодняшний день применяются критериальные значения HbA1с, предложенные ВОЗ и IEC.
Существует еще один важный аспект в обсуждении точности определения предиабета: однократное измерение HbA1c обладает чувствительностью 49% при специфичности 79%, в то время как определение глюкозы натощак – 25 и 94% соответственно [10]. Посредством изолированной оценки HbA1c возможно идентифицировать 14% лиц с нарушенной толерантностью к глюкозе, 9% – с нарушенной гликемией натощак и 33% – с обоими отклонениями от нормы [11]. Кроме того, при использовании HbA1c для диагностики предиабета следует учитывать вероятность наличия у пациента генетически обусловленных гемоглобинопатий, талассемии и дефицита железа. Это говорит о необходимости проявлять настороженность и подтверждать диагноз предиабета с помощью дополнительного измерения уровня глюкозы в крови перед началом лечения.
ADA рекомендует ориентироваться на более низкий порог гликемии, чем ВОЗ, для определения нарушения гликемии натощак. В теории сниженный порог уровня глюкозы мог бы обеспечить более раннее выявление нарушений метаболического статуса и широкое окно для последующей профилактики их развития, однако на практике более низкие ее показатели не отражают с большей точностью реальный риск развития СД и не дают существенных преимуществ в плане профилактики этого заболевания. Метаанализ 16 исследований с участием 76 513 человек, у 8208 из которых за период наблюдения 11,1 (4,9–21,7) лет был диагностирован СД, показал, что все анализируемые критерии предиабета достаточно тесно ассоциировались с диагностированием СД и помогали идентифицировать лиц с высоким риском развития диабета в течение ближайших 5 лет с достаточно хорошей точностью: отношение шансов (95% доверительный интервал) от 3,78 (3,11–4,60) до 8,36 (4,88–14,33). Все переменные в моделях с множественной корректировкой были связаны с риском развития СД, при этом максимально сильная связь прослеживалась для семейного анамнеза диабета (отношение шансов от 1,53 до 1,64) [12].
В когортных исследованиях среди населения в целом предиабет, определявшийся по критериям ВОЗ и ADA, был связан с повышенным риском развития СД, сердечно-сосудистых осложнений и заболеваний почек [13, 14]. Вместе с тем сохраняются противоречивые сообщения о риске повторных жизнеугрожающих событий, связанных с предиабетом, у пациентов с ишемической болезнью сердца (ИБС), что можно объяснить разными подходами к выявлению этого состояния.
Так, в проспективном когортном исследовании (период наблюдения в среднем 3,2 года) с участием 4088 пациентов со стабильной ИБС распространенность предиабета составила 67% при определении в соответствии с критериями ADA и 34% – согласно критериям ВОЗ. Только предиабет по критериям ВОЗ ассоциировался с повышенным риском серьезных неблагоприятных сердечно-сосудистых событий: общая смертность, нефатальный инфаркт миокарда или инсульт (относительный риск (ОР) 1,50; 95% ДИ: 1,10–2,06), в то время как по критериям ADA данная ассоциация была менее выраженной (скорректированный ОР 1,17; 95% ДИ: 0,81–1,68). Оптимальное пороговое значение HbA1c для прогнозирования основных неблагоприятных сердечно-сосудистых событий составило 5,85%. Эти результаты свидетельствуют о том, что влияние предиабета на исходы пациентов со стабильной ИБС зависит от критериев его диагностирования, при этом пороговое значение HbA1c, равное 5,85%, является потенциально эффективным маркером риска [15].
На конгрессе Европейской ассоциации по изучению диабета (EASD) в 2023 г. исследователи из Великобритании представили данные о повышенном уровне смертности при нарушениях углеводного обмена среди женщин в более молодом возрасте, в сравнении с мужчинами, что объясняется поздней диагностикой СД 2-го типа у представительниц женского пола. В связи с этим было предложено пересмотреть критерии СД 2-го типа у женщин в возрасте моложе 50 лет в период пременопаузы, а именно снизить пороговый уровень HbA1с c 48 ммоль/моль (6,5%) до 46 ммоль/моль (6,4%). Такое изменение могло бы способствовать более раннему выявлению нарушений углеводного обмена у этой категории женщин, улучшить качество и ожидаемую продолжительность их жизни [16].
Таким образом, применение более низких порогов гликемии для диагностики предиабета, которые, в частности, предлагают специалисты ADA, позволит выявлять гораздо большее количество пациентов из группы риска с последующим пожизненным индивидуальным наблюдением за ними со стороны системы здравоохранения. Однако такой подход может повлечь за собой дополнительные материальные и временные расходы. В связи с этим огромное значение приобретают общие мероприятия по изменению образа жизни на популяционном уровне как краеугольный камень профилактики предиабета.
ПРЕДИАБЕТ И РИСК РАЗВИТИЯ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ
В настоящее время специалисты единодушны во мнении, что предиабет – это междисциплинарная комплексная проблема, требующая от врачей многих специальностей, особенно врачей-терапевтов и врачей общей практики, внимательного отношения к соответствующим пациентам, так как раннее начало превентивных мер способно замедлить риск развития СД 2-го типа и его осложнений. При этом нарушенный метаболизм глюкозы ассоциирован не только с высокой вероятностью развития СД 2-го типа в течение ближайших 3–6 лет [17], но и вносит определенный вклад в риск возникновения и прогрессирования сердечно-сосудистых заболеваний (ССЗ), инсульта и микрососудистых осложнений. Подобная ассоциация верна как для пациентов, еще не имеющих ССЗ в анамнезе, так и для лиц с наличием кардиоваскулярных патологий [18].
При анализе когорты пациентов, участников рандомизированного клинического исследования CHARM (Candesartan in Heart failure Assessment of Reduction in Mortality and Morbidity), включенных в исследование в США и Канаде, у 18% человек с сердечной недостаточностью и сниженной фракцией выброса левого желудочка (ФВ ЛЖ) и у 16% с сердечной недостаточностью и сохраненной ФВ ЛЖ имелась нормогликемия (HbA1c <6,0%), у 20 и 22% соответственно – предиабет (HbA1c 6,0–6,4%). Частота клинических комбинированных исходов была выше у пациентов с недиагностированным СД (отношение шансов 2,75; 95% ДИ: 1,83–4,11) и предиабетом (отношение шансов 1,18; 95% ДИ: 0,75–1,86) относительно пациентов с нормогликемией [19].
Результаты ретроспективного когортного исследования Sasaki N. et al. подтверждают ключевую роль профилактических мероприятий в снижении риска развития артериальной гипертензии (АГ) и ее осложнений, особенно в период предиабета и на ранних этапах СД. Кроме того, в этой работе была показана более высокая частота развития АГ у лиц старше 65 лет, чем в более молодом возрасте, при любом варианте нарушения метаболизма глюкозы [20].
В данное исследование были включены 2136 лиц среднего возраста (1022 с нормальным уровнем глюкозы натощак / нормальной толерантностью к глюкозе, 418 – с нарушенной гликемией натощак, 466 – с нарушенной толерантностью к глюкозе, 230 – с СД) и 3426 пожилых людей (1762 с нормальным уровнем глюкозы натощак / нормальной толерантностью к глюкозе, 599 – с повышенным уровнем глюкозы, 781 – с нарушенной толерантностью к глюкозе, 284 – с СД). Средний возраст участников исследования составил 66,2 года, индекс массы тела (ИМТ) – 22,7 кг/м2. В течение 59 мес наблюдения у 459 лиц среднего возраста и у 1170 лиц пожилого возраста развилась АГ. В среднем возрасте вероятность развития АГ была выше у лиц с нарушенной гликемией (отношение шансов 1,40; p=0,019), нарушенной толерантностью к глюкозе (отношение шансов 1,49; p=0,004) и СД (отношение шансов 1,55; p=0,013), чем у пациентов с нормальным уровнем глюкозы натощак и отсутствием нарушения толерантности к глюкозе. Ожирение оказалось ассоциированным с развитием АГ у пациентов, имеющих нарушенную гликемию натощак и нормальные гликемические показатели [20].
Во время пандемии COVID-19 пациенты с предиабетом были подвержены более тяжелому течению новой коронавирусной инфекции, имели повышенный риск развития осложнений и менее благоприятный прогноз заболевания, что обусловлено гипергликемией, хроническим воспалением низкой степени активности, нарушением механизмов иммунного ответа и прокоагулянтным состоянием на фоне предиабета.
Таким образом, раннее выявление нарушений углеводного обмена может дать возможность разработать комплекс эффективных немедикаментозных и медикаментозных мероприятий для снижения риска развития и прогрессирования ССЗ.
ФАКТОРЫ РИСКА, АССОЦИИРОВАННЫЕ С ПРЕДИАБЕТОМ («ГРУППА НЕГАТИВНЫХ ПРЕДЗНАМЕНОВАНИЙ»)
СД 2-го типа является мультифакторным гетерогенным заболеванием, основой патогенеза которого служат инсулинорезистентность (ИР) и недостаточная функция β-клеток поджелудочной железы. Гетерогенность СД формируется до его клинической манифестации, хотя это положение пока не нашло отражение в современном определении раннего нарушения метаболизма глюкозы. В то время как изолированная нарушенная толерантность к глюкозе в основном связана с ожирением и ИР, первичным нарушением при изолированной нарушенной гликемии выступает дисфункция β-клеток с изменением секреции инсулина [21]. Нарушенная гликемия и нарушенная толерантность к глюкозе представляют собой разные состояния, имеющие общие «перекрестные» проявления, в связи с чем они включены в понятие предиабета, несмотря на разные клинические особенности и прогноз.
Рассматривают две основные гипотезы формирования ранних стадий нарушений метаболизма глюкозы. Первая фокусируется на дисфункции β-клеток как ключевой аномалии. Наследственная предрасположенность и метаболический стресс провоцируют гиперстимуляцию β-клеток, приводя к вторичной гиперинсулинемии. Базальная гиперинсулинемия способствует развитию ИР посредством нескольких механизмов. Избыток инсулина связан с липогенезом и ожирением, что вызывает ИР. Неадекватный ответ клеток и тканей организма на высокие уровни циркулирующего инсулина также рассматривается как адаптивный ответ, защищающий от гипогликемии. В конечном итоге в этом сценарии β-клетка выходит из строя. Такой ход событий в большей степени связан с нарушенной гликемией, чем с нарушенной толерантностью глюкозы, и типичен преимущественно для лиц молодого возраста без ожирения или без абдоминального ожирения [22].
Другая гипотеза рассматривает гиперинсулинемию как ведущий компонент и рассматривает ее как компенсаторную реакцию в ответ на снижение чувствительности тканей к инсулину. В развитие ИР вносят вклад многочисленные факторы и их взаимодействия, включая чрезмерное калорийное питание и прием пищевых добавок, переизбыток насыщенных жирных кислот, адипокины (адипонектин, резистин, лептин) и гепатокины (фетуин-А), изменение метаболизма желчных кислот, заболевания желудочно-кишечного тракта, кишечную микробиоту и хроническое воспаление, вызванное ожирением.
В результате воздействия этих факторов β-клетки истощаются, снижается секреция инсулина, что способствует развитию и прогрессированию СД 2-го типа. ИР обычно ассоциирована с ожирением и нарушенной толерантностью к глюкозе [22–24].
На фоне предиабета снижается количество β-клеток поджелудочной железы, изменяется функция эндотелия, развивается артериальная жесткость, увеличивается липолиз, снижается уровень инкретина, возрастает продукция глюкозы печенью, нарушается регуляция глюкагона и цитокинов. Новые сведения о роли микробиоты кишечника и его связи с кардиометаболическими расстройствами, включая ожирение, СД, дислипидемию, также рассматриваются в тесной ассоциации с предиабетом. Будущие исследования помогут прояснить хронологию связи между дисбактериозом кишечника и ранними нарушениями обмена глюкозы [25].
Риск развития СД зависит не только от промежуточного статуса гликемии (предиабета), но и множества других показателей (возраста, пола, ИМТ, пищевых привычек, генетических, экологических или этнических характеристик человека), что обусловливает множество предрасполагающих факторов, причин и вариабельность временного периода перехода от предиабета к СД (рис. 1).

В последние годы выделен ряд патологических состояний, при которых достаточна высока вероятность развития ранних нарушений углеводного обмена, что требует более тщательного контроля при их наличии. К ним относятся:
- абдоминальное ожирение (окружность талии более 80 см у женщин и более 94 см у мужчин);
- избыточная масса тела;
- малоподвижный образ жизни;
- неалкогольная жировая болезнь печени;
- синдром поликистозных яичников;
- рождение ребенка массой более 4 кг или менее 2,5 кг;
- гестационный СД;
- гестационная АГ;
- ранняя менопауза (возраст до 40 лет);
- черный акантоз и акне – кожные маркеры предиабета.
Курение, как активное, так и пассивное, связано с хроническим воспалением и способствует переходу от нормогликемии к гипергликемии и развитию ИР за счет снижения поглощения глюкозы периферическими тканями [26]. Регулярное питание без овощей и фруктов (отношение шансов 3,74; 95% ДИ: 1,93–7,66) провоцирует развитие ранних нарушений обмена глюкозы, а согласно многофакторному регрессионному анализу, пищевые привычки (β=1,20, p=0,002) относятся к значимым факторам влияния на формирование предиабета [27].
Бессимптомное вялотекущее системное воспаление лежит в основе нарушения метаболизма глюкозы и служит пусковым механизмом каскада событий, обусловленных атеросклерозом, ожирением, СД, дислипидемией и АГ. Фундаментальная роль длительного воспаления продолжает оставаться в центре внимания многих исследований. Хотя показан определенный вклад воспаления в развитие и прогрессирование указанных патологий и состояний, на сегодняшний день не доказана эффективность специально разработанной противовоспалительной терапии у пациентов с предиабетом, СД, ожирением или с АГ, что требует дальнейшего детального изучения этого вопроса.
Изменения, предшествующие СД, выражены по-разному в зависимости от индивидуальных особенностей человека, что позволяет выделять фенотипы пациентов с предиабетом: с метаболически здоровым ожирением и метаболически нездоровым ожирением, с метаболически здоровой и нездоровой жировой дистрофией печени, с повышенным отложением жира в поджелудочной железе и др. Обсуждается роль ИР головного мозга в развитии различных фенотипов предиабета. Фенотипирование пациентов с предиабетом является достаточно сложным и кропотливым процессом, но в перспективе позволит улучшить стратификацию больных по степени риска с учетом бремени глобальной эпидемии СД [28].
Врачу-терапевту или врачу общей практики, наблюдающих мультиморбидных пациентов, необходимо учитывать и потенциально диабетогенные свойства многих лекарственных средств: глюкокортикоидов, некардиоселективных бета-адреноблокаторов, блокаторов медленных кальциевых каналов, тиазидных диуретиков, статинов, альфа-интерферонов.
СКРИНИНГ ПРЕДИАБЕТА И ПРИНЦИПЫ ПРОФИЛАКТИКИ
Ранние нарушения углеводного обмена не сопровождаются клиническими проявлениями, хотя именно в этот период формируется основа для развития СД и ССЗ, в связи с чем необходимо регулярное проведение мероприятий по скринингу предиабета. Выявление предрасполагающих факторов риска наряду с лабораторной диагностикой (определением уровня глюкозы плазмы натощак, проведением теста на нарушение толерантности к глюкозе или оценкой уровня HbA1c) рассматривается как необходимое мероприятие для диагностики предиабета.
В 2022 г. были опубликованы результаты по оценке распространенности предиабета у пациентов, обращающихся за медицинской помощью в первичное звено здравоохранения. Диагноз предиабета был поставлен в 20% случаев, притом что лабораторные показатели соответствовали критериям предиабета только у 14,3% участников исследования; это подтверждает необходимость использования доступных опросников для выявления и постановки диагноза. Кроме того, исследование показало, что лишь у 37,0% пациентов с лабораторными признаками предиабета было диагностировано это состояние, что указывает на нарушение соблюдения врачами первичного звена установленных алгоритмов постановки соответствующего диагноза [29].
В последнее время постоянно ведутся поиск и разработка доступных шкал или моделей, способных определить риск развития СД и предсказать прогноз пациента. FINDRISK – один из первых опросников, разработанных для оценки 10-летнего риска развития СД [30]. Канадский опросник Canadian Diabetes Risk (CANRISK) также позволяет точно оценить возможную вероятность развития диабета. Его результаты достаточно легко интерпретировать, суммируя баллы по каждому из 12 вопросов и затем сравнивая результаты с пороговыми баллами для каждой из трех категорий риска – низкой (<21 балла), умеренной (21–32 балла) и высокой (>32 баллов) [31].
Согласно рекомендациям ADA, все взрослые люди с избыточной массой тела или ожирением, имеющие один или несколько факторов риска развития СД, должны проходить тестирование на предиабет. В отсутствие дополнительных факторов риска необходимо проводить скрининг лиц в возрасте от 45 лет. Скрининг нарушений обмена глюкозы также рекомендован женщинам на сроке беременности 24–28 нед [32]. Европейские и американские специалисты диабетической ассоциации адаптировали онлайн-калькулятор оценки вероятности развития СД, который включает ведущие факторы риска этого заболевания (рис. 2) [33].
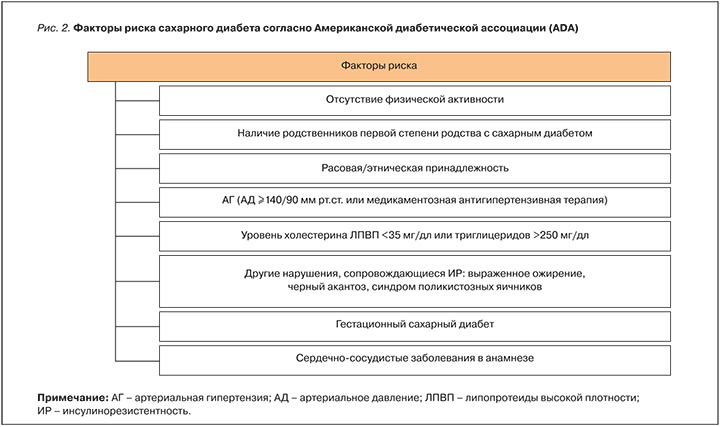
В России для оценки риска развития ранних нарушений обмена глюкозы предложен опросник-калькулятор ДИАРИСК, который при результате от 7 до 11 баллов с высокой долей вероятности позволяет предположить наличие предиабета [34].
Поскольку в настоящее время активно используется мультимаркерный подход к скринингу, диагностике и профилактике ведущих хронических неинфекционных заболеваний, учет комбинации различных факторов развития нарушений углеводного обмена способен облегчить скрининг предиабета и помочь идентифицировать группу уязвимых пациентов, у которых вероятность осложнений будет максимально высокой.
Подход к скринингу предиабета, предложенный Wagner R., включает ориентацию на совокупность индивидуальных особенностей (фенотипов), ассоциированных не только с высоким риском развития СД, но и ССЗ атеросклеротического генеза (рис. 3) [35].
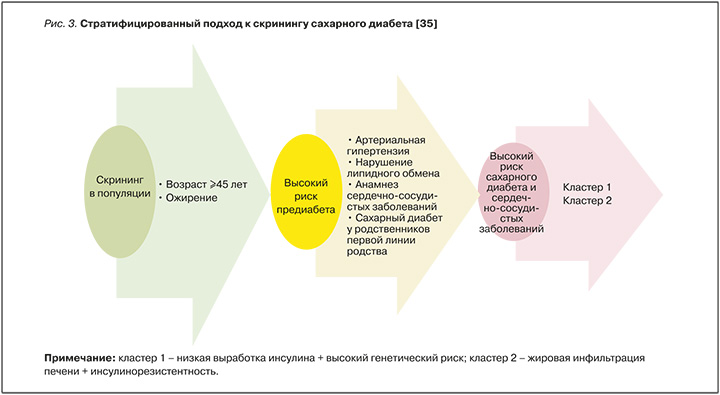
Рациональное питание и подвижный образ жизни служат необходимыми мероприятиями, а контроль гликемии – фундаментальной целью при комплексном ведении пациентов с ССЗ, независимо от наличия СД. Предиабет относится к тем клиническим состояниям, при которых пациент ежедневно и постоянно должен следовать всем немедикаментозным и медикаментозным рекомендациям врача, вести «дневник самоконтроля» за симптомами и регулярно проходить обследования с целью профилактики, диагностики и лечения осложнений. Активное использование простых и перспективных методов, таких как низкоуглеводная диета, диета с высоким содержанием белка, ограниченное по времени питание и высокоинтенсивные интервальные тренировки, самоконтроль за симптомами заболевания, могут помочь людям с нехваткой времени добиться улучшения показателей факторов риска нарушений углеводного обмена, включая снижение массы тела и контроль гликемии (HbA1c и уровень глюкозы в плазме крови натощак) [36].
Программа «Интенсивное изменение образа жизни» продемонстрировала возможность замедления прогрессирования предиабета в СД 2-го типа за счет снижения массы тела более чем на 10% от исходного веса в результате сокращения приема калорий и увеличения физической активности (180 мин/нед). Из 223 человек, включенных в исследование PROP-ABC (ClinicalTrials.gov ID: NCT02027571), в этой программе приняли участие 158 пациентов (70% женщин) в возрасте 53,3±9,28 года с предиабетом (ИМТ 30,6±6,70 кг/м2).
Ежемесячные личные консультации (face-to-face contact) с врачом в течение первых 6 мес и последующие ежеквартальные визиты дополнялись контактом по электронной почте и онлайн-визитами. Личный контакт пациента с врачом тесно коррелировал со снижением веса (r=0,98, p <0,0001). Изменение пищевых привычек способствовало снижению массы тела на 5 кг в течение 3 мес. В свою очередь, количество минут упражнений коррелировало с количеством шагов на шагомере (r=0,47, p <0,0001) [37].
ЗАКЛЮЧЕНИЕ
Учитывая неуклонное нарастание количества пациентов с предиабетом, необходимо своевременное выявление ранних нарушений метаболизма глюкозы, особенно у пациентов с классическими факторами риска ССЗ или уже имеющимися макро- или микрососудистыми осложнениями. Текущие критерии диагностики предиабета достаточно точны в предсказании риска развития СД, но различаются в отношении прогнозирования ССЗ и их осложнений. Возможно, универсальное определение предиабета с более низкими пороговыми значениями гликемии для профилактики СД и более высокими пороговыми значениями для стратификации риска поможет улучшить прогнозирование течения предиабета. ВОЗ считает, что диагноз предиабет необходимо заменить на более предпочтительный термин – «промежуточная гипергликемия», который более точно указывает на возможные последствия предиабета и необходимость его рассмотрения как отдельного состояния. В Международной классификации болезней 11-го пересмотра ожидается определение предиабета как заболевания, а не как «лабораторной находки». Такое решение подчеркивает важность проблемы для общественного восприятия и обоснованную с медицинской точки зрения потребность в лечении этой патологии.



