В современной аритмологии катетерная радиочастотная абляция (РЧА) субстрата фибрилляции предсердий (ФП) является наиболее перспективным и стремительно развивающимся методом лечения больных с этой аритмией [1, 2]. В 2009 г. опубликованы результаты выполненных в 90 центрах по всему миру РЧА при ФП более чем у 16 000 пациентов. Эти данные свидетельствуют о том, что эффективность процедуры в отношении пароксизмального, персистирующего и длительно
персистирующего варианта течения аритмии может достигать 84, 75 и 71% соответственно. При этом необходимость в проведении повторных процедур по поводу рецидивов аритмий возникает у каждого третьего пациента [3].
Спектр аритмий, по поводу которых проводятся повторные операции, включает помимо собственно ФП
также фокусные предсердные аритмии, атипичное трепетание предсердий (АТП) и во многом предопределяется особенностями проведения первичной процедуры РЧА [4].
При проведении первичной процедуры РЧА субстрата ФП с использованием методики, сочетающей
изоляцию легочных вен и РЧ-модификацию субстрата аритмии в области задней стенки левого предсердия (ЛП), причиной развития постабляционных левопредсердных аритмий чаще всего служит АТП [5]. Одной из распространенных разновидностей циркуляции re-entry является ПМТП по часовой стрелке или против нее, на долю которой, по некоторым данным, приходится более 50% всех циклов re-entry в ЛП (по некоторым данным, до 87%) [4]. Считается, что критическим участ ком ПМТП является так называемый митральный истмус — участок в ЛП, ограниченный кольцом митрального клапана и устьем левой нижней легочной вены (ЛНЛВ) [6]. Тем не менее РЧ-воздействия в области митрального истмуса, выполняемые из полости ЛП, т.е. эндокардиально, и со стороны свода коронарного синуса (КС), т.е. эпикардиально, в 60% случаев не приводят к достижению полной двунаправленной блокады проведения в зоне интереса [4].
В современной медицинской литературе данные об электрофизиологических основах и результатах РЧА при постабляционном ПМТП, а также и о результатах последующего клинического наблюдения за этой категорией пациентов немногочисленны, а число пациентов, принимавших участие в исследованиях, невелико [4—9].
В ряде публикаций, тем не менее, продемонстрировано, что критическое звено ПМТП не ограничивается только митральным перешейком. Так, в работе S. Tzeis и соавт. показано, что линейные РЧ-воздействия в области передней стенки ЛП могут купировать ПМТП [7]. По данным A. Chugh и соавт. (2004), у некоторых больных проксимальные отделы КС могут являться критическим
участком, ответственным за поддержание постабляционного ТП [8].
На основании собственного клинического опыта, накопленного в ходе проведения повторных сессий
РЧА у пациентов с рецидивирующими ПМТП, нами установлено, что нанесение РЧ-воздействий в области эндокардиальных отделов так называемого инфериосептального перешейка в ЛП (участок между кольцом митрального клапана и устьем правой нижней легочной вены — ПНЛВ) и в области свода КС (эпикардиальные отделы инфериосептального перешейка) нередко приводит к купированию АТП или сопровождается изменением длины цикла аритмии [9].
В этой связи нам представлялось актуальным сравнить эффективность РЧА митрального и левого нижнесептального перешейков у пациентов при лечении постабляционного перимитрального атипичного ТП.
Цель исследования: сравнить результаты катетерной РЧА митрального и нижнесептального истмусов в ЛП при лечении ПМТП у больных мерцательной аритмией, ранее оперированных методом РЧ-изоляции легочных вен и модификации анатомического субстрата аритмии в ЛП.
Материал и методы
Клиническая характеристика пациентов. В клиническое исследование включены 214 пациентов (43 женщины, средний возраст 51,4±13,6 года), которым с использованием системы нефлюороскопического внутрисердечного картирования были выполнены операции РЧА по поводу пароксизмальной (n=76 пациентов, 51%), персистирующей (n=25, 16%) и хронической форм ФП
(n=66, 33%).
У 24 (11%) пациентов (6 женщин, средний возраст 57,1±9,3 года) в период от 3 до 18 мес (6,1±2,9 мес) после первичной сессии РЧА при ФП были выполнены 36 повторных эндокардиальных электрофизиологических исследований (эндоЭФИ) и РЧА с помощью системы нефлюороскопического картирования. Причиной повторного вмешательства с использованием РЧ-энергии в этой группе пациентов являлись: ФП — у 4 (11%), фокусная левопредсердная тахикардия — у 6 (17%), re-entry-аритмии вокруг устьев легочных вен — у 2 (5%) и перимитральное АТП — у 24 (67%) (рис. 1).
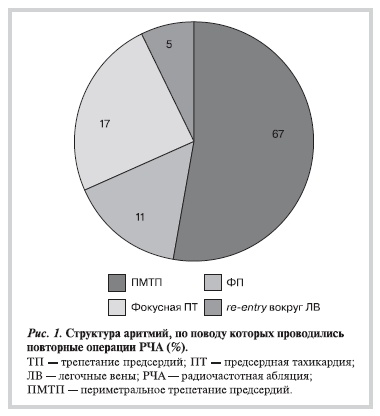
В настоящее исследование включены 20 пациентов (3 женщины, средний возраст 57,1±9,3 года) с рецидивирующим постабляционным ПМТП, верифицированным в ходе проведения эндоЭФИ и повторной процедуры РЧА (подробнее см. подразделы «ЭндоЭФИ. Трехмерная реконструкция ЛП и РЧА»). В табл. 1 представлены клинические характеристики пациентов, включенных в исследование.
Таблица 1. Клиническая характеристика пациентов (n=20).
Таблица 2. Сравнительная оценка радиочастотного воздействия на эндокардиальные и эпикардиальные отделы митрального и инфериосептального перешейков.
Во всех случаях пациенты принимали антиаритмические препараты I, III класса (в большинстве случаев кордарон — 15 пациентов). Для контроля частоты сердечных сокращений на фоне АТП использовали комбинацию антиаритмической терапии (ААТ) с β-адреноблокаторами (у 8 пациентов), верапамилом (у 2) и дигоксином (у одного) (см. табл. 1). Кроме того, все пациенты продолжали принимать антикоагулянтную терапию (варфарин в дозировке, поддерживающей международное нормализованное отношение в диапазоне от 2 до 3). За 3 сут до операции варфарин отменялся.
Операции эндоЭФИ и РЧА выполняли после подписания пациентом информированного согласия и при
условии отсутствия противопоказаний.
ЭндоЭФИ. Трехмерная реконструкция ЛП и РЧА. Во время процедуры эндоЭФИ анестезиологическое пособие проводили с использованием метода сочетанной анестезии. Под местной анестезией 0,5% раствором новокаина по методике Сельдингера выполняли катетеризацию правой и левой бедренных вен, левой подключичной вены. Через интродьюсер 8Fr, установленный в левой подключичной вене, декаполярный диагностический электрод проводили в коронарный синус. Через интродьюсер 8Fr, установленный в левой бедренной вене, диагностический электрод 6Fr размещали в верхушке правого желудочка. Мониторирование 12 отведений поверхностной электрокардиограммы (ЭКГ), внутрисердечных биполярных электрограмм с электродных пар диагностических и картирующего электродов осуществляли с помощью электрофизиологической системы Sensis с установленными диапазонами фильтрации 30—500 Гц. Для проведения диагностического протокола электрокардиостимуляции использовали наружный электрокардиостимулятор UHS-20 с установленной длительностью импульса 2 мс.
Методом программированной и/или асинхронной стимуляции с дистальной и/или проксимальной пар электрода, расположенного в КС, определяли режимы индукции клинической аритмии.
Для осуществления доступа абляционного электрода в ЛП под рентгеновским и внутрисердечным эхокардиографическим контролем пунктировали межпредсердную перегородку.
С помощью системы нефлюороскопического картирования CARTO XP (Biosense Webster) картирующим
электродом на фоне клинической аритмии осуществляли трехмерную активационную реконструкцию ЛП, определяли направление распространения фронта деполяризации цикла перимитрального ТП (рис. 2, см. на вклейке). Диагноз атипичного ПМТП подтверждался в том числе и на основании верификации классических критериев «вхождения» в цикл тахикардии при электрокардиостимуляции из области дистальной пары электрода КС и/или абляционного электрода, позиционированного
в области митрального истмуса [10].
РЧА в ЛП проводилась с помощью этого же квадриполярного орошаемого электрода с контролем по температуре и установленными лимитами по мощности и по температуре (до 40 Вт и до 43°С соответственно) со скоростью открытоконтурного орошения 17 мл/мин.
При проведении РЧА в КС лимит по мощности и температуре устанавливали в пределах 30 Вт и 43 ºС соответственно.
В ходе эндокардиальной процедуры для профилактики тромбоэмболических осложнений, связанных с проведением РЧА в ЛП, пациентам с помощью дозатора постоянно внутривенно вводили гепарин с первоначальной скоростью 1000 ед/ч через транссептальный интродьюсер.
Дизайн исследования. Протокол исследования состоял из 4 этапов.
Первым этапом РЧА проводили в области митрального перешейка — от устья ЛНЛВ к кольцу митрального клапана (эндокардиальные отделы митрального перешейка).
На втором этапе абляционный катетер извлекали из ЛП и устанавливали в дистальные отделы КС, где
в области свода проводили РЧА (эпикардиальные отделы митрального истмуса).
Третий этап заключался в линейном РЧ-воздействии в области нижнесептального перешейка. Для этого абляционный катетер вновь проводили в полость ЛП, где выполняли линейное РЧ-воздействие от устья ПНЛВ к кольцу митрального клапана (эндокардиальные отделы инфериосептального перешейка).
Четвертый этап заключался в РЧ-воздействии в области свода проксимальных отделов КС (эпикардиальные отделы инфериосептального перешейка). Для этого абляционный катетер извлекали из ЛП и устанавливали в проксимальных отделах КС (рис. 3).
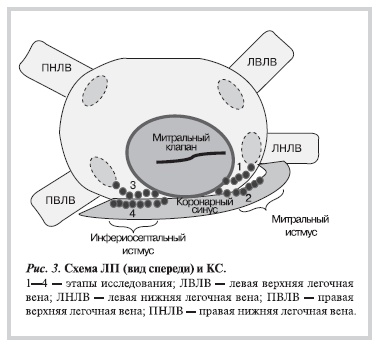
Конечные точки РЧА на каждом этапе. На каждом этапе определяли влияние РЧА на цикл АТП (восстановление синусового ритма и/или изменение длины цикла аритмии). В случае, если на фоне РЧ-воздействий ПМТП сохранялось (несмотря на снижение амплитуды предсердного эндокардиального сигнала, регистрируемого с дистальной пары картирующего электрода, на 80%, по сравнению с исходной величиной), переходили к выполнению следующего этапа протокола исследования.
Клиническое наблюдение после РЧА. Ведение пациентов в раннем и отдаленном периодах не отличалось от стандартного ведения пациентов, оперированных по поводу ФП методом РЧА в ЛП [11].
Методы статистической обработки результатов исследования. Расчет выполняли с использованием
приложения пакета статистического анализа данных Statistica 6.0 for Windows. Для оценки количественных показателей применяли непараметрические критерии (Вилкоксона, Ньюмена—Кейлса). Данные представлены в виде среднего значения ± стандартное отклонение вычисленных величин. Различия считали статистически значимыми при р<0,05.
Результаты
Атипичное перимитральное ТП с длиной цикла 248±55 мс (от 190 до 305 мс) верифицировано в 24 случаях у 20 пациентов. В 17 случаях индукция ПМТП возникала при проведении программированной или асинхронной ЭКС с проксимальной или дистальной электродной пары катетера, позиционированного в КС. В 7 случаях ПМТП характеризовалось длительно персистирующей аритмией.
В ходе выполнения транссептальной пункции у 2 пациентов верифицировано патентное овальное окно. Осложнений, связанных с осуществлением доступа в ЛП, не отмечено.
Первый этап — РЧА эндокардиальной порции левого истмуса. При РЧ-воздействии на область митрального истмуса в ЛП синусовый ритм восстанавливался в 6 случаях, изменение длины цикла тахикардии отмечено в 5 случаях (рис. 4, см. на вклейке). Средняя длительность РЧ-воздействий в области митрального истмуса составила 12±7 мин.
Второй этап — РЧА эпикардиальной порции левого истмуса. Восстановление синусового ритма наблюдалось при РЧА в области свода дистального КС в 3 случаях, изменение длины цикла тахикардии отмечено еще в 2 случаях. Средняя длительность воздействия в этих отделах КС составила 3,2±1,1 мин (рис. 5, см. на вклейке).
Третий этап — РЧА эндокардиальной порции инфериосептального перешейка. РЧА эндокардиальных отделов инфериосептального перешейка привела к восстановлению синусового ритма в 3 случаях, к увеличению длины цикла атипичного ТП — в 6. Средняя длительность РЧ-воздействий 11±2 мин (рис. 6, см. на вклейке).
Четвертый этап — РЧА эпикардиальной порции инфериосептального перешейка. В 12 случаях синусовый ритм восстанавливался во время РЧ-воздействия в области крыши проксимальных отделов КС (четвертый этап) (рис. 7, см. на вклейке).
Таким образом, РЧ-воздействия в области эндокардиальных (первый этап) и эпикардиальных (второй этап) отделов митрального перешейка привели к восстановлению синусового ритма только в 9 случаях, в то время как продолжение РЧА в области эндокардиальных (третий этап) и эпикардиальных (четвертый этап) отделов инфериосептального перешейка привело к восстановлению синусового ритма в оставшихся 15 случаях (р<0,05). Эндокардиальные и эпикардиальные РЧ-воздействия
в области митрального истмуса сопровождались изменением длины цикла перимитрального ТП в 7 случаях, а при РЧА в области эндокардиальных и эпикардиальных отделов инфериосептального истмусов изменения длины цикла тахикардии отмечались в 6 случаях (см. табл. 2).
Результаты клинического наблюдения после РЧА. В раннем послеоперационном периоде (до 3 мес после последней повторной процедуры РЧА) у 4 (20%) пациентов однократно регистрировались суправентрикулярные нарушения ритма, которые были эффективно купированы дополнительным внутривенным введением кордарона в 3 случаях или приемом анаприлина в одном.
Повторные операции по поводу рецидивирующего ПМТП выполнены в период от 3 до 12 мес инициальной сессии РЧА 4 пациентам. Через 12 мес клинического наблюдения у 2 пациентов, несмотря на проводимую ААТ, сохранялись эпизоды рецидивирующего АТП, у 18 (90%) пациентов сохранялся устойчивый синусовый ритм, при этом в 14 (70%) случаях аритмический синдром не рецидивировал в отсутствие ААТ.
Через 2,8±1,8 года (от 1 года до 5 лет) под клиническим наблюдением остаются 12 пациентов: у 2 отмечается рецидивирующее течение аритмического синдрома (атипичное ТП), устойчивый синусовый ритм сохраняется у 10, из которых у 8 ААТ не проводится (рис. 8).
Рисунок 8. Результаты клинического наблюдения за пациентами, оперированными по поводу постабляционного перимитрального ТП.
Обсуждение
Первое клиническое и электрофизиологическое описание атипичного перимитрального ТП датируется 2000 г. P. Jais и соавт. представили данные клинического наблюдения за 22 пациентами с атипичным левопредсердным ТП. На долю ПМТП (re-entry по периметру митрального клапана) приходилось 75% всех левопредсердных АТП. Авторами было установлено, что для ПМТП критическим для его поддержания являлся участок между кольцом митрального клапана и устьем ЛНЛВ, который и получил название митрального истмуса [6].
Этой же группой авторов в 2004 г. предложена методика верификации двунаправленного блока проведения в митральном перешейке при проведении РЧА субстрата мерцательной аритмии. Авторы декларировали возможность достижения блока проведения при абляции эндокардиальной порции митрального истмуса (из полости ЛП) только в 32% случаев, а при нанесении дополнительных воздействий в области эпикардиальной порции перешейка (из дистальных отделов КС) блок проведения достигался в 87% случаев [12]. Последующее клиническое наблюдение за этими пациентами свидетельствовало, что достижение блока проведения в митральном истмусе ассоциируется с меньшей частотой рецидивов постабляционного ПМТП [12].
Согласно полученным нами данным, РЧА в области митрального перешейка (эндокардиальной и эпикардиальной порций) влияет на цикл ПМТП в 66% случаев и только в 37,5% приводит к восстановлению синусового ритма. На наш взгляд, объяснением этому может служить сложность анатомии митрального перешейка, включающего как эпикардиальные (в КС), так и эндокардиальные (в ЛП) волокна. Более того, сама РЧА в КС представляет собой манипуляцию, сопровождающуюся высоким риском перфорации стенки КС и/или повреждением огибающей коронарной артерии
[14, 15]. Во избежание перечисленных осложнений используются временны`е и мощностные ограничения РЧ-воздействий, которые следует проводить только в области свода КС (ближе к ЛП). Несомненно, что даже после проведения экстенсивной РЧА в области как эндокардиальных, так и эпикардиальных отделов митрального истмуса в этой зоне, может сохраняться возможность проведения электрического импульса (см. рис. 4 и 5, В, см. на вклейке) [13].
В этой связи остается актуальным вопрос об альтернативных критических участках цикла перимитрального re-entry. В 2010 г. в работе, представленной S. Tzeis и соавт., показано, что линейные РЧ-воздействия в области передней стенки ЛП купируют постабляционное перимитральное
ТП у 55% пациентов, а у оставшихся 45% меняют цикл атипичного ТП (формируют новый, не связанный с митральным кольцом цикл re-entry). Обращает внимание, что авторами не принимается во внимание возможное проведение по эпикардиально расположенным волокнам, которое может иметь значение в поддержании перимитрального re-entry [7]. Впервые о возможности купирования перимитрального re-entry при РЧА в КС упоминают A. Chugh и соавт. в работе, опубликованной в 2005 г. В этом исследовании принимали участие 40 пациентов (возраст 55±9 лет, 25 мужчин) с постабляционным левопредсердным ТП. Результаты показали, что перимитральное ТП прекращалось после РЧ-воздействий в КС у 12 пациентов, при этом в 4 случаях синусовый ритм восстанавливался при нанесении РЧ-аппликаций в области проксимальных отделов КС. Авторы сделали вывод, что проксимальные отделы КС могут быть вовлечены в цикл re-entry и являться его критическим участком [8].
В отличие от данных A. Chugh и соавт., результаты, полученные в нашем исследовании, свидетельствуют о том, что РЧА в проксимальных отделах КС достоверно чаще приводит к восстановлению синусового ритма (в 12 из 24 случаев). На наш взгляд, объяснением этому может быть то, что проксимальные отделы КС рассматривались нами как эпикардиальная часть инфериосептального перешейка. РЧА в этой области проводилась после предшествующего нанесения линейных РЧ-воздействий в эндокардиальных отделах инфериосептального перешейка (третий этап),
что сопровождалось увеличением длины цикла ПМТП в 25% случаев (см. рис. 6 и 7, см. на вклейке).
Причины, лимитирующие нанесение РЧ-воздействий в области проксимальных отделов КС, не отличаются от тех, которые обсуждалась нами выше в отношении дистальных отделов КС. Более того, верификация блока проведения в инфериосептальном перешейке может быть затруднена из-за его сложной анатомической организации, и, следовательно, целесообразность ее проведения в ходе настоящего исследования нам представлялась сомнительной.
Таким образом, нами установлено, что РЧА эндокардиальных и эпикардиальных отделов инфериосептального перешейка сопровождается восстановлением синусового ритма достоверно чаще, чем РЧА эндокардиальной и эпикардиальной порций митрального перешейка, а это противоречит ранее принятым представлениям о локализации критического участка ПМТП [8].
В этой связи важная роль РЧА инфериосептального перешейка при проведении повторных сессий РЧА по поводу постабляционного ПМТП нам представляется очевидной, так как имеет позитивное клиническое значение, в том числе в отдаленном периоде наблюдения за этой группой пациентов (см. рис. 8).
Ограничения исследования. Полученные нами результаты актуализируют необходимость проведения исследования, заключающегося в сравнении двух групп пациентов, в одной из которых РЧА проводилась бы только в области эндокардиальных и эпикардиальных структур митрального истмуса, а в другой — только инфериосептального. В этом случае будет возможно судить о том, какой из левопредсердных истмусов имеет определяющее значение в поддержании и купировании ПМТП.
В нашем исследовании не проводилась верификация блока проведения после выполнения РЧ-воздействий в области как митрального, так и инфериосептального перешейков. Во-первых, это было обусловлено тем, что процедуры выполнялись на фоне ААТ. Во-вторых, анатомическая организация перешейков чрезвычайно сложна и РЧ-воздействия в области КС чреваты развитием угрожающих жизни осложнений, а прогностическое значение этой техники у пациентов данной группы не является доказанным.
Заключение
Радиочастотная абляция эндокардиальных и эпикардиальных отделов нижнесептального перешейка в левом предсердии достоверно чаще приводит к купированию перимитрального атипичного трепетания предсердий у пациентов, оперированных ранее по поводу фибрилляции предсердий.



