Согласно современным клиническим рекомендациям по лечению острого коронарного синдрома (ОКС) с подъемом сегмента ST (пST), в случае невозможности выполнения первичной ангиопластики в течение 2 ч от момента первого контакта врача с больным необходимо провести тромболитическую терапию (ТЛТ). Если через 90 мин от начала ТЛТ отсутствуют признаки реперфузии коронарной артерии (КА), показано экстренное чрескожное коронарное вмешательство (ЧКВ). В случае реперфузии миокарда проведение ЧКВ показано через 3—24 ч после ТЛТ [1]. Эти рекомендации основаны на исследованиях и регистрах, которые выполнены в основном в странах Западной Европы и Северной Америки. Однако в каждой стране, тем более в России, существуют особенности оказания помощи больным ОКС. В частности, при сравнении Европейского регистра пациентов с ОКСпST (2010) с аналогичным регистром в Томске оказалось, что среди российских пациентов больше курильщиков, меньше мужчин, выше частота дислипидемии, гипертонической болезни; эти больные позже поступают в стационар (больше период от начала ангинозного приступа). В результате риск летального исхода в течение 30 дней по индексу GRACE у наших пациентов почти в 3 раза выше: 9,1% против 3,2% [2]. Вероятно, это является одной из причин того, что, по данным отечественного регистра РЕКОРД, сохраняется высокая госпитальная смертность среди этих больных — 16,7% [3]. Кроме того, в России широко применяется стрептокиназа. В частности, в Томске часто используется ускоренное введение 750 тыс. ед. стрептокиназы на догоспитальном этапе, что не практикуется в других странах [4]. С учетом этих и других особенностей отечественной медицины возникает вопрос: адекватны ли выше представленные алгоритмы лечения в наших условиях? Или целесообразно ставить задачу выполнения первичной ангиопластики у всех больных? Для решения этого вопроса необходимы исследования и регистры, проводимые в условиях реальной клинической практики в нашей стране.
Цель работы — сравнить эффективность и безопасность первичной ангиопластики и фармакоинвазивной реваскуляризации у больных ОКСпST.
Материал и методы
В исследование включали больных ОКСпST на догоспитальном этапе в Томске, которым в первые 6 ч от начала заболевания предполагалось проведение реперфузионных мероприятий. В исследование включили 289 пациентов. На догоспитальном этапе они были рандомизированы в 2 группы методом конвертов: больных 1-й группы (n=146) доставляли на первичное ЧКВ; больным 2-й группы (n=143) в рамках фармакоинвазивной тактики на догоспитальном этапе проводили тромболизис и после этого доставляли в стационар. ТЛТ на догоспитальном этапе выполняли стрептокиназой (n=71), которую вводили внутривенно в дозе 750 тыс. ед. за 5—10 мин, или тенектеплазой (n=72), которую вводили внутривенно болюсом в дозе, рассчитанной с учетом массы тела. Выбор тромболитика проводил врач бригады скорой медицинской помощи по своему предпочтению, но чаще – в зависимости от наличия того или иного препарата. Решение о дальнейшей тактике принимали через 90 мин после введения тромболитического препарата. Если наблюдались признаки реперфузии КА (снижение сегмента ST на ≥50%), ЧКВ выполняли в плановом порядке через 3—24 ч после введения тромболитического препарата. При неэффективности ТЛТ, т.е. в отсутствие признаков реперфузии КА, больного как можно раньше направляли на спасительное ЧКВ. Всем больным на догоспитальном этапе назначали наркотические анальгетики, гепарин (максимум 4 тыс. ед.) и ацетилсалициловую кислоту 250 мг внутрь, а также по показаниям β-адреноблокаторы, антагонисты кальция, седативные и антигистаминные препараты. При поступлении в стационар все больные получали нагрузочную дозу клопидогрела 300 мг.
Проводили анализ следующих показателей: время от начала болевого синдрома до введения тромболитического препарата на догоспитальном этапе (боль—игла), частота реперфузии миокарда через 90 мин после введения тромболитического препарата, время от введения тромболитического препарата до признаков реперфузии миокарда (снижение сегмента ST на ≥50% в информативных отведениях), время от начала болевого синдрома до раздувания баллона при первичной ангиопластике (боль—баллон), время от введения тромболитического препарата до раздувания баллона при спасительной ангиопластике, общее время ишемии миокарда у каждого больного, степень кровотока в инфаркт-связанной коронарной артерии (ИСКА) по шкале TIMI во время коронарографии (КГ), частота синдрома no-reflow, который диагностировали визуально во время ЧКВ по недостаточной миокардиальной перфузии на фоне полностью восстановленного кровотока (TIMI 3), размер некроза миокарда по QRS-индексу при поступлении и перед выпиской, фракция выброса левого желудочка по данным ультразвукового исследования сердца на 7-е сутки заболевания, частота и степень геморрагических осложнений по шкале TIMI, частота летальных исходов, рецидивов инфаркта миокарда (ИМ), рецидивов ишемии миокарда (приступы стенокардии, сопровождающиеся динамикой сегмента ST), инсультов.
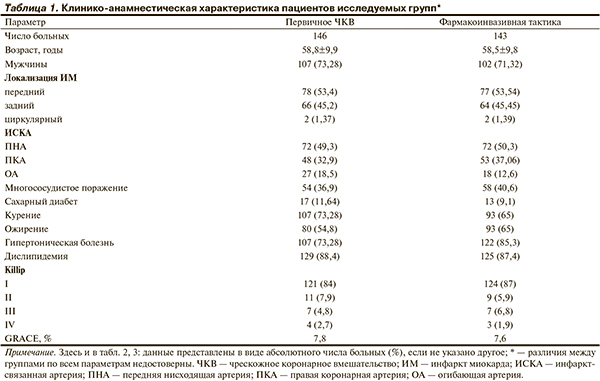
Как представлено в таблице 1, по основным клиникоанамнестическим характеристикам и риску летального исхода в течение 30 дней по шкале GRACE группы пациентов между собой не различались.
Статистическую обработку данных проводили при помощи статистического пакета Statistica 6. Значимость различий оценивали с помощью t -критерия Стьюдента. Различие считали статистически значимым при p<0,05. Данные представлены в виде средняя±ошибка средней.
Результаты
Частота реперфузии КА через 90 мин после ТЛТ на догоспительном этапе в группе фармакоинвазивной тактики составила 76,2% (109 больных), после введения стрептокиназы и тенектеплазы — 67,7 и 83,3% соответственно (p=0,002).
В группе фармакоинвазивной тактики ТЛТ проведена через 118,5±63,5 мин от начала ангинозного приступа, т.е. в течение первых 2 ч. У пациентов с неэффективной ТЛТ время от введения тромболитического препарата до ангиопластики составило 154,6±36,6 мин. Общее время ишемии миокарда в этой группе достигало 224,65±71 мин. Это статистически значимо меньше, чем в группе первичной ангиопластики (278±184 мин; р<0,01). Таким образом, в наших условиях фармакоинвазивная тактика репефузионных мероприятий обеспечивает сокращение времени ишемии миокарда на 54 мин, т.е. почти на 1 ч.
Эффективность ангиопластики по частоте достижения кровотока TIMI-3 после ЧКВ была выше в группе фармакоинвазивной тактики: 80,5% против 71,4% (р<0,005). Частота развития синдрома no-reflow была значительно ниже во 2-й группе: 1,4% против 11,6% (р<0,003). В группе первичного ЧКВ с развившимся синдромом no-reflow 2 пациента умерли на фоне кардиогенного шока.
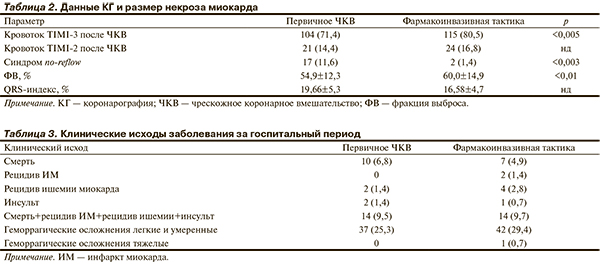
При определении размера некроза миокарда обращает на себя внимание, что во 2-й группе фракция выброса левого желудочка оказалась статистически значимо больше, чем в 1-й группе: 60,0±14,9% против 54,9±12,3% (р<0,01); это может свидетельствовать о том, что фармакоинвазивная тактика обеспечивает сохранение жизнеспособного миокарда эффективнее, чем первичная ангиопластика (табл. 2). Различий по QRS-индексу между группами не обнаружено.
Значимого различия по частоте и тяжести геморрагических осложнений между группами не обнаружено (табл. 3). Во 2-й группе выявлен один случай тяжелого геморрагического осложнения: в первые сутки заболевания после введения тенектеплазы развился геморрагический инсульт с последующим летальным исходом.
По основным клиническим исходам заболевания — летальному исходу, рецидиву ИМ, рецидиву ишемии миокарда, инсультам — группы между собой также не различались. Основным механизмом смерти у большинства больных был кардиогенный шок: у 9 и 3 пациентов в 1-й и 2-й группах соответственно. Кроме того, в группе первичного ЧКВ у одного пациента причиной смерти явилась рецидивирующая фибрилляция желудочков, а в группе фармакоинвазивной тактики — 1 кровоизлияние в мозг, 2 разрыва миокарда с тампонадой сердца, 1 рецидивирующая фибрилляция желудочков. Рецидивов ИМ в 1-й группе не было, во 2-й группе рецидив ИМ произошел у 2 больных на 3-и и 6-е сутки заболевания. В 1-й группе было 2 ишемических инсульта, во 2-й — один геморрагический. Частота развития комбинированной конечной точки (смерть+рецидив ИМ+рецидив ишемии+ инсульт) также между группами не различалась.
Обсуждение
В настоящее время не вызывает сомнения, что в первые часы острого ИМ главной целью лечебных мероприятий является восстановление кровотока в ИСКА. Этого можно достичь двумя способами: ТЛТ или первичным ЧКВ. У каждого из этих способов есть преимущества и недостатки. Если делать выбор между ними при поступлении больного в стационар с возможностью выполнения первичного ЧКВ, то предпочтение необходимо отдавать ЧКВ как методу, который позволяет более эффективно снижать летальность [5, 6]. Однако если ТЛТ проводить значительно раньше, на догоспитальном этапе, то эти два метода можно сочетать, что носит название «фармакоинвазивная реперфузия коронарной артерии». Именно такой подход оказывается не только не хуже первичной ангиопластики в исследованиях GRACIA-2, WEST [7, 8], но и превосходит ее по эффективности, в том числе при длительной транспортировке в ЧКВ-центры, в исследовании NORDISTEMI и регистре FAST-MI [9, 10], что и нашло свое отражение в современных клинических рекомендациях. Однако это преимущество догоспитальной ТЛТ проявляется только в отсутствие возможности проведения первичной ангиопластики в течение 2 ч от первого контакта врача с пациентом, т.е. в нашей клинической практике — это время осмотра больного врачом бригады скорой медицинской помощи на догоспитальном этапе. Что такое эти 2 часа? Это время, в течение которого у большинства больных, которым введен тромболитический препарат, происходит реперфузия КА. Таким образом, основным критерием, который определяет сравнительную эффективность этих двух методов лечения, остается ожидаемое время восстановления кровотока в ИСКА. Что произойдет быстрее: медикаментозная реперфузия после введения тромболитического препарата или механическая реканализация? При этом надо учитывать, что если эффективность ЧКВ в плане реканализации КА практически не зависит от времени боль—баллон, то при ТЛТ такая зависимость есть: чем раньше проводится тромболизис, тем он более эффективен, тем меньше время игла—реперфузия. Это обусловлено тем, что чем меньше «возраст» тромба, тем легче он поддается медикаментозному лизису. Исходя из этого в рекомендациях предлагается дифференцированный подход к приемлемой задержке времени до первичной ангиопластики: в первые 2 ч заболевания ТЛТ необходимо проводить, если предполагаемое время до баллона превышает 90 мин, а после 2 ч заболевания возможное время задержки до введения баллона увеличивается до 2 ч [1].
В выполненном нами исследовании обнаружено, что у большинства включенных во 2-ю группу пациентов тромболизис на догоспитальном этапе удалось провести в течение первых 2 ч от начала ангинозного приступа. Известно, что эффективность ТЛТ и первичного ЧКВ, которые выполняются в первые 3 ч заболевания, по влиянию на летальность не различается [11]. Таким образом, полученный нами результат по времени проведения ТЛТ уже дает основание ожидать благоприятного течения заболевания в этой группе. Выполнить первичную ангиопластику в 1-й группе удалось в среднем только через 278 мин, т.е. примерно через 4,5 ч от начала ангинозного приступа. Поэтому, несмотря на то что спасительную ангиопластику после неэффективной ТЛТ проводили также с большой задержкой времени — 154 мин, т.е. только через 2,5 ч после введения тромболитического препарата, общее время ишемии миокарда при фармакоинвазивной тактике сократилось почти на 1 ч по сравнению с таковым при первичной ангиопластике. Такое сокращение времени ишемии миокарда логично привело к спасению части миокарда, что проявилось более высокой фракцией выброса левого желудочка в группе больных с догоспитальным тромболизисом.
Обращает на себя внимание длительная задержка как первичной (первый медицинский контакт—баллон), так и спасительной (игла—баллон) ангиопластики: примерно по 2,5 ч. Это обусловлено как проблемами транспортировки пациентов по городу с перегруженными транспортом улицами, так и несовершенством логистики движения пациентов в клинике. Для решения этих проблем в настоящее время в Томске выделяются полосы движения только для общественного транспорта, в том числе автомобилей скорой медицинской помощи, а также изменена схема движения пациентов с ОКС в клинике: пациенты из приемного покоя, минуя палату интенсивной терапии, попадают на операционный стол. Это позволило в течение последнего года сократить время до ангиопластики примерно на 35 мин.
Несколько неожиданным было резкое снижение частоты развития синдрома no-reflow при ЧКВ после ТЛТ по сравнению с первичным ЧКВ. Механизмы развития этого синдрома очень сложны и окончательно не выяснены. Эффективные методы борьбы с этим феноменом не разработаны [12]. Один из основных предполагаемых механизмов его развития — это микроэмболия дистального русла при механическом разрушении тромба в КА [13, 14]. Вероятно, в отличие от первичного ЧКВ, разрушение тромба под влиянием ТЛТ происходит относительно постепенно, без формирования большого количества микроэмболов, которые могут окклюзировать дистальное русло. ЧКВ у этих больных проводится уже при открытой артерии, в которой или находятся только остатки тромба, или тромботические массы отсутствуют в результате их медикаментозного лизиса.
В основе другой версии возникновения феномена no-reflow лежит повреждение миокарда и микрососудистого русла в условиях острой ишемии, которое в ответ на реперфузию/реоксигенацию в значительной степени прогрессирует, препятствуя восстановлению полноценного кровотока в бассейне ИСКА. Эти процессы усиливаются при увеличении времени ишемии миокарда. Фармакоинвазивная реперфузия миокарда в наших условиях уменьшает это время по сравнению с первичной ангиопластикой, что также может быть причиной уменьшения частоты развития синдрома no-reflow в этой группе больных.
Известно, что исходная проходимость коронарной артерии 2—3-й степени по TIMI при экстренном ЧКВ приводит к улучшению исходов вмешательства по сравнению с исходной проходимостью 0—1-й степени [15—17]. Можно предположить, что одной из причин этого является различная частота развития синдрома no-reflow. Известно также, что прогноз для жизни пациента при развитии синдрома no-reflow значительно хуже, чем без него [18].
Различия по частоте реперфузии КА после введения стрептокиназы и тенектеплазы на догоспитальном этапе ожидаемы. В рамках исследования GUSTO-1, в котором впервые показано преимущество альтеплазы перед стрептокиназой по влиянию на летальность, проводилось подисследование, в котором некоторым больным выполнялась экстренная ангиопластика [19]. Оказалось, что если через 90 мин после введения тромболитического препарата эффективный кровоток в ИСКА (2—3-й степени по TIMI) был выше в группе алтеплазы (81% против 60%), то через 180 мин это различие исчезало (76 и 74% соответственно). Таким образом, хотя в итоге эти тромболитические препараты одинаково часто «открывают» КА, но алтеплаза делает это быстрее. Прямого сравнения стрептокиназы и тенектеплазы не проводилось, но, учитывая одинаковую эффективность алтеплазы и тенектеплазы [20], этот результат можно экстраполировать и на сравнительную эффективность стрептокиназы и тенектеплазы. По нашим данным, медленное болюсное введение 750 тыс. ед. стрептокиназы «открывает» КА на 36 мин быстрее, чем капельное введение 1,5 млн ед. [4]. Однако даже этой повышенной скорости не хватает, чтобы достичь временны'х показателей эффективности тенектеплазы. Несмотря на это болюсное введение стрептокиназы широко применяется в Томске. Во-первых, этот препарат более доступен (он на порядок дешевле) и в отличие от тенектеплазы всегда есть у бригад скорой медицинской помощи и в стационаре. Во-вторых, стрептокиназа — более безопасный препарат в отношении риска развития геморрагического инсульта. Поэтому она может быть более предпочтительной у пациентов с повышенным риском такого осложнения: у больных старческого возраста, артериальной гипертензией, с нарушением мозгового кровотока в анамнезе, особенно при нижнем, относительно небольшом ИМ, позже 4 ч от его развития. В таких случаях эффект от проведения тромболизиса предполагается невысокий и риск развития геморрагического инсульта может превышать ожидаемую пользу [21].
Таким образом, согласно данным нашего исследования, фармакоинвазивная стратегия реперфузии миокарда при ОКС с использованием догоспитального тромболизиса не только является альтернативой, но и имеет преимущества перед первичной ангиопластикой. С учетом особенностей отечественной организации медицинской помощи не представляется возможным проведение первичной ангиопластики большинству пациентов в течение 90—120 мин от первого осмотра врачом на догоспитальном этапе. Это справедливо как для больших городов, так и особенно для населенных пунктов, которые находятся вдали от катетеризационных лабораторий. В этом отношении Россия не является уникальной страной, даже по сравнению со многими странами Запада. В частности, в США, стране с высоко развитой системой медицинской помощи, в реальной клинической практике среднее время первый медицинский контакт—баллон в 1999—2002 гг. достигало 180 мин, т.е. 3 ч [22], а в одном из последних исследований по реперфузии миокарда при ИМ (FINESS) в группе с первичной ЧКВ оно составило 2,2 ч [23]. При этом в США в отличие от Европы значительно труднее организовать догоспитальный тромболизис. Причина этого состоит в том, что в США менее 1/3 пациентов с подъемом сегмента ST используют скорую медицинскую помощь или службу спасения 911, сотрудники которых не являются квалифицированными медиками, а большинство пациентов транспортируются родственниками или друзьями в отделения скорой помощи [24]. В России сущест вует развитая система скорой медицинской помощи, что позволяет решать задачу широкого применения догоспитального тромболизиса, за которым должно следовать выполнение коронарной ангиографии и ЧКВ [25].
Выводы
Фармакоинвазивная реперфузия миокарда при остром инфаркте миокарда с подъемом сегмента ST с использованием догоспитального тромболизиса по сравнению с первичной коронарной ангиопластикой в Томске уменьшает время ишемии миокарда на 54 мин, увеличивает частоту достижения кровотока TIMI-3 после ЧКВ: 80,5% против 71,4% (p=0,002) и более эффективно сохраняет фракцию выброса левого желудочка: 60,0±14,9% против 54,9±12,3% (р<0,01).
Проведение догоспитального тромболизиса перед коронарной ангиопластикой уменьшает частоту развития синдрома no-reflow по сравнению с первичной ангиопластикой у больных острым инфарктом миокарда: 1,4% против 11,6% (р<0,003).