Несмотря на экономические затраты, направленные на повышение эффективности диагностики и лечения, сердечно-сосудистые заболевания остаются основной причиной смертности населения развитых стран мира. Стандартизация алгоритма обследования пациентов с клиникой ишемической болезни сердца (ИБС) способствует раннему выявлению атеросклеротического поражения коронарных артерий и снижению риска развития острого коронарного синдрома (ОКС). В течение последнего десятилетия компьютерная томография (КТ) сердца и коронарных артерий с внутривенным контрастированием вошла в стандарты диагностики стабильной ИБС и ОКС. Появление компьютерных томографов нового поколения с 64 и более рядами детекторов позволило значительно улучшить качество изображений и достоверность оценки состояния коронарного русла. Особенно это касается аппаратов с широким детектором (320 рядов), позволяющих за один оборот рентгеновской трубки одномоментно получать 640 томографических срезов толщиной 0,5 мм, захватывающих всю область сердца. Такой режим томографии исключает артефакты от движения стола, значительно снижает артефакты от сердечных сокращений и лучевую нагрузку.
КТ В АЛГОРИТМЕ ОБСЛЕДОВАНИЯ БОЛЬНЫХ ИБС
Данные многоцентровых исследований доказали, что КТА обладает высокой отрицательной прогностической ценностью [1–4]. Это послужило основанием включения КТ в международные рекомендации для диагностики ИБС у пациентов низкого и среднего риска в качестве альтернативы стресс-тестам (класс рекомендаций IIa, уровень доказательности C) [5], а также для исключения окклюзирующего поражения коронарных артерий и дифференциальной диагностики с расслаивающей аневризмой аорты и тромбоэмболией легочной артерии у больных с атипичным затяжным болевым синдромом в грудной клетке без специфических изменений на ЭКГ и отрицательным тестом на тропонин (класс рекомендаций IIa, уровень доказательности A) [6]. Аналогичные положения отражены в отечественных публикациях и рекомендациях по ИБС и ОКС [7–10].
В исследованиях PROMISE (Prospective Multicenter Imaging Study for Evaluation of Chest Pain, всего 10 003 больных) и SCOT-HEART (Scottish Computed Tomography of the Heart; всего 4146 больных) было показано, что КТА по крайней мере так же эффективна, как и стандартные методы диагностики ИБС [11, 12]. В исследовании PROMISE пациенты с неуточненной ИБС были рандомизированы на две группы: пациенты, которым выполнялась КТА, и пациенты, прошедшие нагрузочные тесты на ИБС (из которых в 68% случаев была выполнена сцинтиграфия миокарда по протоколу покой/нагрузка). Конечная точка оценивалась по развитию серьезных неблагоприятных сердечных событий (смерть, инфаркт миокарда, нестабильная стенокардия и осложнения после инвазивных вмешательств, основные процедурные осложнения) на протяжении двухлетнего наблюдения. Следует особо подчеркнуть, что включение КТА в алгоритм обследования пациентов с загрудинной болью ассоциируется с уменьшением случаев острого инфаркта миокарда (ОИМ) как в группе стабильной ИБС, так и в группе ОКС в отдаленном периоде [13]. Метаанализ рандомизированных исследований (включая представленные выше) показал, что применение КТА в качестве альтернативного метода диагностики ИБС снижает риск развития ОИМ на 31% (отношение шансов составило 0,69; 95% доверительный интервал (ДИ) 0,49–0,98) [14]. Например, в исследовании SCOT-HEART выполнение КТА не только улучшило диагностическую достоверность в отношении этиологии ангинозных приступов, но и привело к четырехкратному увеличению назначения аспирина и статинов [15]. Такая тактика, вероятнее всего, и повлияла на снижение случаев ОИМ на 50% в течение 2-летнего наблюдения.
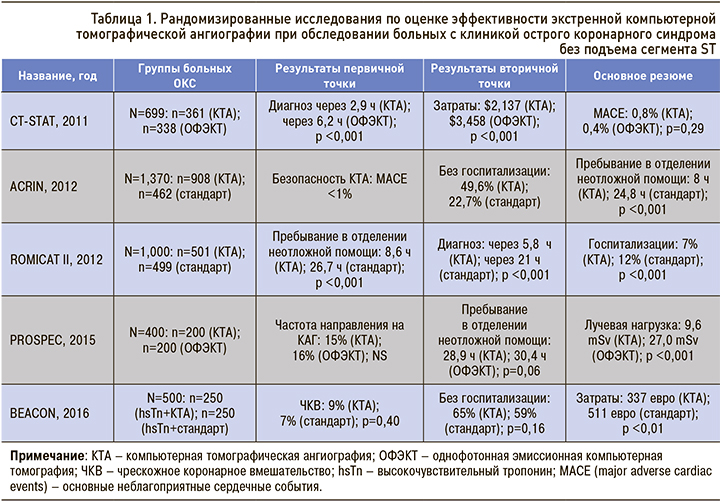
Результаты многоцентровых исследований CT-STAT, ACRIN, ROMICAT II, PROSPEC, DEACON [16] показали эффективность экстренной КТА при обследовании пациентов с подозрением на ОКС без подъема сегмента ST: в группе больных, которым проводилась КТА, по сравнению с группой стандартного обследования быстрее устанавливался диагноз, было меньше ненужных госпитализаций, что привело к значительному сокращению финансовых затрат (табл. 1).
ВЫЯВЛЕНИЕ НЕСТАБИЛЬНЫХ АТЕРОСКЛЕРОТИЧЕСКИХ БЛЯШЕК МЕТОДОМ КТ
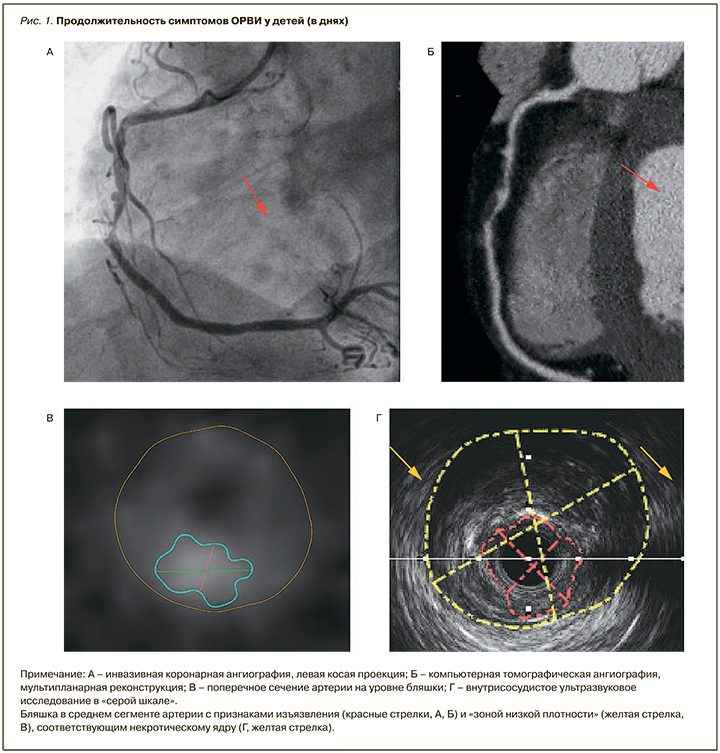
В дополнение к оценке морфологии коронарного русла и выраженности стеноза КТА позволяет оценить непосредственно сосудистую стенку и атеросклеротическую бляшку (АСБ). Отметим, что наличие в АСБ зоны низкой рентгеновской плотности менее 30 единиц Хаунсфилда, которое часто сочетается с феноменом «кольцевидного свечения» (линейный участок повышенной плотности по периферии АСБ), является косвенным КТ-признаком наличия в бляшке большого липидного ядра [17].
В одном из последних анализов результатов исследования PROMISE было доказано, что наличие признаков нестабильности АСБ по данным КТА, таких как наличие участка пониженной плотности в ее структуре с феноменом «кольцевидного свечения» и положительное ремоделирование артерии в месте локализации АСБ, приводило к значительному повышению риска развития острых коронарных событий (скорректированное отношение рисков составило 1,73; 95% ДИ 1,13–2,62) даже после поправки на факторы риска и тяжесть стеноза [18]. Прогностическая ценность нестабильных бляшек по данным КТА была особенно очевидна среди пациентов с необструктивным поражением коронарных артерий.
Результаты приведенных исследований показывают, что в случаях незначительного сужения коронарных артерий функциональные тесты на выявление ишемии могут оказаться неинформативными, в то время как КТА позволяет точно определить степень стеноза, наличие положительного ремоделирования артерии и состав атеросклеротической бляшки по аналогии с внутрисосудистым ультразвуковым исследованием (рис. 1).
ПЕРСПЕКТИВНЫЕ НАПРАВЛЕНИЯ КТ В ДИАГНОСТИКЕ ИБС
Разработка КТ нового поколения, в частности аппараты с широким детектором, позволили значительно улучшить качество изображений за счет возможности одномоментно получать томографические срезы всей области сердца.
Впервые о возможностях КТ с 320 рядами детекторов в оценке перфузии миокарда сообщили
B.S.Ko et al. [19], используя в качестве референтного метода коронарную ангиографию (КАГ) с определением фракционного резерва кровотока (ФРК). КТА выполнялась дважды: в покое (по стандартному протоколу) и повторно на фоне внутривенного введения аденозина. Специфичность КТА в выявлении преходящей ишемии миокарда составила 98%, однако общая диагностическая точность наличия стеноза и преходящего дефекта перфузии по данным КТА составила 80%. Результаты стандартной КТА и КТА с оценкой перфузии совпадали лишь в 58% (дефект перфузии и стеноз ≥50% или отсутствие дефекта перфузии и стеноз ≤50%).
В исследовании A. Nasis et al. [20] данные КТА с оценкой перфузии миокарда сопоставлялись с результатами однофотонной эмиссионной компьютерной томографией (ОФЭКТ). Комплексная оценка состояния коронарного русла и перфузии миокарда по данным КТА улучшали предсказательную ценность метода в диагностике ишемии миокарда: чувствительность, специфичность, положительная и отрицательная предсказательная значимость составили соответственно 94; 98; 94; 98%, а средняя лучевая нагрузка – 9,2±7,4 мЗв по сравнению с 13,2±2,2 мЗв для ОФЭКТ (p <0,001). Данные результаты послужили предпосылкой к многоцентровому исследованию CORE-320, которое включало 381 пациента с болевым синдромом в грудной клетке [21]. Всем пациентам была проведена КТА в покое и на фоне введения аденозина. Данные КТА с оценкой перфузии миокарда сравнивались с результатами референтных методов – ОЭКТ и КАГ. Чувствительность, специфичность, положительная прогностическая значимость, отрицательная прогностическая значимость и точность стандартной КТА составили соответственно 93; 54; 55; 93 и 69%. Те же показатели для КТА с оценкой перфузии составили соответственно 78; 73; 64; 85 и 75%. Чувствительность совмещенного исследования оказалась ниже, а специфичность и общая точность выше, чем при использовании стандартной КТА. Такие результаты являются предпосылкой для дальнейших многоцентровых исследований, направленных на изучение возможностей КТА в выявлении ишемии миокарда.
При обследовании больных с подтвержденной ИБС использование КТА для решения вопроса о целесообразности реваскуляризации остается открытым. Данные большинства клинических исследований по оценке диагностической точности КТА, по сравнению с селективной коронарной ангиографией (КАГ), показали, что визуальная оценка стеноза при КТА, как правило, переоценивает тяжесть поражения. Соответственно интенсивно изучаются методы преодоления этого ограничения для более точной оценки функциональной значимости стеноза. Наиболее актуально определение значимости так называемых пограничных стенозов, которые составляют 50–70% диаметра просвета артерии.
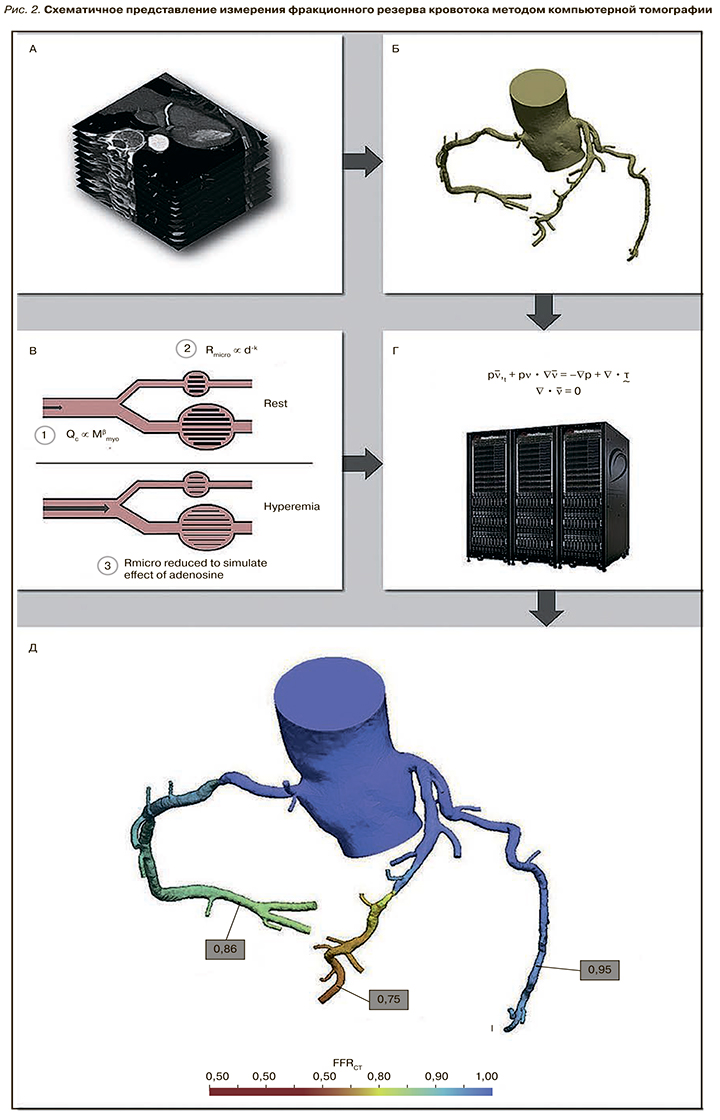
Методом выбора в оценке гемодинамической значимости стеноза коронарной артерии считается инвазивное измерение ФРК, выполняемое одномоментно с селективной КАГ – ФРККАГ [22–25]. В последние годы были разработаны математические 3D-модели для неинвазивного измерения ФРК с помощью постпроцессинговой обработки данных КТА – ФРККТА. Методика определения ФРККТА с помощью математического моделирования на основе принципов гидродинамики показана на рисунке 2.
Начиная с 2011 г. в международных крупномасштабных исследованиях была осуществлена клиническая валидация ФРККТА с инвазивной оценкой ФРК в качестве референтного метода [27–30]. Анализ общих результатов показал, что применение КТА с последующим определением ФРК для решения вопроса о целесообразности реваскуляризации миокарда ассоциировано со снижением числа необоснованных инвазивных диагностических вмешательств, неблагоприятных клинических исходов, улучшением качества жизни пациентов, в особенности пациентов с пограничными стенозами коронарных артерий, и снижением материальных затрат.
ЗАКЛЮЧЕНИЕ
Таким образом, анализ опубликованных исследований показал, что современные разработки в области КТ позволяют расширить рамки стандартного исследования сердца и сосудов. Новые модальности открыли возможность определять анатомические и функциональные параметры, включая состояние просвета коронарных артерий, состава атеросклеротической бляшки, оценку ФРККТА и перфузии миокарда. Выявление признаков нестабильности бляшки методом КТА позволяет проводить раннюю стратификацию риска развития ОКС у больных с различными формами ИБС. В настоящее время оценка перфузии миокарда и ФРККАГ осуществляется в рамках крупномасштабных научных исследований и не является надежным диагностическим инструментом, одобренными официальными рекомендациями. Однако определение этих параметров методом КТА обладает несомненным научным потенциалом и клинической целесообразностью при обследовании больных с «пограничными» стенозами коронарных артерий.


