В медицине не существует аксиом; данные новых исследований, свободный доступ к которым обеспечивает глобальная система медицинской информации, могут менять, порою самым коренным образом, устоявшиеся научные концепции и терапевтические подходы. Так, на наших глазах уходит в прошлое представление о прямой зависимости между селективностью нестероидных противовоспалительных препаратов (НПВП) в отношении циклооксигеназы (ЦОГ)-2 и риском развития кардиоваскулярных катастроф.
 НПВП – эффективное, надежное и удобное средство контроля боли, связанной с повреждением и воспалением. К сожалению, этот класс препаратов не является безопасным: их использование сопряжено с риском целой серии «класс-специфических» нежелательных реакций (НР), среди которых в последнее десятилетие наибольшее значение придается осложнениям со стороны сердечно-сосудистой системы (ССС) [1]. Их патогенез определяется основным фармакологическим действием НПВП – блокадой ЦОГ-2 и опосредованным подавлением синтеза простагландина (ПГ) Е2 и простациклина. Как известно, ЦОГ-2-зависимый синтез ПГЕ2 в ткани почек является одним из важнейших механизмов контроля артериального давления при артериальной гипертензии (АГ), а простациклин, который активно образуется в области атеросклеротических бляшек (на фоне воспаления сосудистой стенки), оказывает мощное антитромботическое действие, препятствуя локальной агрегации тромбоцитов. Соответственно, любые НПВП (как селективные, так и неселективные [н-НПВП] в отношении ЦОГ-2) способны вызывать дестабилизацию АГ и способствовать развитию сосудистых тромбозов [1–3]. Правда, способность н-НПВП обратимо блокировать ЦОГ-1 тромбоцитов (необратимым ингибитором ЦОГ-1 является только аспирин) и подавлять синтез тромбоксана А2 – одного из наиболее мощных факторов, вызывающих агрегацию тромбоцитов, теоретически может снизить их протромботический потенциал. Именно поэтому сформировалось устойчивое мнение, что н-НПВП менее опасны в отношении развития патологии ССС, чем селективные НПВП – коксибы [4, 5].
НПВП – эффективное, надежное и удобное средство контроля боли, связанной с повреждением и воспалением. К сожалению, этот класс препаратов не является безопасным: их использование сопряжено с риском целой серии «класс-специфических» нежелательных реакций (НР), среди которых в последнее десятилетие наибольшее значение придается осложнениям со стороны сердечно-сосудистой системы (ССС) [1]. Их патогенез определяется основным фармакологическим действием НПВП – блокадой ЦОГ-2 и опосредованным подавлением синтеза простагландина (ПГ) Е2 и простациклина. Как известно, ЦОГ-2-зависимый синтез ПГЕ2 в ткани почек является одним из важнейших механизмов контроля артериального давления при артериальной гипертензии (АГ), а простациклин, который активно образуется в области атеросклеротических бляшек (на фоне воспаления сосудистой стенки), оказывает мощное антитромботическое действие, препятствуя локальной агрегации тромбоцитов. Соответственно, любые НПВП (как селективные, так и неселективные [н-НПВП] в отношении ЦОГ-2) способны вызывать дестабилизацию АГ и способствовать развитию сосудистых тромбозов [1–3]. Правда, способность н-НПВП обратимо блокировать ЦОГ-1 тромбоцитов (необратимым ингибитором ЦОГ-1 является только аспирин) и подавлять синтез тромбоксана А2 – одного из наиболее мощных факторов, вызывающих агрегацию тромбоцитов, теоретически может снизить их протромботический потенциал. Именно поэтому сформировалось устойчивое мнение, что н-НПВП менее опасны в отношении развития патологии ССС, чем селективные НПВП – коксибы [4, 5].
Репутация коксибов значительно пострадала после нашумевшей истории с изъятием из обращения рофекоксиба. Это было связано с «кардиотоксичностью» данного препарата, подтвержденной крупными рандомизированными контролируемыми исследованиями (РКИ) и достоверно большей, чем у других НПВП или плацебо [6]. «Тень» от рофекоксиба упала на все селективные НПВП, которые многие эксперты рассматривали как гомогенную группу НПВП, исходя из особенностей их фармакологического действия [4, 5, 7]. Так, например, поступили N. Bhala и соавт., представившие один из последних и наиболее крупных мета-анализов РКИ, в которых определялся риск осложнений со стороны ССС и желудочно-кишечного тракта (ЖКТ) при использовании коксибов, диклофенака, ибупрофена и напроксена [8]. Эта работа включала анализ данных 280 РКИ, в которых различные НПВП сравнивались с плацебо (n=124 513) и 474 РКИ, где НПВП сравнивались с другими препаратами этой группы (n=229 296). Коксибы в этой работе рассматриваются в целом, при этом в сравнении с плацебо относительный риск (ОР) кардиоваскулярных осложнений, включавших инфаркт миокарда (ИМ), инсульт и смерть из-за сосудистых катастроф, составил для этих препаратов 1,37 (95% доверительный интервал [ДИ] 1,14–1,66).
 Повышение риска кардиоваскулярных осложнений более чем на треть – несомненно, серьезная проблема коксибов. Но, как оказалось, среди н-НПВП низкую частоту осложнений со стороны ССС демонстрировал лишь напроксен: ОР 0,93, (95% ДИ 0,69–1,27), а типичные представители н-НПВП диклофенак и ибупрофен не отличались по этому показателю от коксибов: ОР 1,41 (95% ДИ 1,12–1,78) и 1,44 (95% ДИ 0,89–2,33) соответственно. Как видно, исследование N. Bhala и соавт. полностью разрушает концепцию особой «кардиотоксичности» селективных ингибиторов ЦОГ-2: у больных, принимавших типичные н-НПВП, диклофенак и ибупрофен, сосудистые катастрофы возникали столь же часто, как и при использовании коксибов. Любопытно отметить, что «суммарный» анализ показал для коксибов неудовлетворительные результаты в плане риска ЖКТ осложнений – где, казалось бы, эти препараты должны были бы демонстрировать очевидное преимущество в сравнении с н-НПВП. Согласно результатам данного мета-анализа, они значительно чаще вызывали поражение ЖКТ, чем плацебо (ОР 1,81 [95% ДИ 1,17–2,81]) и не отличались по этому показателю от диклофенака (ОР 1,89 [95% ДИ 1,16–3,09]). Впрочем, риск ЖКТ осложнений при использовании ибупрофена и напроксена оказался примерно в 4 раза выше по сравнению с плацебо.
Повышение риска кардиоваскулярных осложнений более чем на треть – несомненно, серьезная проблема коксибов. Но, как оказалось, среди н-НПВП низкую частоту осложнений со стороны ССС демонстрировал лишь напроксен: ОР 0,93, (95% ДИ 0,69–1,27), а типичные представители н-НПВП диклофенак и ибупрофен не отличались по этому показателю от коксибов: ОР 1,41 (95% ДИ 1,12–1,78) и 1,44 (95% ДИ 0,89–2,33) соответственно. Как видно, исследование N. Bhala и соавт. полностью разрушает концепцию особой «кардиотоксичности» селективных ингибиторов ЦОГ-2: у больных, принимавших типичные н-НПВП, диклофенак и ибупрофен, сосудистые катастрофы возникали столь же часто, как и при использовании коксибов. Любопытно отметить, что «суммарный» анализ показал для коксибов неудовлетворительные результаты в плане риска ЖКТ осложнений – где, казалось бы, эти препараты должны были бы демонстрировать очевидное преимущество в сравнении с н-НПВП. Согласно результатам данного мета-анализа, они значительно чаще вызывали поражение ЖКТ, чем плацебо (ОР 1,81 [95% ДИ 1,17–2,81]) и не отличались по этому показателю от диклофенака (ОР 1,89 [95% ДИ 1,16–3,09]). Впрочем, риск ЖКТ осложнений при использовании ибупрофена и напроксена оказался примерно в 4 раза выше по сравнению с плацебо.
Но группа коксибов не может считаться однородной. Относящиеся к ней препараты, а их сегодня осталось всего два – целекоксиб и эторикоксиб, имеют различный профиль безопасности. Так, частота «класс-специфических» осложнений на фоне приема целекоксиба достаточно низка, что позволяет рассматривать этот препарат как один из наиболее удачных представителей группы НПВП. Целекоксиб – весьма популярное лекарство, которое широко используется для контроля боли при различных заболеваниях и патологических состояниях [1]. В частности, целекоксиб прекрасно зарекомендовал себя в качестве эффективного средства для лечения наиболее распространенного заболевания суставов – остеоартрита (ОА). Преимущества этого препарата при ОА подтверждает представленный в 2016 г. C. Xu и соавт. мета-анализ 15 РКИ, в которых целекоксиб сравнивался с плацебо (n=7868). По всем параметрам оценки эффективности целекоксиб достоверно превосходил действие «пустышки». При этом его переносимость оказалась очень хорошей – суммарный риск развития НР на фоне активной терапии и в контроле практически не различался: ОР 1,04 (95% ДИ 0,99–1,09). Правда, при использовании целекоксиба, в сравнении с плацебо, чаще отмечалась диспепсия, но при этом общее число отмен из-за осложнений было примерно одинаковым – ОР 1,12 (95% ДИ 0,82–1,52). Важно то, что использование целекоксиба не повышало риск развития серьезных НР, таких как желудочно-кишечное кровотечение и кардиоваскулярные катастрофы – ОР 0,78 (95% ДИ 0,51–1,19) [9].
 Низкий риск ЖКТ осложнений при использовании целекоксиба подтверждает мета-анализ 52 РКИ (n=51 048). В этой работе оценивали частоту кровотечений и перфораций верхних отделов ЖКТ, тонкой и толстой кишки, развития клинически выраженных язв и анемии (снижение уровня гемоглобина >20 г/л), связанной с кишечной кровопотерей, на фоне приема целекоксиба, н-НПВП и плацебо. Частота этих осложнений составила 1,0, 2,3 и 0,9 эпизода на 100 пациентов-лет соответственно [10].
Низкий риск ЖКТ осложнений при использовании целекоксиба подтверждает мета-анализ 52 РКИ (n=51 048). В этой работе оценивали частоту кровотечений и перфораций верхних отделов ЖКТ, тонкой и толстой кишки, развития клинически выраженных язв и анемии (снижение уровня гемоглобина >20 г/л), связанной с кишечной кровопотерей, на фоне приема целекоксиба, н-НПВП и плацебо. Частота этих осложнений составила 1,0, 2,3 и 0,9 эпизода на 100 пациентов-лет соответственно [10].
В пользу целекоксиба говорят также результаты мета-анализа 28 эпидемиологических исследований (выполненных с января 1980 г. по май 2011 г.), в которых оценивали относительный риск развития ЖКТ осложнений при использовании различных НПВП. Целекоксиб продемонстрировал минимальный риск – отношение шансов (ОШ) составило 1,45 (95% ДИ 1,17–1,81). Аналогичный показатель был получен еще только для одного НПВП – ацеклофенака (ОШ 1,43 [95% ДИ 0,65–3,15]). Для всех других НПВП опасность ЖКТ осложнений была отчетливо выше: при использовании ибупрофена ОШ 1,84 (95% ДИ 1,54–2,20), диклофенака – ОШ 3,34 (95% ДИ 2,79–3,99), мелоксикама – ОШ 3,47 (95% ДИ 2,19–5,50), нимесулида – ОШ 3,83 (95% ДИ 3,2–4,6), кетопрофена – ОШ 3,92 (95% ДИ 2,70–5,69), напроксена – ОШ 4,1 (95% ДИ 3,22–5,23) и индометацина – ОШ 4,14 (95% ДИ 2,19–5,90) [11].
Имеется серьезный клинический материал, показывающий, что риск кардиоваскулярных осложнений при использовании целекоксиба также ниже, чем при использовании всех других НПВП, за исключением напроксена. Это демонстрирует, в частности, масштабная работа S. Trelle и соавт., которые провели мета-анализ 31 РКИ (n=116 429), в которых оценивали число осложнений со стороны ССС для н-НПВП (напроксена, диклофенака, ибупрофена) и с-НПВП (целекоксиба, эторикоксиба, лумирококсиба и рофекоксиба), а контролем служило плацебо. Изучалась суммарная частота эпизодов ИМ, инсульта и смерти вследствие сосудистых катастроф. Согласно полученным данным, целекоксиб имел умеренный кардиоваскулярный риск: ОШ 1,43 (95% ДИ 0,94–2,16). По этому показателю он уступал напроксену – ОШ 1,22 (95% ДИ 0,78–1,93), но был лучше, чем эторикоксиб – ОШ 1,55 (95% ДИ 0,74–3,17), диклофенак – ОШ 1,6 (95% ДИ 0,85–2,99) и ибупрофен – ОШ 2,26 (95% ДИ 1,11–4,89) [12].
Довольно низкую «кардиотоксичность» целекоксиба показывает и мета-анализ 25 популяционных исследований, включавший 18 независимых популяций. Риск развития ИМ при использовании целекоксиба лишь немного превышал аналогичный показатель для напроксена ОР 1,12 (95% ДИ 1,00–1,24) и 1,06 (95% ДИ 0,94–1,20) соответственно. Другие НПВП демонстрировали худшие показатели: ибупрофен – ОР 1,14 (95% ДИ 0,98–1,31), диклофенак – ОР 1,38 (95% ДИ 1,26–1,52), эторикоксиб – ОР 1,97 (95% ДИ 1,35–2,89) [13].
Нужно отметить, что целекоксиб относительно мало влияет на артериальное давление и менее опасен в плане дестабилизации АГ, чем другие НПВП. Это очень важно, поскольку АГ является серьезным фактором риска развития таких жизнеугрожающих осложнений, как ИМ, инсульт и сердечная недостаточность (СН) [14]. В отношении последней патологии ценные данные были получены в недавней работе A. Arfè и соавт., которые провели анализ взаимосвязи между приемом НПВП и развитием СН. В ходе этого ретроспективного исследования проводилось сравнение приема НПВП у 92 163 больных, госпитализированных в связи с СН в Нидерландах, Германии, Великобритании и Италии за период с 2000 г. по 2010 г., и 8 246 403 лиц без данной патологии, составивших соответствующий по полу и возрасту контроль. В среднем прием НПВП ассоциировался с умеренным нарастанием риска СН: ОР 1,19 (95% ДИ 1,17–1,22). Тройку препаратов, показавших наибольший риск развития этой патологии, составили кеторолак – ОР 1,83 (95% ДИ 1,66–2,02), эторикоксиб – ОР 1,51 (95% ДИ 1,41–1,62) и индометацин – ОР 1,51 (95% ДИ 1,33–1,71). Наименьший риск оказался у целекоксиба – ОР 0,96 (95% ДИ 0,90–1,02) [15].
Как видно, имеются серьезные доказательства, что целекоксиб – представитель семейства коксибов, вызывает осложнения со стороны ССС как минимум не чаще, чем любые другие НПВП. Уровень кардиоваскулярного риска при использовании этого препарата фактически такой же, как у напроксена, который практически всеми ведущими экспертами считается наиболее «кардиобезопасным» НПВП [1, 2, 7].
Однако окончательно подтвердить данный факт, крайне важный для реальной клинической практики, могло лишь хорошо организованное РКИ. И такое исследование было, наконец, выполнено.
Публикация результатов РКИ PRECISION (Prospective Randomized Evaluation of Celecoxib Integrated Safety vs. Ibuprofen Or Naproxen), состоявшаяся в конце 2016 г., – давно ожидаемое и яркое научное событие. Впервые в мире была выполнена масштабная работа, где частота НР при использовании НПВП специально изучалась на популяции больных с высоким кардиоваскулярным риском [16]. В ходе этого исследования оценивали применение трех НПВП – целекоксиба, ибупрофена и напроксена у 24 081 больного ОА и ревматоидным артритом (РА) с выраженными болями, требующими регулярной анальгетической терапии. Основным критерием отбора пациентов для участия в PRECISION стало наличие установленного кардиологического заболевания или высокий суммарный кардиоваскулярный риск. Ниже приведены конкретные критерии включения [17]:
- АГ;
- дислипидемия: ЛПНП >160 мг/ дл (4,1 ммоль/л) или ЛВП <35 0="" 9="" li="">
- прием статинов, фибратов, омега-3-содержащих препаратов;
- курение (в течение последних 30 дней или > 15 сигарет в день);
- наследственный анамнез по заболеваниям ССС;
- наличие в анамнезе микроальбуминурии;
- гипертрофия миокарда левого желудочка, подтвержденная данными ЭКГ.
В проведении PRECISION были задействованы более 1000 исследовательских центров в 16 странах мира. На сегодняшний день это одно из наиболее крупных исследований безопасности НПВП. Правда, по своим масштабам PRECISION уступает программе MEDAL, в которой сравнивали эторикоксиб в дозе 90 и 60 мг/сут и диклофенак в дозе 150 мг/сут у 34 701 больного ОА и РА [18]. Хотя основной целью программы MEDAL также была оценка НР со стороны ССС, ее критерии включения не предполагали наблюдения группы больных со столь высоким кардиоваскулярным риском, как в PRECISION. В этом можно убедиться, сравнив характеристику исследуемых групп в данных работах (табл. 1).
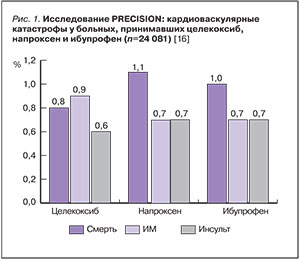
Исследование PRECISION предполагало гибкую систему назначения НПВП, и в зависимости от выраженности боли суточная доза препаратов могла меняться: целекоксиб от 100 до 200 мг 2 раза/сут, ибупрофен – от 600 до 800 мг 3 раза/ сут, напроксен – от 375 до 500 мг 2 раза/сут. При этом, учитывая высокий риск ЖКТ осложнений, все больные в течение всего срока исследования получали ингибитор протонной помпы эзомепразол в дозе 20–40 мг/сут. Минимальный срок активной фазы исследования должен был составить 18 мес с дальнейшим амбулаторным наблюдением до 3-х лет. В итоге средняя продолжительность лечения составила 20,3±16,0 мес, а средний срок наблюдения – 34,1±13,4 мес. Основными критериями оценки являлась частота сосудистых катастроф (смерти от заболеваний ССС, нефатальных ИМ и инсультов). Частота этих осложнений в группе целекоксиба оказалась как минимум не выше, чем у принимавших напроксен и ибупрофен (оценка ITT, Intention-to-Treat Population, рис. 1).
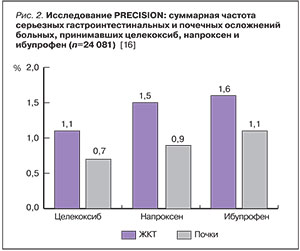
Важно отметить, что целекоксиб реже вызывал дестабилизацию АГ, потребовавшей госпитализации (0,3%), чем напроксен (0,4%, отличие статистически незначимо) и ибупрофен (0,5%, р<0,05). В отношении госпитализаций по поводу СН отличия между исследуемыми препаратами не было: их частота во всех трех группах составила по 0,6%. При этом суммарная оценка серьезных осложнений со стороны ЖКТ, включая развитие выраженной железодефицитной анемии, показала статистически значимое преимущество целекоксиба в сравнении с напроксеном и ибупрофеном. Частота ренальных осложнений в группе целекоксиба была статистически значимо ниже, чем в группе ибупрофена; между группами целекоксиба и напроксена различий в частоте этой патологии выявлено не было (оценка ITT, рис. 2).
Таким образом, исследование PRECISION показало, что частота развития сосудистых катастроф на фоне длительного приема целекоксиба, даже у пациентов с высоким кардиоваскулярным риском, не выше, чем при использовании н-НПВП, в т.ч. напроксена, который традиционно считается наиболее «кардиобезопасным» препаратом этой группы. При этом число летальных исходов, связанных с ИМ, инсультом и внезапной коронарной смертью у больных, принимавших целекоксиб, оказалось даже несколько меньше (правда, статистически незначимо), чем у лиц, получавших напроксен и ибупрофен.
В отношении негативного влияния на ЖКТ, даже с учетом того факта, что все больные получали эффективную гастропротективную терапию, целекоксиб оказался безопаснее препаратов сравнения. В сравнении с ибупрофеном он также статистически значимо реже вызывал осложнения со стороны почек.
Напрашивается совершенно очевидный вывод: в соответствие с результатами PRECISION, целекоксиб по всем параметрам оказался более безопасным препаратом, чем н-НПВП.
Следует напомнить, что в упомянутой выше программе MEDAL другой представитель группы коксибов – эторикоксиб продемонстрировал далеко не столь блестящие результаты. Правда, число кардиоваскулярных осложнений при использовании эторикоксиба и диклофенака не различалось, их суммарное число составило 1,24 и 1,30 на 100 пациентов/лет [18]. Но диклофенак, по данным многочисленных РКИ и популяционных исследований, существенно чаще вызывает осложнения со стороны ССС, чем другие НПВП, поэтому сравнение с таким препаратом едва ли говорит в пользу эторикоксиба. Кроме того, эторикоксиб в обеих дозировках достоверно чаще вызывал дестабилизацию АГ, чем диклофенак [18, 19]. Но при этом, что принципиально важно, эторикоксиб не показал какого-либо преимущества в сравнении с диклофенаком в отношении развития серьезных ЖКТ осложнений, их число составило 0,30 и 0,32 на 100 пациентов/лет [18, 20].
Таким образом, результаты исследования PRECISION закрывают тему о «класс-специфическом» повышении риска осложнений со стороны ССС при использовании селективных ингибиторов ЦОГ-2. Опасность развития любых НР, связанных с НПВП, – как кардиоваскулярной патологии, так и поражения ЖКТ, определяется индивидуальными параметрами конкретного представителя данной лекарственной группы, его биохимическими свойствами и особенностями фармакокинетики. Оценивать безопасность НПВП, ориентируясь на формальные фармакологические характеристики тех или иных НПВП, в т.ч. селективность в отношении ЦОГ-2, сегодня представляется ошибочным. Ведь клинический опыт опровергает теоретические рассуждения. Так, по данным серии РКИ, типичный н-НПВП ибупрофен в высоких дозах достаточно часто вызывает осложнения со стороны ССС, а наиболее селективный ЦОГ-2 ингибитор эторикоксиб (по результатам MEDAL) демонстрирует частоту ЖКТ кровотечений, равную диклофенаку.
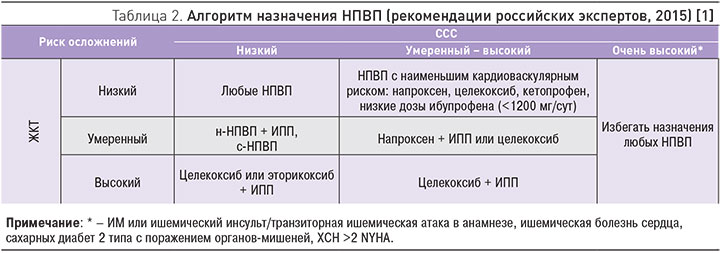
Новые данные по безопасности целекоксиба имеют и чисто практический аспект. Они убедительно подтверждают правильность схемы рационального применения НПВП, разработанной российскими экспертами и представленной в печати в начале 2015 г. (табл. 2). Тем не менее, поскольку целекоксиб демонстрирует очевидное преимущество при комбинированной оценке безопасности (кардиоваскулярная + ЖКТ) в сравнении с напроксеном, его следует поставить на первое место в вертикальном столбце «умеренный–высокий кардиоваскулярный риск» как препарат выбора в данной клинической ситуации.
Разумеется, даже самые благоприятные результаты в отношении применения целекоксиба у больных с высоким кардиоваскулярным риском не могут менять принципиальной рекомендации российских экспертов не использовать любые НПВП у лиц, перенесших кардиоваскулярные катастрофы и/или имеющих клинически выраженную ишемическую болезнь сердца.



