В практике современного врача встречается огромное количество схожих и перекрестных симптомов и синдромов, составляющих клиническую картину заболевания, которые требуют тщательного дифференциально-диагностического подхода на пути верификации диагноза. В связи с этим особое место занимают диффузные заболевания соединительной ткани (ДЗСТ). Но даже среди этой группы встречается заболевание, отличающееся разнообразием клинической картины, свойственной нескольким ревматологическим диагнозам.
Синдром Шарпа [синонимы: смешанное заболевание соединительной ткани (СЗСТ), недифференцированное заболевание соединительной ткани] представляет собой смешанное заболевание соединительной ткани аутоиммунного генеза, характеризующееся наличием отдельных признаков системной красной волчанки (СКВ), ревматоидного артрита (РА), системной склеродермии (ССД) и дерматомиозита/полиомиозита в сочетании с высоким титром антител к ядерному рибонуклеопротеину U1-RNP. Как самостоятельная нозологическая форма выделен Г. Шарпом и соавт. в 1972 г. Частота встречаемости составляет всего 2 на 100 000 человек. Преимущественно болеют люди старше 30 лет; соотношение случаев заболевания у женщин и мужчин от 9:1 до 16:1 [1].
ЭТИОЛОГИЯ, ДИАГНОСТИКА, ПРОГНОЗ
Сегодня основными этиологическими факторами возникновения синдрома Шарпа являются генетические механизмы, так как описаны случаи заболевания у близких родственников с одним HLA-фенотипом. Так, у 66% пациентов повышенный титр АТ RNP ассоциируется с HLA-DR4-фенотипом. Существуют предположения, что имеется мимикрия между 33 полипептидом U1-RNP и аналогичным компонентом в ретровирусах животных организмов. В основе патогенеза заболевания лежат иммунные нарушения, которые проявляются высоким титром U1-RNP (антинуклеарных антител, относящихся к IgG, крапчатого вида свечения при непрямой иммунофлюоресценции), снижение супрессорной функции Т-лимфоцитов за счет пенетрации U1-RNP-антител Th II типа посредством Fc-рецепторов, образование циркулирующих иммунных комплексов (ЦИК) и снижение уровня компонентов комплемента [2].
Для синдрома Шарпа характерна полиморфная клиническая картина, включающая синдром Рейно, поражение кожи, суставов, мышц, легких, ЖКТ и реже поражения сердца, почек и ЦНС (табл. 1).
Необходимо отметить, что суставной синдром встречается в 3/4 случаев и проявляется артритом (проксимальных межфаланговых, пястно-фаланговых и лучезапястных суставов), сходным с ревматоидным, но без прогрессирующего поражения суставного хряща и эпифизов. Иногда наблюдаются аваскулярные некрозы головок бедренных костей вследствие поражения сосудистой стенки, остеолиз ногтевых фаланг, а также синдром Тибержа–Вейсенбаха (отложение в мягких тканях конечностей глыбок кальция). У 2/3 больных определяется кожный синдром, характеризующийся отечностью рук («сосискообразные пальцы») без индурации и атрофии в отличие от ССД. Очень редко наблюдаются изъявления и в своем исходе гангрена кончиков пальцев. Высыпания в области скул имеют вид эритематозной сыпи, как при СКВ, но без дальнейшего рубцевания. Зачастую у больных с синдромом Шарпа можно наблюдать одни из основных симптомов дерматомиозита – «лиловые очки» (периорбитальный отек с фиолетовым оттенком) и эритематозные пятна над суставами рук. У 70% пациентов диагностируется поражение пищевода в виде дисфункций, редко вызывающих жалоб. В основном это снижение амплитуды перистальтики и давления сфинктера, что приводит к рефлюкс-эзофагиту со всеми своими отдаленными последствиями. Крайне редко в патологический процесс вовлекаются другие отделы ЖКТ. Одним из самых грозных, но редких осложнений СЗСТ является поражение легких в виде интерстициального пневмонита, экссудативного плеврита. Наблюдаемая инфильтрация пораженных тканей лимфоцитами и плазматическими клетками, осуществляемая в среднем и внутреннем слоях крупных сосудов, приводит к местным пролиферативным реакциям и развитию одного из самых тяжелых осложнений данного заболевания – легочной гипертензии [2, 3]. Данные осложнения приводят к значительному снижению показателей функции внешнего дыхания (ФВД) и качества жизни. Поражение сердца – еще более редкое проявление синдрома Шарпа, чем поражение легких. Проявляется экссудативным перикардитом, миокардитом, пролапсом митрального клапана и аортальной недостаточностью. Клиническая картина поражения почек при синдроме Шарпа обусловлена тем, что депозиты комплемента и IgG и IgM обнаруживаются в дермоэпителиальном стыке, в стенках сосудов мышц и клубочков почек. В сравнении с волчаночным нефритом при СКВ мембранозная нефропатия в данном случае носит относительно доброкачественный характер, что отдельные авторы связывают с протективной функцией анти U1-RNP. Напротив, высокий титр антител к двухцепочечной ДНК (anti-dsDNA) обусловливает более тяжелое поражение почек при СКВ. Также описаны случаи неврологических осложнений (поражение тройничного нерва, полинейропатии, церебральный васкулит, менингит, эпилепсия) [1].
 Необходимо упомянуть, что начало синдрома Шарпа может протекать в различных клинических вариантах:
Необходимо упомянуть, что начало синдрома Шарпа может протекать в различных клинических вариантах:
- преимущественно с сосудистыми проявлениями (синдром Рейно, легочная гипертензия, антифосфолипидный синдром);
- по полимиозитоподобному варианту (миозиты, интерстициальное поражение легких, гипотония пищевода);
- с эрозивным полиартритом, склеродактилией, положительным АЦЦП.
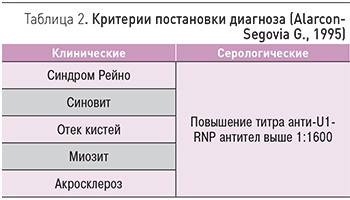
СЗСТ выражаются целым комплексом клинико-иммунологических синдромов системного воспалительного поражения соединительной ткани, что не позволяет точно определить границы данной нозологии и существенно затрудняет диагностику. Однако систематическое выявление у пациентов (78,2%) с данной патологией U1-RNP-антител, направленных против белков рибонуклеопротеина, содержащего U1 малую ядерную рибонуклеиновую кислоту, позволяет говорить о том, что данные антитела являются маркерами синдрома Шарпа [1]. Что касается показателей общеклинических лабораторных исследований, то они довольно неспецифичны: у 1/3 пациентов наблюдается анемия, лейкопения, повышение СОЭ, наиболее редко тромбоцитопения [4]. Для постановки диагноза СЗСТ используются следующие серологические и клинические критерии (Alarcon-Segovia G., 1995) (табл. 2): положительная реакция на анти-U1-РНП-антитела в титре 1:1600 и выше; отек кистей, синовит, миозит, синдром Рейно, акросклероз [1]. В соответствии с этими критериями диагноз «синдром Шарпа» наиболее достоверен при наличии серологического и по крайней мере 3 клинических критериев [2]. В случае преобладания у больного 3 «склеродермических маркеров», таких как отек кистей, синдром Рейно и акросклероз, необходимо учитывать четвертый признак (миозит или синовит). Критерием исключения диагноза является положительный тест на анти-Sm-антитела [1].
 Прогноз «синдрома Шарпа», как правило, благоприятный. Возможна полная клиническая ремиссия. Ухудшению прогноза заболевания способствует наличие легочной гипертензии, поражения почек и тяжелого синдрома Рейно.
Прогноз «синдрома Шарпа», как правило, благоприятный. Возможна полная клиническая ремиссия. Ухудшению прогноза заболевания способствует наличие легочной гипертензии, поражения почек и тяжелого синдрома Рейно.
РАЗБОР КЛИНИЧЕСКОГО СЛУЧАЯ БОЛЬНОЙ С СИНДРОМОМ ШАРПА
Пациентка Ш., 46 лет, жительница г. Перми, была госпитализирована в 22 ревматологическое отделение ГКБ № 15 им. О.М. Филатова г. Москвы в плановом порядке по программе «Москва – столица здоровья» в феврале 2018 г. При поступлении в стационар предъявляла жалобы на периодическое побеление, посинение кончиков пальцев кистей обеих рук, боли в икроножных мышцах, лучезапястных и коленных суставах, снижение массы тела на 17 кг за 4 мес.
Со слов пациентки, считает себя больной с июля 2017 г., когда на отдыхе в г. Сочи при подъеме на высокогорье появились первые симптомы в виде инспираторной одышки. Пациентка расценила данный приступ как проявление смены климата. Одышка купировалась через сутки после самостоятельного приема пациенткой таблетки фуросемида 40 мг. Через 2–3 дня на фоне незначительной физической нагрузки аналогичный приступ повторился, но купировался самостоятельно с последующим появлением боли в икроножных мышцах («как после перенапряжения»).
 После возвращения домой в г. Пермь пациентка отметила симметричный отек кистей рук, а также появление умеренно болезненных уплотнений округлой формы на ладонной поверхности пальцев рук. Самостоятельно применяла глюкокортикостероидные мази без значимого эффекта. Спустя месяц пациенткой впервые было отмечено посинение кончиков пальцев рук, в связи с чем она обратилась к кардиологу по месту жительства.
После возвращения домой в г. Пермь пациентка отметила симметричный отек кистей рук, а также появление умеренно болезненных уплотнений округлой формы на ладонной поверхности пальцев рук. Самостоятельно применяла глюкокортикостероидные мази без значимого эффекта. Спустя месяц пациенткой впервые было отмечено посинение кончиков пальцев рук, в связи с чем она обратилась к кардиологу по месту жительства.
Кардиологом был выставлен диагноз «гипертоническая болезнь II ст., 3 ст., риск 3. ИБС? ХСН I/II ФК». Пациентке была выполнена ЭхоКГ, по результатам которой была выявлена гипертрофия миокарда левого желудочка, митральная и трикуспидальная регургитация 1 ст.; фракция выброса левого желудочка удовлетворительная. На основании лабораторных исследований крови (Hb – 114,7 г/л, MCH – 26,96 пг, MCHC – 314 г/л, железо сыворотки – 6,4 мкмоль/л) также был выставлен диагноз «анемия железодефицитная легкой степени тяжести». Пациентке рекомендован трипликсам по 10 мг 1 раз в день и консультация ангиохирурга.
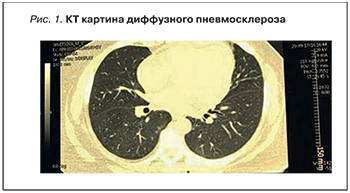
При посещении ангиохирурга сосудистой патологии не было выявлено. Еще через месяц пациентку стали беспокоить скованность и болезненность при движениях в локтевых суставах, а также боли в икроножных мышцах, в связи с чем обратилась к ревматологу. На основании всех вышеперечисленных жалоб был выставлен диагноз «синдром Рейно». В течение месяца проводилось лечение препаратом метипред, рекомендованное ревматологом, без положительного эффекта. Эпизоды одышки не прекратились, в связи с чем была назначена компьютерная томография (КТ) органов грудной клетки, которая выявила очаги диффузного пневмосклероза и наличие жидкости в перикарде (рис. 1). По данным спирометрии патологии не выявлено.
В октябре 2017 г. к вышеперечисленным жалобам присоединились зябкость кистей, сухость и зуд кожи, высыпания на коже груди, живота, гиперемия лица. Пациентка обратилась в ревматологическое отделение краевой клинической больницы г. Перми, была госпитализирована.
Проведено лечение: метипред – по 8 мг утром, плаквенил – по 400 мг на ночь, курантил – по 75 мг, пентоксифиллин 2% – 5,0 в/в кап., верошпирон – по 5 мг утром, амлодипин – по 5 мг на ночь, каптоприл – по 25 мг, метопролол – по 25 мг, омепразол – по 20 мг вечером, электрофорез никотиновой кислотой и эуфиллина на кисти. Выписана с незначительным улучшением.
 Настоящее ухудшение произошло в феврале 2018 г., когда ко всем вышеперечисленным жалобам присоединилось онемение в области языка и носогубных складок. При общем осмотре состояние было удовлетворительное, сознание ясное, положение активное. Телосложение пациентки гиперстеническое: рост 166 см, вес 103 кг. Кожные покровы обычной окраски, влажные. Видимые слизистые розового цвета, чистые. Подкожно-жировая клетчатка выражена, пастозность кистей, голеней и стоп. Мышцы голеней умеренно болезненны, тонус сохранен с обеих сторон. Суставы при пальпации безболезненны, при движении умеренная болезненность в локтевых и коленных суставах. В области ладоней и пальцев рук наблюдаются посинение и покраснение, дистальные участки конечностей холодные на ощупь (рис. 2). Тоны сердца ритмичные, АД 140/90 мм рт.ст., ЧСС 72 уд/мин. При аускультации легких было выявлено жесткое дыхание без хрипов, ЧДД 17 в мин.
Настоящее ухудшение произошло в феврале 2018 г., когда ко всем вышеперечисленным жалобам присоединилось онемение в области языка и носогубных складок. При общем осмотре состояние было удовлетворительное, сознание ясное, положение активное. Телосложение пациентки гиперстеническое: рост 166 см, вес 103 кг. Кожные покровы обычной окраски, влажные. Видимые слизистые розового цвета, чистые. Подкожно-жировая клетчатка выражена, пастозность кистей, голеней и стоп. Мышцы голеней умеренно болезненны, тонус сохранен с обеих сторон. Суставы при пальпации безболезненны, при движении умеренная болезненность в локтевых и коленных суставах. В области ладоней и пальцев рук наблюдаются посинение и покраснение, дистальные участки конечностей холодные на ощупь (рис. 2). Тоны сердца ритмичные, АД 140/90 мм рт.ст., ЧСС 72 уд/мин. При аускультации легких было выявлено жесткое дыхание без хрипов, ЧДД 17 в мин.
По данным клинических исследований были установлены следующие отклонения: креатинин – 103 мкмоль/л, АСТ – 34 Ед/л, КФК – 469 Ед/л, ЛДГ – 467 Ед/л, СРБ – 8,25 мг/л, IgG – 17,9 г/л, RNP (68kD\A\C) обнаружено; Sm/RNP обнаружено; ANA-screen индекс позитивности 11,8.
На УЗИ органов брюшной полости: УЗ-признаки гепатомегалии, диффузных неспецифических изменений печени и поджелудочной железы, неполное удвоение почек.
 При проведении ЭхоКГ определены дилатация предсердий, утолщение межжелудочковой перегородки, ускорение потока на аортальном клапане, митральная и трикуспидальная регургитация, показатели локальной и глобальной систолической функции ЛЖ сердца в пределах нормы. Перикард без патологии. Уплотнение стенок аорты.
При проведении ЭхоКГ определены дилатация предсердий, утолщение межжелудочковой перегородки, ускорение потока на аортальном клапане, митральная и трикуспидальная регургитация, показатели локальной и глобальной систолической функции ЛЖ сердца в пределах нормы. Перикард без патологии. Уплотнение стенок аорты.
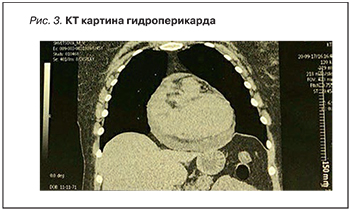
По результатам КТ органов грудной клетки свежих очаговых и инфильтративных изменений в легких не обнаружено, при сравнении с предоставленным исследованием от 20.09.2017 не отмечено видимой динамики. Выявлены незначительное количество жидкости в полости перикарда (рис. 3), атеросклероз аорты и коронарных артерий, медиастинальная и аксиллярная лимфаденопатия.
В условиях 22 ревматологического отделения на основании жалоб, анамнеза и проведенных исследований был выставлен основной диагноз «смешанное заболевание соединительной ткани, хроническое течение, средняя активность: артралгии, артриты, миалгии, повышение КФК, перикардит, синдром Рейно, лимфаденопатия, иммунологические изменения (RNP(68kD\A\C; Sm/RNP), ANA «+». Сопутствующий диагноз: «артериальная гипертензия II ст., 2 ст., риск ССО 3. Неалкогольная жировая болезнь печени. Ожирение 2 ст».
Пациентке проводилось и была рекомендована на постоянный прием следующая терапия:
- микофенолата мофетил – по схеме длительно;
- преднизолон (по 20 мг/сут) или метилпреднизолон (по16 мг/сут) с последующим решением вопроса о снижении дозы по рекомендации ревматолога по месту жительства;
- препараты кальция – по 1000 мг/сут;
- ацетилсалициловая кислота – по 100 мг/сут;
- амлодипин – по 10 мг/сут под контролем уровня артериального давления.
На фоне проводимой терапии за время пребывания в стационаре ГКБ № 15 им. О.М. Филатова г. Москвы пациентка отмечает улучшение самочувствия, явления синдрома Рейно значительно уменьшились, боли в суставах и мышцах купировались, одышка не беспокоит. Выписана для продолжения наблюдения и лечения у ревматолога по месту жительства (рис. 4).
ЗАКЛЮЧЕНИЕ
Полярность мнений относительно необходимости и целесообразности выделения синдрома Шарпа как самостоятельной нозологии уже не одно десятилетие волнует ревматологические сообщества не только в России, но и за рубежом. Сочетание симптомов, в разной степени свойственных различным ДЗСТ, объясняет диагностические затруднения при распознавании данного синдрома. Особенностью и трудностью дифференциальной диагностики представленного клинического случая стали проявления дебюта заболевания, которой включил не кожно-суставные проявления синдрома Рейно, а симптомы дыхательной недостаточности и поражение листков перикарда. Течение заболевания подобного рода диктует необходимость глобального пересмотра концепции типичных клинических проявлений данного синдрома (синдром Рейно, полиартрит, миозит).
Кроме того, следует повторить, что необходим тщательный дифференциально-диагностический поиск для выявления истинного диагноза заболеваний соединительной ткани, для которых в различной степени выраженности характерны проявления синдрома Шарпа.




