Наследственный ангиоотек (НАО) – потенциально жизнеугрожающее, генетически детерминированное, орфанное заболевание. На сегодняшний момент очень остро стоят проблемы гиподиагностики этого заболевания. Задержка постановки диагноза НАО даже в развитых странах составляет не менее 5 лет, тогда как в России эта цифра колеблется от 13 до 20 лет. Учитывая распространенность заболевания в общей популяции – примерно 1:10 000–150 000 человек – и общее население РФ (147 млн человек), можно предположить, что пациентов с этим диагнозом должно быть от 2940 до 4900 чел. Вместе с тем на сегодня количество зарегистрированных в федеральном регистре больных составляет лишь чуть больше 200 человек. Пациенты без диагноза НАО годами наблюдаются у врачей различных специальностей, имея массу других диагнозов, подчас самых невероятных, и вследствие этого остаются без патогенетически обоснованной специализированной медицинской помощи, подвергаются необоснованным оперативным вмешательствам и погибают от фатальной асфиксии.
Помимо низкой информированности врачебного сообщества о НАО, ключевой проблемой, не позволяющей адекватно помочь пациентам с этим заболеванием, является отсутствие организованного взаимодействия между специалистами различных профилей (аллергологами-иммунологами, врачами скорой и неотложной медицинской помощи, терапевтами, хирургами, стоматологами, дерматовенерологами, анестезиологами-реаниматологами, педиатрами, генетиками, акушерами-гинекологи, гематологами и т.д.), которые могут столкнуться с данной категорией пациентов [1]. До настоящего времени маршрутизация пациентов с подозрением на НАО недостаточно скоординирована. Это происходит во всех субъектах РФ даже при полноценной государственной гарантии лекарственного обеспечения пациентов, страдающих НАО. Целью настоящей статьи является привлечь внимание врачей различных специальностей к этой проблеме.
НАО относится к группе первичных иммунодефицитов с аутосомно-доминантным наследованием и неполной пенетрантностью, которое связано с качественным или количественным генетически детерминированным дефектом генов, кодирующих синтез ингибитора эстеразы компонента комплемента C1. НАО проявляется в виде рецидивирующих отеков кожи и слизистых оболочек дыхательных путей, желудочно-кишечного и урогенитального трактов.
Код по МКБ-10: D 84.1 – дефект в системе комплемента.
ПАТОГЕНЕЗ И КЛАССИФИКАЦИЯ
Дефицит ингибитора С1-эстеразы и ряда других факторов приводят к нарушению ингибирования С1r и C1s компонентов комплемента. Следствием этого становится увеличение образования брадикинина из кининогена. Брадикинин взаимодействует с рецепторами к брадикинину 2 типа на эндотелиальных клетках, что ведет к повышению проницаемости капилляров, экстравазации внутрисосудистой жидкости и в совокупности образованию отека.
К характерным особенностям отека при НАО относятся отсутствие зуда, гиперемии кожи, сопутствующей крапивницы, отсутствие эффекта от лечения глюкокортикостероидами (ГКС) и антигистаминными препаратами.
Типы НАО приведены в таблице 1.

Первый тип НАО характеризуется аутосомно-доминантным типом наследования и встречается у 80–92% всех пациентов. Болезнь отличается абсолютным количественным дефицитом ингибитора С1 фактора комплемента (C1INH), при этом уровень его варьирует в пределах 5–30% от нормальных значений.
Второй тип НАО (15% среди всех типов НАО) отличается снижением функциональной активности C1INH, хотя уровень С1-ингибитора может оставаться в пределах или быть несколько выше нормы.
Третий тип НАО характеризуется нормальными или почти нормальными антигенными и функциональными уровнями C1INH. Ранее его называли эстрогензависимым вариантом ангиоотека. В настоящее время выделяют группу пациентов с рецидивирующими ангиоотеками и семейным анамнезом заболевания, у которых была выявлена локализованная в V хромосоме мутация в гене, кодирующем XII фактор свертываемости крови. Наличие указанного генетического дефекта влечет за собой изменение его функциональной активности и, как следствие, нарушение кининового профиля, что приводит к повышению продукции брадикинина.
ОСОБЕННОСТИ КЛИНИЧЕСКОГО ТЕЧЕНИЯ НАСЛЕДСТВЕННОГО АНГИООТЕКА
Обычно НАО дебютирует в первые 2 десятилетия жизни, чаще в пубертатный период. У 40% больных заболевание развивается в возрасте до 5 лет, у 50% – до 10 лет. В пубертатном периоде течение заболевания может утяжелиться в связи с гормональной перестройкой организма.
Как правило, при рождении и в раннем детском возрасте (за исключением редких случаев) НАО ничем себя не проявляет. Тем не менее случаи отека верхних дыхательных путей бывают и у детей, причем у них из-за меньшего диаметра дыхательных путей асфиксия развивается быстрее. Частота приступов НАО – в значительной степени варьирующийся показатель. Отличительной чертой НАО является постепенная динамика симптомов: отеки достаточно медленно нарастают в течение 12–36 ч и разрешаются в течение 2–5 дней, тогда как абдоминальные симптомы исчезают в течение 12–36 ч.
К потенциальным триггерам обострения НАО относятся:
- механическая травма, интенсивность которой может быть разной – от легкого сдавления одеждой или легкого ушиба до перелома кости;
- хирургическое вмешательство, малоинвазивные диагностические процедуры, экстракция зуба;
- прием некоторых лекарственных средств: ингибиторов АПФ, пероральных эстрогенсодержащих контрацептивов, препаратов гормонозаместительной терапии;
- инфекции, стресс, алкоголь.
Клиническая картина НАО характеризуется появлением рецидивирующих плотных, безболезненных незудящих отеков, локализующихся практически на любых участках тела: верхних и нижних конечностях (руки, стопы, бедра и др.), на лице (периорбитальная область, губы), в полости рта (язык, мягкое нёбо), на шее, туловище, конечностях, слизистых оболочках верхних отделов дыхательных путей и урогенитального тракта.
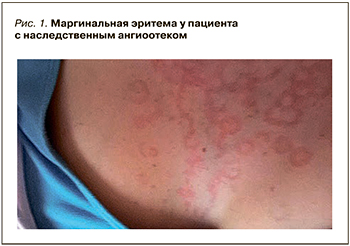 Атаки НАО обычно идут по предсказуемому пути. Многие из них начинаются с продрома или ауры: у пациента обычно наблюдаются дрожь, покалывание, слабость, разбитость, мраморность кожи. Зуд и крапивница для НАО не характерны, однако примерно треть всех случаев ангиоотеков сопровождается кольцевидной или маргинальной эритемой (erithemaannulare), обильными бледными высыпаниями мультиформного характера, не сопровождающимися зудом, жжением и местной гиперемией (рис. 1). Продромальный период предшествует приступу за несколько часов или за день (продолжительность предшествующих симптомов – до 1 дня) у 50% пациентов с НАО [3]. Также достаточно часто в период продрома встречаются гриппоподобные состояния, парестезии, усталость, нарушение пищеварения, неспецифическая сыпь и другие неспецифические симптомы.
Атаки НАО обычно идут по предсказуемому пути. Многие из них начинаются с продрома или ауры: у пациента обычно наблюдаются дрожь, покалывание, слабость, разбитость, мраморность кожи. Зуд и крапивница для НАО не характерны, однако примерно треть всех случаев ангиоотеков сопровождается кольцевидной или маргинальной эритемой (erithemaannulare), обильными бледными высыпаниями мультиформного характера, не сопровождающимися зудом, жжением и местной гиперемией (рис. 1). Продромальный период предшествует приступу за несколько часов или за день (продолжительность предшествующих симптомов – до 1 дня) у 50% пациентов с НАО [3]. Также достаточно часто в период продрома встречаются гриппоподобные состояния, парестезии, усталость, нарушение пищеварения, неспецифическая сыпь и другие неспецифические симптомы.
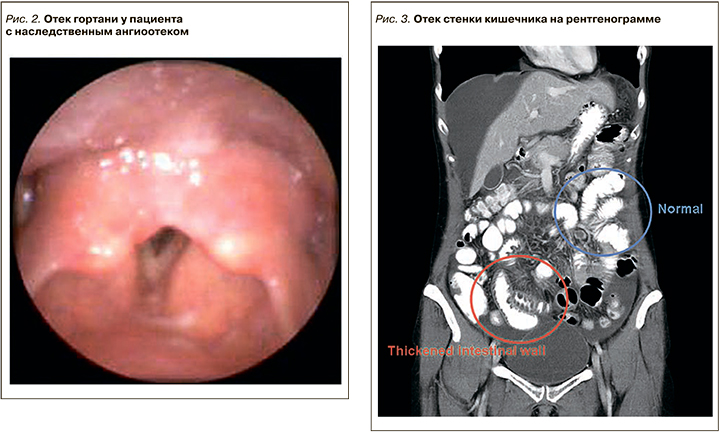
При поражении верхних дыхательных путей отек обычно располагается выше гортани, захватывая губы, язык и глотку. Ангиоотек может распространяться на верхние дыхательные пути с вовлечением пищевода, гортани и проявляться дисфагией, дисфонией, симптоматикой обструкции дыхательных путей, напоминающей в ряде случаев бронхиальную астму, и прогрессировать вплоть до асфиксии. Отеки гортани (рис. 2), проявляющиеся осиплостью голоса, афонией, стридорозным дыханием, хотя бы один раз в жизни отмечаются у 50% больных. В тяжелых случаях они приводят к асфиксии и смерти. До 25% больных погибают от отека гортани в возрасте до 30 лет.
При вовлечении слизистых оболочек различных органов развивается следующая клиника НАО:
- со стороны пищевода – дисфагия;
- желудок – тошнота, рвота;
- кишечник – боли в животе, признаки кишечной непроходимости;
- мочевой пузырь – дизурия, анурия;
- мозговые оболочки, внутреннее ухо – тошнота, рвота, головокружение, менингеальные симптомы.
У более половины больных НАО наблюдаются выраженные абдоминальные отеки, вызванные отеком различных участков слизистой оболочки желудочно-кишечного тракта (ЖКТ). Кожные симптомы во время абдоминальных отеков, как правило, остаются или усиливаются.
Развитию приступов абдоминальных отеков при НАО часто предшествуют ощущения спазмов в околопупочной области, слабость, тошнота, спастические боли в эпигастрии. Некоторые пациенты предъявляют жалобы на ощущения «отеков внутренних органов». Отек в области абдоминальных органов, как правило, сопровождается выраженным болевым абдоминальным синдромом, тошнотой, рвотой и диареей. Клиническая картина часто напоминает «острый живот» или кишечную непроходимость. Клинически болевой синдром проявляется разлитой болью в брюшной полости, кишечными коликами, возможна тонкокишечная непроходимость. У ряда пациентов наблюдается первичный генез рецидивирующей тонкокишечной непроходимости – forme fruste (приостановление в развитии или скрытое течение заболевания), и в этом случае только исследование концентрации С4-фракции комплемента позволяет правильно поставить диагноз [1]. Боли в животе бывают настолько интенсивными, что их иногда называют «брюшная мигрень», а сопровождающие болевой симптом общие явления (тахикардия, колебания артериального давления, головокружение, головная боль и др.) – «вегетативная буря».
Выброс жидкостей в интерстициальное и перитонеальное пространство во время абдоминальных атак может привести к клинически значимой гипотонии. Приступы могут длиться от 12 до 36 ч и часто проходят в тяжелой форме, снижая дееспособность, качество жизни пациентов, и могут быть сопряжены со значительными осложнениями и риском смерти. У детей отек ЖКТ может имитировать «острый живот», причем оценить у них частоту таких отеков трудно, так как «боли в животе» – распространенный симптом, особенно у младенцев.
Необходимо учитывать, что у части пациентов многие годы может наблюдаться клиника только в виде изолированной абдоминалгии. Эта группа больных не попадает в поле зрения терапевтов или аллергологов-иммунологов. Атаки НАО проходят у них только в абдоминальной форме. Около 30% больных подвергаются хирургическому вмешательству в связи с подозрением на острую хирургическую патологию. У больных НАО даже описан феномен «географического живота» – результат операций, характеризующийся наличием многочисленных послеоперационных рубцов. Пациентам проводят лапаротомию, обусловленную отеком внутренних органов (аппендэктомию, холецистэктомию, нефрэктомию, гинекологические операции), при операции выявляют ограниченный отек кишечника и признаки асептического воспаления. При ультразвуковом обследовании и компьютерной томографии отмечается отек слизистой оболочки интестинальной стенки, а также свободная жидкость в брюшной полости. Пациенты с рецидивирующим абдоминальным синдромом, при котором заболевания ЖКТ не подтверждаются лабораторно-функциональными методами, нуждаются в дополнительном обследовании для исключения патологии системы комплемента.
Атака НАО может характеризоваться сочетанием отека кожи, слизистых оболочек и поражения ЖКТ. При атипичном течении заболевания отеки могут отсутствовать, возможны описанные выше изолированные абдоминалгии, характерны полиартралгии. В очень редких случаях описаны эпилептический приступ, уртикарии, кожная пурпура, синдром Рейно. Редкими проявлениями НАО являются плевральный выпот, динамическое нарушение мозгового кровообращения с гемипарезом (при локальном отеке головного мозга), дизурия и задержка мочи (при отеке мочевого пузыря и уретры), отеки мышц (спины, шеи, плеча, предплечья и др.) и суставов (плечевых, бедренных).
Редко, при локализации отеков на лице в патологический процесс могут вовлекаться менингеальные оболочки с развитием менингеальных симптомов (ригидность затылочных мышц, резкая цефалгия, рвота, иногда судороги). При поражении лабиринтных систем развивается синдром Меньера, что выражается головокружением, тошнотой, рвотой. Все эти симптомы могут встречаться как одновременно, так и по отдельности. Тяжесть симптомов наследственных отеков очень вариабельна и не коррелирует с плазменным уровнем C1INH.
Клинические проявления НАО 3 типа с нормальным уровнем C1INH напоминают проявления НАО 1 и 2 типа, однако имеют следующие отличия:
- появление первых клинических симптомов чаще всего в течение второго десятилетия жизни;
- меньшее число приступов;
- более длинные интервалы между приступами;
- более высокий процент приступов периферических и фасциальных отеков;
- более редкие абдоминальные приступы;
- отсутствие предшествующей приступу кольцевидной эритемы;
- более поздний возраст начала проявления приступов.
НАО 3 типа обычно протекает тяжелее у женщин, чем у мужчин. Отличительная особенность болезни у женщин – зависимость симптомов от высокого уровня эстрогенов; соответственно для нее характерны обострения болезни во время беременности, применение эстрогенсодержащих пероральных контрацептивов или заместительной терапии эстрогенами при лечении климактерического синдрома.
ДИАГНОСТИКА
Диагноз НАО ставится на основании данных анамнеза, особенностей клинической картины, лабораторного обследования [2].
В пользу наследственного ангиоотека свидетельствуют анамнестические данные:
- семейный анамнез отеков различной локализации, особенно случаи гибели родственников от отека гортани;
- частые госпитализации с клиникой «острого живота» без выявления впоследствии причин, способных обусловливать возникшие симптомы (патологий ЖКТ, хирургической патологии и т.п.);
- связь отеков с механическим воздействием (ударом, уколом, травмой). В таких случаях удар в живот может вызвать клиническую картину «острого живота» без повреждения внутренних органов;
- отек гортани часто возникает при стоматологических манипуляциях. Связь с травмой, физическим и эмоциональным напряжениями, острыми респираторными заболеваниями позволяют в первую очередь думать о наличии НАО;
- ухудшение течения заболевания во время беременности (особенно при плоде женского пола) на фоне приема эстрогенсодержащих препаратов;
- связь отеков с приемом ингибиторов АПФ и бета-блокаторов, рецепторов ангиотензина II.
На амбулаторном приеме пациенту с жалобами на проявления рецидивирующих отеков без явлений крапивницы рекомендуется задавать уточняющие вопросы, приведенные в таблице 2.

ЛАБОРАТОРНАЯ ДИАГНОСТИКА
Для лабораторного подтверждения диагноза НАО используется ряд тестов: определение концентрации С4 компонента системы комплемента, концентрации и функциональной активности ингибитора С1-эстеразы [2].
У пациентов старше 40 лет, с поздним дебютом ангиоотека для проведения дифференциального диагноза необходимо дополнительно определять наличие антител к ингибитору С1-эстеразы, С1q и по показаниям ряд других маркеров.
Кроме того, для диагностики НАО активно используются генетические исследования. При этом необходимо подчеркнуть, что установление генетического дефекта не является обязательным для диагноза НАО: у 5–10% больных НАО при проведении полноценного генетического исследования мутация не обнаруживается. Объем обследования и его целесообразность определяет врач ‒ аллерголог-иммунолог.
В соответствии с общепринятыми стандартами диагноз НАО базируется на двух последовательно установленных снижениях концентрации C4, концентрации (количественной) и/или функциональной активности ингибитора С1-эстеразы. Длительность периода между исследованиями должна составлять 1–3 мес [4].
Диагностический комплекс в виде низкого уровня C4 и низкой функциональной активности ингибитора С1-эстеразы как скрининговый критерий диагноза НАО обладает специфичностью 98–100% и негативной предиктивной значимостью 96% [5].
Все дети из семей с НАО должны быть обследованы как можно раньше на предмет наличия у них этого заболевания. При этом надо учитывать, что достоверные данные, позволяющие установить этот диагноз, могут быть получены при повторном обследовании после 12 мес. В ряде случаев у детей раннего возраста для диагностики НАО при наличии выявленной мутации у родителей достаточно использовать генетические исследования.
Все пациенты с подозрением на НАО 1 и 2 типа (т.е. страдающие рецидивирующим ангиоотеком в отсутствие видимой причины) и все члены семей пациентов с установленным диагнозом НАО должны пройти скрининговое обследование с определением уровней С4, количества протеина C1INH и функциональных уровней C1INH в крови. При патологически низких параметрах эти исследования для подтверждения диагноза следует выполнить повторно [6].
Измерение уровней в крови функциональной активности ингибитора С1, содержание протеина ингибитора С1 и С4 – основные лабораторные исследования, используемые при диагностике НАО1 и 2 типа. Если результаты свидетельствуют об отклонении от нормы, исследование следует повторить; нормальные результаты могут потребовать повторения исследований в момент приступа ангиоотека.
Следует подчеркнуть важность обследования близких родственников больного, поскольку лица с неустановленным диагнозом НАО в 35% случаев подвержены риску смерти.
ЗАКЛЮЧЕНИЕ
Знание особенностей НАО врачами всех специальностей, несомненно, будет способствовать своевременной диагностике этого заболевания, соответственно назначению адекватной базисной терапии пациентам. В конечном итоге это прервет тот мучительный круг страданий, в котором годами находятся пациенты с НАО, и обеспечит им достойное качество жизни.



