Главной задачей лечения остеопороза (ОП) является предупреждение его осложнений – остеопоротических или низкоэнергетических переломов, как впервые возникших, так и повторных. Достижение этой цели возможно только в случае регулярного и длительного применения современной патогенетической терапии.
Для назначения лечения необходимо первоначально диагностировать ОП. В настоящее время критериями установления данного диагноза служат:
 1) наличие низкоэнергетических переломов крупных костей скелета (бедренной кости, тел(а) позвонков(а), множественных переломов) в анамнезе или выявленных при обследовании независимо от результатов рентгеноденситометрии или FRAX (при условии исключения других заболеваний скелета);
1) наличие низкоэнергетических переломов крупных костей скелета (бедренной кости, тел(а) позвонков(а), множественных переломов) в анамнезе или выявленных при обследовании независимо от результатов рентгеноденситометрии или FRAX (при условии исключения других заболеваний скелета);
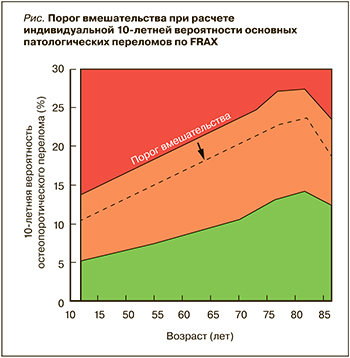
2) высокая индивидуальная 10-летняя вероятность основных остеопоротических переломов (результат оценки FRAX соответствует российскому порогу вмешательства и/или превышает его) независимо от показателя рентгеноденситометрии (рис.);
3) снижение минеральной плотности кости (МПК) на ≥2,5 стандартных отклонений по Т-критерию в шейке бедренной кости и/или в целом в проксимальном отделе бедренной кости и/или в поясничных позвонках (L1–L4, L2–L4), измеренной двухэнергетической рентгеноденситометрией (dual-energy X-ray absorptiometry – DXA), у женщин в постменопаузе и мужчин старше 50 лет [1].
При этом необходимо исключить все возможные другие причины повышенной хрупкости скелета, для чего проводятся клинический и биохимический анализ крови и изучается анамнез.
АРСЕНАЛ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ ДЛЯ ЛЕЧЕНИЯ ОСТЕОПОРОЗА
Для лечения ОП в арсенале российских врачей есть широкий спектр лекарственных средств с доказанной эффективностью в отношении снижения риска переломов. Среди противоостеопоротических препаратов ведущее место занимают антирезорбтивные средства – бисфосфонаты и деносумаб, которые рассматриваются как лекарства первого выбора у пациентов как с умеренным, так и высоким риском переломов. У больных с умеренным риском рекомендуется начинать лечение с пероральных бисфосфонатов; это могут быть алендроновая кислота, которая принимается в дозе 70 мг 1 раз в неделю, или ризедроновая кислота (35 мг 1 раз в неделю), или ибандроновая кислота (150мг 1 раз в месяц). Длительность терапии составляет до 5 лет при хорошей переносимости и приверженности пациента лечению. При достижении клинического эффекта (отсутствии переломов за время приема препарата и приросте и стабилизации МПК) может быть сделан перерыв в лечении до 2–5 лет, однако пациенты должны находиться под ежегодным диспансерном наблюдением для оценки возможности возобновления терапии в случае возникновения перелома при низком уровне травмы или отрицательной динамике при денситометрическом обследовании [2].
При неэффективности пероральных бисфосфонатов следует рассмотреть вопрос о переходе на парентеральные препараты. Признаками неэффективности служат ≥2 низкоэнергетических перелома и/или снижение МПК на ≥5% в позвоночнике или ≥4% в проксимальном отделе бедренной кости при двух последовательных измерениях, а также при наличии анализа крови на маркеры костного обмена, отсутствие достоверного снижения этих маркеров через 6 мес лечения на 25% от первоначального уровня [3]. Кроме того, парентеральные средства могут быть рекомендованы при плохой переносимости пероральных бисфосфонатов, невозможности пациента находиться в вертикальном положении, активных заболеваниях верхних отделов желудочно-кишечного тракта (эзофагит, язвенная болезнь) [2].
В форме раствора для внутривенного введения выпускаются два бисфосфоната – золедроновая кислота (5 мг/100 мл внутривенно капельно 1 раз в год) и ибандроновая кислота (3 мг/3 мл внутривенно струйно 1 раз в 3 мес). Для парентерального (подкожно 60 мг 1 раз в 6 мес) введения предназначен и деносумаб – генно-инженерный биологический препарат, являющийся полным человеческим моноклональным антителом и также относящийся к антирезорбтивным средствам. Лечение этими препаратами назначается на 3 года; при достижении клинического эффекта после применения золедроновой или ибандроновой кислоты можно уйти на так называемые лекарственные каникулы [4], тогда как после остановки лечения деносумабом необходимо перевести пациента на алендроновую кислоту через 6 мес или на золедроновую кислоту через 6 мес + 65 дней после последней инъекции для предотвращения потери МПК и увеличения риска переломов позвонков (это связано с обратимостью действия деносумаба после его отмены) [5].
У больных с высоким риском остеопоротических переломов (возраст >75 лет и/или Т-критерий в бедре <-2,5 стандартных отклонений или высокий 10-летний риск переломов по FRAX®) или имевших ранее переломы бедра/позвонков целесообразно продолжить лечение при хорошей переносимости пероральными бисфосфонатами или деносумабом курсом до 10 лет, а при использовании золедроновой кислоты – до 6 лет [6].
При высоком риске переломов, наличии множественных переломов позвонков и других костей скелета, а также при неэффективности или непереносимости антирезорбтивной терапии следует назначить терипаратид, который имеет анаболическое действие на кость при интермиттрующем введении. Однако, прежде чем его рекомендовать, необходимо исключить у пациента гиперкальциемию, гиперпаратиреоз, метаболические заболевания скелета (кроме самого ОП), повышение уровня щелочной фосфатазы неясного генеза, а также онкозаболевание и костные метастазы. Терипаратид применяется в виде ежедневных подкожных инъекций в дозе 20 мкг/ сут. Длительность лечения препаратом ограничена 24 мес, после чего для закрепления результата, достигнутого на фоне его введения, рекомендовано назначить средства с антирезорбтивным действием – золедроновую кислоту (для сохранения достигнутого эффекта) или деносумаб (для дальнейшего прироста МПК) длительностью не менее года [1].
В настоящее время не рекомендуется использовать стронция ранелат в рутинной практике для лечения ОП ввиду высокого риска сердечно-сосудистых осложнений и тромбоэмболии [1].
О РОЛИ ИСТОЧНИКОВ КАЛЬЦИЯ И ВИТАМИНА D
Полноценное действие лекарственных средств, непосредственно влияющих на клетки костной ткани, невозможно без адекватного содержания в организме кальция. Это связано в первую очередь с тем, что кальций является основным макроэлементом в человеческом организме, при этом более 99% его локализуется в скелете в составе кристаллов гидроксиапатита (Ca10(PO4)6(OH)2). Он не синтезируется в организме, а поступает с продуктами питания. Основным источником его выступают молочные продукты, в которых кальций присутствует в максимальных количествах и в форме, наиболее легкой для транспорта и всасывания в кишечнике. Кальций выводится через кишечник, почки и кожу, что требует постоянного возмещения его потерь. Если этого не происходит, то развивается гипокальциемия, которая запускает повышенную продукцию паратгормона с последующим усилением костной резорбции и снижением МПК [7].
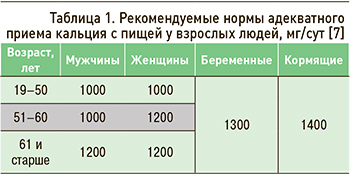 В различные возрастные периоды жизни человеку требуются разные дозы потребления кальция (табл. 1).
В различные возрастные периоды жизни человеку требуются разные дозы потребления кальция (табл. 1).
Для нормального всасывания кальция в кишечнике необходим достаточный уровень витамина D в крови. Гиповитаминоз D ассоциируется не только с отрицательным кальциевым балансом и снижением минерализации костной ткани, но и ведет к деструкции мышечных волокон с развитием слабости мышц, которая сопряжена с высоким риском падений, способствующих возникновению переломов, особенно у пациентов с ОП.
 Витамин D образуется в коже из провитамина D под действием ультрафиолетовых лучей спектра В (длина волны 290–315 нм). Кроме того, он поступает в организм с пищей. Продукты, являющиеся источником этого витамина, представлены в таблице 2.
Витамин D образуется в коже из провитамина D под действием ультрафиолетовых лучей спектра В (длина волны 290–315 нм). Кроме того, он поступает в организм с пищей. Продукты, являющиеся источником этого витамина, представлены в таблице 2.
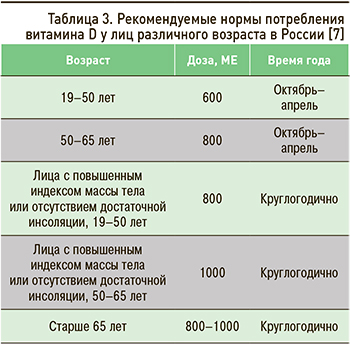
Как и для кальция, количество необходимого суточного потребления витамина D зависит от возраста человека. В то же время для одних людей профилактический его прием показан только в течение месяцев с наименьшей инсоляцией, а для других – круглогодично (табл. 3).
В реальности поступление кальция и витамина D извне редко достигает значений, необходимых для поддержания нормального костного обмена. Так, при рекомендуемой суточной норме 1000–1200 мг кальция для женщин в постменопаузе и мужчин 50 лет и старше среднее потребление его с продуктами питания значительно ниже: 683±231 мг/ сут и 635±276 мг/сут соответственно. По данным же социальной программы «Остеоскрининг. Россия», необходимое количество кальция получали с пищей только 9% женщин и 6% мужчин [8]. Значительные колебания в потреблении молочных продуктов были связаны с особенностями питания в различных регионах проживания, религиозным календарем и временем года.
 В силу географического расположения России выше 41° северной широты вся ее территория расположена в зоне низкой инсоляции не только зимой, но и летом, так как ультрафиолетовые лучи фильтруются через озоновый слой под более косым зенитным углом. Кроме того, интенсивность солнечного излучения, доходящего до Земли, зависит от толщины слоя облаков и загрязненности атмосферы. Например, в Москве, расположенной на уровне 55,75° северной широты, всего 93 ясных солнечных дня в году, тогда как пасмурных – 188. Для сравнения: в Ростове-на-Дону (47,23° северной широты) солнечных дней почти в 2 раза больше (176 дней в году), а пасмурных – почти вдвое меньше (100) [9].
В силу географического расположения России выше 41° северной широты вся ее территория расположена в зоне низкой инсоляции не только зимой, но и летом, так как ультрафиолетовые лучи фильтруются через озоновый слой под более косым зенитным углом. Кроме того, интенсивность солнечного излучения, доходящего до Земли, зависит от толщины слоя облаков и загрязненности атмосферы. Например, в Москве, расположенной на уровне 55,75° северной широты, всего 93 ясных солнечных дня в году, тогда как пасмурных – 188. Для сравнения: в Ростове-на-Дону (47,23° северной широты) солнечных дней почти в 2 раза больше (176 дней в году), а пасмурных – почти вдвое меньше (100) [9].
Дефицит витамина D широко распространен среди россиян. По данным исследования, проведенного в Москве, такой дефицит (концентрация витамина D в крови менее 20 или 50 нмоль/л) наблюдался у 70,3% женщин в постменопаузе, а его нормальное значение было выявлено только у 3,2% обследованных лиц [10]. Наряду с этим отмечались сезонные колебания данного показателя, а наиболее низкий уровень витамина D был зафиксирован в декабре–марте. В Ростове-на-Дону при обследовании более 5 тыс. человек дефицит и недостаточность витамина D обнаружены у 43,3 и 38,8% лиц соответственно [11]. На севере нашей страны в Архангельске среди жителей в возрасте 24–60 лет дефицит и недостаточность витамина D были зарегистрированы у 70% обследованных лиц, причем среди подростков и студентов этот показатель достигал 80–99% [12]. В Санкт-Петербурге 90,9% взрослых людей 19–75 лет и 93% детей 7–17 лет также имели сниженный уровень витамина D [13].
В 2017 г. вышел консенсус экспертов Европейского общества клинических и экономических аспектов остеопороза, остеоартрита и мышечно-скелетных заболеваний (ESCEO) и Международного фонда по остеопорозу (IOF), в котором на основании имеющихся доказательств лицам с высоким риском низкого потребления кальция и недостаточности витамина D, а также тем, кто получает лечение по поводу остеопороза, рекомендуется принимать препараты кальция в сочетании с витамином D [14].
ФАКТОР КОМПЛАЕНТНОСТИ
Существенную роль в терапии ОП играет тщательное выполнение врачебных рекомендаций. Преждевременное прекращение или нарушение предписанного режима приема препаратов снижают эффективность патогенетических средств, уменьшают потенциальные терапевтические преимущества для пациента и сводят к минимуму все усилия, направленные на профилактику низкоэнергетических переломов. Необходимость строгого соблюдения врачебных предписаний ярко продемонстрирована в исследовании Curtis J.R. et al.: у больных, принимавших менее 50% рекомендованной курсовой дозы бисфосфонатов, по сравнению с пациентами, приверженность у которых достигала 90%, риск переломов возрастал на 40% [15]. В свою очередь, по данным Tang B.M. et al., повышение приверженности лечению препаратами кальция и витамина D с 50–59 до 80% и более ведет к снижению риска переломов по сравнению с плацебо на 5 и 24% соответственно [16].
Поскольку лечение ОП должно проводиться длительно (3–5 лет и более), проблема приверженности является весьма значимой для данной нозологии, что признано на уровне Всемирной организации здравоохранения (ВОЗ). Эксперты ВОЗ поставили ОП в один ряд с такими распространенными хроническими заболеваниями, как гипертоническая болезнь, сахарный диабет, бронхиальная астма, для которых недостаточное выполнение рекомендаций по лечению или преждевременное его прерывание признаны «мировой проблемой огромной значимости». В отчете ВОЗ, посвященном лечению хронических заболеваний, отмечено, что пациенты тщательно выполняют врачебные рекомендации в течение длительного времени не более чем в 50% случаев.
В ряде клинических наблюдений выявлена высокая приверженность противоостеопоротической терапии (65–80%), что авторы объясняют регулярным врачебным контролем. Вместе с тем в условиях реальной клинической практики длительное соблюдение пациентами с ОП назначений врача отмечается лишь в небольшом количестве случаев. Так, Berry S.D. et al. показали, что у пациентов старших возрастных групп комплаентность через 6 мес от начала терапии препаратами кальция и витамина D составила лишь 58% [17].
Результаты, полученные отечественными авторами, в целом согласуются с зарубежными исследованиями. Так, по данным О.М. Лесняк и соавт., только 14% пациентов с ОП начинают рекомендованное лечение, при этом 16% прекращают терапию в течение 3–6 мес от начала приема медикаментов. Среди тех, кто продолжает лечение, только 40% делают это регулярно [18]. В исследовании Ю.А. Сафоновой и Е.Г. Зоткина к концу первого года лечения комбинированными препаратами кальция и витамина D приверженность лечению пациентов с ОП моложе 70 лет составила всего 42,6% [19].
Результаты некоторых исследований свидетельствуют об улучшении исполнения назначений врача при наличии дополнительных консультаций и программ обучения пациентов, телефонных контактов с ними. Такими способами возможно повышение приверженности терапии до 68–80%. Для некоторых пациентов немалое значение может иметь и форма выпуска препарата [20].
Патогенетически обоснованным оптимальным вариантом восполнения дефицита кальция и витамина D является прием комбинированных препаратов, так как каждый из их компонентов необходим для полноценного проявления эффекта другого. Более того, соединение в одной таблетке двух действующих веществ способствует уменьшению общего количества принимаемых препаратов, а, следовательно, служит одним из способов преодоления низкой приверженности лечению.
Необходимо отметить, что пациентам часто рекомендуется прием комбинированных препаратов кальция и витамина D дважды в день. Однако исследования в различных терапевтических дисциплинах показали, что соблюдение режима терапии при однократном приеме лекарственного средства в течение дня достоверно лучше, чем при двукратном и более. В двух центрах Москвы и Санкт-Петербурга было проведено исследование по изучению приверженности лечению и предпочтения пациентов при различных схемах назначения препарата, содержащего кальций и витамин D. Оказалось, что большинство опрошенных лиц предпочло бы однократный прием двукратному [21].
В настоящее время рекомендуется подбирать необходимую дозировку кальция, предварительно подсчитывая поступающее его количество с пищей. Дополнительный прием кальция оправдан, если суточный пищевой рацион содержит меньше 800 мг этого макроэлемента, а использование добавок витамина D целесообразно для пациентов с риском или подтвержденной недостаточностью витамина D, а также для лиц, получающих противоостеопоротическое лечение [14].
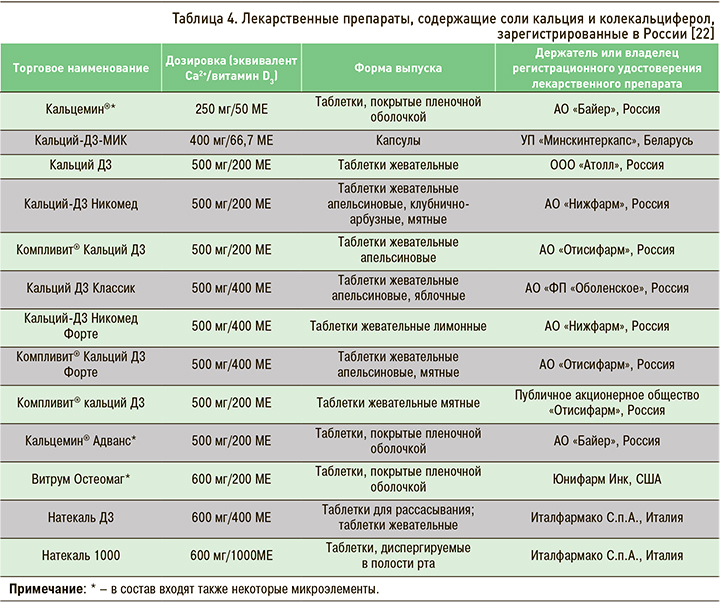
Персонализация терапии ОП стала возможна благодаря наличию комбинированных препаратов с различным содержанием кальция и витамина D в одной таблетке (табл. 4).
Очень часто пациентам требуется дополнительно принимать не более 600 мг элементарного кальция в сутки. При этом большинство комбинированных препаратов содержат в 1 таблетке оптимальное количество кальция (500–600 мг), но недостаточную дозу колекальциферола (50–200–400 МЕ), поэтому таким пациентам дополнительно назначают нативный витамин D в форме таблеток или капель; к сожалению, это также может повлиять на точное выполнение врачебных назначений и уменьшить приверженность больных лечению. С учетом этого фактора обращает на себя внимание препарат Натекаль 1000, который появился на фармрынке России позже многих других комбинированных средств. Он выпускается в таблетках, диспергируемых в полости рта и не требующих запивания водой, и содержит эквивалент 600 мг элементарного кальция в форме карбоната и увеличенную до 1000 МЕ дозировку колекальциферола. Как было указано выше, среднее потребление кальция с продуктами питания в России составляет чуть более 600 мг; следовательно, использование этого препарата позволит большинству людей достичь рекомендованную ежедневную норму приема этого макроэлемента на фоне достаточной дозы нативного витамина D.
ЗАКЛЮЧЕНИЕ
Таким образом, в клинической практике имеется широкий выбор фармакологических средств для обеспечения эффективной профилактики остеопоротических переломов различной локализации. Вместе с тем для достижения желаемого результата терапии необходимо сочетание множества факторов, среди которых наиболее важными становятся обоснованный выбор лекарственного препарата, длительность и правильность его использования, а также приверженность пациента к лечению. Кроме того, следует всегда помнить о необходимости приема кальция и витамина D, а расширение линейки комбинированных форм делает возможным индивидуализировать лечение с учетом реальной потребности пациентов в этих веществах. В свете вышесказанного становится ясным, насколько важна роль врача как в определении тактики ведения пациента, так и мотивации больного к соблюдению полученных рекомендаций.


