ВВЕДЕНИЕ
История применения гепаринов берет свое начало в 30-х гг. XX в. Сам гепарин был совершенно случайно открыт в 1916 г. McLean J., когда тот, будучи студентом-медиком Университета Джона Хопкинса, изучал тромбопластическую активность фосфолипидов печени человека [1]. Молодой американский исследователь обнаружил, что изучаемый гепар-фосфатид не только не повышает свертывание крови, но и, наоборот, обладает антикоагулянтой активностью [1]. В клинической практике гепарин был впервые использован в 1935 г. выдающимся американо-канадским врачом и физиологом Best C.H. (одним из тех, кто первым выделил из секрета поджелудочной железы инсулин для практического применения) [2].
В настоящее время известно, что гепарины представляют собой смесь полисахаридных субстанций, которые состоят из различного количества чередующихся в различных вариантах остатков Д-глюкозамина и уроновой кислоты, подверженных разной степени сульфирования. Коммерческие гепарины производятся из разного сырья и неодинаковыми технологическими методами, что определяет различие в их антикоагулянтных свойствах [3].
Механизм антикоагулянтного действия гепарина заключается в снижении фибринообразования за счет угнетения функции активированного II фактора (тромбина) и активированного фактора Х (Ха) [4]. Антикоагулянтное действие гепарина реализуется только при наличии в крови достаточного количества антитромбина III. В комплексе с антитромбином гепарин ингибирует и другие прокоагулянты – факторы IXа, XIа, XIIа [4].
НИЗКОМОЛЕКУЛЯРНЫЕ ГЕПАРИНЫ
Фракционирование гепаринов показало, что ингибицией активного фактора Ха занимаются лишь низкомолекулярные гепарины (НМГ) [3]. Первый гепарин низкого молекулярного веса был создан институтом Choay и получил название Nadroparin (надропарин); он стал выпускаться компанией Sanofi под наименованием Фраксипарин (1985) [5]. В последующие годы были получены и другие НМГ, отличающиеся молекулярной массой, а следовательно, и антикоагулянтной/противотромботической активностью: далтепарин, парнапарин, эноксапарин, тинзапарин и бемипарин [6].
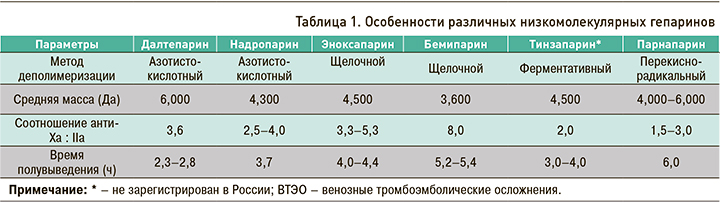
Практическому врачу важно помнить, что применяемые на сегодняшний день НМГ могут готовиться из различного сырья, кроме того, они производятся с помощью различных технологий в ходе азотнокислой, гепариназной или щелочной деполимеризации, которой иногда может сопутствовать реакция бензиллирования. В связи с этим НМГ отличаются друг от друга и не являются взаимозаменяемыми; они имеют уникальный профиль клинической эффективности, и переносить результаты, полученные при использовании одного препарата, на другой неправомерно [6, 7]. В таблице 1 представлены особенности различных НМГ.
ПЛЕЙОТРОПНЫЕ ЭФФЕКТЫ НИЗКОМОЛЕКУЛЯРНЫХ ГЕПАРИНОВ
Наряду с противотромботическим эффектом, НМГ обладают иными (неантикоагулянтными) свойствами: ингибируют активность комплемента, модулируют фактор роста (ФР), молекулы адгезии и миграцию лейкоцитов, обладают антипролиферативным действием, активируют липопротеинлипазы, фибринолиз, влияют на сократимость миометрия [8]. Также НМГ оказывают противовоспалительное действие, в том числе у пациентов с хронической обструктивной болезнью легких [9], бронхиальной астмой [10], язвенным колитом [11], красным плоским лишаем [12].
ПРИМЕНЕНИЕ НИЗКОМОЛЕКУЛЯРНЫХ ГЕПАРИНОВ У НЕХИРУРГИЧЕСКИХ БОЛЬНЫХ
Профилактику и лечение венозных тромбоэмболических осложнений (ВТЭО) с использованием НМГ следует проводить терапевтическим пациентам следующих категорий: госпитализированным больным с выраженной сердечной недостаточностью, тяжелым заболеванием легких, протекающим с дыхательной недостаточностью; пациентам, вынужденным соблюдать постельный режим и имеющим один из следующих факторов риска ВТЭО – активное злокачественное новообразование, ВТЭО в анамнезе, сепсис, острое неврологическое заболевание, воспалительные заболевания кишечника [13].
Для определения вероятности возникновения ВТЭО используется шкала оценки риска тромбоэмболических осложнений у терапевтических пациентов (табл. 2) [13].
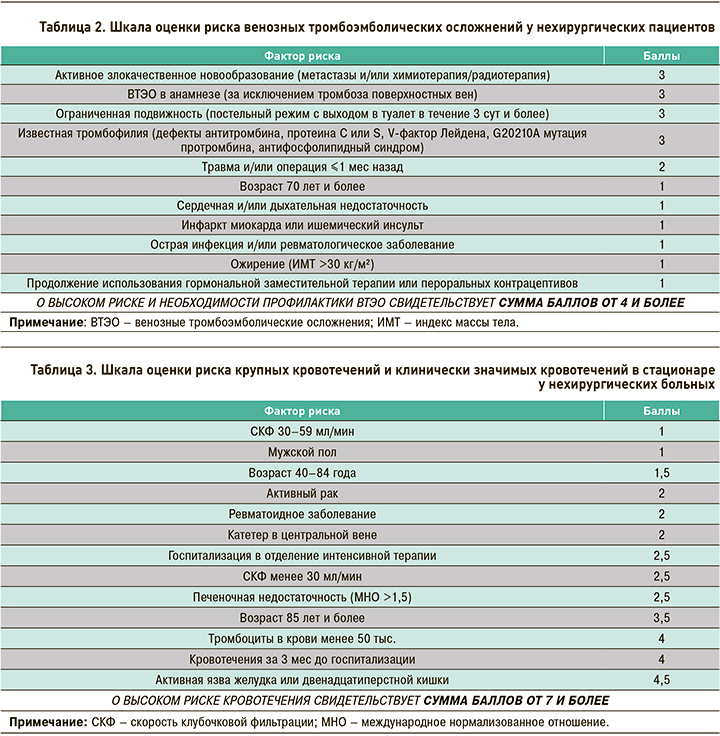
Помимо этого, у нехирургических больных необходима оценка риска геморрагических осложнений (табл. 3) [13]. Профилактические мероприятия следует начинать как можно скорее после поступления пациента в стационар. Медикаментозная профилактика ВТЭО должна продолжаться от 6 до 21 сут вплоть до восстановления двигательной активности или выписки (в зависимости от того, что наступит раньше).
Онкологическим больным после обширных оперативных вмешательств при наличии дополнительных факторов риска рекомендуется длительная НМГ-профилактика ВТЭО в течение 28 дней [14].
В отношении отдельных пациентов с сохраняющимися факторами риска ВТЭО (в частности, при длительном ограничении двигательного режима) можно рассмотреть вопрос о продлении использования антикоагулянтов на срок до 6 нед (более длительная медикаментозная профилактика не изучена) [13].
В метаанализе рандомизированных исследований, сравнивавших профилактическую эффективность надропарина, эноксапарина и дальтепарина с нефракционированными гепаринами (НФГ), показано, что риск развития бессимптомных ВТЭО снижался на 4% при назначении эноксапарина, на 10% – дальтепарина и на 39% – надропарина [15].
Высокий риск кровотечений не предполагает автоматического отказа от медикаментозной профилактики ВТЭО, но требует более тщательной оценки соотношения пользы и риска подобных вмешательств. При этом увеличения частоты побочных эффектов на фоне лечения надропарином не наблюдалось [15].
По данным проспективного рандомизированного двойного слепого исследования, выполненного Simonneau G. et al., частота больших кровотечений при лечении оперированных больных эноксапарином составила 11,5%, а при лечении надропарином – всего 7,3%. То есть снижение относительного риска больших кровотечений составило 37%, что было статистически достоверным различием (р=0,012) [16].
ИСПОЛЬЗОВАНИЕ НАДРОПАРИНА ПРИ ПРОВЕДЕНИИ ГЕМОДИАЛИЗА
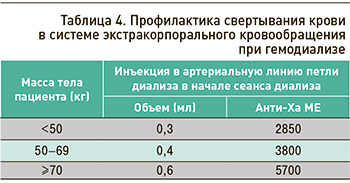
В случае применения надропарина для профилактики свертывания крови в системе экстракорпорального кровообращения при гемодиализе его доза должна устанавливаться для каждого пациента индивидуально, с учетом технических условий проведения диализа. Препарат вводится однократно в артериальную линию петли диализа в начале каждого сеанса (табл. 4) [13]. Пациентам, не имеющим повышенного риска развития кровотечения, рекомендованы начальные дозы надропарина, достаточные для проведения 4-часового сеанса диализа, в зависимости от массы тела.
Как уже отмечалось выше, НМГ не могут считаться взаимозаменяемыми. Каждый из них имеет специфические показания, дозы и особенности применения. Они могут различаться по началу введения и длительности использования в тех или иных клинических ситуациях, что зависит от реакции организма конкретного больного, особенностей действия и изученности того или иного препарата [17]. Поэтому при выборе лекарственного средств из группы НМГ необходимо убедиться, что препарат рекомендован производителем к применению у определенной категории больных. При назначении антикоагулянта следует придерживаться дозировок и методики использования, изложенных в рекомендациях производителя.
В таблице 5 указаны лечебные и профилактические дозы надропарина кальция для терапевтических пациентов с высоким риском ВТЭО-осложнений [13]. Дозировка этого НМГ должна корректироваться с учетом состояния функции почек. Так, при клиренсе креатинина менее 50 мл/ мин профилактическую дозу надропарина необходимо уменьшить на 25–33%. Такая же корректировка требуется и в случае подбора лечебной дозировки препарата при клиренсе креатинина 30–50 мл/мин. При клиренсе креатинина менее 30 мл/мин надропарин кальция противопоказан [13].

НАДРОПАРИН КАЛЬЦИЯ В ЛЕЧЕНИИ COVID-19 У ВЗРОСЛЫХ
Следствием тяжелого течения синдрома высвобождения цитокинов при COVID-19 может стать развитие нарушений свертывания крови. Для начальных стадий этого заболевания характерно развитие гиперкоагуляции без признаков потребления и развития синдрома диссеминированного внутрисосудистого свертывания (ДВС-синдрома). Коагулопатия при COVID-19 сопровождается активацией системы свертывания крови, что определяется по значительному повышению концентрации D-димера в крови. Число тромбоцитов при этом умеренно снижено, незначительно удлинено протромбиновое время, значительно повышен уровень фибриногена [18].
Таким образом, коагулопатия при COVID-19, наряду с признаками, свойственными развернутой фазе ДВС-синдрома в виде высокого уровня D-димера, не имеет типичных признаков потребления фибриногена и тромбоцитов. Коагулопатия при COVID-19 связана с повышенным риском смерти. Кроме того, у больных COVID-19 часто обнаруживают артериальный и венозный тромбоз. Всем пациентам, госпитализированным в стационар, показано назначение НМГ как минимум в профилактических дозах, причем такое профилактическое лечение должно продолжаться хотя бы до выписки пациента из стационара [18]. Нет доказанных преимуществ какого-либо одного НМГ по сравнению с другими. При недоступности НМГ/ фондапаринукса натрия или противопоказаниях к ним возможно использование НФГ [18].
Для диагностики ДВС-синдрома при COVID- 19 рекомендуется использовать критерии Международного общества тромбоза и гемостаза (табл. 6).
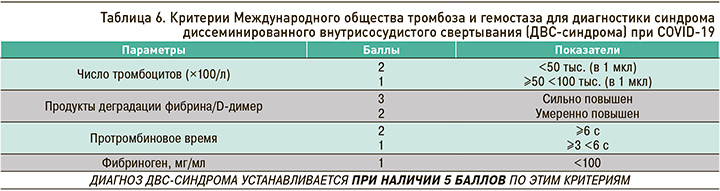
Надропарин кальция, наряду с другими НМГ, применяется у взрослых для лечения COVID-19. С профилактической целью он вводится подкожно в дозе 3800 анти-Ха МЕ (0,4 мл) 1 раз/сут при массе тела ≤70 кг или 5700 анти-Ха МЕ (0,6 мл) 1 раз/сут при массе тела >70 кг. С лечебной целью надропарин кальция применяется также подкожно в дозировке 86 анти-Ха МЕ/кг 2 раза/сут [18].
В России надропарин кальция выпускается компанией «Сотекс» под названием Детромбин® в растворе для подкожного введения с максимальным количеством дозировок 2850, 3800, 4750, 5700, 6650, 7600, 8550, 9500 Анти-Ха ME, что соответствует 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1,0 мл [19]. Необходимо отметить, что дозировка 0,9 мл (8550 Анти-Ха МЕ) есть только у этого препарата, что обеспечивает дополнительные удобства при терапии пациентов с массой тела 90–100 кг. Также возможно использовать дозы 0,5 мл (4750 Анти-Ха МЕ) и 0,7 мл (6650 Анти-Ха МЕ). Детромбин® показан для профилактики тромбоэмболических осложнений, лечения тромбоэмболии легочной артерии средней/тяжелой степени тяжести или тромбозов глубоких вен, профилактики свертывания крови при гемодиализе, лечения нестабильной стенокардии и инфаркта миокарда без зубца Q [19]. Надропарин кальция включен в методические рекомендации по профилактике и лечению новой коронавирусной инфекции у взрослых (COVID-19) [18].
По данным рандомизированного слепого перекрестного исследования 60 лежачих пациентов пожилого возраста, переносимость надропарина была значительно лучше, чем у эноксапарина [20]. Так, частота развития гематом при лечении надропарином составляла 13%, тогда как при введении препарата сравнения – 21% (p <0,05). Кроме того, надропарин реже, чем эноксапарин (p <0,05), вызывал такие осложнения в месте инъекции, как припухлость (1,7 против 8,3%), отек (1,7 против 8,3%), боль (16,7 против 31,7%), чувство жжения (20,0 против 26,6%) и зуд (6,7 против 20,0%) [20].
ЗАКЛЮЧЕНИЕ
НМГ нашли широкое распространение в клинической практике, в том числе среди нехирургических больных. Они используются для профилактики и лечения ВТЭО у терапевтических пациентов, госпитализированных с выраженной сердечной недостаточностью, тяжелыми заболеваниями легких, протекающих с дыхательной недостаточностью, у больных, вынужденных соблюдать постельный режим и имеющих один из факторов риска ВТЭО (активное злокачественное новообразование, ВТЭО в анамнезе, сепсис, острое неврологическое заболевание, воспалительные заболевания кишечника). Одним из наиболее широко используемых НМГ является надропарин (Детромбин®). Литературные данные и клиническая практика показывают, что переносимость этого лекарственного средства значительно лучше, чем у эноксапарина.



