ВВЕДЕНИЕ
Вопросы коррекции астении приобретают все большую актуальность в современном мире. Симптомы астении – одно из самых частых клинических проявлений различных заболеваний вне зависимости от пола и возраста пациентов. Сам термин «астения» (от греч. a – отсутствие, sthenos – сила) обозначает патологическое состояние, характеризующееся развитием выраженной слабости при минимальной активности или без таковой [1].
Врачи первичного амбулаторного звена, особенно терапевты, в последнее время часто сталкиваются с астенией у пациентов, перенесших инфекционное заболевание, например острую респираторную или новую коронавирусную инфекцию. При этом, как уже было замечено, астения сопровождает течение множества заболеваний и отнюдь не только инфекционного генеза [2]. Астенические симптомы присутствуют во всех периодах развития болезней: в продромальном, когда слабость, разбитость и утомляемость выступают главными неспецифическими симптомами; в разгаре заболевания, когда слабость может достигать максимальной выраженности; в период выздоровления, когда именно астения зачастую вновь становится ведущим клиническим проявлением [3, 4].
Таким образом, астения – это важный сигнал о неблагополучии в состоянии здоровья человека. Наряду с выраженной слабостью, резким уменьшением физической и интеллектуальной работоспособности основные ее клинические признаки включают повышенную раздражительность, гиперчувствительность или непереносимость громких звуков и яркого освещения, появление разнообразных болевых ощущений в теле и конечностях, развитие или усугубление расстройств сна, нарушения в работе желудочно-кишечного тракта и некоторые другие симптомы [1, 2].
Какие процессы в организме человека приводят к формированию такого букета неспецифических проявлений? Описанию патогенеза астении посвящено много работ, большинство из которых связывает появление ее симптомов с развитием энергетического дисбаланса в клетках организма человека с дальнейшим истощением функциональных резервов, необходимых для развития компенсаторных реакций [5–7]. К факторам, провоцирующим развитие симптомов астении, также относят воздействие стрессовых ситуаций и неблагоприятных привычек, ослабляющих иммунную и психоэмоциональную устойчивость организма. Наиболее частые причины развития клеточного энергетического дисбаланса у пациентов в терапевтической практике представлены в таблице 1.
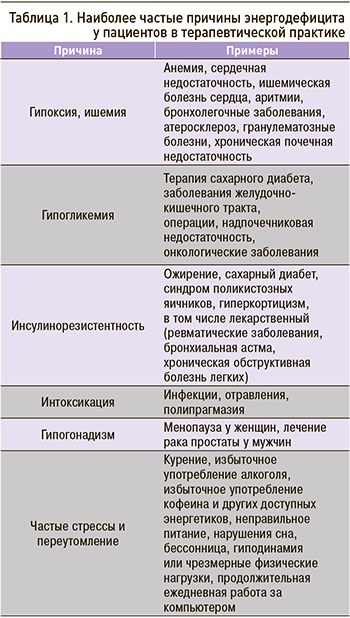
Общий принцип развития данных нарушений заключается в недостаточном синтезе или снижении утилизации энергетических субстратов клетками организма, следствием чего становится ухудшение клеточного метаболизма. Это, в свою очередь, запускает так называемый порочный круг патогенетических процессов, сопровождающих появление симптомов астении (рис. 1).
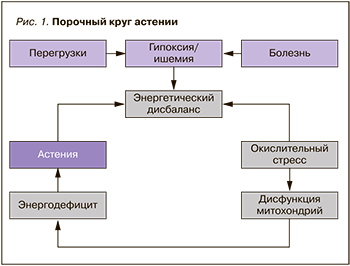
Таким образом, коррекция энергодефицита и клеточного метаболизма должны быть обязательными компонентами комплексной патогенетической терапии состояний, клинически проявляющихся различными признаками астении. Применяемые в настоящее время медикаментозные методы лечения астении включают специфическую этиопатогенетическую терапию, направленную на причины возникновения этого состояния, неспецифическую терапию, влияющую на регуляцию клеточного метаболизма, а также прием общеукрепляющих (стандартные поливитаминные комплексы с профилактическими дозировками) и симптоматических средств [2, 6]. Однако оптимальная терапевтическая стратегия в данном случае – выбор препарата с целенаправленным влиянием как на процессы синтеза энергии в клетках, так и на нейтрализацию последствий интоксикации организма продуктами обмена и окислительного стресса. Перспективным патогенетическим лекарственным средством, соответствующим заявленным эффектам нормализации энергообмена клетки и дезинтоксикации, является мельдоний (Милдронат®), который обладает дополнительными положительными эффектами в отношении состояния сосудистой стенки и микроциркуляции, а также активирующим действием на центральную нервную систему [8–10].
В связи с высокой частотой встречаемости симптомов астении среди пациентов врачей первичного звена и необходимостью выбора оптимальной терапии было спланировано и проведено многоцентровое контролируемое рандомизированное клиническое исследование ТОНУС. Целью его стала оценка эффективности и безопасности терапии препаратом Милдронат® у пациентов с астенией различного генеза. Исследование ТОНУС представляло собой две параллельные ветви наблюдения: ТОНУС-1, включавшую пациентов с симптоматической астенией и не имевших сопутствующих хронических заболеваний, и ТОНУС-2, в которую были отобраны пациенты с астенией и хроническими сердечно-сосудистыми (ССЗ) либо цереброваскулярными заболеваниями (ЦВЗ). Подробный дизайн и обзор основных результатов исследования ТОНУС был дан авторами в публикации за 2022 г. в одном из отечественных научных журналов [11].
Особенный интерес для практического врача в рамках изучения результатов исследования ТОНУС представляет многочисленная группа пациентов с астенией, не имевших в анамнезе указаний на ССЗ или ЦВЗ (ветвь исследования ТОНУС-1). Учитывая отсутствие на сегодняшний день клинических рекомендаций для терапевтов по ведению пациентов с различными вариантами астении, представленные результаты могут быть полезны для понимания перспективы в подборе оптимальных вариантов лечения этого состояния в реальной клинической практике.
МАТЕРИАЛ И МЕТОДЫ
Исследование ТОНУС проводилось с февраля по июнь 2021 г. в 26 городах России. Всего было обследовано 5179 пациентов, обратившихся с основными жалобами астенического характера в амбулаторно-поликлинические учреждения здравоохранения по месту жительства за консультацией к врачам первичного звена – терапевтам, кардиологам и неврологам.
Критерии включения пациентов в исследование ТОНУС:
- мужчины и женщины в возрасте от 18 до 75 лет включительно;
- пациенты, показавшие результат по визуальной аналоговой шкале астении (VAS-A) более 5 баллов;
- пациенты, подписавшие информированное согласие на участие в исследовании.
Критерии невключения:
- наличие симптомов депрессии на момент обращения (более 7 баллов по шкале HADS);
- признаки хронического алкоголизма, лекарственной и наркотической зависимости;
- установленные иные психиатрические заболевания;
- терминальные стадии поражения почек и печени;
- ранее установленная гиперчувствительность к мельдонию;
- беременность, период кормления ребенка грудью;
- отказ пациента от участия в исследовании;
- участие пациента в других клинических исследованиях в тот же момент времени;
- какое-либо состояние, препятствующее применению препарата Милдронат® в соответствии с противопоказаниями, мерами предосторожности и специальными предупреждениями, указанными в инструкции по медицинскому применению препарата.
Исходно всем пациентам проводилось клиническое обследование, состоявшее из анализа жалоб и анамнеза, оценки общего состояния, измерения основных антропометрических и гемодинамических параметров, а также скрининга на депрессию по шкале HADS и на астению – по шкале VAS-A. После проверки на соответствие критериям включения/невключения всем отобранным пациентам выполнялось дополнительное обследование, включавшее шкалу самооценки астении (MFI-20); тест «Таблицы Шульте» (W. Schulte table) с оценкой параметров работоспособности и внимания, а также расчетом таких показателей, как эффективности работы (ЭР), степени врабатываемости (ВР) и психической устойчивости (ПУ); шкалу общего клинического впечатления (Clinical Global Impression Scale, CGI) для динамической оценки тяжести состояния и эффективности терапии.
В ветвь исследования ТОНУС-1, объединившую пациентов с симптоматической астенией без сопутствующих ССЗ или ЦВЗ, было набрано 1728 пациентов, которым был установлен один из диагнозов по МКБ-10: F48.0 «Неврастения»; G93.3 «Синдром утомляемости после перенесенной вирусной болезни»; Z73.0 «Состояние истощения жизненных сил»; R53 «Недомогание и утомляемость». Все пациенты дали информированное согласие на участие в исследовании.
Далее все участники были рандомизированы в две группы: в основной группе к терапии был добавлен препарат Милдронат® в суточной дозе 500 мг, в контрольной – поливитаминный комплекс, содержащий стандартный набор витаминов в профилактических дозах. Длительность терапии в обеих группах составила 14 дней. Для всех пациентов были проведены 3 визита к врачу: первый – в день включения в исследование, второй – на 7-й день, третий – на 14-й день. На втором и третьем визитах всем участники прошли повторное обследование с применением всех методик первого визита. Исследование было выполнено в соответствии с Хельсинской декларацией, принятой в июне 1964 г. и пересмотренной в октябре 2000 г. (Эдинбург, Шотландия).
Статистическая обработка полученных результатов выполнялась с помощью программы SPSS 20.0 и программой среды R. Переменные представлены в виде Me (Q25; Q75), где Мe – медиана (Median), Q25 – 25-й процентиль, Q75 – 75-й процентиль, а доли и частоты – в виде «Me (СI 95%)», где Me – медиана, CI 95% – 95% доверительный интервал. Для оценки достоверности различий применялись критерий Манна–Уитни (для несвязанных групп), критерий χ2 Пирсона с поправкой на непрерывность, точный критерий Фишера. При оценке CI 95% для долей и частот использовался метод Уилсона. Различия считались достоверными при уровне p <0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Исходные характеристики пациентов, отобранных в ветвь исследования ТОНУС-1, представлены в таблицах 2 и 3. Для удобства анализа полученных данных участники были дополнительно разделены на две подгруппы, включавшие два разных этиопатогенетических вида астении – «постинфекционную» и «не связанную с инфекцией». Такое решение было обусловлено значимой долей пациентов, обратившихся к терапевту с симптомами астении, возникшими вскоре после перенесенного вирусного заболевания. Среди установленных перенесенных инфекционных заболеваний у пациентов были отмечены не только случаи новой коронавирусной инфекции, но и сезонные острые респираторные инфекции, а также грипп и вирусные пневмонии.
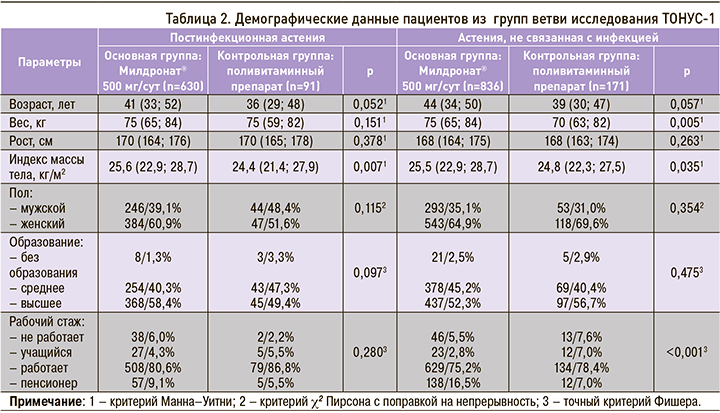
Как хорошо видно из данных таблиц 2 и 3, пациенты из ветви исследования ТОНУС-1, перенесшие инфекционное заболевание, были в целом сопоставимы в основной и контрольных группах по исходным клинико-демографическим характеристикам, кроме значения индекса массы тела (ИМТ), которое, хоть и отличалось между подгруппами, но оставалось в пределах значений избыточной массы тела. В подгруппах пациентов, не переносивших инфекционное заболевание, также отмечались небольшие различия в значениях массы тела и ИМТ между контрольной и основными группами, но они тоже оставались в пределах значений избыточной массы тела. Таким образом, исходные характеристики включенных в исследование пациентов ввиду отсутствия достоверных различий по основным демографическим признакам и клиническим проявлениям астении позволили провести корректное сравнение после проведенного курса терапии.
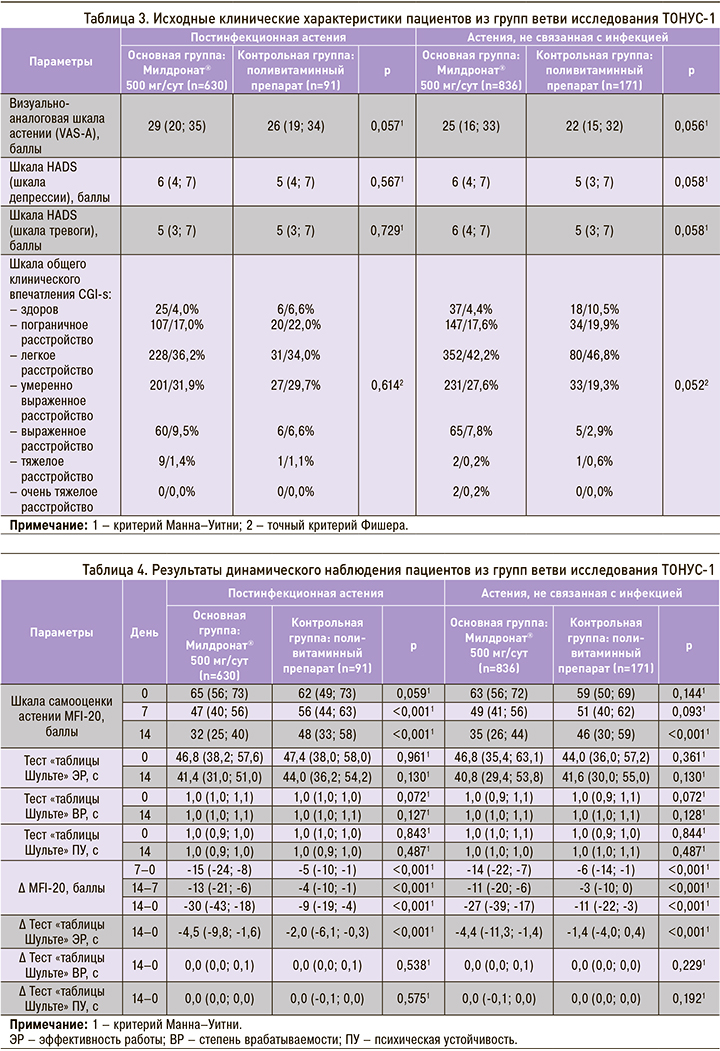
Результаты динамической оценки основных клинических проявлений астении во всех группах сравнения ветви исследования ТОНУС-1 приведены в таблице 4. Из этих данных видно, что за время наблюдения у всех пациентов с астенией после инфекционного заболевания, независимо от получаемой терапии, отмечалось улучшение самочувствия и показателя эффективности работы (ЭР). Однако в основной группе пациентов, получавших Милдронат® в суточной дозе 500 мг в течение 14 дней, восстановление шло более интенсивно, чем в контрольной, о чем свидетельствует значимое улучшение параметров внимания и работоспособности. Отмеченное достоверное увеличение показателя ЭР в основной группе составило 4,5 с, что почти в два раза выше достигнутого значения этого показателя в контроле. Положительная динамика состояния и самочувствия у пациентов основной группы, оцененная по шкале MFI- 20, более чем в три раза превысила аналогичные показатели в контрольной группе. Эти значимые положительные изменения были отмечены исследователями уже на 2-м визите, т.е. всего через 7 дней от начала терапии препаратом Милдронат®, и в дальнейшем изучаемые показатели продолжали улучшаться.
В подгруппах пациентов, не переносивших инфекционное заболевание (см. табл. 4), также отмечалось улучшение состояния по шкале MFI- 20, достигшее достоверного различия между группами к концу наблюдения. Следует особо подчеркнуть, что у пациентов, получавших Милдронат®, имели место более высокие темпы восстановления работоспособности в сравнении с группой контроля, где пациенты принимали поливитаминные комплексы. Так, общее улучшение значения показателя ЭР за 14 дней терапии в основной группе пациентов составило 4,4 с, а в контрольной – лишь 1,4 с (различия достоверны, р <0,001). Также и темпы улучшения самочувствия, оцененные по шкале MFI-20, в группе Милдроната оказались почти в 2,5 раза выше и составили к концу наблюдения -27 (-39; -17) баллов против -11 (-11; -3) в группе контроля, что свидетельствует о высокой эффективности даже краткосрочной терапии этим лекарственным препаратом.
Принимая во внимание общую положительную тенденцию в самочувствии у всех участников к окончанию наблюдения, следует, тем не менее, отметить более высокие темпы восстановления и степень улучшения самочувствия у пациентов, получавших Милдронат®. Об этом ярко свидетельствуют значимые различия между группами в количестве баллов по шкале MFI-20, начиная уже со 2-го визита (см. табл. 4), которые сохранялись до конца наблюдения. В контрольной группе пациентов, получавших поливитаминный комплекс, достоверное снижение баллов наблюдалось только к 3-му визиту и было почти в три раза менее выражено, чем в основной группе. Возможность сравнить эффективность терапии астенических симптомов препаратом Милдронат® в настоящем исследовании и в предыдущих наблюдениях говорит о сопоставимости полученных результатов и подтверждает клиническую обоснованность данного лечения [12–19].
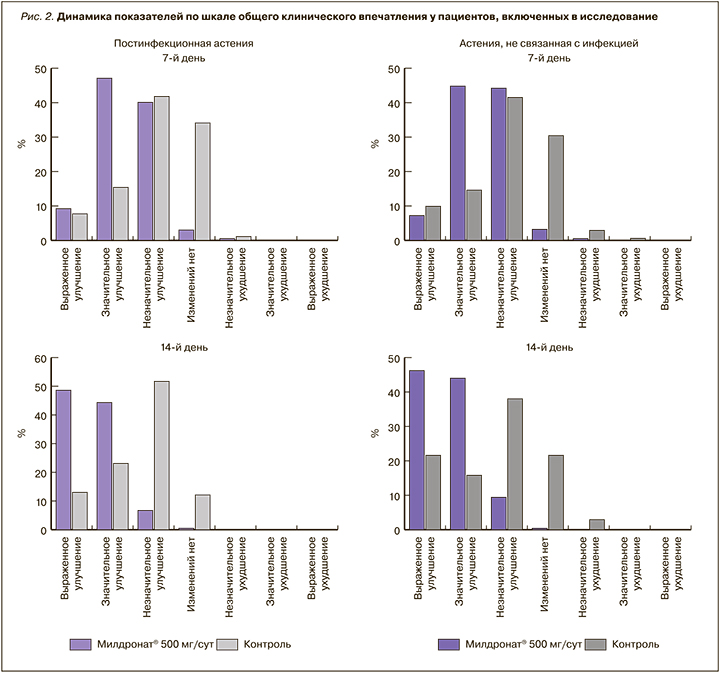
Полученные результаты также нашли подтверждение в положительной динамике показателей по шкале CGI-I, которая показана на рисунке 2. Так, в подгруппах основной группы, получавшей Милдронат®, имело место достоверное увеличение доли участников со «значительным» и «выраженным» клиническим улучшением состояния уже к 7-му дню терапии в сравнении с группой пациентов, получавших поливитамины. На момент окончания наблюдения доля участников исследования в группе препарата Милдронат®, у которых клиническое улучшение состояния расценивалось врачами как «значительное» и «выраженное», составила более 90%, а в контроле – менее 41%. Необходимо подчеркнуть сопоставимую эффективность терапии препаратом Милдронат® как у пациентов с астенией, перенесших инфекционное заболевание, так и без такового.
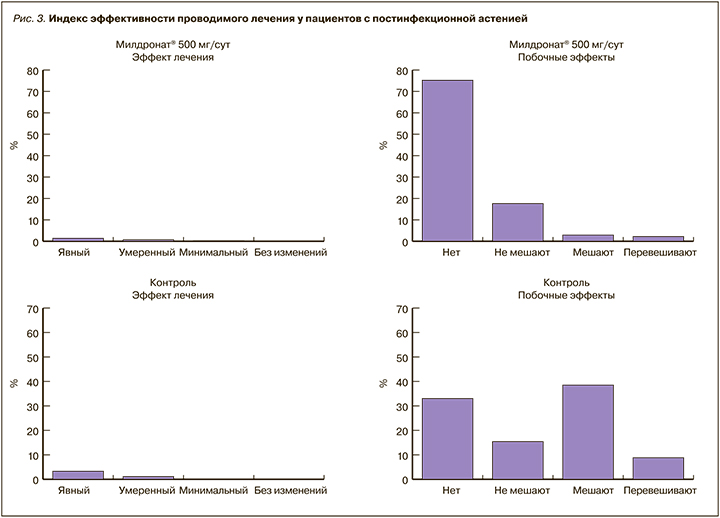
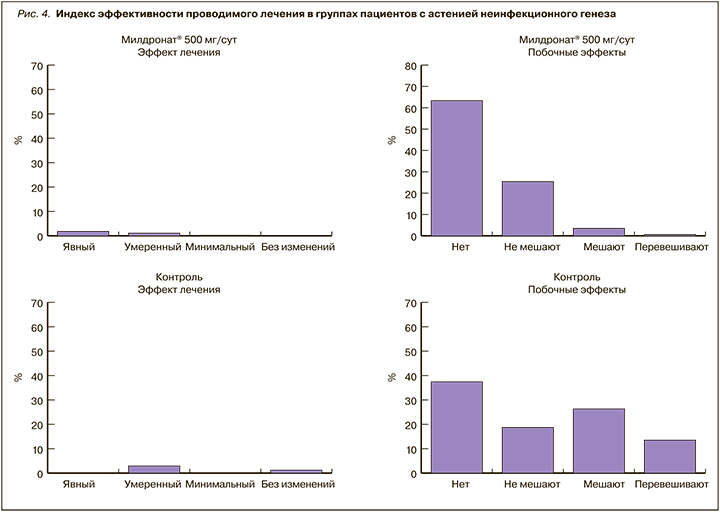
Показатель индекса эффективности изучаемых в исследовании стратегий лечения астении показан на рисунках 3 и 4. На них хорошо видно, что в основной группе доля пациентов с максимальным индексом эффективности «явное улучшение и отсутствие побочных эффектов» к 14-му дню терапии составила более 75% для пациентов с постинфекционной астенией и более 63% для пациентов с астенией неинфекционного генеза, что значительно превысило аналогичные значения в контрольной группе. Добавим, что к окончанию исследования в подгруппах контрольной группы доля пациентов без отмеченного улучшения состояния составляла до 22%. Оценка переносимости терапии в обеих группах продемонстрировала низкую частоту нежелательных явлений, связанных с приемом препарата Милдронат® или поливитаминных комплексов. Серьезных побочных эффектов ни в одной из групп зафиксировано не было.
Таким образом, полное восстановление работоспособности, отмечаемое пациентами и врачами и подтвержденное нормализацией показателей теста «таблицы Шульте», шкалы MFI-20 и шкалы CGI-I к 3-му визиту, могут считаться главными критериями выздоровления для пациента с астенией без тяжелых сопутствующих заболеваний (ССЗ или ЦВЗ). Полученные результаты говорят о возможности достижения полноценного восстановления в группе пациентов, получавших препарат Милдронат®. Это может означать наличие значимых патогенетических преимуществ такой терапии и дает основания рекомендовать ее для широкого применения в клинической практике.
ЗАКЛЮЧЕНИЕ
Таким образом, результаты исследования ТОНУС- 1 свидетельствуют об эффективности лечения симптоматической астении препаратом Милдронат® в дозе 500 мг/сут в течение 14 дней у широкого круга пациентов в терапевтической практике.



