ВВЕДЕНИЕ
Аллергический ринит (АР) – заболевание, сопровождающееся IgE-опосредованным воспалением слизистой оболочки полости носа (которое развивается под действием аллергенов) и наличием ежедневно проявляющихся в течение часа и более хотя бы двух из следующих симптомов: заложенности носа, ринореи, зуда в полости носа, чихания. В развитии заболевания выделяют раннюю и отсроченную фазы, протекающие с характерными симптомами и формированием неспецифической назальной гиперреактивности [1–6].
Обструктивное апноэ сна (ОАС) – состояние, характеризующееся храпом, периодическим спадением верхних дыхательных путей на уровне глотки и прекращением легочной вентиляции при сохраняющихся дыхательных усилиях, снижением уровня кислорода в крови, грубой фрагментацией сна и избыточной дневной сонливостью. Степень тяжести ОАС определяется по количеству респираторных событий в час (индекс апноэ/гипопноэ, ИАГ). При легкой степени тяжести ИАГ составляет ≥ 5 и < 15, при средней – ≥ 15 и < 30, при тяжелой – ≥ 30 [7, 8].
Сочетание АР и ОАС считается крайне неблагоприятным, прежде всего с точки зрения влияния на качество сна, работоспособность и когнитивные функции больного. Цель данной статьи – обзор литературы, посвященной коморбидности АР и ОАС, ее распространенности, патогенетическим механизмам и возможностям эффективной терапии.
РАСПРОСТРАНЕННОСТЬ СОЧЕТАНИЯ АР И ОАС У ВЗРОСЛЫХ
Частота АР, по данным исследований, проведенных в разных странах мира, варьирует в пределах 4–32%, в России – 10–24% [1, 4–6].
Распространенность ОАС составляет в среднем около 24% у мужчин и около 9% у женщин, однако может быть существенно выше в популяции пациентов с сопутствующими заболеваниями, такими как ожирение, метаболический синдром, артериальная гипертензия, сахарный диабет, гипотиреоз и ряд других [9–14].
Сосуществование АР и ОАС – достаточно частое явление в клинической практике, при этом ряд авторов рассматривает АР в качестве независимого фактора риска ОАС.
Согласно результатам метаанализа с участием 6086 пациентов, частота встречаемости АР у взрослых с различными нарушениями дыхания во сне равнялась 22,8% (95% доверительный интервал (ДИ): 15,0–30,6), у больных с ОАС – 35,2% (95% ДИ: 25,6–44,7), однако значимых различий в группах пациентов с ОАС с или без сопутствующего АР по таким показателям, как индекс массы тела, окружность шеи, ИАГ и балл по опроснику сонливости Эпворта, выявлено не было [15]. Эти данные коррелируют с результатами работы, в которой ОАС было диагностировано у 35% пациентов с АР против 10% в контрольной группе [16], и с данными таиландского исследования, где показатель распространенности пациентов с высоким риском развития ОАС среди больных с АР составил 23,3%, что в два раза превышало аналогичное значение в общей популяции [17].
ВЛИЯНИЕ АР И ОАС НА СОН
Известно, что пациенты с АР часто предъявляют жалобы на нарушения сна, дневную сонливость, утомляемость, снижение работоспособности. Этому есть ряд объяснений. Прежде всего, основные симптомы АР, такие как заложенность носа и ринорея, могут негативно сказываться на качестве сна, способствовать накоплению усталости и снижению работоспособности. Кроме того, отрицательно влиять на сон могут провоспалительные медиаторы – гистамин, лейкотриены (ЛТ), интерлейкин 1β (ИЛ-1β) и ИЛ-4, которые, играя ключевую роль в патогенезе АР, также участвуют в регуляции цикла «сон – бодрствование», когнитивных функций и памяти [18–21]. В частности, Krouse H.J. et al. опубликовали результаты исследования, в котором показано, что у пациентов с АР уровень ИЛ-1b, ИЛ-4 и ИЛ-10 выше, чем у лиц без аллергической патологии, и это прямо коррелирует с укорочением фазы быстрого сна и удлинением процесса засыпания [22].
Частые пробуждения в течение ночи, нарушения фазовой структуры сна, дневная сонливость относятся к хорошо изученным клиническим проявлениям ОАС. При этом ряд авторов получил данные, что и при этой патологии повышается продукция ИЛ-1, ИЛ-4, ИЛ-6 и фактора некроза опухоли-альфа (ФНО-α), которые могут индуцировать воспаление и вызывать назальную обструкцию (рис. 1) [23–26].

Дополнительным механизмом преходящей гипоксии и фрагментации сна у пациентов с ОАС выступает оксидативный стресс с гиперпродукцией активных форм кислорода. В то же время окислительный стресс, возникающий вследствие дисбаланса между усилением окислительных процессов в организме и недостаточной активностью антиоксидантной защиты, может способствовать повышению интенсивности воспаления на фоне АР [24, 27].
Также при ОАС установлена прямая корреляция между повышением отношения Т-хелперов 17-го типа к регуляторным Т-лимфоцитам (Th17/Treg) и ИАГ. Th17 имеют чрезвычайно важное значение в развитии аллергической реакции как продуценты ИЛ-17, а Treg управляют иммунным ответом и вовлечены в формирование иммунологической толерантности. Дисбаланс Th17 и Treg при АР и ОАС соответственно может способствовать прогрессированию той и другой патологии независимо от того, какой патологический процесс развился раньше [28–31].
В качестве возможного механизма нарушений сна при АР обсуждается и тригеминокардиальный рефлекс, который при стимуляции любого участка тройничного нерва приводит к кардиореспираторным расстройствам, включая апноэ. Такую стимуляцию тройничного нерва у больных АР могут вызывать назальная обструкция или ринорея [32].
Таким образом, очевидно, что и АР, и ОАС обладают целым комплексом механизмов, потенциально вызывающих нарушения сна.
ПАТОГЕНЕЗ АР И ОАС ПРИ СОЧЕТАННОМ ТЕЧЕНИИ
Назальная обструкция и ОАС
Заложенность носа при АР ассоциируется с увеличением риска развития среднетяжелого или тяжелого ОАС в 1,8 раза и, по мнению ряда авторов, может считаться независимым фактором риска ОАС, так как нормальное носовое дыхание – один из факторов поддержания нормального тонуса дыхательных путей [33, 34]. Объясняется это тем, что, хотя участок, где наступает нарушение проходимости верхних дыхательных путей во время сна, расположен в нижней части носоглотки и в ротоглотке, не менее 50% сопротивления верхних дыхательных путей приходится именно на полость носа. При этом увеличивается перепад давления между имеющимся в просвете дыхательных путей (отрицательное давление) и атмосферой (положительное давление), и чем выше сопротивление в полости носа, тем меньший воздушный поток проходит через глотку [35–38].
Fitzpatrick M.F. et al. подтвердили эти наблюдения, продемонстрировав повышение сопротивления дыхательных путей при дыхании через рот в сравнении с носовым дыханием. Авторы провели рандомизированное перекрестное исследование и сопоставили сопротивление дыхательных путей во время сна при дыхании через нос и через рот у 12 здоровых добровольцев (средний возраст 30 ± 4 года) без избыточного веса и нарушений носового дыхания. В период бодрствования какой-либо разницы не было обнаружено как в положении лежа на боку, так и на спине. А вот во время сна были зафиксированы явное увеличение сопротивления верхних дыхательных путей, рост числа эпизодов апноэ и гипопноэ, а также уменьшение продолжительности сна при ротовом дыхании [39]. Чтобы выяснить, характерна ли такая особенность для пациентов с ОАС, Koutsourelakis I. et al. выполнили исследование у 28 пациентов с ОАС (ИАГ 26 ± 5 / ч) и 13 пациентов с храпом без ОАС (ИАГ 1,3 ± 0,3 / ч). У включенных в испытание лиц не имелось патологии носа, и при риноманометрии определялось нормальное назальное сопротивление в положении сидя и лежа на спине в период бодрствования. Во время сна у больных с апноэ оказались более частыми периоды ротового или смешанного дыхания по сравнению с пациентами с храпом без ОАС. Авторами была отмечена положительная корреляция между периодами дыхания через рот и величиной ИАГ и отрицательная корреляция с показателями насыщения кислородом, что подтверждает значимую роль носового дыхания в поддержании стабильности верхних дыхательных путей [40].
Olsen K.D. et al. изучили влияние экспериментальной носовой обструкции на сон здоровых добровольцев. В исследовании участвовали 8 мужчин в возрасте от 30 до 50 лет без избыточной массы тела, нарушений сна и патологии носа в анамнезе. Одну ночь они дышали через нос, вторую – с заложенным носом (для моделирования назальной обструкции использовались ватные тампоны с вазелином, заложенные в преддверие носа). В результате были получены данные о большем числе пробуждений, изменений положения тела во сне и значимом увеличении количества эпизодов апноэ и гипопноэ при обструкции носа [41].
В исследовании с аналогичным дизайном влияние назальной обструкции на сон оценивалось при помощи полисомнографии у 10 здоровых добровольце в возрасте от 25 до 45 лет. Оно проводилось в течение трех ночей подряд: первая ночь в стандартных условиях, вторая – с моделированием назальной обструкции, третья – без обструкции. Результаты работы соответствовали полученным ранее [41], т. е. отмечались более частые пробуждения и значимое увеличение количества эпизодов апноэ/гипопноэ при назальной обструкции (общее число эпизодов 88 ± 34) по сравнению с периодом без обструкции (общее число эпизодов 34 ± 19) [42].
Все эти данные соответствуют современным представлениям о том, что у пациентов с ОАС преобладает ротовое дыхание, предрасполагающее к окклюзии глотки и эпизодам обструктивного апноэ во сне.
Ротовое дыхание
Когда рот во время сна открыт, нижняя челюсть перемещается вниз, смещая в этом же направлении язык. Изменение положение языка связано с уменьшением диаметра глотки и укорочением мышц, расширяющих верхние дыхательные пути, что нарушает их работу, т. е. ротовое дыхание механически увеличивает сопротивление воздушному потоку и еще больше повышает риск развития ОАС или утяжеляет его течение. Пассивное напряжение мягких тканей лица и шеи приводит к тому, что нижняя челюсть растет больше каудально, чем кпереди, и это тоже увеличивает вероятность развития ОАС в данной популяции [38, 43–46].
Значимую роль ротового дыхания в патогенезе ОАС подтверждают результаты исследования, в котором изучалось влияние CPAP-терапии на частоту и продолжительность такого дыхания у пациентов с ОАС. До начала терапии ИАГ был 55,8 ± 26 и снижался при ее проведении до 8,0 ± 3,4. Количество эпизодов ротового дыхания уменьшилось с 35,2 ± 19,7 в час перед лечением до 5,0 ± 5,2 в час после него (p < 0,01). Значения общей продолжительности ротового дыхания в период сна до и после CPAP-терапии составили 13,5 ± 10,2 и 4,6 ± 5,5 мин. в час соответственно (p < 0,05) [47].
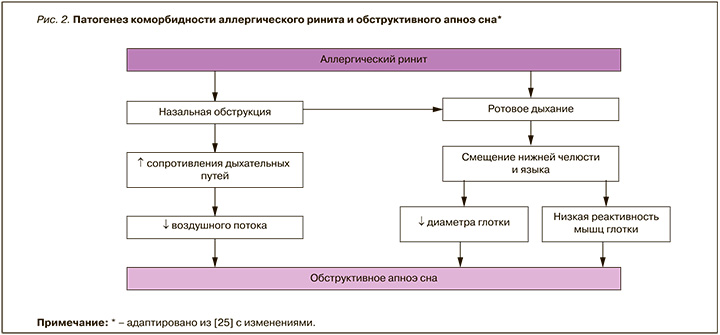
Таким образом, очевидно, что назальная обструкция, являющаяся одним из основных симптомов АР, лежит в основе патогенеза коморбидности и оказывает значимое влияние на течение ОАС (рис. 2).
ВЛИЯНИЕ ТЕРАПИИ АР НА ТЕЧЕНИЕ ОАС
В связи с вышесказанным возникает закономерный вопрос: может ли лечение АР отразиться на течении ОАС?
Согласно клиническим рекомендациям, для достижения контроля симптомов АР рекомендованы интраназальные и системные Н1-антигистаминные средства, интраназальные глюкокортикостероиды (инГКС), интраназальные препараты кромоглициевой кислоты и антагонисты лейкотриеновых рецепторов (АЛР). Для купирования симптомов в случае обострений дополнительно могут быть использованы назальные деконгестанты и системные глюкокортикостероиды. При коморбидности АР и ОАС изучено применение трех групп лекарственных средств: инГКС, АЛР и назальных деконгестантов [1].
Интраназальные глюкокортикостероиды
ИнГКС – наиболее эффективные препараты для лечения АР ввиду их выраженного противовоспалительного действия и способности влиять на все этапы патогенеза заболевания. Средства этой группы уменьшают количество тучных клеток, эозинофилов, Т-лимфоцитов, ингибируют синтез ими провоспалительных медиаторов, подавляют экспрессию молекул адгезии в слизистой оболочке полости носа. При систематическом применении инГКС это приводит к купированию основных симптомов АР. Одновременно благодаря низкой системной биодоступности инГКС практически не проявляют системных эффектов, имеют высокий профиль безопасности, что позволяет использовать их в течение длительного времени в качестве средств базисной терапии персистирующего АР.
Получены убедительные данные о том, что регулярное применение инГКС для лечения АР может одновременно положительно влиять и на течение ОАС. Так, в рандомизированном плацебо-контролируемом исследовании с участием 23 пациентов с храпом и АР (13 пациентов с ИАГ ≥ 10 и 10 пациентов без апноэ) через 4 нед. лечения в общей популяции включенных больных ИАГ был значимо ниже в группе, получавшей флутиказона пропионат, по сравнению группой плацебо: 11,9 (22,6) и 20 (26,3) соответственно (p < 0,05). Та же тенденция наблюдалась в группе пациентов с ОАС: 23,3 (21,3) против 30,3 (31,9) соответственно (p < 0,05). В то же время на фоне применения инГКС не было отмечено значимых изменений в показателях сатурации кислорода, храпа и качества сна [48].
В другом исследовании изучался интраназальный мометазон, который применялся в дозе 200 мкг 2 р./ сут. в течение 10–12 нед. у пациентов с ОАС, имеющих сопутствующий аллергический (n = 34) или неаллергический ринит (нАР) (n = 21). Авторы оценивали результаты полисомнографии, качество сна, дневную сонливость до и после лечения, а также выполняли иммуногистохимическое исследование назального биоптата для определения типа воспаления. В этом исследовании не было получено статистически достоверных данных о положительном влиянии мометазона на ИАГ в исследуемой популяции в целом, однако при сравнении между подгруппами больных с АР и нАР более значимое снижение ИАГ имело место среди пациентов с АР: 11,0 ± 20,6 против 3,3 ± 15 (p = 0,01). Значимое улучшение показателя сатурации кислородом, более высокий балл по шкале сонливости Эпворта также были получены только в группе пациентов с АР. Снижение количества эозинофилов было выявлено у больных с АР в биоптатах, взятых с трех разных участков (нижних носовых раковин, носоглотки, язычка), тогда как у пациентов с нАР – только в биоптате из носоглотки. Снижение экспрессии CD4 Т-лимфоцитов у пациентов с АР также было обнаружено в биоптатах со всех трех зон, а при нАР – только в биоптате, взятом с нижних носовых раковин. В результате исследователи сделали вывод о положительном влиянии интраназального мометазона на состояние пациентов с ОАС только при сопутствующем АР [49].
Meltzer E.O. et al. в двойном слепом плацебо-контролируемом исследовании оценивали влияние мометазона фуроата в дозе 200 мкг/сут. на назальные симптомы, включая назальную обструкцию, показатели сна, качество жизни и дневную активность, у пациентов с АР и сопутствующими нарушениями сна. Из 30 человек, включенных в исследование, 20 были распределены в группу, получавшую указанный инГКС, 10 – в группу плацебо. После лечения в группе, получавшей мометазон, наблюдались положительная динамика назальных симптомов, показателей сна по шкале сонливости Эпворта и повышение повседневной активности. ОАС у пациентов, участвовавших в исследовании, не было [50].
В работе Acar M. et al. эффективность мометазона исследовалась при АР и ОАС у 80 пациентов в возрасте от 30 до 50 лет. Участники были разделены на четыре группы, получавшие мометазона фуроат в суточной дозе 200 мкг, дезлоратадин 10 мг/ сут., их комбинацию или плацебо соответственно. В группах мометазона фуроата и мометазона фуроата в комбинации с дезлоратадином отмечались достоверное снижение ИАГ, улучшение качества сна. Достоверных различий между этими группами выявлено не было, а значит, эффективность лечения определялась применением мометазона, но не антигистаминного препарата [51].
Результаты, полученные в исследованиях у взрослых, подтверждаются данными исследований с аналогичным дизайном, проведенных в педиатрической популяции [52–54].
Таким образом, можно заключить, что применение инГКС может быть рекомендовано в качестве базисной терапии пациентам с АР и ОАС.
Антагонисты лейкотриеновых рецепторов
АЛР являются одними из эффективных средств базисной терапии АР с оптимальным профилем эффективности и безопасности. При систематическом применении они подавляют активность эозинофильного воспаления, способствуют уменьшению эозинофилии крови и слизистой оболочки дыхательных путей, снижают выраженность симптомов АР [55, 56]. В свете обсуждаемой нами проблемы интересен факт выявления повышенной экспрессии лейкотриеновых рецепторов в ткани миндалин у детей с ОАС [57].
Большая часть исследований по оценке эффективности АЛР при ОАС выполнялась в педиатрической популяции; согласно результатам метаанализа, опубликованного в 2021 г., представлены убедительные доказательства в пользу применения препарата монтелукаст для лечения ОАС у детей [58].
Что касается исследований у взрослых, то эффективность противовоспалительной терапии при ОАС легкой степени тяжести исследовалась в работе Smith D.F. et al. В двойное слепое рандомизированное исследование включались лица в возрасте от 21 года и старше с ИАГ ≤ 15, которые в течение 12 нед. получали монтелукаст и флутиказон (основная группа) или плацебо (контрольная группа). По окончании терапии у пациентов основной группы увеличились общая продолжительность сна (p = 0,02) и продолжительность фазы быстрого сна (p = 0,05), однако достоверного роста ИАГ и балла по шкале сонливости Эпворта установлено не было (p = 0,37–0,46) [59].
Следовательно, если целесообразность применения АЛР в терапии ОАС у детей можно считать доказанной, то для подтверждения такой рекомендации применительно к взрослым требуются дальнейшие исследования.
Назальные деконгестанты
Назальные деконгестанты, согласно действующим клиническим рекомендациям, служат средствами скорой помощи для купирования назальной обструкции у больных АР, что предполагает их применение в течение ограниченного периода и не позволяет предположить возможность стойкого терапевтического эффекта при ОАС [1]. Соответствующих исследований у пациентов с сочетанным течением ОАС и АР не проводилось, а имеющиеся данные о применении назальных деконгестантов при ОАС и назальной обструкции свидетельствуют об отсутствии их достоверного терапевтического эффекта [60, 61]. Учитывая эту особенность, а также значимые побочные эффекты этой группы лекарственных средств, их использование при АР и сопутствующем ОАС с целью уменьшения выраженности последнего представляется нецелесообразным.
ЗАКЛЮЧЕНИЕ
Сочетание АР и ОАС является достаточно распространенным и неблагоприятным с точки зрения отрицательного влияния на течение обоих заболеваний. Это определяет необходимость выбора лекарственных средств для лечения АР с учетом данной коморбидности. В настоящее время, исходя из результатов ряда исследований, к средствам, имеющим подтвержденную эффективность и безопасность у больных с АР и ОАС, можно отнести инГКС и АЛР. Вместе с тем, учитывая небольшой объем данных, на которых базируется наше утверждение, следует признать важность проведения дальнейших исследований в этом направлении.



