Фибрилляция предсердий (ФП), являясь наиболее распространенной аритмией, ассоциируется с повышением риска смерти, развития инсульта, хронической сердечной недостаточности (СН) и необходимости обращения за медицинской помощью, в том числе стационарной, со снижением качества жизни [1—3].
Риск развития ишемического инсульта (ИИ) и системных эмболий не различается при постоянной, персистирующей или пароксизмальной ФП, в случае наличия или отсутствия симптомов, поэтому форма ФП не учитывается при оценке индивидуального риска развития тромбоэмболических осложнений (ТЭО) [4—6].
Принятие решения о необходимости восстановления синусового ритма у больных ФП — сложная задача, требующая от врача учета целого ряда параметров, связанных с оценкой как потенциального риска/пользы для пациента, его ожиданий от лечения и способности его адекватно придерживаться, так и особенности течения заболевания.
С одной стороны, ФП приводит к целому комплексу патофизиологических изменений миокарда, ключевым из которых для развития ТЭО является дисфункция миокарда предсердий, особенно ушка левого предсердия (УЛП). Нарушения кровотока при ФП характеризуются стазом крови в левом предсердии (ЛП), снижением скорости кровотока в УЛП и наличием спонтанных эхосигналов при чреспищеводной эхокардиографии (ЧП-ЭхоКГ), активацией тромбоцитов и повышением уровня концентрации С-реактивного белка — маркера воспаления. При этом повышается уровень D-димера, фибриногена (маркеров тромбообразования и гиперкоагуляции), уровень маркеров повреждения эндотелия (Р-селектин, фактор Виллебранда), активируются тромбоциты [7—13]. Изменения эндокарда включают нарастающую дилатацию предсердий, повреждение эндокарда и отек/фиброэластическую инфильтрацию внеклеточного матрикса. Дискоординированная контрактильная деятельность предсердий способствует стазу крови в полости ЛП и, более всего, в УЛП, где локализуются практически 90% образующихся тромбов [11, 13].
По данным Американской ассоциации сердца за 2011 г., ФП увеличивает риск развития инсульта в 5 раз во всех возрастных группах по сравнению с общей популяцией [14—16]. Риск развития ИИ и системных эмболий, как отмечено ранее, не различается при постоянной, персистирующей или пароксизмальной ФП, поэтому форма ФП не учитывается при оценке индивидуального риска развития ТЭО [4, 5, 8].
С другой стороны, учитывая отсутствие достоверных различий по смертности, количеству госпитализаций, качеству жизни при сравнении 2 стратегий: контроль ритма и контроль частоты сердечных сокращений (ЧСС) в крупных клинических исследованиях STAF PIAF (2000), AFFIRM (2002), RACE (2002), STAF (2003), HOT-CAFE (2004), AF-CHF (2008), J-RHYTHM (2009), выбор тактики контроля ритма или ЧСС не является строго регламентированным и предоставляется на усмотрение врача [1, 2, 17—24].
По последним данным, более 50% кардиологов отдают предпочтение контролю ритма сердца перед контролем ЧСС [25—27].
Согласно современным клиническим рекомендациям, в ряде ситуаций предпочтение следует отдавать контролю ритма: при сохранении выраженных симптомов ФП (индекс EHRA ≥2), несмотря на адекватный контроль ЧСС; при ФП, сопровождающейся СН, для купирования симптомов; у молодых пациентов, у которых не исключается возможность катетерной абляции; у пациентов с вторичной ФП, у которых удалось устранить триггер или субстрат аритмии (например, ишемию или гипертиреоз) [1, 2].
Независимо от вида кардиоверсии (фармакологическая или электрическая) существует повышенный риск развития тромбоэмболий. В связи с этим назначение антикоагулянтов (АК) признано обязательным перед плановой кардиоверсией, если ФП сохраняется более 48 ч или длительность ее неизвестна. Антикоагулянтную терапию (АКТ) следует продолжать, по крайней мере, в течение 4 нед после кардиоверсии, учитывая риск развития тромбоэмболий, связанный с дисфункцией ЛП и УЛП (так называемое оглушение предсердий) [28]. При наличии факторов риска (ФР) развития инсульта или рецидива ФП, что случается достаточно часто и зачастую протекает бессимптомно [29], лечение АК проводят пожизненно даже при сохранении синусового ритма после кардиоверсии [1, 2].
Если эпизод ФП продолжается менее 48 ч, то кардиоверсию можно выполнить в неотложном порядке под прикрытием внутривенного введения нефракционированного гепарина (НФГ) с последующей инфузией или подкожным введением низкомолекулярного гепарина (НМГ). У пациентов с ФП >48 ч и нарушением гемодинамики (стенокардия, инфаркт миокарда — ИМ, шок или отек легких) следует провести неотложную кардиоверсию. Перед восстановлением ритма назначают НФГ или НМГ. После кардиоверсии назначают пероральные АК. Длительность АКТ (4 нед или пожизненно) зависит от наличия ФР развития инсульта, рассчитанного по шкалам CHADS2 и CHA2DS2-VASс [1, 2] (рис. 1).
Обязательная 3-недельная АКТ перед кардиоверсией может быть сокращена, если при ЧП-ЭхоКГ не будет выявлен тромб в ЛП или УЛП. С помощью этого метода можно выявить не только тромб в УЛП или в других участках этой камеры сердца, но и спонтанные эхосигналы или атеросклеротическую бляшку в аорте. Кардиоверсия под контролем ЧП-ЭхоКГ может служить альтернативой 3-недельной АКТ перед восстановлением ритма, когда имеются опытный персонал и технические возможности, а также когда необходима ранняя кардиоверсия, или АКТ невозможна (отказ пациента или высокий риск кровотечений), или имеется высокая вероятность тромба в ЛП или УЛП [28, 30]. Если при ЧП-ЭхоКГ обнаружен тромб, то перед кардиоверсией назначают НФГ или НМГ на фоне приема пероральных АК [1, 2].
В случае наличия тромба в ЛП или УЛП следует проводить лечение пероральными АК и повторить ЧП-ЭхоКГ. При растворении тромба может быть проведена кардиоверсия, после которой назначают пожизненную терапию пероральными АК. Если тромб сохраняется, можно отказаться от восстановления ритма в пользу контроля частоты желудочкового ритма, особенно если симптомы ФП контролируются, учитывая высокий риск тромбоэмболий на фоне кардиоверсии [1, 2].
Долгое время единственной группой АК, используемых для длительной профилактики ТЭО у больных с ФП, оставались антагонисты витамина К (АВК), что нашло отражение и в современных рекомендациях, где подробно описана антитромботическая терапия (АТТ) именно с позиций назначения АВК [1, 2]. Однако их прием сопряжен с рядом трудностей.
Действие АВК (в частности, наиболее широко используемого из них варфарина) реализуется за счет блокирования витамин К-зависимых факторов свертывания крови (II, VII, IX, X) [31]. Варфарин обладает непредсказуемой фармакокинетикой и фармакодинамикой вследствие как генетических особенностей пациентов (определяющих наличие резистентных и гиперчувствительных к варфарину больных), так и специфики его метаболизма (выраженное лекарственное и пищевое взаимодействие) [32—35]. АВК характеризуются длительным началом и окончанием действия, имеют короткий промежуток времени для терапевтических мероприятий, балансирующий между неэффективностью в отношении предупреждения ИИ и других ТЭО и повышенным риском геморрагических осложнений как результата неадекватной гипокоагуляции [36]. Ввиду этого эффективная и безопасная терапия варфарином обусловливает необходимость регулярного мониторинга такой терапии и коррекции дозы препарата[1, 2].
Для лабораторного контроля степени гипокоагуляции на фоне применения АВК используется унифицированный показатель — международное нормализованное отношение (МНО), который представляет собой специально рассчитанный протромбиновый индекс. Целевой диапазон МНО для больных с неклапанной ФП независимо от возраста составляет от 2,0 до 3,0 [1, 2].
Доля времени нахождения МНО в целевом диапазоне, приближающаяся к 100%, сложно достижима даже при проведении крупных международных исследований, в которых затрачиваются большие усилия по контролю МНО и дозы варфарина; в реальной клинической практике такого результата достичь еще труднее, поэтому поддерживать МНО в целевом диапазоне удается, в лучшем случае, только на протяжении 65% (ACTIVE W, 2006) — 76,2% (AuriculAе, 2012) времени [37—41].
Для пациента мониторинг гипокоагуляции означает необходимость наблюдения у врача, компетентного в проведении терапии АВК. Однако отсутствие должной организации помощи больным, получающим терапию варфарином (отсутствие специализированных центров, не предусмотренное стандартами оказания медицинской помощи необходимое количество определений МНО при подборе дозы варфарина и контроле терапии), приводит к нерегулярным визитам к врачу и большому временному разрыву между измерением МНО и коррекцией дозы препарата [42]. Все эти трудности при применении непрямых АК зачастую приводят к отказу больных от начала или продолжения лечения, а также к тому, что прием варфарина в условиях затруднительного мониторинга сопряжен и с неэффективной гипокоагуляцией, и с высоким риском развития геморрагических осложнений [38, 39, 43].
Закономерно, что ограничения и трудности применения АВК для пролонгированной АТТ стимулировали исследователей к поиску альтернативных АК, которые бы применялись перорально в фиксированных дозировках, имели бы предсказуемые фармакологические характеристики, низкое пищевое и лекарственное взаимодействие и не требовали, таким образом, постоянного регулярного лабораторного контроля [32, 44—49].
Так как процесс коагуляции является каскадным и многокомпонентным, соответственно множеству возможных точек приложения и разрабатывались новые АК. В противовес АВК, действующим сразу на комплекс факторов свертывания, новые АК селективно блокируют активные формы отдельных факторов коагуляционного каскада [32, 44—50].
Одним из препаратов, которые могут служить достойной альтернативой варфарину, является дабигатран [44, 46—49, 51, 52]. Дабигатран назначается перорально в виде пролекарства дабигатрана этексилата, который под действием циркулирующих в плазме эстераз быстро метаболизируется в активный дабигатран. Биодоступность дабигатрана примерно 6%, период полувыведения в среднем составляет 12—17 ч, максимальная концентрация препарата в плазме после приема внутрь достигается в течение 0,5—2 ч. Выделение дабигатрана осуществляется преимущественно почками (на 80%) [49, 52, 53].
Антикоагулянтный эффект дабигатрана имеет линейный дозозависимый обратимый характер, что позволяет добиться стабильной гипокоагуляции при назначении этого препарата в фиксированной дозе, не требующей постоянной коррекции и лабораторного контроля. Препарат не метаболизируется с участием цитохромов CYP-450 и вследствие этого не имеет существенных лекарственных взаимодействий [47, 48, 54, 55]. В 2009 г. опубликованы результаты крупного рандомизированного исследования RE-LY (The Randomized Evaluation of Long-Term Anticoagulation Therapy), включавшего 18 113 больных с ФП, в котором сравнивались эффективность и безопасность АТТ дабигатраном в дозе 110 мг 2 раза в день, дабигатраном в дозе 150 мг 2 раза в день и варфарином в дозе, необходимой для поддержания МНО в целевом диапазоне от 2,0 до 3,0. Результаты исследования RE-LY показали, что дабигатран в дозе 110 мг 2 раза в сутки не уступал варфарину в профилактике ИИ и системных эмболий (1,69% в год в группе варфарина, 1,53% в год в группе дабигатрана), однако вызывал меньшее число геморрагических осложнений (2,71% в год для дабигатрана против 3,36% в год в группе варфарина), а в дозе 150 мг 2 раза в сутки превосходил варфарин по эффективности (ИИ и системные эмболии 1,11% в год в группе дабигатрана), причем риск кровотечений в обеих группах не имел значимых различий [51, 53, 56].
Частота внутри- и внечерепных кровотечений в обеих группах дабигатрана была меньше, чем в группе варфарина, у пациентов моложе 75 лет; у больных старше 75 лет отмечено увеличение риска внечерепных кровотечений в обеих группах дабигатрана, при этом по частоте возникновения внутричерепных кровотечений достоверных различий не выявлено [56].
Важно отметить, что дабигатран в дозе 150 мг 2 раза в сутки по сравнению с варфарином достоверно снижал риск смерти от всех причин [51]. В дозе 150 мг 2 раза в сутки дабигатран тем больше превосходил варфарин по эффективности в плане профилактики ИИ и системной эмболии, чем выше был риск развития ТЭО. Наиболее выраженное преимущество отмечено среди пациентов группы высокого риска (3 балла и более по шкале CHADS2) [57].
При первоначальной обработке данных исследования RE-LY выявлено увеличение частоты ИМ в обеих группах дабигатрана. Однако в последующем проведенный анализ электрокардиограмм (ЭКГ) выявил 28 так называемых немых ИМ, определяемых по появлению нового патологического зубца Q на ЭКГ. После включения в анализ дополнительных данных достоверных различий в частоте ИМ между группами дабигатрана и варфарина выявлено не было [58].
Предшествующее использование АВК не отразилось на эффективности дабигатрана в обеих исследуемых дозах [59].
Представляет большой практический интерес применение дабигатрана у пациентов, подвергающихся кардиоверсии. В рамках исследования RE-LY произведено 1983 кардиоверсии у 1270 пациентов. ЧП-ЭхоКГ перед проведением кардиоверсии была выполнена у 25,5% больных в группе, получающей дабигатран в дозе 150 мг 2 раза в сутки, у 24,1% в группе дабигатрана в дозе 110 мг 2 раза в сутки и у 13,3% больных, получавших варфарин. Частота обнаружения тромбов в полостях сердца, успешность кардиоверсии, а также частота развития ИИ в течение 30 дней после кардиоверсии достоверно не различались во всех 3 группах пациентов. Эти данные свидетельствуют о сопоставимой эффективности дабигатрана с варфарином как АК при проведении кардиоверсии [60].
Существенным преимуществом дабигатрана перед варфарином при проведении кардиоверсии является быстрое начало действия препарата [60] (см. таблицу).
Таблица. Сравнительные характеристики варфарина и дабигатрана этексилата
Еще одно преимущество дабигатрана заключается в стабильности его гипокоагуляционного эффекта, что особенно важно в течение 1-й недели после восстановления синусового ритма, когда риск развития ТЭО особенно высок, а подбор дозы варфарина для достижения терапевтического МНО часто приходится именно на этот уязвимый период и ассоциирован с нестабильностью антитромботического эффекта варфарина. Терапевтическая концентрация дабигатрана в плазме достигается в пределах 2 ч после приема, тогда как при применении варфарина часто требуется дополнительное введение парентеральных АК в качестве переходной терапии, если МНО не находится в целевом диапазоне и ли если пациент не получал ранее АВК.
Из представленных данных можно сделать вывод, что дабигатран обладает доказанной эффективностью в профилактике ТЭО у больных с ФП и имеет ряд существенных преимуществ перед АВК. Дабигатран был зарегистрирован в странах Европы, США, Японии, Российской Федерации и вошел в американские, европейские и российские рекомендации по лечению ФП как альтернатива варфарину у больных, которым показана АТТ пероральными АК [1—3].
Согласно рекомендациям Европейского кардиологического общества и Всероссийского научного общества к ардиологов, п ациентам с н изким р иском кровотечений по индексу HAS-BLED дабигатран можно назначать в дозе 150 мг 2 раза в день, учитывая более высокую эффективность в профилактике ИИ и системных эмболий по сравнению с варфарином, более низкую частоту внутричерепных кровотечений и сходную частоту развития тяжелых кровотечений. Пациентам с более высоким риском развития кровотечения (индекс HAS-BLED ≥3) дабигатран может быть назначен в дозе 110 мг 2 раза в день, учитывая соизмеримую с АВК эффективность и более низкую частоту геморрагических осложнений. Больным с одним клинически значимым неосновным ФР по шкале CHA2DS2-VASc может быть назначен дабигатран в дозе 110 мг 2 раза в день [1, 2].
Из 2 исследуемых в RE-LY режимов приема дабигатрана Управление по контролю за качеством пищевых продуктов и лекарственных препаратов США (FDA) одобрило использование только дозы дабигатрана 150 мг 2 раза в сутки. Причиной тому послужило мнение о большем значении необратимых последствий ИИ и системных эмболий, чем нефатальных внечерепных кровотечений [61]. FDA зарегистрировало также дозу дабигатрана 75 мг 2 раза в сутки для больных с клиренсом креатинина 15—30 мл/мин, исходя из данных о фармакологических характеристиках препарата, однако такой режим приема не изучался в клинических исследованиях [3].
В качестве примера возможного применения дабигатрана этексилата при проведении электрической кардиоверсии приводим наше наблюдение.
Больной Н., 57 лет, обратился клинику с жалобами на одышку при привычной нагрузке, быструю утомляемость, слабость, периодически чувство неритмичного сердцебиения и перебоев в работе сердца.
В анамнезе у больного в течение 5 лет артериальная гипертония с максимальным повышением артериального давления до 180 и 120 мм рт.ст., при этом постоянную антигипертензивную терапию не получал, эпизодически принимал блокаторы кальциевых каналов (амлодипин). Последние 3 года больной неоднократно отмечал перебои в работе сердца, при этом на ЭКГ в поликлинике регистрировалась желудочковая экстрасистолия. Ухудшение состояния отметил в течение последних 7 дней до момента обращения, когда снизилась толерантность к нагрузке, больной при повседневной активности стал отмечать немотивированную слабость, нехарактерную утомляемость, а также одышку при подъеме на 2-й этаж лестницы. Кроме того, в течение 7 дней впервые стал ощущать неритмичное учащенное сердцебиение, более выраженное при нагрузке.
Объективно кожные покровы сухие, теплые, обычной окраски, видимых отеков нет, дыхание везикулярное, границы относительной тупости сердца расширены умеренно влево, тоны сердца приглушены, аритмичные, определяется акцент II тона на аорте, слабый систолический шум с p.m. на верхушке и в точке Боткина—Эрба. При измерении АД — 170 и 110 мм рт.ст.
На снятой ЭКГ впервые зафиксирована ФП, тахисистолическая форма, со средней ЧСС 122 уд/мин.
Больной был госпитализирован. Исследованы структура и функция щитовидной железы (патологии не выявлено), почек (скорость клубочковой фильтрации >90 мл/ч), печени (уровень трансаминаз, билирубина, общего белка в норме). В биохимическом анализе крови выявлена дислипидемия IIа типа по Фредриксену. Было назначено лечение: ингибиторы ангиотензинпревращающего фермента, диуретики, β-адреноблокаторы, блокаторы кальциевых каналов, статины.
Таким образом, состояние больного было расценено как возникновение симптомов СН на фоне развившегося пароксизма тахисистолической ФП. С учетом наличия артериальной гипертонии, СН согласно отечественным и зарубежным рекомендациям больной имеет высокий риск развития ТЭО (CHADS2=2), показана АТТ пероральными АК.
Учитывая категорический отказ пациента от приема варфарина из-за нежелания часто сдавать кровь для контроля МНО, в качестве АТТ использовался дабигатран 110 мг 2 раза в день.
С учетом первого в анамнезе пароксизма ФП, отсутствия предшествующей специфической АТТ, отсутствия указаний на вторичный генез аритмии была избрана тактика восстановления синусового ритма. Исходя из данных, полученных при опросе больного, ФП существовала более 48 ч. Согласно рекомендациям в такой ситуации необходима предварительная адекватная (МНО 2,0—3,0 в случае использования антагонистов витамина К) АКТ в течение как минимум 3 нед до кардиоверсии, альтернативой которой служит исключение тромбов в ЛП и в УЛП по данным ЧП-допплер-ЭхоКГ.
Было принято решение о проведении ЧП-ЭхоКГ для определения возможности и целесообразности восстановления синусового ритма. На 2-й день лечения была выполнена ЧП-допплер-ЭхоКГ: в УЛП визуализировался рыхлый тромб с частично подвижной головкой, выявлено значительно выраженное спонтанное контрастирование в полости ЛП (рис. 2), в связи с чем синусовый ритм не был восстановлен.
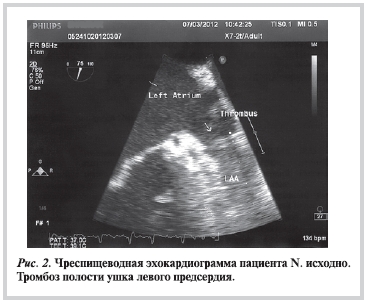
За время стационарного лечения стабилизировалось артериальное давление, улучшилась переносимость нагрузки, но сохранялись одышка, слабость, чувство неритмичного сердцебиения. Больной был выписан с рекомендациями о дальнейшем приеме дабигатрана 110 мг 2 раза в день и повторном выполнении ЧП-допплер-ЭхоКГ через 4 нед для растворения внутрисердечного тромба.
Больной продолжал получать АК, другие назначенные препараты. При повторной ЧП-допплер-ЭхоКГ, проведенной через 4 нед постоянного приема дабигатрана, посторонних включений в камерах сердца не обнаружено, умеренно выражено спонтанное контрастирование в полости и УЛП (рис. 3). Была произведена успешная электрическая кардиоверсия, назначена терапия для удержания синусового ритма.
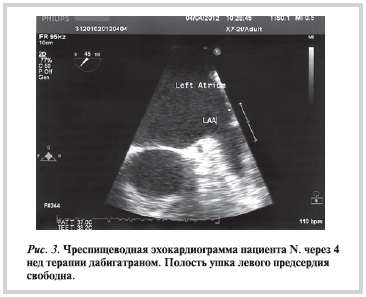
Таким образом, дабигатрана этексилат может успешно применяться при проведении кардиоверсии у больных с ФП, являясь эффективной и простой в применении альтернативой АВК.
Однако стоимость перехода от терапии АВК к использованию дабигатрана достаточно высока. Несмотря на отсутствие затрат на постоянный лабораторный контроль, стоимость самого препарата значительно превысила расходы на ведение пациентов, получающих стандартную терапию АВК. Так, в США стоимость дабигатрана примерно в 20 раз превышает стоимость варфарина. Однако недавно было опубликовано несколько исследований, в которых продемонстрировано преимущество дабигатрана по соотношению затраты/эффективность перед варфарином. При высоком риске развития ИИ (индекс CHADS2 ≥3), при индексе CHADS2≥2 и сопутствующем высоком риске развития геморрагических осложнений, а также у больных с лабильным и неустойчивым МНО дабигатран в дозе 150 мг 2 раза в день оказался экономически более выгодным, чем варфарин [62—64]. В Российской Федерации проведено фармакоэкономическое исследование, в котором показано, что дабигатрана этексилат может служить эффективной в фармакоэкономическом аспекте альтернативой варфарину у российских пациентов с ФП [65].



