Уже не вызывает сомнений, что уровень холестерина (ХС) липопротеидов низкой плотности (ЛНП) является фундаментальной детерминантой риска развития сердечно-сосудистых заболеваний (ССЗ) и причинным фактором прогрессирования атеросклероза [1, 2]. Результаты многих рандомизированных клинических исследований неизменно свидетельствуют о том, что снижение уровня ХС ЛНП с помощью терапии статинами является безопасным и крайне эффективным методом снижения риска развития инфаркта миокарда (ИМ), инсульта и сердечно-сосудистой смертности в целом [3—5].
Наряду с другими липидснижающими лекарственными препаратами (такими как никотиновая кислота, фибраты, эзетимиб и др.) только статины рекомендованы ведущими мировыми обществами по лечению атеросклероза в качестве монотерапии [6—8]. Секрет эффективности статинов кроется в их многочисленных, отличных от воздействия на липиды, плейотропных свойствах [9]. В пользу этого свидетельствуют и следующие данные.
В настоящее время нет сомнений, что концентрация ХС ЛНП вносит вклад в суммарный риск развития ССЗ. При этом ведущей целью терапии статинами является снижение уровня ХС ЛНП, однако исходный уровень ЛНП не всегда служит эффективным маркером для выявления группы пациентов, у которых прогнозируется польза от терапии статинами (рис. 1) [1, 10]. Так, по данным некоторых мета-анализов, относительный риск (ОР) сердечно-сосудистых осложнений (ССО) при терапии статинами не зависит от исходного уровня ХС ЛНП [10, 11]. Кроме того, в мета-анализе 14 плацебо-контролируемых клинических исследований с применением статинов (90 000 пациентов) выявлено, что ОР развития ССЗ снижался на 23% у пациентов с исходным уровнем ХС ЛНП как >4,5 ммоль/л, так и <4,5 ммоль/л [12]. Последующий обновленный мета-анализ, в который было включено 12 дополнительных исследований, показал, что высокие дозы статинов снижают риск развития ССЗ эффективнее, чем средние дозы, независимо от исходного уровня ХС ЛНП [13].

Таким образом, помимо липидснижающего действия статинов, их плейотропные эффекты вносят существенный вклад в известное влияние на клинические исходы. К нелипидным свойствам статинов относятся: уменьшение системного асептического воспаления (снижение активности свободнорадикального окисления, влияние на цитокиновый пул), антиагрегантное действие, влияние на процессы фиброза и ремоделирования [9, 14]. Все эти процессы суммарно приводят к улучшению функционального состояния эндотелия [14—16].
Глубокое понимание механизмов прогрессирования атеротромботического процесса, путей терапевтического воздействия, анализ доказательной базы применения статинов послужили предпосылкой к изменению курса американских рекомендаций на использование интенсивного режима применения статинов (аторвастатин 80 мг, розувастатин 20—40 мг) у пациентов высокого риска [8].
Особенности розувастатина. Благодаря бурному развитию медицины, основанной на доказательствах, мы знаем, что все препараты из группы статинов способны снижать исходные уровени ХС ЛНП, однако максимального его снижения удается достичь с помощью розувастатина. В этом отношении интересны результаты исследования MERCURY I, в котором при применении 10 мг розувастатина в 60—80% случаев были достигнуты целевые уровни ХС ЛНП [17].

Показательны также результаты исследования STELLAR, в которое был включен 2431 пациент с гиперхолестеринемией (исходные уровни ХС ЛНП от 4,1 до 6,4 ммоль/л) [18]. Все участники были рандомизированы в 4 группы приема различных препаратов из группы статинов (симвастатин, правастатин, аторвастатин, розувастатин). При сходной суточной дозе препарата 40 мг в группе правастатина наблюдалось снижение ХС ЛНП на 29,7%, в группе симвастатина — на 38,8%, в группе аторвастатина — на 47,8%, в группе розувастатина — на 55%.
 Чем же объясняется высокая эффективность терапии розувастатином по сравнению с другими статинами? Необходимо указать, что розувастатин является синтетическим статином четвертого поколения и представляет собой активную форму лекарственного препарата. Более 90% фармакологической активности по ингибированию циркулирующей ГМГ-КоА-редуктазы обеспечивается розувастатином и около 10% — его метаболитами. Выраженный эффект снижения уровня ХС у розувастатина обусловлен продолжительным периодом его полувыведения (19 ч), что позволяет длительно блокировать активность ключевого фермента биосинтеза ХС. Более того, розувастатин подвергается ограниченному метаболизму (10%) и обладает гидрофильными свойствами. Основным изоферментом, участвующим в метаболизме этого статина, является CYP2C9, в то время как изоферменты CYP2C19, CYP3A4 и CYP2D6 практически не вовлечены в метаболизм [19].
Чем же объясняется высокая эффективность терапии розувастатином по сравнению с другими статинами? Необходимо указать, что розувастатин является синтетическим статином четвертого поколения и представляет собой активную форму лекарственного препарата. Более 90% фармакологической активности по ингибированию циркулирующей ГМГ-КоА-редуктазы обеспечивается розувастатином и около 10% — его метаболитами. Выраженный эффект снижения уровня ХС у розувастатина обусловлен продолжительным периодом его полувыведения (19 ч), что позволяет длительно блокировать активность ключевого фермента биосинтеза ХС. Более того, розувастатин подвергается ограниченному метаболизму (10%) и обладает гидрофильными свойствами. Основным изоферментом, участвующим в метаболизме этого статина, является CYP2C9, в то время как изоферменты CYP2C19, CYP3A4 и CYP2D6 практически не вовлечены в метаболизм [19].
Такие свойства дают розувастатину преимущества при необходимости применения препарата в высоких дозах у пациентов с несколькими заболеваниями, при которых вероятность межлекарственных взаимодействий очень велика.
В России первым препаратом, биоэквивалентным оригинальному розувастатину, стал мертенил («Гедеон Рихтер») [20]. Препарат зарегистрирован в 2010 г. и с успехом применяется на протяжении 5 лет.
В клинической практике применение статинов осуществляется в трех главных направлениях: первичная профилактика, вторичная профилактика и терапия при остром коронарном синдроме (ОКС). За последние 5 лет завершено несколько клинических исследований (в том числе на территории Российской Федерации), в которых изучалось применение мертенила в дозе 10—40 мг/сут у больных разных категорий. В исследованиях получены данные о высокой гиполипидемической эффективности, переносимости и безопасности этого статина. Проанализируем имеющиеся результаты клинических исследований отдельно для каждой группы пациентов.
Первичная профилактика. Самым «ярким» исследованием в области изучения первичной профилактики ССЗ стало исследование JUPITER (Justification for the Use of statins in Primary prevention: an Intervention Trial Evaluating Rosuvastatin), в котором производилась оценка влияния терапии оригинальным препаратом розувастатина в дозе 20 мг у лиц с нормальным уровнем ХС ЛНП и концентрацией высокочувствительного С-реактивного белка (вч-СРБ) ≥2 мг/л [21].
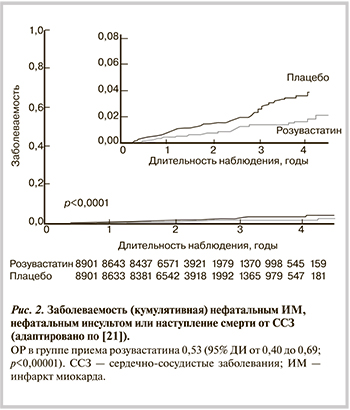
Результаты исследования изменили подход к первичной профилактике ССЗ. Так, применение розувастатина 20 мг привело к статистически значимому снижению числа ССО. Комбинированный риск развития ИМ, инсульта, артериальной реваскуляризации, госпитализации по поводу нестабильной стенокардии или сердечно-сосудистой смерти был ниже на 44% в группе вмешательства по сравнению с группой плацебо (p<0,00001) (рис. 2). Корреляция между эффективностью терапии и снижением уровня вч-СРБ выявлялась независимо от уровня ХС ЛНП.
С точки зрения эффективности и безопасности применения мертенила в качестве первичной профилактики у пациентов группы умеренного риска развития ССЗ показательны опубликованные в 2014 г. результаты открытого многоцентрового наблюдательного исследования «От 5 до 40» [22]. В этом исследовании принял участие 3591 пациент из групп умеренного, высокого и очень высокого риска развития ССЗ и с первичной гиперлипидемией IIа и IIб типов, не достигший целевых уровней ЛНП на фоне монотерапии статинами в течение 3 мес и более, а также никогда не принимавший статины. В исследование не включали лиц, получавших ранее терапию розувастатином.
 Среди всей выборки у 33% (n=1183) были определены признаки субклинического атеросклероза, выявляемые при оценке толщины интимы—медии (ТИМ). Средние показатели липидного состава крови в группе пациентов, ранее не получавших статины, и у лиц с умеренным нарушением липидного обмена составляли: общий холестерин (ОХС) 5,98±1,2 ммоль/л; ХС ЛНП 3,82±0,98 ммоль/л. Терапия мертенилом 5 мг/сут в течение 8 нед привела к снижению уровня ХС ЛНП на 35% и ОХС на 27,4% (p<0,01 для обоих показателей). Авторы данной работы отмечают, что сопоставимые данные по эффективности и безопасности розувастатина в дозе 5 мг получены нашими зарубежными коллегами [22, 23]. Лечение больных в дозе 10 мг/сут привело к снижению уровня ХС ЛНП на 41,1%, ОХС на 30% и триглицеридов (ТГ) на 19,1% (p<0,01), повышению уровня ХС липопротеидов высокой плотности (ЛВП) на 6,3% (p<0,05). Показатели безопасности (аспартатаминотрансфераза — АсАТ, аланинаминотрансфераза — АлАТ, креатинкиназа — КК) для обеих групп достоверно не отличались от исходных значений.
Среди всей выборки у 33% (n=1183) были определены признаки субклинического атеросклероза, выявляемые при оценке толщины интимы—медии (ТИМ). Средние показатели липидного состава крови в группе пациентов, ранее не получавших статины, и у лиц с умеренным нарушением липидного обмена составляли: общий холестерин (ОХС) 5,98±1,2 ммоль/л; ХС ЛНП 3,82±0,98 ммоль/л. Терапия мертенилом 5 мг/сут в течение 8 нед привела к снижению уровня ХС ЛНП на 35% и ОХС на 27,4% (p<0,01 для обоих показателей). Авторы данной работы отмечают, что сопоставимые данные по эффективности и безопасности розувастатина в дозе 5 мг получены нашими зарубежными коллегами [22, 23]. Лечение больных в дозе 10 мг/сут привело к снижению уровня ХС ЛНП на 41,1%, ОХС на 30% и триглицеридов (ТГ) на 19,1% (p<0,01), повышению уровня ХС липопротеидов высокой плотности (ЛВП) на 6,3% (p<0,05). Показатели безопасности (аспартатаминотрансфераза — АсАТ, аланинаминотрансфераза — АлАТ, креатинкиназа — КК) для обеих групп достоверно не отличались от исходных значений.
Кроме того, представляет интерес работа по оценке эффективности мертенила у женщин (n=47, средний возраст 35±2,6 года) с эстрогендефицитом, дислипидемией и гипертонической болезнью (ГБ) в отсутствие клинических признаков атеросклероза коронарных артерий и периферических сосудов [24]. Пациентки были распределены в 2 группы: группа антигипертензивной терапии экватором и группа комбинированной терапии экватором и мертенилом 10 мг/сут. Первичными конечными точками являлись снижение уровня ХС ЛНП и улучшение параметров структурно-функционального состояния сосудистого русла через 6 мес терапии. По реультатам данного исследования в группе комбинированной терапии мертенилом 10 мг (розувастатин) и экватором (лизиноприл, амлодипин) по сравнению с терапией экватором статистически значимо выявлено улучшение структурно-функциональных показателей сосудистой стенки общей сонной артерии, функции эндотелия (р<0,05); зарегистрировано уменьшение ТИМ с 0,85±0,2 до 0,76±0,3; снижение уровня ХС ЛНП с 4,4±1,7 до 2,9±1,1 ммоль/л через 6 мес лечения (табл. 1). Нежелательных побочных эффектов выявлено не было.
Совершенно другую цель ставили перед собой исследователи, проводившие оценку влияния розувастатина на параметры суточного мониторирования электрокардиограммы у больных системной красной волчанкой (СКВ) с признаками субклинического атеросклероза в сравнении со здоровыми лицами (n=30) [25].
Больные СКВ с изменениями в липидограмме и/или изменением ТИМ (n=53) были рандомизированы в 2 группы, в одной из которых в дополнение к стандартной терапии основного заболевания был назначен мертенил в дозе 10 мг/сут. Исходно в группе больных СКВ отмечено статистически значимое увеличение частоты нарушений ритма сердца в виде наджелудочковых и желудочковых экстрасистол, в том числе высоких градаций по сравнению с группой здоровых лиц. Результаты исследования показали статистически значимое снижение частоты регистрации наджелудочковых экстрасистол, суточного количества наджелудочковых и желудочковых экстрасистол в группе гиполипидемической терапии. Авторы интерпретируют полученные данные как доказательство реализации плейотропных свойств розувастатина и отмечают, что результаты проведенной работы не противоречат результатам подобных исследований, но проведенных в популяциях больных ГБ, ишемической болезнью сердца (ИБС) [25—27].
Вторичная профилактика. Вторичная профилактика осуществляется у пациентов с уже имеющейся ИБС. Опыт зарубежных коллег и наш собственный нашел отражение в результатах опубликованных исследований.
Так, в ходе выполнения исследования SATURN (Study of Coronary Atheroma by Intravascular Ultrasound: Effect of Rosuvastatin versus Atorvastatin), включавшего больных со стабильным течением ИБС [28], проводилось сравнение эффективности двух статинов в максимально применяемой суточной дозе: розувастатина 40 мг и аторвастатина 80 мг в течение 2 лет. Результаты исследования демонстрировали частоту достижения целевых уровней ХС ЛНП менее 1,81 ммоль/л в группе розувастатина 40 мг и группе аторвастатина 80 мг — у 72,1 и 56,1% больных соответственно (p<0,001), но при меньшей частоте развития побочных эффектов в случае использования аторвастатина.
Кроме того, в этом исследовании с использованием внутрисосудистого ультразвукового исследования выявлен выраженный регресс процентного объема атеросклеротической бляшки (p=0,17) в группе применения розувастатина.
В исследовании TIGER были обследованы 2564 пациентов с дислипидемией (ОХС более 5 ммоль/л, ХС ЛНП более 3 ммоль/л, ТГ более 1,7 ммоль/л), причем пациенты представляли собой разнородную группу (без ГБ, с ГБ, сахарный диабет 2-го типа, метаболический синдром) [29]. Все участники исследования были разделены на 2 группы: с нормальным уровнем вч-СРБ и с вч-СРБ > 3мг/л. Была продемонстрирована тесная корреляция между уровнем вч-СРБ и ХС ЛНП (коэффициент корреляции — 0,61; t = 17,2). В исследовании TIGER терапия розувастатином (Xeter — торговое название препарата мертенил в Венгрии, «Гедеон Рихтер») в дозе 10—40 мг проводилась всем пациентам по показаниям с целью достижения целевых уровней (ОХС менее 4,5 ммоль/л, ХС ЛНП менее 2,5 ммоль/л, ТГ менее 1,7 ммоль/л). Спустя 6 мес терапии у 52,2% пациентов был достигнут целевой уровень ОХС; у 54,3% — целевой уровень ХС ЛНП и у 53,3% — целевой уровень ТГ. К концу 6-го месяца наблюдения средний уровень вч-СРБ снизился с 3,76±1,95 до 2,2±1,09 мг/л (p<0,001). Снижение уровня вч-СРБ сопровождалось более активным снижением концентрации ОХС, ХС ЛНП (рис. 3).

Возвращаясь к ранее упомянутому исследованию «От 5 до 40», рассмотрим другой аспект этой работы, а именно эффективность применения мертенила в течение 8 нед в группе высокого и очень высокого риска. Напомним, что результаты оценивались в 2 подгруппах: пациенты, ранее принимавшие терапию статинами и не достигнувшие целевых уровней ХС ЛНП (n=785), и пациенты, никогда не получавшие статины (n=2806) [22]. В 1-й подгруппе на фоне терапии розувастатином в дозе 10—20 мг/сут наблюдалось дополнительное снижение уровня ХС ЛНП на 29,8%, уровня ОХС на 19%. Исходно средний уровень ХС ЛНП составлял 3,42±0,8 ммоль/л. Примечательно, что во 2-й подгруппе на фоне терапии розувастатином 20 мг/сут добились снижения уровня ХС ЛНП на 50,9%; при приеме розувастатина в максимальной дозе 40 мг добились снижения уровня ХС ЛНП на 53,3%.
В целом достижение целевого уровня ХС ЛНП в группе очень высокого риска (ниже 1,8 ммоль/л) за короткий срок (8 нед) отмечено у 28% пациентов, принимавших 20 мг/сут розувастатина. На фоне применения мертенила 40 мг/сут этих значений достиг каждый третий больной (31%) (рис. 4). Целевого уровня ХС ЛНП в группе высокого риска (<2,5 ммоль/л) смогли достичь 70 и 72% больных, принимавших мертенил в дозе 20 и 40 мг/сут соответственно.
Переносимость и безопасность препарата были удовлетворительными. Даже при применении высоких доз мертенила побочные эффекты в виде повышения уровней АлАТ и АсАТ менее чем в 3 раза выше верхней границы нормы отмечены всего у 11 (1,4%) из 782 пациентов, принимавших мертенил в суточной дозе 20 мг, и 1 (1,9%) пациента из 52, получавших мертенил в дозе 40 мг/сут, что не потребовало отмены препарата.
Представляет большой практический интерес исследование «40×40» [30]. В названии исследования заложена основная цель авторов: оценить гиполипидемическую эффективность, безопасность и переносимость препарата мертенил (розувастатин, «Гедеон Рихтер») в максимальной дозе 40 мг/сут у 40 больных группы очень высокого риска развития ССЗ («40×40») в течение 24 нед терапии. Причем в исследование включались именно те пациенты, которые не достигали целевого уровня ХС ЛНП на фоне текущей терапии статинами в повседневной клинической практике.

Исходный уровень ХС ЛНП составил 3,6±1,1 ммоль/л, что в 2 раза превышало рекомендованный целевой уровень для пациентов данной группы риска (менее 1,8 ммоль/л). Средняя суточная доза статинов для больных, включенных в исследование, эквивалентная дозе розувастатина, составила 11,9 мг. Результаты проведенного исследования показали дополнительное снижение уровня ХС ЛНП через 6 мес терапии розувастатином 40 мг на 34,7%, снижение уровня ОХС на 23,1% (рис. 5). Целевых значений достигли 27% пациентов (10 из 37). Показатели активности АсАТ, АлАТ при монотерапии розувастатином в дозе 40 мг/сут через 24 нед терапии статистически значимо не отличались от исходных.
Другой важный блок исследований посвящен изучению влияния мертенила не только на липидный состав крови, но и на маркеры системного воспаления. Так, в одной из работ, выполненных в 2013 г., изучалась динамика маркеров системного воспаления у больных с хронической сердечной недостаточностью (ХСН) ишемической природы (n=96) [31]. У всех пациентов в анамнезе имелся ИМ разного срока давности. На фоне приема мертенила в суточной дозе 20 мг в течение 12 нед выявлены снижение уровней провоспалительных цитокинов (α-фактор некроза опухоли, интерлейкин-6), С-реактивный белок сыворотки крови (определяемого классическим методом) и положительная динамика показателей ремоделирования сердца по данным эхокардиографии.
 Важной вехой в изучении плейотропных влияний статинов стало внедрение в клиническую практику методов инструментального выявления дисфункции эндотелия. Так, в сравнительном рандомизированном исследовании СТРЕЛА [9, 14—16] изучались эффекты терапии статинами на показатели микроциркуляции и скорости пульсовой волны у пациентов с ГБ высокого риска (SCORE ≥5%). В исследование были включены 82 пациента, которые были распределены в 2 группы: группа приема мертенила 5—10 мг/сут и группа приема аторвастатина 10—20 мг/сут. Результаты исследования свидетельствуют о статистически значимом более выраженном снижении показателей индексов жесткости, аугментации (по данным ангиоскана), приросте амплитуды пульсовой волны в группе приема мертенила 5—10 мг/сут [16].
Важной вехой в изучении плейотропных влияний статинов стало внедрение в клиническую практику методов инструментального выявления дисфункции эндотелия. Так, в сравнительном рандомизированном исследовании СТРЕЛА [9, 14—16] изучались эффекты терапии статинами на показатели микроциркуляции и скорости пульсовой волны у пациентов с ГБ высокого риска (SCORE ≥5%). В исследование были включены 82 пациента, которые были распределены в 2 группы: группа приема мертенила 5—10 мг/сут и группа приема аторвастатина 10—20 мг/сут. Результаты исследования свидетельствуют о статистически значимом более выраженном снижении показателей индексов жесткости, аугментации (по данным ангиоскана), приросте амплитуды пульсовой волны в группе приема мертенила 5—10 мг/сут [16].
Неожиданные данные получены при изучении эффектов статинов в когорте больных хронической обструктивной болезнью легких (ХОБЛ) [32]. Как известно, используемая в настоящее время терапия ХОБЛ практически не влияет на прогноз заболевания. Имеющееся системное воспаление, хроническая гипоксемия, наличие других классических факторов риска развития ССЗ приводят к тому, что основной причиной смерти пациентов с ХОБЛ являются ССО (ИМ, инсульт).
Такая высокая степень коморбидности у пациентов с ХОБЛ послужила предпосылкой к исследованию дисфункции эндотелия (по данным уровня вч-СРБ и др.), клинического течения ХОБЛ II—IV стадии у 40 пациентов на фоне терапии мертенилом в суточной дозе 5—10 мг в течение 6 мес [32]. Все участники были распределены в 2 группы: группа терапии (n=21) и контрольная группа.
Все пациенты по результатам анализа липидного состава крови в группе терапии достигли целевых уровней ХС ЛНП. На фоне приема мертенила уровень вч-СРБ уменьшился с 8,5 (3,8;11,8) до 3,9 (2,27; 6,2) мг/л (p<0,001). Через 6 мес лечения пациенты из группы приема статина отметили уменьшение выраженности симптомов ХОБЛ (Δ= –20%) и ограничения физической активности (Δ= –25,4%; p<0,05). В контрольной группе подобных изменений не обнаружено.
Авторы исследования делают вывод о возможности коррекции системного воспаления у больных ХОБЛ благодаря плейотропным эффектам розувастатина.
Во всех описанных работах изучалась эффективность терапии розувастатином у лиц с первичной гиперхолестеринемией. В то же время распространенность семейной гиперхолестеринемии (СГХС) — наследуемого по аутосомно-доминантному типу заболевания, обычно вызываемого мутацией гена рецептора ЛНП — также очень высока [1, 33], что вызывает большие трудности в лечении больных данной категории. При наличии гетерозиготной формы СГХС манифестация ИБС наблюдается в период 30—40 лет, при гомозиготной форме СГХС — первый ИМ, инсульт диагностируют в подростковом возрасте и на втором десятилетии жизни (рис. 6).
Недавно проведенное проспективное открытое исследование, в котором изучались эффективность и безопасность терапии мертенилом в суточной дозе 40 мг в течение 16 нед у пациентов с СХГС (n=40) показало, что монотерапия розувастатином 40 мг/сут способствовала снижению уровня ХС ЛНП на 55,1% (р<0,001) и уровня АpоВ-100 на 45,1% (р<0,001), снижение уровня ТГ составило 20,1% (р<0,01) [34]. Показатели активности АлАТ, АсАТ и КК через 16 нед терапии статистически значимо не отличались от исходных и не превышали в 1,5 раза верхнюю границу нормы.
Кроме того, через 16 нед терапии было выявлено снижение уровня вч-СРБ с 0,34 (0,03; 0,62) до 0,13 (0,05; 0,19) (р=0,029). Авторы отмечают, что уровень снижения вч-СРБ при терапии мертенилом был подобен таковому при терапии оригинальным розувастатином (результаты исследований JUPITER и ANDROMEDA) [21, 35].
Таким образом, во многих исследованиях получены сходные показатели, свидетельствующие о высокой гиполипидемической эффективности, противовоспалительной активности, переносимости и безопасности розувастатина (мертенила) у больных разных групп риска развития ССЗ.
ОКС. История изучения эффективности и безопасности применения статинов при ОКС началась с момента получения результатов исследования MIRACL (Myocardial Ischemia Reduction with Aggressive Cholesterol Lowering), согласно которым применение высокой дозы аторвастатина у больных с ОКС имело ряд преимуществ [36].
Позже с целью сравнительной характеристики применения различных статинов у больных с ОКС (n=754) было предпринято исследование LUNAR с тремя параллельными группами (1:1:1): розувастатин 20 мг, розувастатин 40 мг и аторвастатин 80 мг [37]. Длительность терапии составила 12 нед. За основной показатель эффективности лечения принималось снижение уровня ХС ЛНП, измеренного прямым путем. Изначально средние концентрации ХС ЛНП были сходными во всех 3 группах и находились в диапазоне от 3,44 до 3,59 ммоль/л. Среднее изменение концентрации ХС ЛНП в целом в течение 6 и 12 нед терапии при использовании розувастатина 40 мг было статистически значимо более выраженным, чем в случае применения аторвастатина 80 мг (p=0,02). Кроме того, было отмечено повышение уровня ХС ЛВП на 8,1% в группе терапии розувастатином 40 мг. Однако частота стойкого прекращения приема препарата в связи с развившимися признаками миопатии составила 3,7% в группе приема розувастатина 20 мг, 6,1% — в группе розувастатина 40 мг и 9,1% — в группе аторвастатина 80 мг.

В России проведено 2 исследования по применению мертенила у больных ОКС [38, 39].
Так, авторы первого исследования изучали динамику концентрации ХС ЛНП у мужчин (n=21; средний возраст 50,9±11,3 года), которые госпитализировались в палату интенсивной терапии отделения неотложной кардиологии НИИ скорой помощи им. Н.В. Склифосовского с предположительным диагнозом ОКС [38]. До госпитализации пациенты не принимали статины. Анализ липидограммы оценивали при поступлении и через 2 нед приема мертенила 20 мг/сут.
По результатам данной работы на фоне приема статина уровень ХС ЛНП снизился на 46,3% (в среднем с 3,79±1,01 до 1,95±0,73 ммоль/л). В ходе наблюдения за больными ни в одном из случаев не было отмечено увеличения активности печеночных трансаминаз в 3 раза выше верхней границы нормы, а также случаев развития миопатии.
В другом исследовании авторы изучали влияние терапии розувастатином в суточной дозе 40 мг на липидный обмен и микроциркуляцию у больных с ОКС (n=78) [39]. До госпитализации пациенты не принимали статины. Все пациенты были распределены на 2 сравнимые группы методом случайной выборки. В основную группу вошел 31 пациент (средний возраст 63,2±7,3 года), во вторую — 47 пациентов (средний возраст 60,9±8,2 года). Обе группы получали стандартную базисную терапию. Пациенты основной группы получали дополнительно мертенил в дозе 40 мг 1 раз в сутки, который назначали в 1—2-е сутки ОКС.
Через 30 дней терапии статином все пациенты в основной группе достигли целевых уровней ОХС, ХС ЛНП. Обнаружено статистически значимое снижение уровня ОХС на 43,5%, ХС ЛНП — на 59,1%, ТГ — на 32,5%. Общая частота развития ишемических осложнений в группе розувастатина уменьшилась на 83,8% (р<0,05), средняя продолжительность приступа ишемии сократилась на 59,4% (р<0,05), что значительно превышало динамику этих показателей в контрольной группе (табл. 2).
Резюмируя, можно констатировать, что полученные данные в целом коррелируют с результатами исследования LUNAR. Применение генерика розувастатина может быть приемлемой альтернативой использованию оригинального препарата. Однако необходимость в проведении крупных многоцентровых исследований по прямому сравнению оригинального препарата и генериков остается актуальной в современной кардиологии.
Оригинал и генерик: прямое сравнение. Как говорится в русской пословице: «Лакомый кусок напоследок оставляют», так и мы отложили в завершение обзора эффектное сравнительное рандомизированное одноцентровое в параллельных группах исследование мертенила («Гедеон Рихтер») и крестора («ASTRAZENECA UK Ltd.») у пациентов с первичной гиперлипидемией (n=28) [40].
Согласно критериям включения в исследовании приняли участие пациенты в возрасте от 18 до 70 лет с уровнем ХС ЛНП натощак ≥3,0 ммоль/л, но <6,5 ммоль/л, уровнем ТГ <4,5 ммоль/л. Все пациенты были рандомизированы в 2 группы: группа терапии оригинальным препаратом розувастатина 10 мг/сут и группа терапии мертенилом 10 мг/сут. Результаты работы показали сходную степень снижения уровня ХС ЛНП и частоту достижения целевого уровня ХС ЛНП в группе мертенила и в группе крестора. Применение обоих препаратов характеризовалось хорошей переносимостью и высокой безопасностью (табл. 3).
Заключение
Как известно, частота развития осложнений сердечно-сосудистых заболеваний в странах с низким или средним доходом населения намного превышает соответствующий уровень в экономически развитых странах. Одной из причин этого являются экономические трудности «претворения в жизнь» клинических рекомендаций. Так, по данным крупного обсервационного исследования, в странах с низким уровнем дохода на душу населения частота приема препаратов, относящихся к антиагрегантам, β-адреноблокаторам, ингибиторам ангиотензинпревращающего фермента (или блокаторам рецепторов ангиотензина II) и статинам, составляет 8,8, 9,7, 5,2 и 3,3% соответственно (p<0,0001 для каждого класса препаратов) [41]. В связи с этим встает вопрос о более широком использовании эффективных биоэквивалентных препаратов, в том числе из группы статинов, для преодоления разрыва между сводами правил рекомендаций и клинической практикой. В этом отношении, опираясь на данные медицины, основанной на доказательствах, применение мертенила следует признать правильным решением проблемы улучшения качества лечения больных с сердечно-сосудистыми заболеваниями.



