Ввиду высокой стоимости койко-дня, а также предупреждения развития внутрибольничной инфекции одним из актуальных в современном здравоохранении является вопрос сокращения длительности пребывания пациентов в стационаре, в том числе в отделениях реанимации и интенсивной терапии (ОРИТ) с сохранением качества оказываемой медицинской помощи. В связи с этим актуальным является поиск факторов, оказывающих влияние на длительность лечения. Выявление подобных факторов позволило бы оптимизировать подходы к терапии, обеспечивающие достижение более высоких клинических результатов в кратчайшие сроки и, как следствие, обеспечило бы более высокую клинико-экономическую эффективность применяемых при ведении пациентов медицинских технологий.
Порядок выделения групп пациентов при выборе тактики лечения должен основываться на анализе как клинической, так и экономической эффективности применяемых медицинских технологий с целью достижения оптимального соотношения качества проводимого лечения и затрат на ведение пациента.
Отсутствие инструментов, позволяющих прогнозировать длительность пребывания пациента в стационаре, в отдельных случаях затрудняет выбор тактики лечения пациента. Количественное выражение качественных показателей позволяет облегчить и объективизировать процесс принятия решений, а также оптимизировать процесс оказания медицинской помощи с целью получения наилучших результатов.
Цель исследования: разработка шкалы оценки риска увеличения длительности пребывания пациента в ОРИТ после перенесенного коронарного шунтирования (КШ) на основании факторов, влияющих на длительность такого пребывания.
Материал и методы
В исследование были включены 69 пациентов ГБУЗ МО МОНИКИ им. М.Ф. Владимирского, которым проводилось КШ без использования аппарата искусственного кровообращения в 2014 г.
Для оценки практики ведения пациентов со стабильным течением ишемической болезни сердца в условиях стационара была разработана карта регистрации пациента. Карта включала четыре информационных блока по следующим разделам: 1) паспортная часть; 2) проведенное вмешательство; 3) информация о длительности пребывания в ОРИТ; 4) данные о количестве лабораторных и инструментальных исследований, а также величины показателей, полученных при исследованиях.
Средняя длительность пребывания больных в стационаре составила 26,03 дня при 95% доверительном интервале (ДИ) от 28,06 до 23,99 (р=0,05), средняя длительность пребывания в ОРИТ — 1,54 дня (при 95% ДИ от 1,55 до 1,52; р=0,05). Минимальная продолжительность пребывания составила 1 сут (62% пациентов), максимальная — 7 дней (1,4% пациентов).
Средний возраст пациентов в данной группе составил 62,58 года, средний возраст мужчин 62,87 года, женщин 61,17 года, доля пенсионеров 30%.
Распределение хирургических вмешательств: аортокоронарное шунтирование (АКШ) проведено в 20% случаев, АКШ+маммарокоронарное шунтирование (МКШ) — в 24%, бимаммарокоронарное шунтирование (БМКШ) и МКШ в 23 и 24% случаев соответственно. В 59% случаев при проведении вмешательств были использованы только артериальные шунты, в 4% случаев – исключительно венозные шунты, в 37% — их комбинация. Среднее число артериальных шунтов на пациента составило 2,45, венозных — 0,58. Доля пациентов с сахарным диабетом – 0,2.
Поиск факторов, влияющих на сроки пребывания пациента в ОРИТ, включал анализ основных клинических, лабораторных и инструментальных показателей. В качестве возможных предикторов увеличения длительности пребывания в ОРИТ рассмотрены интраоперационная кровопотеря, данные анализов крови, возраст пациентов, тип операции и вид шунта.
Для количественной оценки во избежание затруднений в интерпретации использованы 5-балльные шкалы. Степени влияния каждого из факторов на длительность пребывания пациента в ОРИТ, а также сила влияния каждого из факторов определены на основании опроса экспертов.
На основании данных из историй болезни пациентов, перенесших КШ, произведен анализ уровней глюкозы и лактата у пациентов, находящихся в ОРИТ в послеоперационном периоде. Анализ лабораторных показателей выполнялся с помощью диагностического оборудования Radiometer ABL800 Flex.
Всего произведено 361 измерение глюкозы и 356 измерений лактата в венозной крови, т.е. по 5,2 измерения каждого показателя на пациента.
Аналогичным образом проведен анализ связи между типом шунта, возрастом, объемом интраоперационной кровопотери и длительностью пребывания в стационаре в целом и в ОРИТ.
Результаты
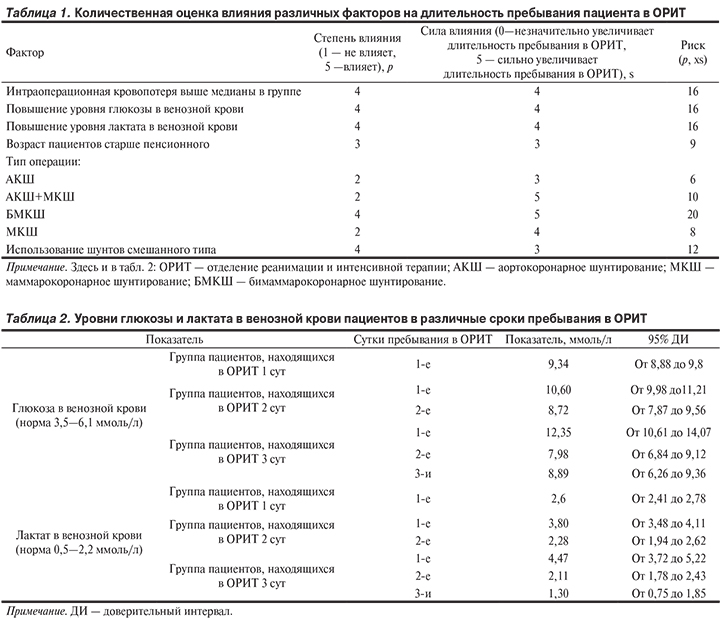
Всего опрошены 6 экспертов. Результаты оценки степени и силы влияния каждого из рассматриваемых факторов на длительность пребывания пациентов в ОРИТ представлены в табл. 1. Согласно представленным в ней данным, предикторами увеличения длительности пребывания в ОРИТ являются проведение БМКШ, высокая кровопотеря, а также повышение уровней глюкозы и лактата в венозной крови.
На основании анализа данных историй болезни уровни глюкозы и лактата в венозной крови достоверно различаются в зависимости от длительности пребывания пациентов в ОРИТ (табл. 2).
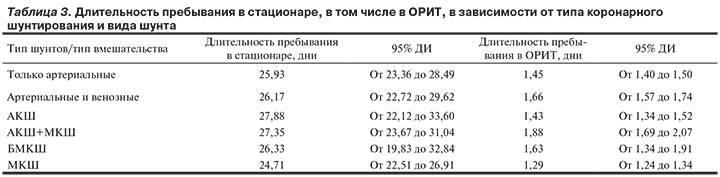
Выявлены различия по уровню глюкозы в течение 1-х суток пребывания пациентов в ОРИТ из групп пациентов, находящихся в ОРИТ на протяжении 1-х и 2-х суток и 1-х и 3-х суток.
Настоящее различие уровней глюкозы можно считать достоверным, в то время как различия уровня глюкозы в течение 2 суток пребывания в группах не являются достоверными.
 Уровень лактата в венозной крови также различается в указанных группах пациентов, при этом достоверные различия выявлены в группах пациентов, находившихся в ОРИТ на протяжении 1-х и 2-х суток и 1-х и 3-х суток (рис. 2).
Уровень лактата в венозной крови также различается в указанных группах пациентов, при этом достоверные различия выявлены в группах пациентов, находившихся в ОРИТ на протяжении 1-х и 2-х суток и 1-х и 3-х суток (рис. 2).
Таким образом, повышение уровней глюкозы и лактата более 10,6 и 3,8 ммоль/л соответственно является предиктором увеличения длительности пребывания пациента в ОРИТ.
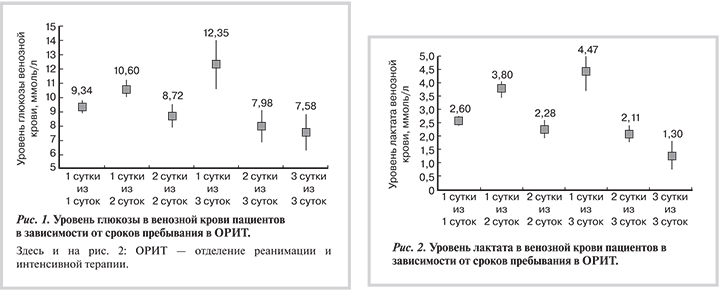
Аналогичным образом проведен анализ связи между типом шунта и длительностью пребывания в стационаре и в ОРИТ, результаты представлены в табл. 3
Согласно приведенным данным, сочетанное использование артериальных и венозных шунтов соответствует более длительному пребыванию пациентов в ОРИТ, в то время как длительность пребывания в стационаре достоверно не изменяется. Однако полученные данные имеют низкий уровень доказательности.
Наименьшая длительность пребывания в ОРИТ отмечается в группе МКШ, наибольшая — в группе АКШ+МКШ.
Средняя продолжительность пребывания пациентов непенсионного возраста в стационаре составила 25 дней (при 95% ДИ от 27,6 до 22,4 дня; р=0,05), пациентов пенсионного возраста — 28,69 дня (при 95% ДИ от 29,9 до 24,4; р=0,05), длительность пребывания в ОРИТ для тех же групп составила 1,64 дня (при 95% ДИ от 2,11 до 1,69 дня; р=0,05) и 1,44 дня (95% ДИ от 1,61 до 1,26 дня; р=0,05).
Средний объем интраоперационной кровопотери пациентов составил 427±134 мл. Объем кровопотери превысил указанный показатель у 13% пациентов и составил в среднем 472 мл, длительность пребывания в стационаре в указанной группе составила 27,3 дня (при 95% ДИ от 31,85 до 22,75 дня; р=0,05), в ОРИТ — 1,54 дня (при 95% ДИ от 1,28 до 1,79 дня; р=0,05). У 87% пациентов объем кровопотери не превышал 427 мл и составил в среднем 377 мл. Длительность пребывания в стационаре в этом случае составила 25,1 дня (при 95% ДИ от 37,8 до 22,32 дня; р=0,05), в ОРИТ — 1,4 дня (при 95% ДИ 1,12 до 1,68 дня; р=0,05).
Таким образом, не выявлено корреляции между интраоперационной кровопотерей и длительностью пребывания пациентов в стационаре и ОРИТ, а также возрастом и длительностью пребывания пациентов в стационаре и ОРИТ.
Обсуждение
Качественная оценка риска, не привязанная к количественной шкале, может быть использована для расстановки приоритетов, в то время как неясным остается вопрос реального увеличения длительности пребывания пациента в ОРИТ.
Для прогнозирования ситуации целесообразно определение количественных диапазонов, т.е. присвоение числовых значений каждому из параметров, исходя из влияния на длительность пребывания пациента в ОРИТ, а также силы этого влияния. Выбор пороговых значений критичности риска является крайне важным. Очевидно, что тяжесть последствий в медицинских организациях зачастую является более значимым фактором риска, чем его вероятность, например развитие осложнений, несовместимых с жизнью, после процедуры должно явиться триггером к разработке подходов, позволяющих избежать данного вмешательства либо модифицировать его с целью снижения риска. В целом алгоритм принятия решений должен быть основан на дезагрегированной оценке как частоты развития рисков, так и на их тяжести (рис. 3).
В настоящее время отсутствуют данные, обладающие высоким уровнем доказательности и убедительности доказательств касательно повышения риска развития осложнений в раннем послеоперационном периоде в случае использования венозных шунтов при проведении КШ. При этом, начиная с 1986 г., исследователи отмечают различия в выживаемости в группах пациентов, у которых были использованы венозные и артериальные шунты — во втором случае смерть наступает в более поздние сроки [1].
В то же время немногочисленны исследования, в которых произведена сравнительная оценка результатов после КШ с использованием артериальных шунтов по сравнению с КШ шунтами смешанного типа. Наиболее достоверным и близким по дизайну к реальной практике ведения пациентов в МОНИКИ явилось исследование T.A. Schwann и соавт. [2], включившее 6384 пациента, которые перенесли КШ с формированием не менее 2 шунтов. Осуществлялось сравнение между КШ с использованием артериальных шунтов и КШ с использованием шунтов смешанного типа. Критериями исключения являлись проведение только МКШ или БМКШ, а также необходимость коррекции заболеваний клапанного аппарата сердца. Средний возраст мужчин и женщин в исследовании составил 62 и 66 лет соответственно. Различий по смертности на протяжении 30 дней после хирургического вмешательства в группах артериального и смешанного шунтирования обнаружено не было: смертность в группе артериального шунтирования среди мужчин и женщин составила 1,3 и 1,2% соответственно (р=1,0), в группе применения шунтов смешанного типа — 1,4 и 1,9% (р=0,664), в то время как риск смерти в отдаленном периоде (со 2-го по 144-й месяц) в группе артериального шунтирования был существенно ниже — отношение шансов (ОШ) 0,65 при 95% ДИ от 0,54 до 0,79 для мужчин и 0,75 при 95% ДИ от 0,57 до 0,99 для женщин. Смертность за указанный период среди мужчин в группе артериального и смешанного шунтирования составила 10,4 и 28,3% соответственно, среди женщин — 13,6 и 28,5%. Таким образом, использование артериальных шунтов имеет преимущества с позиции увеличения продолжительности жизни по сравнению с использованием сочетания артериальных и смешанных шунтов. Однако информации о длительности пребывания пациентов в отделении интенсивной терапии и/или длительности инотропной поддержки представлено не было.
Основным нейромедиатором стресса является кортикотропин-рилизинг-фактор, способствующий активации адренокортикотропного гормона в аденогипофизе и глюкокортикоидов в корковом веществе надпочечников. За счет стимуляции гликогенолиза в печени и глюконеогенеза происходит мобилизация глюкозы, проявляющаяся в виде гипергликемии [3]. Кроме того, повышение уровня глюкозы может быть одним из проявлений синдрома гиперметаболизма, сопровождающего критические состояния различной этиологии и проявляющегося повышением уровней контринсулярных гормонов, активацией липолиза и протеолиза [4, 5]. Факторами, способствующими усилению и поддержанию гипергликемии при хирургических вмешательствах, являются также применение симпатомиметиков, стимулирующих β-адренорецепторы, таких как адреналин, и препаратов группы глюкокортикостероидов [6].
По данным ряда авторов [7, 8], причиной гипергликемии в первые 24 ч после хирургического вмешательства является снижение скорости метаболизма, сопровождающейся замедлением окисления глюкозы и пирувата, а также уменьшением потребности тканей в кислороде. Результаты исследований G.E. Umpierrez и соавт. [9] и J.C. Preiser и соавт. [10] свидетельствуют о наличии достоверной связи между повышением уровня глюкозы в крови и ухудшением клинических результатов лечения, повышением летальности, увеличением длительности пребывания пациентов в ОРИТ. По данным В.П. Шано [11], коррекция гипергликемии в послеоперационном периоде позволяет улучшить клинические результаты: применение инсулинотерапии позволяет снизить количество гнойно-септических осложнений на 15,9%, а также сократить длительность пребывания в ОРИТ в 1,25 раза.
Выводы
Факторами, достоверно влияющими на длительность пребывания в отделении реанимации и интенсивной терапии пациентов, которые перенесли коронарное шунтирование, являются повышение уровней глюкозы и лактата в венозной крови, тип применяемых шунтов, а также вид шунтирования.
Повышение уровня лактата в венозной крови более 3,8 ммоль/л в 1-е сутки пребывания в отделении реанимации и интенсивной терапии является предиктором длительного пребывания (более 1,5 сут) в отделении реанимации и интенсивной терапии.
Повышение уровня глюкозы в венозной крови более 10,6 ммоль/л в 1-е сутки пребывания в отделении реанимации и интенсивной терапии является предиктором длительного пребывания (более 1,5 сут) в отделении реанимации и интенсивной терапии.
Единовременное использование артериальных и венозных шунтов приводит к увеличению длительности пребывания пациентов в отделении реанимации и интенсивной терапии.
Длительность пребывания в отделении реанимации и интенсивной терапии в случае проведения маммарно-коронарного шунтирования достоверно меньше, чем в случае проведения других видов шунтирования.
Объем кровопотери и возраст пациентов не влияют на длительность пребывания их в отделении реанимации и интенсивной терапии.



