Фибрилляция предсердий (ФП) является фактором риска (ФР) развития ряда сердечно-сосудистых осложнений (ССО), наиболее тяжелое из которых — кардиоэмболический инсульт. Примерно каждый 5-й ишемический инсульт (ИИ) является следствием ФП [1, 2]. В составе комплексной профилактики инсультов пациентам с ФП, относящимся к группам высокого и умеренного риска, назначается терапия антагонистами витамина К (варфарин) или новыми пероральными антикоагулянтами [3—6].
Одно из главных отличий новых пероральных антикоагулянтов от варфарина заключается в устойчивой фармакокинетике, что позволяет принимать препараты в фиксированной дозе без необходимости индивидуального подбора дозы и регулярного мониторинга антикоагулянтной активности по международному нормализованному отношению (МНО). Этот аспект особенно важен в условиях российской клинической практики, когда, согласно оценочным данным, около 25% пациентов с ФП не имеют возможности получать надлежащий контроль МНО [7]. При этом даже в условиях поликлиники в Москве в соответствии с анализом медицинской документации адекватный контроль МНО проводился лишь в 8% случаев назначения варфарина пациентам с ФП [8].
В настоящее время в Российской Федерации доступны 3 препарата из класса новых пероральных антикоагулянтов: апиксабан, дабигатрана этексилат и ривароксабан. Из них дабигатран является прямым ингибитором тромбина, а ривароксабан и апиксабан — прямыми ингибиторами Xa фактора. Клиническая эффективность и безопасность апиксабана, дабигатрана и ривароксабана изучена в рандомизированных клинических исследованиях, в которых они сравнивались с варфарином, — ARISTOTLE [9], RE-LY [10], ROCKET-AF [11] (табл. 1). Кроме того, эффективность и безопасность апиксабана подтверждена и по отношению к монотерапии ацетилсалициловой кислотой (АСК) в отдельном рандомизированном исследовании AVERROES [12]. Прямых сравнительных исследований между новыми пероральными антикоагулянтами не проведено.
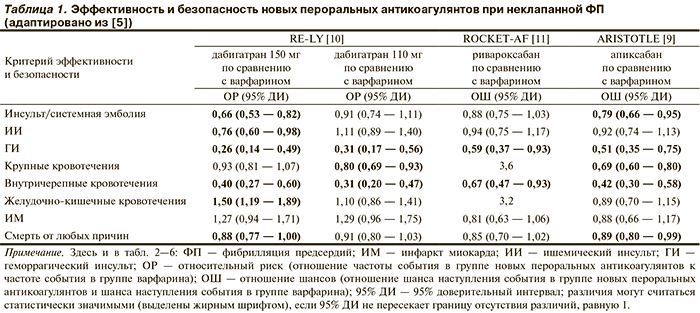
Рандомизированные клинические исследования показали, что применение апиксабана и дабигатрана в дозе 150 мг по сравнению с варфарином приводит к статистически значимому снижению риска развития тромбоэмболических осложнений (инсультов или системной тромбоэмболии) на 21% (р=0,01) и 35% (р<0,001) соответственно. Для ривароксабана и дабигатрана в дозе 110 мг продемонстрирована неменьшая эффективность по сравнению с варфарином в отношении риска развития тромбоэмболических осложнений (р<0,001). Для всех препаратов найдено статистически значимое снижение риска развития геморрагического инсульта (ГИ) и других внутричерепных кровотечений. Кроме того, апиксабан и дабигатран в дозе 110 мг по сравнению с варфарином статистически значимо снижали частоту крупных внечерепных кровотечений (на 31 и 20% соответственно). Следует отметить, что у пациентов, получавших дабигатран в дозе 150 мг, зафиксировано статистически значимое увеличение частоты желудочно-кишечных кровотечений и в 2 раза повышалась вероятность диспепсии.
Таким образом, по результатам клинических исследований, все 3 новых пероральных антикоагулянта не уступают в эффективности профилактики тромбоэмболических осложнений варфарину — сложившемуся стандарту лечения пациентов с неклапанной ФП, но в целом превосходят его по критериям безопасности. При этом апиксабан является единственным препаратом из этой группы, который продемонстрировал преимущество по сравнению с варфарином одновременно в отношении риска развития инсульта/системной эмболии, крупных кровотечений, внутричерепных кровотечений и смерти от любых причин.
Соответственно, перед клиническими специалистами стоит вопрос, какой из 3 доступных новых пероральных антикоагулянтов выбрать. Однозначного ответа на него в настоящее время не существует. При выборе препарата рекомендуется учитывать ряд факторов, таких как характеристики пациентов, переносимость препарата и стоимость лечения [6].
Целью данного исследования была оценка эффективности затрат на профилактику тромбоэмболических осложнений у пациентов с неклапанной ФП апиксабаном по сравнению с дабигатраном и ривароксабаном с точки зрения российского бюджетного здравоохранения.
Материал и методы
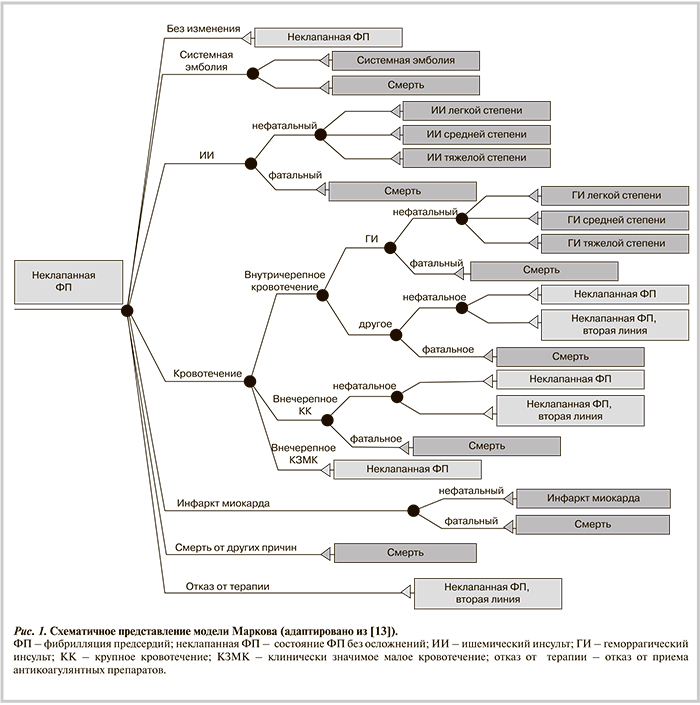
Модель. Для проведения клинико-экономического анализа использована модель Маркова, позволяющая прогнозировать течение заболевания у пациентов с неклапанной ФП и учесть затраты на лечение [13, 14]. Упрощенная схема использованной модели представлена на рис. 1. В связи с тем что подробное описание принципов и параметров моделирования было опубликовано ранее [13, 14], в данной статье приведена краткая характеристика данной модели.
Течение заболевания представлено в модели в виде перехода пациентов между марковскими состояниями, которые отражают развитие основных ССО, наблюдающихся в реальной клинической практике у пациентов с ФП: системная эмболия; ИИ (легкий, средней тяжести и тяжелый); ГИ (легкий, средней тяжести и тяжелый); другое внутричерепное кровотечение; крупное внечерепное кровотечение (как желудочно-кишечное, так и иное); клинически значимое малое кровотечение; инфаркт миокарда (ИМ); госпитализация по поводу иных ССО (включая транзиторную ишемическую атаку, тромбоз глубоких вен, сердечную недостаточность, загрудинные боли неясной этиологии и др.); смерть.
Степень тяжести функционального состояния больного после инсульта оценивалась по модифицированной шкале Рэнкина (mRS): инсульт легкой степени (mRS 0—2), инсульт средней тяжести (mRS 3—4), тяжелый инсульт (mRS 5) и инсульт с летальным исходом (mRS 6). Распределение пациентов по степени тяжести инсульта соответствовало данным российской клинической практики*. При первичном ИИ доля пациентов с mRS 0—2 при выписке была принята равной 51%, с mRS 3—4 — 19%, с mRS 5 — 1%, с летальным исходом — 29%. При повторном ИИ доля пациентов с mRS 0—2 при выписке была принята равной 39%, с mRS 3—4 — 28%, с mRS 5—0%, с летальным исходом — 33%. При первичном ГИ доля пациентов с mRS 0—2 при выписке была принята равной 17,5%, с mRS 3—4 — 17,5%, с mRS 5—0%, с летальным исходом — 65%. Для повторного ГИ было сделано допущение, что распределение по степени тяжести больных соответствовало таковому для первичного ГИ.
 В базовом варианте анализ осуществляли на период дожития пациентов. Продолжительность марковского цикла, во время которого могло развиться одно из взаимоисключающих клинических событий, составляла 6 нед. Модель предполагала переход с новых пероральных антикоагулянтов на АСК в качестве терапии второй линии как при развитии кровотечений (внутричерепных и крупных внечерепных), так и в связи с отказом от антикоагулянтной терапии по другим причинам. После перехода на АСК у пациентов могли развиваться те же осложнения, что и при терапии новыми пероральными антикоагулянтами.
В базовом варианте анализ осуществляли на период дожития пациентов. Продолжительность марковского цикла, во время которого могло развиться одно из взаимоисключающих клинических событий, составляла 6 нед. Модель предполагала переход с новых пероральных антикоагулянтов на АСК в качестве терапии второй линии как при развитии кровотечений (внутричерепных и крупных внечерепных), так и в связи с отказом от антикоагулянтной терапии по другим причинам. После перехода на АСК у пациентов могли развиваться те же осложнения, что и при терапии новыми пероральными антикоагулянтами.
Предполагали, что после ИИ и системной эмболии все пациенты продолжали прием антикоагулянтов; после ГИ и ИМ пациенты полностью прекращали прием антикоагулянтов; после внутричерепных кровотечений 44% пациентов временно прекращали прием антикоагулянтов на период 6 нед, а 56% пациентов переходили на АСК; после желудочно-кишечных и других больших кровотечений 75% пациентов продолжали прием антикоагулянтов, а 25% переходили на АСК [13]. Пациенты, принимавшие АСК в качестве терапии второй линии, после ИИ/системной эмболии переходили на терапию варфарином [13]. При переходе пациентов на АСК риск возникновения ССО соответствовал результатам анализа в группе пациентов, получавших АСК в исследовании AVERROES [12].
В модели была учтена как общая смертность пациентов (с учетом половозрастной таблицы смертности населения РФ за 2010 г. [15]), так и смертность, обусловленная развитием ССО. Летальность при ИМ (16%) соответствовала данным федеральной статистики по РФ [16]. Летальность при внутричерепных кровотечениях была принята равной 36,5% [17], при прочих больших кровотечениях, включая желудочно-кишечные, — 5,1% [18].
Риск развития инсульта (как ишемического, так и геморрагического) был скорректирован на распределение пациентов по результатам оценки по шкале CHADS2 на момент начала терапии. В модели было учтено возрастание риска развития инсульта, системной эмболии, ИМ и кровотечений с увеличением возраста пациентов [13].
Системная эмболия и ИМ рассматривались в качестве абсорбирующих состояний, т.е. в дальнейшем не предполагалось развития любых других сердечно-сосудистых исходов. После первичного инсульта допускалось развитие только одного повторного инсульта. Риск развития повторного инсульта (как ишемического, так и геморрагического) был принят равным 2,72 в расчете на 100 пациенто-лет, независимо от вида антикоагулянтной терапии [4].
Относительный риск развития клинических исходов. В исследовании проведено сравнение апиксабана в дозе 5 мг 2 раза в сутки с ривароксабаном в дозе 20 мг 1 раз в сутки, дабигатраном в дозе 150 мг 2 раза в сутки и дабигатраном в дозе 110 мг 2 раза в сутки. В соответствии с инструкцией по применению дабигатрана предполагалось снижение дозы препарата со 150 до 110 мг 2 раза в день у пациентов старше 80 лет [19, 20].
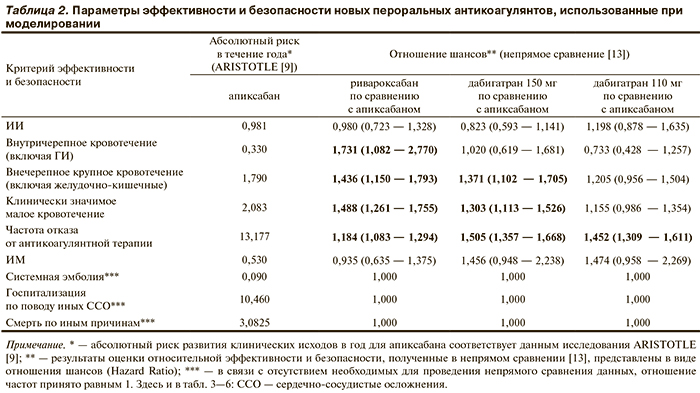
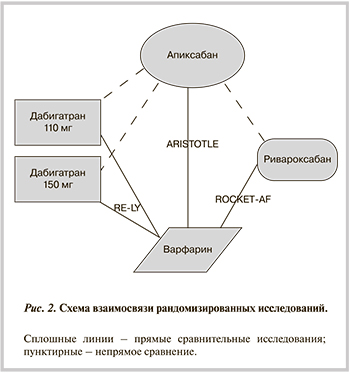
Абсолютный риск развития ССО при терапии апиксабаном соответствовал данным исследования ARISTOTLE [9]. Относительный риск развития ССО при терапии ривароксабаном и дабигатраном по сравнению с апиксабаном соответствовал данным непрямого сравнения, результаты которого приведены в статье G. Lip и соавт. [13] (рис. 2).
При проведении непрямого сравнения сделано допущение, что данные клинических исследований ARISTOTLE, RE-LY и ROCKET-AF сопоставимы с точки зрения методологического качества, популяции пациентов и изучаемых исходов. Однако на полученные в непрямом сравнении результаты могли оказать влияние следующие факторы:
- исследование ROCKET-AF включало более тяжелых пациентов (требовалось наличие ≥2 ФР развития инсульта) по сравнению с ARISTOTLE и RE-LY (было достаточно 1 ФР для включения в исследование);
- методологическое качество исследования RE-LY (открытый дизайн) несколько ниже, чем двойных слепых исследований ARISTOTLE и ROCKET-AF, и клиническая эффективность дабигатрана по сравнению с варфарином могла оказаться завышенной [21].
По результатам непрямого сравнения (табл. 2) не найдено статистически значимых различий по частоте развития ИИ между апиксабаном и другими новыми пероральными антикоагулянтами. При этом апиксабан продемонстрировал статистически значимо меньший риск возникновения ГИ и других внутричерепных кровотечений по сравнению с ривароксабаном; статистически значимо меньший риск возникновения внечерепных крупных кровотечений (включая желудочно-кишечные) и клинически значимых малых кровотечений по сравнению с ривароксабаном и дабигатраном в дозе 150 мг. Кроме того, апиксабан статистически значимо превосходил препараты сравнения в отношении частоты отказа от антикоагулянтной терапии.
 В связи с отсутствием сравнительных данных, в процессе моделирования принято допущение, что риск системной эмболии, госпитализации по поводу иных ССО и смерти по иным причинам является одинаковым для всех 3 новых пероральных антикоагулянтов.
В связи с отсутствием сравнительных данных, в процессе моделирования принято допущение, что риск системной эмболии, госпитализации по поводу иных ССО и смерти по иным причинам является одинаковым для всех 3 новых пероральных антикоагулянтов.
Популяция пациентов. В рамках модели рассмотрены пациенты с неклапанной ФП без противопоказаний к терапии антагонистами витамина К. Выбор популяции был обоснован тем, что непрямое сравнение новых пероральных антикоагулянтов проводили с использованием результатов рандомизированных клинических исследований, в которых участвовали пациенты без противопоказаний к назначению варфарина.
Клинико-демографические характеристики пациентов с ФП соответствовали российским данным [25]. Средний возраст пациентов на момент начала терапии составлял 70 лет; доля мужчин была равна 64,7%; средняя оценка по шкале CHADS2 была равна 2 баллам. В модели было сделано допущение, что распределение пациентов в зависимости от риска развития инсульта по шкале CHADS2 со временем остается неизменным.
Расчет медицинских затрат. В исследовании учтены только прямые медицинские затраты, включающие затраты на антикоагулянтную терапию, терапию ССО и мониторинг. Затраты на терапию осложнений включали стоимость госпитализации и реабилитации пациентов, которые соответствовали базовому тарифу ОМС по Санкт-Петербургу на 2014 г. Затраты на апиксабан (эликвис, «Бристол-Майерс Сквибб»), ривароксабан (ксарелто, «Байер Шеринг Фарма АГ») и дабигатран (прадакса, «Берингер Ингельхайм Интернешнл ГмбХ») были рассчитаны на основании средневзвешенной цены госзакупок за 2013 г. (табл. 3).
Показатели клинико-экономической эффективности.
В качестве показателей клинико-экономической эффективности рассчитаны коэффициенты эффективности дополнительных затрат (ICER — incremental cost-effectiveness ratio) в расчете на 1 дополнительный год жизни и на 1 дополнительный год жизни с учетом качества (QALY — quality adjusted life year). Качество жизни пациентов соответствовало данным международного исследования [22].
С целью учета бóльшей значимости затрат и клинических преимуществ в настоящее время по сравнению с отдаленным будущим (дисконтирование), затраты и продолжительность жизни дисконтировали на 3,5% в год.
Анализ чувствительности. Надежность полученных результатов оценивали с помощью анализа чувствительности результатов к изменению основных параметров моделирования. Было изучено влияние следующих параметров на результаты исследования:
- снижение исходного возраста пациентов (до 60 и 50 лет);
- использование равной частоты отказа пациентов от антикоагулянтной терапии, соответствующей частоте отказа от апиксабана в исследовании ARISTOTLE, и расчет без учета отказа пациентов от терапии.
Результаты и обсуждение
Ожидаемое количество ССО при терапии новыми пероральными антикоагулянтами в течение периода дожития когорты из 1000 пациентов с неклапанной ФП без учета отказа от терапии представлено в табл. 4.
Из табл. 4 видно, что, если не учитывать вероятность отказа пациентов от антикоагулянтной терапии, апиксабан по сравнению с дабигатраном и ривароксабаном характеризуется лучшим профилем безопасности, в частности, меньшей вероятностью развития внутричерепных, крупных внечерепных, а также клинически значимых малых кровотечений. При этом по эффективности в отношении предотвращения тромбоэмболических исходов апиксабан превосходит дабигатран 110 мг, сопоставим с ривароксабаном и несколько уступает дабигатрану в дозе 150 мг. В то же время, по сравнению с дабигатраном в дозе 150 мг апиксабан характеризуется меньшей вероятностью развития ИМ. В целом, по сравнению с другими новыми пероральными антикоагулянтами, апиксабан обеспечивает снижение количества летальных исходов, обусловленных развитием ССО.

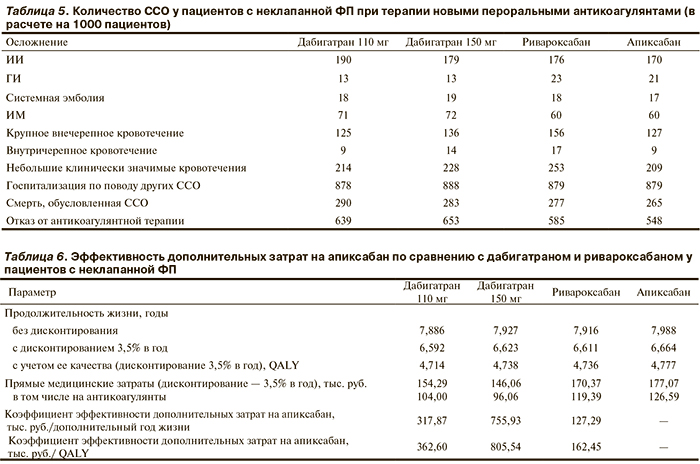
Однако при моделировании развития осложнений ФП в реальной клинической практике необходимо учитывать вероятность отказа пациентов от терапии антикоагулянтами. Количество осложнений при частоте отказа от терапии, рассчитанной на основании данных клинических исследований RE-LY, ROCKET-AF и ARISTOTLE, представлено в табл. 5.
В соответствии с результатами моделирования, пациенты, получающие апиксабан, реже отказываются от антикоагулянтной терапии, чем получающие ривароксабан и дабигатран. Эти данные отражают результаты непрямого сравнения, в котором найдена статистически значимо меньшая частота отказа от терапии апиксабаном по сравнению с двумя другими новыми пероральными антикоагулянтами. За счет более длительного периода приема, терапия апиксабаном по сравнению с другими новыми пероральными антикоагулянтами приводит к развитию меньшего числа ИИ, но при этом различия по числу внутричерепных, крупных внечерепных и клинически значимых небольших кровотечений становятся менее выраженными. Однако и в этом случае апиксабан в целом приводит к меньшему числу летальных исходов в связи с ССО.
Результаты оценки эффективности затрат на новые пероральные антикоагулянты представлены в табл. 6.
По результатам моделирования, терапия апиксабаном обеспечивает увеличение средней продолжительности жизни пациентов с ФП (без дисконтирования) на 0,101 года по сравнению с дабигатраном в дозе 110 мг, на 0,060 года по сравнению с дабигатраном в дозе 150 мг и на 0,072 года по сравнению с ривароксабаном (см. табл. 6). Средняя продолжительность жизни с учетом ее качества при терапии апиксабаном по сравнению с дабигатраном в дозе 110 и 150 мг и ривароксабаном увеличивается на 0,063, 0,038 и 0,041 года соответственно.
Суммарные медицинские затраты на период дожития пациентов с ФП были несколько выше в случае терапии апиксабаном, по сравнению с ривароксабаном и дабигатраном. При этом дополнительные затраты на апиксабан по сравнению с дабигатраном в дозе 110 и 150 мг и ривароксабаном в расчете на 1 дополнительный год жизни составят 317,87, 755,93 и 127,29 тыс. руб., а в расчете на 1 дополнительный год жизни с учетом ее качества — 362,60, 805,54 и 162,45 тыс. руб. соответственно.
В соответствии с рекомендациями ВОЗ [23], терапия может рассматриваться в качестве экономически приемлемой, если затраты на 1 дополнительный год жизни с учетом ее качества (QALY) не превышают утроенной величины валового внутреннего продукта на душу населения (ВВП). Вследствие этого, для бюджетного здравоохранения в Российской Федерации уровень дополнительных затрат на 1 дополнительный QALY не должен превышать 1,4 млн руб. (в 2013 г. ВВП на душу населения составил около 465 тыс. руб. [www.gks.ru]). В случае если затраты на 1 дополнительный QALY не превышают однократной величины ВВП, медицинская технология может рассматриваться как экономически высокоэффективная и рекомендоваться для широкого применения в клинической практике.
Таким образом, на основании результатов данного исследования можно сделать вывод, что терапия апиксабаном является экономически высокоэффективной по сравнению с дабигатраном в дозе 110 мг и ривароксабаном, и экономически приемлемой по сравнению с дабигатраном в дозе 150 мг.
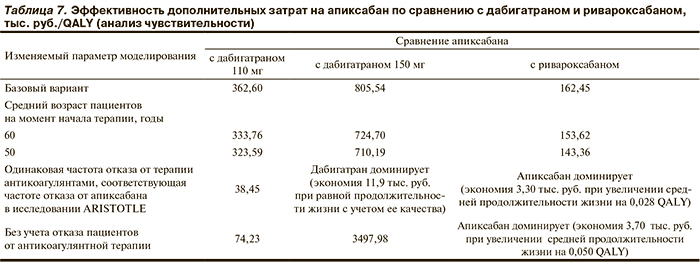
Анализ чувствительности. Данные анализа чувствительности результатов к изменению параметров моделирования представлены в табл. 7.
Снижение возраста пациентов в момент начала терапии влечет за собой увеличение эффективности дополнительных затрат на апиксабан по сравнению с дабигатраном и ривароксабаном, и апиксабан остается экономически приемлемой альтернативой для бюджетного здравоохранения РФ.
Определенное влияние на эффективность затрат оказывает частота отказа от терапии антикоагулянтами. При одинаковой частоте отказа от терапии коэффициент эффективности дополнительных затрат для апиксабана по сравнению с дабигатраном в дозе 110 мг снижается по сравнению с базовым вариантом, т.е. экономическая привлекательность апиксабана повышается. По сравнению с ривароксабаном апиксабан является при данном варианте доминирующей альтернативой, т.е. не только увеличивает среднюю продолжительность жизни с учетом ее качества, но и обеспечивает экономию средств. В то же время при равной частоте отказа от терапии дабигатран в дозе 150 мг доминирует над апиксабаном и при равной продолжительности жизни с учетом ее качества позволяет снизить затраты в среднем на 11,9 тыс. руб. в расчете на 1 пациента.
Если в процессе моделирования не учитывать вероятность отказа от терапии новыми пероральными антикоагулянтами, то апиксабан является экономически высокоэффективной альтернативой дабигатрану в дозе 110 мг и доминирует по отношению к ривароксабану. При этом он обеспечивает минимальное увеличение средней продолжительности жизни с учетом качества (на 0,004 QALY) по сравнению с дабигатраном в дозе 150 мг, но коэффициент эффективности дополнительных затрат в данной ситуации оказывается неприемлемо высоким.
Обсуждение
Результаты базового анализа показали, что у пациентов с неклапанной ФП терапия апиксабаном по сравнению с ривароксабаном и дабигатраном в дозе 110 и 150 мг обеспечивает бо'льшую продолжительность жизни, в том числе с учетом ее качества, и является экономически приемлемой для российского бюджетного здравоохранения. Полученные результаты были устойчивы к изменению возраста пациентов на момент начала терапии, но чувствительны к изменению допущения о различиях между антикоагулянтными препаратами в частоте отказа пациентов от терапии.
К настоящему моменту опубликованы результаты еще одного клинико-экономического анализа применения новых пероральных антикоагулянтов у пациентов с неклапанной ФП в Российской Федерации, в котором также использовалась модель Маркова для прогнозирования развития ССО и затрат на лечение при применении апиксабана, ривароксабана и дабигатрана в дозе 150 мг [24]. Данное исследование и исследование М.В. Авксентьевой и соавт. [24] обладают рядом различий, которые необходимо учитывать при сопоставлении их результатов и выводов.
Во-первых, несмотря на то, что оба исследования основаны на результатах непрямого сравнения новых пероральных антикоагулянтов, выборка пациентов в исследовании [24] ограничена пациентами, имевшими исходно ≥2 ФР развития инсульта по шкале CHADS2. В связи с тем что в сравниваемых моделях использованы разные показатели эффективности и безопасности антикоагулянтной терапии (в модели из исследования [24] использованы комбинированные конечные точки), не представляется возможным корректно сопоставить результаты непрямого сравнения в полной выборке пациентов и в выборке пациентов с ≥2 ФР развития инсульта. Однако стоит отметить, что на основании и того, и другого непрямого сравнения сделаны одинаковые выводы: апиксабан сопоставим с ривароксабаном и дабигатраном 150 мг по эффективности, но характеризуется лучшим профилем безопасности. Ввиду того что в российской популяции пациентов с ФП подгруппа пациентов с одним ФР по шкале CHADS2 составляет около 40% [25], результаты исследования [24] должны быть с осторожностью экстраполированы на общую выборку российских пациентов с ФП. С другой стороны, то, что исследование ROCKET-AF включало более тяжелых пациентов (требовалось наличие ≥2 ФР развития инсульта) по сравнению с ARISTOTLE и RE-LY (было достаточно одного ФР для включения в исследование), могло повлиять на результаты непрямого сравнения для общей выборки пациентов, использованные в данном исследовании.
Во-вторых, в связи с сопоставимой эффективностью новых пероральных антикоагулянтов в отношении развития инсульта/системной эмболии (по результатам непрямого сравнения) авторы исследования [24] применили метод минимизации затрат и не учли статистически значимое преимущество апиксабана перед ривароксабаном и дабигатраном 150 мг в отношении частоты развития крупных внечерепных кровотечений и клинически значимых небольших кровотечений. Кроме того, на анализ медицинских затрат в исследовании [24] могло повлиять использование розничных цен на апиксабан, которые заведомо превышают тендерные цены как минимум на величину розничной надбавки, по сравнению с тендерными ценами на ривароксабан и дабигатран 150 мг.
Особенностью проведенного нами исследования является подробное раздельное моделирование случаев развития ИИ и ГИ и системной эмболии с учетом базового риска развития инсульта по шкале CHADS2, а также распределения пациентов по степени тяжести функционального состояния после острой фазы инсульта согласно модифицированной шкале Рэнкина. При этом указанные параметры моделирования соответствовали данным российской клинической практики. Кроме того, в этой модели учтено влияние частоты отказа пациентов от антикоагулянтной терапии и перехода на терапию второй линии.
К ограничениям проведенного исследования следует отнести то, что в использованной модели у пациентов с ИИ или ГИ допускалось развитие только одного повторного инсульта, а это, скорее всего, не соответствует реальной клинической практике (в модели [24] не предполагалось развитие последующих ССО у пациентов после инсульта/системной эмболии). Ограничение числа последующих ССО было обосновано тем, что в рандомизированных исследованиях новых пероральных антикоагулянтов учитывали только первичные случаи инсульта/системной эмболии, после чего пациенты выбывали из исследований.
В целом необходимо учитывать, что, как и в случае с любым другим исследованием, основанным на методе моделирования, полученные результаты должны быть интерпретированы с учетом принятых допущений и могут отличаться от результатов в реальной клинической практике.
Выводы
Согласно результатам моделирования, апиксабан по сравнению с ривароксабаном и дабигатраном в дозе 110 и 150 мг обеспечивает бо'льшую продолжительность жизни пациентов с неклапанной фибрилляцией предсердий и характеризуется приемлемой для российского бюджетного здравоохранения эффективностью дополнительных затрат.
Благодарность. Авторы выражают свою благодарность Л.Б. Завалий (невролог неврологического отделения для больных с острыми нарушениями мозгового кровообращения с палатой реанимации и интенсивной терапии НИИ скорой помощи им. Н. В. Склифосовского) за предоставление данных диссертационного исследования; В.А. Парфенову (кафедра нервных болезней Первого МГМУ им. И.М. Сеченова, Москва), О.И. Виноградову (клиника неврологии и нейрохирургии, Национальный медико-хирургический центр им. Н.И. Пирогова, Москва), Д.А. Сычеву (кафедра клинической фармакологии и терапии РМАПО, Москва) за участие в работе над адаптацией фармакоэкономической модели к условиям российской клинической практики в качестве экспертов.



