В США и странах европейского союза ежегодно выписывается более 140 млн рецептов на приобретение нестероидных противовоспалительных средств (НПВС)[1, 2]. Высокая противовоспалительная и анальгетическая активность НПВС давно доказана. Препараты активно используются с антифлогистической целью при ревматизме, остеоартрозах, миозитах, как жаропонижающее средство при лихорадках, для облегчения боли различной этиологии [1].
Вместе с тем результаты исследований, выполненных в последние годы, дают основания предполагать повышение риска неблагоприятных сердечно-сосудистых исходов у пациентов, получающих НПВС. И хотя имеющиеся данные носят крайне противоречивый характер, а без опасность НПВС (судя по результатам как проспективных, так и ретроспективных исследований) варьирует в полярных пределах (от «кардиотоксичного» по данным одних исследований до «кардиопротективного» по результатам других), Управление по контролю за качеством пищевых продуктов и лекарственных препаратов США все-таки опубликовало ставшее известным сообщение «в черной рамке», касающееся регламента использования НПВС у больных из группы риска развития сердечно-сосудистых осложнений. Данное предостережение нашло отражение в международных и национальных клинических рекомендациях и коротко его можно представить так: следует избегать назначения НПВС у кардиологических больных, при крайней необходимости препараты должны назначаться в минимальной дозе на минимально короткий срок, при этом предпочтение следует отдавать неселективным ингибиторам циклооксигеназы (ЦОГ).
Кроме того, в рекомендациях нашло место небезосновательное по своей сути утверждение о небезопасности одновременного использования ацетилсалициловой кислоты (АСК) и НПВС. К большому сожалению, опыт прошедших лет, с момента выхода предостережений, продемонстрировал, что их трудно применять в повседневной кардиологической практике.
С одной стороны, основы профилактики сердечно-сосудистых заболеваний, делают «золотым стандартом» необходимость назначения низких доз АСК и в некоторых популяционных группах процент применения АСК приближается к 100. С другой стороны, пациенты с факторами риска развития сердечно-сосудистых заболеваний относятся в основном к старшей возрастной группе и в этой связи имеют сопутствующие заболевания, при которых требуется постоянное использование НПВС. Число таких больных крайне велико. Эти обстоятельства сделали неизбежной необходимость длительного сочетанного использования НПВС и АСК у многих кардиологических больных, заставили пересмотреть отношение исследователей и врачебной общественности к этой проблеме и разобраться в особенностях лекарственного взаимодействия НПВС и АСК.
В настоящей статье предлагается алгоритм выбора НПВС для сочетанного использования с АСК у кардиологических больных.
Ответ в механизме действия
Основным в механизме противовоспалительного действия НПВС является их способность ингибировать фермент циклооксигеназу, катализирующий превращение свободных полиненасыщенных жирных кислот в простагландины, а также другие эйкозаноиды — тромбоксан и простациклин [3].
Существуют две изоформы циклооксигеназы —циклооксигеназа-1 (ЦОГ-1) и циклооксигеназа-2 (ЦОГ-2). В тканях ЦОГ-1 присутствует практически повсеместно. В тромбоцитах он обеспечивает превращение арахидоновой кислоты в тромбоксан. ЦОГ-2 в обычных условиях присутствует в мозге и корковом слое почек. В других тканях экспрессия гена ЦОГ-2 индуцируется определенными стимулами, например, она увеличивается при воспалении.
Роль простагландинов в процессе гемостаза также сложна и связана с взаимодействием различных тканей и простаноидов. Продукция тромбоксана-А2 тромбоцитов — индуктора адгезии и агрегации тромбоцитов, проходит с участием фермента ЦОГ-1 [4—6]. В то же время клетки эндотелия сосудов вырабатывают простагландин I2, обладающий вазодилатирующими и антитромботическими свойствами. ЦОГ-2 ответственен за преобразование арахидоновой кислоты в простагландин I2 [6, 7]. Таким образом, в условиях нормы сохраняется здоровый баланс между тромбоцитарным тромбоксаном-А2 и эндотелиальным простагландином I2. Нарушение этого хрупкого баланса приводит к изменениям в системе гемостаза [6, 7].
Неселективные НПВС конкурентно взаимодействуют с активным участком фермента и ингибируют обе его изоформы (как ЦОГ-2, так и ЦОГ-1). Считается, что основное терапевтическое действие этих средств обеспечивается влиянием на ЦОГ-2, тогда как подавление ЦОГ-1 способствует повреждению слизистой оболочки желудочно-кишечного тракта.
В то же время то, что определяет «гастротоксичность» ингибитора ЦОГ, является главным в формировании «кардиопротективных» свойств АСК. Необходимо отметить, что только для низких доз АСК применимо определение «кардиопротективности». В оптимальной низкой дозе до 100 мг/сут препарат практически полностью подавляет тромбоксаниндуцированную агрегацию тромбоцитов, никак при этом, не влияя на кардиопротективные эффекты ЦОГ-2 [8].
По некоторым данным, 30 мг АСК в сутки может быть вполне достаточно для получения адекватного антитромботического эффекта [8]. Вместе с тем существует небезосновательное утверждение, основанное на результатах некоторых сравнительных исследований различных доз АСК при его длительном применении, о том, что при повышении дозы АСК препарат теряет свои кардиопротективные свойства и проявляет ЦОГ-2 селективные свойства, подавляя ЦОГ-2 ассоциированную кардиопротекцию [9].
Однако в большей степени данная концепция применима к «не аспириновым» НПВС. Измерение и сопоставление степени селективности может быть одним из путей объяснения различий по степени риска развития ССО всех других ингибиторов ЦОГ. Существуют методы измерения концентрации лекарства, необходимой для ингибирования ЦОГ-1 и ЦОГ-2 на 50% (IC50) [3, 10, 11]. Индекс селективности менее 1 указывает на то, что препарат обладает большей ЦОГ-1-селективностью, в то время как индекс более 1 свидетельствует о том, что препарат обладает большей ЦОГ-2-селективностью [12]. Индекс селективности может использоваться в том числе для определения риска развития побочных желудочно-кишечных эффектов, связанных с приемом ингибиторов ЦОГ. Однако, как показали результаты многих клинических исследований, чем выше степень селективности препарата, тем больше риск развития ССО (см. таблицу) [12—14].
Таким образом, первым правилом при выборе НПВС у больных с риском развития ССО является использование низкоселективных ингибиторов ЦОГ. При невозможности использования неселективного НПВС показано применение селективного препарата в минимально возможной дозе на максимально короткий срок.
Большая роль ЦОГ-2
По своей сути в большинстве случаев острое коронарное событие — шаг от хронического течения атеросклеротического процесса до катастрофы, происходящий вследствие эрозии и разрыва атеросклеротической бляшки. Современные представления об атеросклеротическом процессе свидетельствуют о воспалении как о ключевом аспекте в формировании и последующей дестабилизации бляшки [15, 16]. При этом немаловажная роль в этом воспалении отводится ЦОГ-2-зависимому воспалению. [17—19]. Установлено, что при дестабилизации атеросклеротической бляшки происходит гиперэкспрессия ЦОГ-2 как в самой бляшке, так и в ее покрышке (рис. 1).
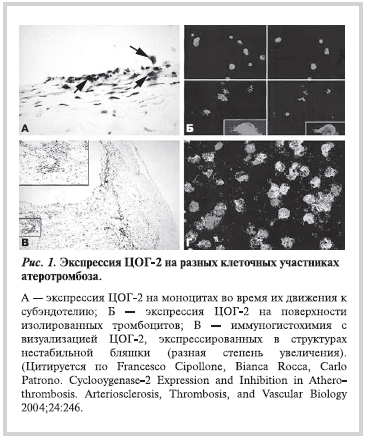
Кроме того, от 8 до 45% пациентов, получающих низкие дозы АСК, демонстрируют лабораторную резистентность к препарату, когда АСК в недостаточной степени снижает уровень тромбоксана А2 [20]. Известно, что для достижения антитромбоцитарного эффекта АСК необходимо ингибирование тромбоксана А2 не менее чем на 90% от исходного [21]. Одной из возможных причин снижения эффективности АСК является ЦОГ-2-зависимый путь образования тромбоцитов [22, 23].
Более того, в случае острого коронарного синдрома (ОКС) происходит стресс-индуцированная экспрессия ЦОГ-2 в клетках-предшественниках тромбоцитов — мегакариоцитах [24]. Это повышает в крови количество тромбоцитов, не чувствительных к низким дозам АСК (см. рис. 1).
В этой связи вполне обосновано рассматривать сердечно-сосудистые эффекты ингибиторов ЦОГ при двух разных клинических ситуациях: остром и хроническом течении атеросклеротического процесса. И также, становится понятной польза от использования НПВС у больных при обострении ИБС, продемонстрированная в некоторых исследованиях, связанная с подавлением ЦОГ-2 зависимого воспаления в области нестабильной бляшки и снижением ЦОГ-2 ассоциированной агрегации тромбоцитов.
Хорошим примером, в данном случае, может служить проспективное исследование по оценке эффективности флурбипрофена у пациентов с острым инфарктом миокарда, подвергшимся системному тромболизису или ангиопластике. Терапия флурбипрофеном выразилась в 70% снижении риска развития повторного инфаркта миокарда по результатам 6-месячного наблюдения. Необходимость в повторной ангиопластике также была существенно ниже [25].
Существуют и ретроспективные доказательства кардиопротективных эффектов неселективных ингибиторов ЦОГ у пациентов после ОКС. В качестве примера можно привести данные Cooperative Cardiovascular Projectcs Medicare database. В исследование были включены пациенты старше 65 лет, госпитализированные по поводу острого инфаркта миокарда и рандомизированные в 3 группы: получавшие после выписки из стационара только НПВС, получавшие только АСК и те, кто принимали АСК и НПВС [26]. Годичная смертность была одинаковой во всех 3 группах. Результат свидетельствует о том, что больные, длительно получавшие НПВС, и те, кто принимал АСК, имели сходный уровень кардиопротекции. В группе больных, принимавших два препарата одновременно (АСК и НПВС), также получен протективный эффект, но он не носил аддитивный характер.
Таким образом, несмотря на то что данная статья не ставит своей основной целью детальное освещение вопросов кардиопротективных свойств НПВС, которые, безусловно, существуют и заслуживают отдельного обсуждения, важно научное понимание потенциальной возможности использования АСК и НПВС у АСК-резистентных больных, а также в условиях стресс-индуцированных экспрессии ЦОГ-2 в мегакариоцитах (при ОКС).
Проблема конкурентных связей
Используя НПВС, следует учитывать, что разные препараты могут по-разному влиять на агрегацию тромбоцитов. По механизму взаимодействия с ЦОГ выделяют 3 группы НПВС:
1) ингибиторы ЦОГ медленного и обратимого действия;
2) ингибиторы ЦОГ медленного и необратимого действия;
3) ингибиторы ЦОГ быстрого обратимого действия.
Данная классификация имеет большое практическое значение в свете обсуждаемой темы. Большинство существующих НПВС являются обратимыми ингибиторами ЦОГ. Скорость и обратимость имеют большое значение для ЦОГ-1. Попав в кровяное русло, препараты быстро вступают во взаимодействие c тромбоцитами, подавляя активность ЦОГ-1 и снижая агрегацию тромбоцитов. При этом агрегация тромбоцитов восстанавливается по мере снижения концентрации препарата крови. В конечном итоге длительность дезагрегантного эффекта в этом случае зависит от длительности действия препарата.
Исключением из списка обратимых ингибиторов ЦОГ является АСК. Попав один раз в кровяное русло и связавшись с рецептором тромбоцита, АСК проявляет дезагрегантную активность на протяжении всего времени жизни тромбоцита (7—8 дней) независимо от конечной концентрации препарата в крови.
При сочетанном использовании АСК и НПВС препараты вступают в конкурентную борьбу за рецептор тромбоцита. «Победителем» при этом чаще становятся ингибиторы быстрого действия, которые лишь временно подавляют ассоциированную с ЦОГ-1 агрегацию тромбоцитов и, освободив рецептор, спустя какое-то время, образуют «оголенные» тромбоциты, на которые необратимый дезагрегантный эффект АСК не успел распространиться.
Группой исследователей на примере ибупрофена была проверена данная теория. В исследовании группа пациентов получали низкую дозу АСК за 2 ч до приема ибупрофена, а затем, после периода «отмывки» — ибупрофен за 2 ч до приема АСК. Для лабораторной оценки дезагрегантной активности использовали наиболее подходящий в этом случае стабильный метаболит тромбоксана А2 —тромбоксан В2. По результатам исследования установлено, что влияние АСК на агрегацию тромбоцитов ослаблялось в случае, когда ибупрофен принимался за 2 ч до АСК, в то время как агрегация не изменялась при приеме АСК перед ибупрофеном [27].
Исходя из изложенного представляется вполне обоснованным в случае необходимости одновременное применение АСК и НПВС, использование НПВС короткого действия, так как препараты длительного действия в большей степени перекрывают временное поле своего взаимодействия с рецептором ЦОГ-1, не оставляя возможности для контакта с АСК, какой бы режим приема при этом ни избирался.
Таким образом, при сочетанном использовании кардиопротективных доз АСК и НПВС рекомендуется назначение АСК, по крайней мере, за 2 ч до НПВС для избегания конкурентного взаимодействия и использование НПВС короткого действия.
Способ и скорость доставки препарата
Необходимо отметить, что помимо особенностей лекарственного взаимодействия и других описанных выше требований, предъявляемых к НПВС при сочетанном использовании с АСК, препараты должны соответствовать представлениям о современном и удобном в применении ингибиторе ЦОГ. В условиях больших ограничений и жестких рамок для НПВС у кардиологических больных необходимо быть уверенным, что препарат остается удобным в применении и является безальтернативным в случае возникновения разных клинических ситуаций у одного больного.
К таким представлениям, помимо прочих известных, относятся наличие формы препарата с быстрым началом действия («рапид») и возможность парентерального введения (см. таблицу).
Таблица. Сравнительная характеристика некоторых НПВС на основании требований, предъявляемых к ингибиторам ЦОГ при их совместном использовании с низкими дозами АСК (выделены в последовательном порядке характеристики, наиболее удовлетворяющие требованиям).
Примечание. НПВС — нестероидные противовоспалительные средства; ЦОГ — циклооксигеназа; IC50 — концентрация лекарства, необходимая для ингибирования ЦОГ—1 и ЦОГ—2 на 50%; * — исключение.
Таким образом, исходя из изложенного, требования к НПВС для сочетанного использования с низкими дозами АСК следующие: неселективный, с низким индексом селективности, с достаточной ЦОГ-2-противовоспалительной активностью, удобной формы выпуска короткодействующий ингибитор ЦОГ.
Данным требованиям из представленных на российском рынке отвечает неселективный короткодействующий оксикам — лорноксикам.
Для подтверждения этого суждения мы провели исследование по оценке эффектов лорноксикама при сочетанном использовании с АСК у пациентов с ОКС без подъема сегмента ST [28, 29]. В данной статье нам представляется целесообразным привести отдельные результаты, касающиеся обсуждаемой темы.
В пилотное исследование были включены 85 больных с ОКС без подъема сегмента ST, получавшие терапию в соответствии с национальными и международными рекомендациями. Больные были рандомизированы в 2 группы: группа пациентов, получавших лорноксикам + АСК (100 мг/сут) в течение 15 дней и контрольная группа (только АСК).
В течение исследования дважды производилась оценка уровня тромбоксана В2: в момент включения больного в исследование и на 15-й день терапии.
У тромбоксана А2, участвующего в агрегации тромбоцитов, в физиологических условиях период полувыведения составляет примерно 37 с. Поэтому уровень тромбоксана А2 определяется путем измерения содержания тромбоксана В2 в сыворотке крови, являющегося его стабильным метаболитом.
Уровень тромбоксана В2 (в пг/мл) определяли иммуноферментным методом с помощью наборов фирмы Assay designs. Порог чувствительности данного метода составил 0,1 пг/мл.
Кроме того, в полученной крови исследовали уровень маркеров воспаления (С-реактивного белка, интерлейкинов — ИЛ-1, ИЛ-6, ИЛ-10).
По результатам исследования, средний уровень тромбоксана В2 у всех больных на момент включения в исследование составил 2,32±0,49 нг/мл. Известно, что максимальный дезагрегантный эффект АСК проявляется в первые сутки от начала приема препарата с более чем 90% снижением уровня тромбоксана. Поэтому низкие уровни тромбоксана связаны с тем, что больные уже получили 100 мг АСК в момент поступления в стационар за 24 ч до рандомизации в исследование и взятия крови.
Выявлены особенности при анализе изменений уровней тромбоксана В2 по группам больных. В контрольной группе пациентов, получавших только АСК, средний уровень тромбоксана В2 в сыворотке крови, взятой на 15-й день наблюдения, снизился с 2,7±0,66 до 1,08±0,11 нг/мл т.е. на 60%.В то же время в группе пациентов, получавших лорноксикам + АСК, произошло 38% увеличение уровня тромбоксана В2 с 1,32±0,14 до 2,13±0,4 нг/мл (р=0,04). Данные представлены на рис. 2.
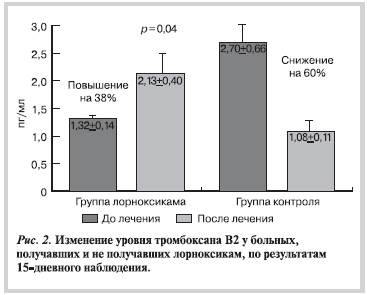
Таким образом, на примере этого исследования доказаны жизнеспособность и достоверность концепции конкурентного лекарственного взаимодействия АСК и НПВС и правдоподобность необходимости приема АСК за 2 ч до применения ингибитора ЦОГ.
Важно, однако, отметить, что сочетанное использование лорноксикама и АСК достоверно повлияло на уровень тромбоксана к 15-му дню наблюдения, но динамика дезагрегантной активности оказалась незначимой при сравнении с предполагаемыми исходными уровнями тромбоксана В2 (без АСК).
Более того, подтвердились все другие утверждения по поводу кардиопротективных свойств лорноксикама. По результатам 6-месячного наблюдения в группе больных, принимавших лорноксикам, зарегистрировано достоверное снижение частоты развития всех сердечно-сосудистых осложнений. Достоверным оказалось уменьшение числа случаев повторной госпитализации по поводу НС в группе, больных получавших лорноксикам. Снижение абсолютного риска всех сердечно-сосудистых исходов составило 24,5% (р=0,006) (рис. 3). В группе больных, получавших лорноксикам, отмечено также достоверное снижение уровней С-реактивного белка, ИЛ-6 и повышение содержания противовоспалительного цитокина ИЛ-10.
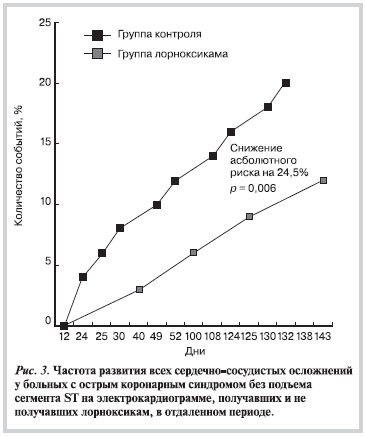
Заключение
С появлением большого арсенала противовоспалительных средств становится ясным, что их объединение в единый класс носит скорее условный характер. Различные по химической структуре, механизму действия, характеру лекарственного взаимодействия, степени дезагрегантной и противовоспалительной активности ингибиторы циклооксигеназы обусловливают необходимость аргументированного подхода к подбору нестероидного противовоспалительного средства у пациентов с ишемической болезнью сердца и факторами риска развития сердечно-сосудистых осложнений, нуждающихся в постоянном получении низких доз ацетилсалициловой кислоты.
Основополагающими моментами при выборе нестероидного противовоспалительного средства у кардиологического больного, уже получающего ацетилсалициловую кислоту с кардиопротективной целью, являются:
1) механизм действия ингибитора циклооксигеназы (предпочтение неселективному ингибитору циклооксигеназы);
2) степень селективности нестероидного противовоспалительного средства (чем меньше индекс селективности, тем выше безопасность);
3) длительность действия препарата (предпочтение отдают препарату короткого действия);
4) время приема нестероидного противовоспалительного средства и ацетилсалициловой кислоты: разница не менее 2 ч во времени приема нестероидного противовоспалительного средства и ацетилсалициловой кислоты при условии назначения ацетилсалициловой кислоты в первую очередь (увеличивает эффективность ацетилсалициловой кислоты и безопасность нестероидного противовоспалительного средства);
5) современные требования к нестероидному противовоспалительному средству: парентеральное введение, форма «рапид» (при клинической необходимости).
Характеристика некоторых ингибиторов циклооксигеназы, имеющихся на российском фармацевтическом рынке, представлена в сводной таблице.



