Различные клинические проявления атеротромбоза — лидирующие причины смертности населения в экономически развитых странах. По данным Всемирной организации здравоохранения, в 2000 г. доля смертей от сердечно-сосудистых (ССЗ) и цереброваскулярных заболеваний составила 52% в структуре общей смертности, превосходя онкологическую патологию (24%) и инфекционные заболевания (19%) [1]. Предполагается, что к 2030 г. число умерших от ССЗ увеличится до 24,2 млн. В связи с этим
остро стоит вопрос об эффективности профилактической стратегии, в том числе в России, которая относится к странам высокого риска.
Нарушения свертываемости крови играют важную роль в патогенезе атеросклероза, инфаркта миокарда (ИМ), ухудшении микроциркуляции и других патологических состояний. Клинические проявления атеротромбоза зависят от локализации атеросклеротической бляшки и размеров тромбов и реализуются в виде разнообразных форм ишемической болезни сердца (ИБС), ишемической
болезни мозга, перемежающейся хромоты и т.д.
Известно, что тромбоциты первыми реагируют на разрыв атеросклеротической бляшки и составляют основу для формирования артериального тромба [2, 3]. Именно такие бляшки служат причиной большинства острых сосудистых катастроф. Характерной особенностью атеротромбоза являются его постоянное прогрессирование и системность поражения сосудов. Больной, перенесший атеротромботический эпизод, имеет повышенный риск повторного события в том же или другом сосудистом бассейне. Например, после первого ИМ вероятность развития второго (включая смерть) увеличивается в 5—7 раз, а мозгового инсульта (МИ) — в 3—4 раза. При ишемическом ИМ риск развития повторного МИ увеличивается в 9 раз, а ИМ — в 2—3 раза (включая внезапную смерть) [4]. Тесная взаимосвязь процессов атерогенеза и тромбообразования делает патогенетически оправданным проведение длительной антитромботической терапии для профилактики сердечно-сосудистых осложнений (ССО) при всех проявлениях атеротромбоза. Ведущая роль в профилактике тромботических осложнений атеросклероза принадлежит препаратам, ингибирующим агрегацию
тромбоцитов (АТ) [5—7]. Не удивительно, что успехи, которые были достигнуты в лечении и профилактике осложнений ССЗ за последние десятилетия, во многом связаны с применением антитромботических препаратов. Одним из самых часто используемых дезагрегантов является ацетилсалициловая кислота (АСК), механизм действия которой связан с угнетением циклооксигеназы —
основного фермента метаболизма арахидоновой кислоты, являющейся предшественником простагландинов, которые играют главную роль в патогенезе воспаления, боли и лихорадки, а также тромбоксана А2, вызывающего АТ. В последние годы активно обсуждаются другие механизмы действия АСК, обнаруженные в экспериментальных и клинических исследованиях. Такие гемостатические
эффекты АСК, как усиление фибринолиза и снижение свертывания крови не связаны с подавлением синтеза ТХА2. Подавляя образование тромбина и превращение фибриногена в фибрин, АСК может тормозить образование тромба. При действии АСК нити фибрина разрыхляются, что облегчает доступ к ним активаторов плазминогена, вызывающих их растворение. Важной особенностью действия АСК является его способность стабилизировать «взрывоопасную» (нестабильную) атероматозную бляшку. АСК подавляет как экспрессию генов, вовлеченных в активацию воспалительных процессов, так
и активацию провоспалительных цитокинов (α-фактора некроза опухоли, и интерлейкина-1β), а также снижает уровень С-реактивного белка [8], что немаловажно, так как воспалительные процессы в бляшке повышают риск ее разрыва. Стабильность атеросклеротической бляшки может увеличиваться и вследствие антиоксидантного действия АСК, защищающего эндотелий сосудов от продуктов перекисного окисления — свободных радикалов ОН– [9].
Доказательная база применения АСК для снижения риска развития ССО в настоящее время одна из наиболее больших и мощных, особенно в рамках вторичной профилактики. Так, по данным мета-анализа Antiplatelet TrialistsÁColla boration, включавшего более 50 исследований, в которых участвовали 100 000 больных, показано, что применение АСК с целью вторичной профилактики снижает сосудистую смертность на 15% и частоту развития несмертельных сосудистых осложнений —
на 30% [10]. В следующем мета-анализе Antithrombotic Trialists© Collaboration, включившем результаты 287 исследований и данные более 20 0000 пациентов из группы высокого риска с установленными ССЗ, было выявлено, что назначение антиагрегантов снижает суммарный риск развития сосудистых осложнений приблизительно на ¼, нефатального ИМ — на ⅓, нефатального МИ — на ¼, сосудистой смерти — на 1/6 [10].
Профилактический эффект терапии АСК тем более очевиден, чем выше риск развития сосудистых осложнений. Если роль антиагрегантов во вторичной профилактике ССО определена, то в первичной профилактике менее ясна. Наиболее четко роль АСК в первичной профилактике описывается результатами мета-анализа Antithrombotic Trialists© Collaboration, опубликованными в 2009 г. [11] и включившего 6 исследований, в которых участвовало около 95 000 лиц с низким риском развития
ССО. Важно, что этот мета-анализ использовал (в отличие от многих других мета-анализов) индивидуальные данные участвовавших в исследовании пациентов. Дозы АСК колебались от 50 до 500 мг/сут, длительность применения — от 3,7 до 10 лет. Мета-анализ показал, что применение АСК достоверно уменьшает риск возникновения тяжелых ССО (0,51% при применении АСК и 0,57% в отсутствие приема АСК; р<0,0001). Этот эффект обеспечивался за счет уменьшения риска возникновения нефатального ИМ; риск МИ и смертность от ССЗ при применении АСК не менялись. В то же время применение АСК повышало риск развития желудочно-кишечных кровотечений и внутричерепных кровоизлияний, хотя общая частота их развития была низкой (0,1% в год при
применении АСК 0,07% в год без применения АСК). Современные клинические рекомендации предлагают, как правило, решать вопрос о целесообразности назначения АСК лицам без признаков ССЗ на основании расчета индивидуального риска. Европейские рекомендации по профилактике ССЗ считают необходимым назначение АСК с целью первичной профилактики всем лицам, у которых риск развития коронарных осложнений превышает 1,5% в год или 10-летний риск развития смертельных ССО, оцененный по шкале SCORE, превышает 10% при условии стабилизации АД [12].
Эффективность АСК при лечении и профилактике ССЗ установлена для широкого диапазона доз —
от 30—50 до 1500 мг/сут. [13], однако согласно современным клиническим рекомендациям с целью повышения безопасности лечения в последние годы АСК назначают в малых дозах. Минимальной эффективной при большинстве ССЗ считается доза АСК 75 мг/сут. Установлено, что увеличение дозы АСК не приводит к повышению эффективности лечения [13]. Объединенный анализ результатов 65 исследований, включивших 59 395 пациентов из группы высокого риска развития сосудистых осложнений, показал, что назначение низких доз АСК (75—150 мг/сут) для длительной терапии
не менее эффективно, чем средних (160—325 мг/сут) или высоких (500—1500 мг/сут) [10]. В рекомендациях Европейского общества по атеросклерозу от 2007 г. достаточной для длительного применения у пациентов из группы высокого риска при проведении первичной профилактики признана доза АСК 75—100 мг/сут [12]. В рекомендациях Всероссийского научного общества кардиологов от 2010 г. по Кардиоваскулярной профилактике оптимальной для длительного применения у пациентов со стабильной формой ИБС и стенокардией (с целью вторичной профилактики) признана доза АСК 75—150 мг/сут [14]. При неотложных клинических состояниях, таких как острый коронарный синдром или острый ишемический мозговой инсульт, когда необходимо быстрое и полное ингибирование активации тромбоцитов, показано использование нагрузочной дозы АСК 160—325 мг. Однако подчеркивается, что в каждой клинической ситуации для минимизации
возможных побочных действий препарата желательно использовать наименьшую дозу АСК, эффективность которой доказана [13], поскольку при использовании малых доз АСК в меньшей степени ингибируется образование простациклина и простагландина Е2 слизистой оболочки желудка, что приводит к ослаблению его местного ульцерогенного эффекта.
Необходимость длительной антитромботической терапии требует жесткого контроля ее безопасности, так как прекращение приема антитромбоцитарных препаратов приводит к увеличению риска развития сосудистых осложнений, таких как ИМ [15] и МИ [16]. Так, при прекращении приема АСК риск развития повторного МИ в течение месяца повышается в 3 раза [16].
Наибольшую опасность представляют церебральные (геморрагический МИ или внутричерепные кровоизлияния) и желудочно-кишечные кровотечения, однако данные осложнения достаточно редки. По результатам мета-анализа, проведенного Antithrombotic Trialists© Collaboration в 2002 г., применение антиагрегантов сопровождалось увеличением числа тяжелых кровотечений в 1,6 раза [10]. При этом геморрагических МИ было больше на 22%, однако их абсолютное количество в каждом исследовании не превышало 1 на 1000 пациентов в год. Важно отметить, что прием антитромбоцитарных препаратов привел к снижению риска развития ишемического МИ на 30%, а общего количества МИ на 22%.
Кровотечения, как правило, возникают у больных, в анамнезе которых регистрировались язвенные кровотечения или другие осложнения язвы желудка. Кроме того, факторами риска кровотечения являются пожилой возраст, применение антикоагулянтов, глюкокортикостероидов, нестероидных противовоспалительных препаратов, а также инфицирование Helicobacter pylori.
Применение кишечнорастворимых или буферных лекарственных форм АСК теоретически может быть
более безопасным [17, 18]. Таблетки АСК, выпускаемые в кишечнорастворимой форме, покрыты оболочкой, в состав которой входят компоненты (целлюлоза, силикон и др.), позволяющие препарату растворяться в щелочной среде двенадцатиперстной кишки, минуя желудок. Это устраняет местное повреждающее действие АСК на слизистую оболочку желудка и улучшает переносимость лечения больными [19]. Безопасность и переносимость кишечнорастворимой формы АСК изучались в многоцентровом проспективном исследовании с участием 577 врачей из Германии [20, 21]. В исследование были включены 1156 пациентов, получавших кишечнорастворимую форму АСК, и 1570 пациентов, принимавших обычную таблетку АСК и переведенные в дальнейшем на прием кишечнорастворимой формы АСК. Пациенты наблюдались в течение 2 лет. В исследовании фиксировались не только «большие» (кровотечения из желудочно-кишечного тракта — ЖКТ), но и «малые» (изжога, диспепсии) нежелательные явления, характеризующие переносимость препарата. Результаты исследования свидетельствовали о снижении частоты развития нежелательных явлений после замены обычной таблетки АСК на кишечнорастворимую форму: доля больных, предъявляющих жалобы на изжогу, достоверно уменьшилась с 37,5 до 19,1% после 3 мес приема кишечнорастворимой
формы АСК и до 10,5% после 2 лет терапии. При этом, если в начале исследования у 3,3% пациентов имелась изжога тяжелой формы и у 13,7% — среднетяжелой, то к концу исследования таковые ее формы отсутствовали. При приеме кишечнорастворимой формы АСК достоверно сократилась распространенность чувства переполнения/наличия болей в желудке с 42 и 42,1% до 23,5 и 18,7%
через 3 мес терапии и до 17,9 и 18,7% после 2 лет лечения. Таким образом, выявлено, что при длительном (двухлетнем) применении АСК переносимость у кишечнорастворимой формы АСК была лучше, чем обычной.
Стоимость кишечнорастворимых форм АСК существенно превосходит обычную. В силу необходимости
длительного приема с целью профилактики ССО стоимость лечения препаратами АСК, как и безопасность, приобретают существенное значение. Облегчить финансовое бремя пациентов может более широкое использование менее дорогих дженерических лекарственных препаратов. С учетом экономической целесообразности в последние 20—25 лет Всемирная организация здравоохранения настоятельно рекомендует странам с ограниченными ресурсами ориентировать свое лекарственное
снабжение преимущественно на закупки дженериков [22]. Количество дженериков для некоторых препаратов исчисляется десятками (например, для эналаприла их более 70) и обычно прямо пропорционально длительности и успешности использования препарата. Доля дженерических препаратов на российском фармацевтическом рынке (по различным данным) составляет от 78 до 95% [23].
Главным преимуществом дженерика перед оригинальным препаратом является более низкая стоимость, а потенциальным недостатком — неполное соответствие по клиническим свойствам. Производители дженериков по своему техническому уровню очень неоднородны, соответственно и эффективность, безопасность и фармацевтические свойства (например, стабильность) дженериков, колеблется в значительных пределах. Только при точном соблюдении технологии производства и подтверждении его качества в исследованиях биоэквивалентности и грамотно спланированных клинических исследованиях можно быть уверенным в том, что препаратдженерик обеспечивает тот же терапевтический эффект, что и оригинальный препарат и является безопасным и эффективным [24, 25]. В российской практике редко проводятся клинические сравнительные исследования
по оценке эффективности и безопасности оригинального и дженерического препаратов. Эквивалентность дженерика оригинальному препарату доказывают с помощью исследований по фармакокинетической эквивалентности (биоэквивалентности). Немногочисленные клинические исследования демонстрируют весьма неоднозначную картину соответствия дженерика оригинальному препарату. Если в ряде случаев наблюдалось полное или почти полное соответствие эффективности оригинального препарата и дженерика [26—27], то в других случаях такого соответствия выявить не удалось [28—31].
Оригинальный препарат АСК в кишечнорастворимой оболочке аспирин кардио давно известен и пользуется заслуженной популярностью. Недавно на российском рынке появился новый дженерический препарат АСК тромбопол, выпускаемый фармацевтическим заводом Польфарма АО (Польша).
Изучение клинической эквивалентности этих препаратов представляет значительный практический интерес, поскольку позволяет оценить их сравнительную клиническую эффективность, а также безопасность терапии аспирином кардио и тромбополом.
Цель исследования — сравнительное изучение дезагрегантной способности препаратов АСК — таблеток тромбопол 75 мг производства фармацевтического завода Польфарма АО (Польша) и таблеток аспирин кардио 100 мг (оба препарата выпускаются в кишечнорастворимой оболочке) у больных с высоким риском развития ССО.
Материал и методы
Дизайн исследования. Двойное слепое рандомизированное перекрестное исследование выполнено у больных с мягкой и умеренной артериальной гипертонией (АГ), у которых имелись показания к применению препаратов АСК. Схема проведения исследования представлена на рис. 1.
Рисунок 1. Схема проведения исследования.
Отбор пациентов. В исследование были включены 14 мужчин и 16 женщин, основные антропометрические и демографические данные которых представлены в табл. 1, а распространенность факторов риска — в табл. 2. Все пациенты на момент включения получали
плановую терапию по поводу имеющихся ССЗ: антигипертензивную терапию — 27 (90%) больных, гиполипидемическую (статины) —13 (43%), АСК — 2 (7%), сахароснижающую — 9 (30%). В качестве гипотензивной и/или антиангинальной терапии 16 (53%) больных получали β-адреноблокаторы. В качестве антигипертензивной терапии 4 (13,3%) больным назначали антагонисты кальция, 21 (70%) — ингибиторы ангиотензинпревращающего фермента, 15 (50%) —диуретики в виде монотерапии или в комбинации. В среднем пациенты принимали 3 препарата для лечения ССЗ.
Таблица 1. Клиническая характеристика больных (n=30).
Таблица 2. Факторы риска развития ССЗ (n=30).
У 15 (50%) пациентов имелась ИБС, из них 10 (33%) перенесли в прошлом ИМ, у 27 (90%) имелась АГ
1—2-й степени, у 12 (40%) — сахарный диабет (СД) 2-го типа, у 2 — пароксизмальная форма мерцательной аритмии (МА), у одного пациента в анамнезе был МИ. Цереброваскулярной болезнью страдали 14 (47%) больных. Все пациенты с ИБС были в стабильном состоянии, из них 2 (6%) эпизодически принимали сублингвально нитроглицерин для купирования приступов стенокардии.
Критериями включения в исследование больных были: возраст 18 лет и старше; высокий риск развития ССО (риск по шкале SCORE ≥ 5%) и наличие показаний к применению препаратов АСК или очень высокий риск в связи с наличием установленных ССЗ или ассоциированных клинических состояний (ИБС, СД, МА, перенесенный МИ, церебральный и периферический атеросклероз и др.); наличие письменного согласия пациента на включение в исследование; для женщин — отрицательный тест на беременность и согласие придерживаться адекватных методов контрацепции.
Критериями исключения из исследования больных были: тяжелая АГ (систолическое артериальное давление — САД ≥180 мм рт.ст. и/или диастолическое артериальное давление — ДАД ≥110 мм рт.ст.), не контролируемое приемом гипотензивных препаратов; наличие выраженных сопутствующих заболеваний; эрозивно-язвенные поражения ЖКТ в анамнезе; нарушение функций почек и печени;
аспириновая бронхиальная астма; геморрагический синдром, авитаминоз К; отягощенный аллергологический анамнез, непереносимость лекарственных препаратов; злоупотребление алкоголем, лекарственными препаратами, наркомания; любые другие медицинские или хирургические состояния, которые, по мнению исследователя, противоречат критериям включения, увеличивают риск
для больного, могут стать причиной досрочного прекращения его участия в исследовании или затруднят трактовку результатов последнего; беременность и период лактации.
Последовательность назначения курсов тестируемого и референсного препарата для каждого больного определяли путем рандомизации методом случайных чисел. Выдаваемый исследуемый препарат был «заслеплен» для пациентов.
Оценка показателей эффективности. Агрегационную способность тромбоцитов определяли по изменению светопропускающей способности образца крови при образовании агрегатов после 2-минутной экспозиции с индуктором агрегации. В качестве индуктора агрегации использовали раствор АДФ в 3 концентрациях (0,5, 1 и 2 мкМ). АТ определяли турбидометрическим методом Born/O,Brien (Born G., 1962) на автоматическом двухканальном лазерном компьютеризированном агрегометре модели 220LA производства, с применением программы «AGGR, версия 2.01)». Принцип регистрации АТ данным методом заключается в том, что при образовании агрегатов происходит
изменение светопропускания образца. Если до добавления индуктора суспензия тромбоцитов более мутная, чем среда без тромбоцитов, то при агрегации наблюдается типичная картина увеличения светопропускания. Кривая изменения интенсивности прошедшего через образец света записывается регистратором и по ней делают выводы о «степени» АТ. Уровень светопропускания богатой
тромбоцитами плазмы принимают за 0, а обедненной тромбоцитами плазмы — за 100%. Регистрация изменений среднего радиуса агрегатов основывается на анализе флуктуаций светопропускания, вызванных хаотическим изменением количества тромбоцитов и их агрегатов в оптическом канале устройства.
Оценку достаточности антиагрегантного эффекта АСК проводили по следующим показателям АТ: снижению АДФ-индуцированной (0,5, 1 и 2 мкг/мл) агрегации тромбоцитов; стабильному отсутствию второй фазы (волны) агрегации с малой дозой АДФ 0,5 мкг/мл; возможным признакам дезагрегации. Отсутствие этих признаков свидетельствует о неэффективном действии АСК.
Таблица 3. Расписание процедур исследования.
Протокол проведения исследования. Перед включением в исследование пациенту, соответствующему критериям отбора, предоставляли полную информацию об изучаемых препаратах, целях, задачах и методах исследования, после чего он подписывал «Информированное согласие на участие в исследовании». До начала исследования все пациенты проходили предварительное обследование
(визит Т1), включающее сбор анамнеза, физикальный осмотр, измерение параметров гемодинамики — артериальное давление (АД), частоту сердечных сокращений (ЧСС), регистрацию электрокардиограммы в 12 отведениях. АД измеряли в покое на доминантной руке в положении сидя после 5 мин отдыха с помощью автоматического прибора производства MediTech . ЧСС отсчитывали
в течение 1 мин.
До начала активного лечения у больных, продолжающих прием обычной сердечно-сосудистой терапии, на 3-й неделе отменяли антиагрегантную терапию («период отмывания»). Через 3 нед пациенту выдавали один из исследуемых препаратов согласно схеме рандомизации с рекомендацией принимать 1 таблетку утром в одно и то же время. Первый прием препарата осуществлялся в клинике в присутствии врача (визит Т0). Непосредственно перед приемом отбирали пробы крови для определения
АТ; измеряли АД и ЧСС. Следующий визит (Т1) назначали через 3 нед, натощак, не принимая исследуемые препараты, спустя 24±1 ч после приема очередной таблетки. На визите Т1 проводили те же исследования, что и на визите Т0. Через 21 день после отмены первого изучаемого препаратов проводили второй аналогичный курс терапии с другим изучаемым препаратом. Визиты в клинику
(Т2 и Т3) и процедуры проводили по той же схеме. В табл. 3 представлены процедуры исследования.
Статистическая обработка данных. Применяли пакеты статистических программ Statistica 6.0 (ANOVA) с использованием как стандартных методов описательной статистики (вычисление средних, стандартных отклонений, ранговых статистик и др.), так и известных критериев значимости (t-критерий Стьюдента, Фишера, Манна—Уитни и др.) методом параметрической статистики, так как число пациентов и правильность распределения позволяли это. Достоверными считали различия при p<0,05. Данные представлены в виде M±m, где М — среднее значение, m— стандартное отклонение среднего.
Длительность исследования для каждого пациента составила 9—12 нед: два курса активного лечения каждым препаратом продолжительностью 3 нед и два 3-недельных периода отмены антиагрегантной терапии перед началом каждого курса.
Результаты
В исследование были включены 30 пациентов, полностью завершили исследование 26 пациентов, исключены из исследования 4 (все из-за нарушения протокола в виде отклонения от графика визитов).
Влияние тромбопола и аспирина кардио на АТ. Данные по влиянию сравниваемых препаратов АСК тромбопола75 мг и аспирина кардио 100 мг на АДФ-индуцированную агрегационную способность тромбоцитов представлены в табл. 4.
Таблица 4. Влияние тромбопола и аспирина кардио на АТ (n=26).
Согласно приведенным данным, 3-недельный прием обоих препаратов приводил к высокодостоверному снижению АТ, индуцированной как низкими (0,5 и 1,0 мкМ), так и высокими (2,0 мкМ) концентрациями АДФ. При этом достоверных межгрупповых различий не выявлено (рис. 2).
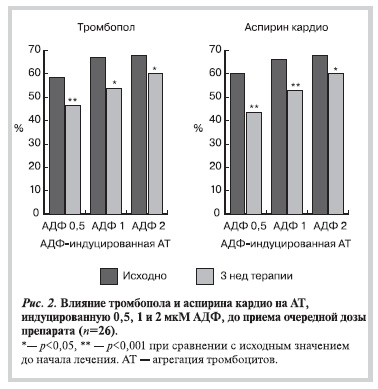
Аналогично достоверно увеличивалась частота выявления элементов дезагрегации на фоне приема обоих препаратов АСК, появлявшейся после 3 нед терапии при индукции АДФ в дозе 0,5, 1 и 2 мкМ: соответственно у 65, 34,5 и 31% больных на фоне приема тромбопола и 65,4, 42,3 и 31% — на фоне приема аспирина кардио (межгрупповые различия статистически недостоверны). Поскольку в нашем исследовании изучалась только АДФ-индуцированная АТ, то критерий Баркагана для оценки аспиринорезистентности, основанный на оценке адреналин-индуцированной агрегации, не применялся.
Трехнедельный прием обоих препаратов не оказывал достоверного влияния на параметры гемодинамики (АД и ЧСС) у больных, получающих гипотензивную терапию, что согласуется с данными литературы (табл. 5).
Таблица 5. Средние значения АД и ЧСС на фоне терапии тромбополом и аспирином кардио (n=26).
Таким образом, проведенный анализ не выявил достоверных различий в дезагрегантной активности сравниваемых препаратов АСК (оригинального и дженерического), выпускаемых в кишечнорастворимой форме несмотря на различия в дозе АСК.
Анализ побочных эффектов. Побочных эффектов, связанных с приемом исследуемого препарата, ни при приеме оригинального, ни при приеме дженерика АСК, зарегистрировано не было. За время участия в исследовании 2 пациента перенесли острое респираторное заболевание, не связаное с приемом исследуемых препаратов и не потребовавшее перерыва в приеме исследуемых препаратов и приема дополнительной терапии.
Обсуждение
Полученные нами данные сравнительного исследования в целом соответствуют данным литературы об антиагрегантной эффективности и безопасности применения препаратов АСК. Достоверное снижение индуцированной высокими дозами АДФ агрегационной способности тромбоцитов через 3 нед приема кишечнорастворимой формы АСК подтверждает заявленную для данной формы выпуска терапевтическую эффективность и свидетельствует о достижении стабильного антиагрегантного
эффекта, достаточного для подавления гиперкоагуляции, которая характерна для острых ситуаций, угрожающих развитием атеротромбоза, что соответствует данным литературы [32—37].
Отсутствие достоверных различий во влиянии исследуемых препаратов на АДФ-индуцированную АТ свидетельствует об эквивалентности антитромботического действия дженерического препарата АСК оригинальному. Однако следует учитывать, что данное исследование выполнено у небольшого числа пациентов и длительность лечения ограничивалась 3 нед для каждого препарата.
АГ часто рассматривается как противопоказание к приему АСК, так как считается, что в этом случае его назначение связано с повышенным риском церебральных кровотечений. В то же время основной
причиной смерти больных АГ являются атеротромботические осложнения — МИ и ИМ. Результаты исследования НОТ показали, что применение малых доз АСК у больных АГ в условиях подобранной гипотензивной терапии приводит к снижению риска развития ИМ без повышения риска развития геморрагического МИ [38]. При мета-анализе 142 клинических исследований, в которых изучалась эффективность вторичной профилактики у 100 000 пациентов, страдавших АГ и без нее, антитромбоцитарная терапия по сравнению с плацебо привела к достоверному снижению общей смертности, а также риска развития нефатального ИМ и МИ и суммарного риска развития основных ССО. В подгруппе больных с АГ (29 исследований; n=10 600) применение антитромбоцитарных препаратов сопровождалось еще более выраженным снижением риска развития основных ССО. Если у всех пациентов, включенных в мета-анализ, снижение абсолютного риска составило 2,4%, то у больных с повышенным АД — 4,1%. Таким образом, АГ является лишним доводом в пользу назначения АСК с целью длительной вторичной профилактики ССО. В нашем исследовании не было выявлено
влияния 3-недельного приема средних терапевтических доз АСК на уровень АД у пациентов с АГ, получающих плановую антигипертензивную терапию. В последних Европейских рекомендациях по АГ указано, что всем пациентам с АГ, имеющим повышенный риск развития ССО, следует назначать низкие дозы АСК в отсутствие противопоказаний и при адекватном контроле АД (ДАД ниже 90 мм рт.ст.) [39].
Наиболее частой причиной прекращения приема АСК в повседневной практике является развитие побочных эффектов, связанных с воздействием на ЖКТ. Следует лишь отметить, что, по данным многоцентровых контролируемых исследований, тяжелые поражения верхних отделов ЖКТ при приеме АСК встречаются относительно редко и связаны, прежде всего, с дозой препарата. Так, согласно результатам мета-анализа 31 рандомизированного плацебо-контролируемого исследования, частота тяжелых кровотечений составила у принимавших низкие (30—81 мг/сут) дозы АСК — менее 1%, средние (100—200 мг/сут) — 1,56% и высокие (283—1300 мг/сут) — более 5% [40]. Частота развития
диспепсических явлений (дискомфорт в эпигастрии, тошнота, рвота, изжога) варьирует от 5,2 до 40% [40]. В нашем исследовании случаев диспепсии не зарегистрировано, несмотря на наличие в анамнезе гастродуоденита у 30% больных.
Заключение
Дженерический препарат ацетилсалициловой кислоты тромбопол фармацевтического завода Польфарма (Польша) и препарат аспирин кардио эквивалентны по дезагрегантному действию и переносимости.



