Митральная недостаточность (МН) является вторым по частоте пороком сердца, при котором требуется хирургическое лечение [1]. В настоящее время основной причиной развития МН у жителей индустриально развитых стран является дисплазия соединительной ткани (ДСТ) [1—5]. В России в последние годы доля операций по коррекции дегенеративных пороков в структуре приобретенных пороков сердца также имеет тенденцию к росту. Так, по данным Л.А. Бокерия и Р.Г. Гудковой, доля таких операций в 2010 г. составляла 26,5%, в 2011 г. — 31,3%, а в 2012 г. — 39,6% (доля ревматических пороков — 47,2%) [6]. В клинической практике основное значение принадлежит болезни Барлоу (24%) и фиброэластическому дефициту (ФЭД) — 76% [7, 8].
Анамнез митрального порока при болезни Барлоу может варьировать от нескольких лет до десятков лет, а при ФЭД — обычно несколько месяцев.
При естественном течении заболевания острая МН имеет плохой прогноз без хирургического вмешательства. При отрыве хорд (например, при ФЭД) клиническое состояние может стабилизироваться после некоторого начального симптоматичного периода. При остром отрыве подклапанных хорд (не острый инфаркт миокарда), что характерно, например, для ФЭД, развивается выраженная митральная регургитация, приводящая к нарушениям гемодинамики — перегрузке левого предсердия, повышению давления в легочных венах и развитию 2-го типа легочной гипертензии по классификации Dana Point (2008), что клинически проявляется характерными признаками – одышкой, снижением толерантности к физической нагрузке (повышение функционального класса – ФК по классификации Нью-Йоркской ассоциации сердца – NYHA), однако, при естественном течении заболевания, согласно [9, 10], у некоторых пациентов отмечается регресс симптоматики (вероятно, за счет компенсаторных сил), таким образом, часть пациентов с яркой, характерной аускультативной картиной митральной недостаточности, выявляемой при проведении профосмотров, могут не предъявлять никаких жалоб, соответственно, такие пациенты классифицируются как бессимптомные. Тем не менее длительная перегрузка объемом приводит к дисфункции левого желудочка (ЛЖ) [9].
При бессимптомном течении 5-летняя смертность составляет 33% вследствие хронической сердечной недостаточности (ХСН) или фибрилляции предсердий (ФП) на фоне консервативной терапии [11].
За 10 лет естественного течения тяжелой митральной регургитации (МР) при ФЭД 90 пациентов умерли или нуждались в операции, смертность составила 6—7% в год [12].
В повседневной практике для определения показаний к хирургическому лечению изолированной МН используют Руководство Американской коллегии кардиологов и Американской ассоциации сердца (ACC/AHA) по ведению пациентов с приобретенными пороками сердца [9] или более позднее Руководство Европейского общества кардиологов и кардиоторакальных хирургов [10].
Согласно рекомендациям (класс I, уровень доказательности данных B), операция показана пациентам с клинически проявляющейся острой тяжелой МР; с хронической тяжелой МР и симптомами ХСН II—IV ФК по классификации NYHA, в отсутствие тяжелой дисфункции ЛЖ (фракция выброса — ФВ >30, конечный систолический размер — КСР <55 мм). Пластика митрального клапана (МК) предпочтительнее замены клапана. Пациенты должны быть направлены в хирургические центры с большим опытом реконструктивных операций на МК (класс I, уровень C). Согласно рекомендациям ACC/AHA [9], выполнимость такой пластики у пациентов при ДСТ в отсутствие симптомов должна быть не менее 90%, а при ФЭД стремится к 100% случаев ввиду общепризнанных преимуществ клапансохраняющих операций перед заменой клапана. Особенно актуальным становится выбор хирургической клиники и конкретного хирурга, в частности, для пациента без клинических проявлений, которому планируется реконструкция МК и которого сложно убедить в необходимости операции. Чаще всего это лица, ведущие активный образ жизни, не желающие пожизненно принимать под регулярным контролем антикоагулянты, а также женщины, планирующие беременность. Немаловажным аспектом является и отсутствие всех возможных протез-зависимых осложнений, связанных с имплантацией искусственных клапанов сердца.
Выбор метода ведения пациентов в отсутствие симптомов до сих пор остается не решенным, рандомизированных исследований, сравнивающих консервативное ведение и хирургическое лечение, не проводилось. Операция у пациентов с выраженной бессимптомной МР оправдана при высокой вероятности выполнимости клапансохраняющей операции [13, 14].
При операциях на МК наиболее значимыми предикторами исхода операции являются возраст пациента, наличие ФП, исходная сократительная функция ЛЖ, легочная гипертензия (ЛГ) и выполнимость пластики МК [15]. Другие исследования показали зависимость исходов от уровня и динамики уровня мозгового натрийуретического пептида (BNP). Уровень BNP ≥105 пг/мл позволяет выявить среди пациентов без клинических симптомов группу высокого риска прогрессирования ХСН, дисфункции ЛЖ и смерти в среднеотдаленные сроки наблюдения [16] и своевременно принять решение в пользу хирургической коррекции.
Таким образом, согласно рекомендациям [10], хирургическое лечение у пациентов в отсутствие симптомов показано:
- I C — при дисфункции ЛЖ (КСР ЛЖ ≥45 мм, ФВ ЛЖ ≤60);
- IIa C — у пациентов с сохранной функцией ЛЖ и впервые возникшей ФП или ЛГ (систолическое давление в легочной артерии — ЛА в покое >50 мм рт.ст.);
- IIa C — с сохранной функцией ЛЖ, высокой вероятностью выполнимости и долговечности пластики клапана, низким хирургическим риском, флотирующей створкой и КСР ЛЖ ≥40 мм;
- IIb C — с сохранной функцией ЛЖ, высокой вероятностью выполнимости и долговечности пластики клапана, низким хирургическим риском и:
- а) увеличением левого предсердия (ЛП) — индекс объема ЛП к площади поверхности тела >60 мл/м2 при наличии синусового ритма или
- б) ЛГ при нагрузке (систолическое давление в ЛА >60 мм рт.ст.).
При изучении зарубежных рекомендаций часто возникает вопрос применимости последних для отдельно взятой страны (России) или клиники в частности.
Цель исследования: изучить непосредственные результаты хирургического лечения изолированной МН дегенеративного генеза в зависимости от функционального состояния больных согласно классификации ХСН по NYHA.
Материал и методы
В рамках выполняемых научных работ мы провели одноцентровое проспективное сравнительное исследование непосредственных клинических исходов хирургического лечения пациентов с выраженной МН при ДСТ в зависимости от функционального состояния согласно классификации ХСН по NYHA.
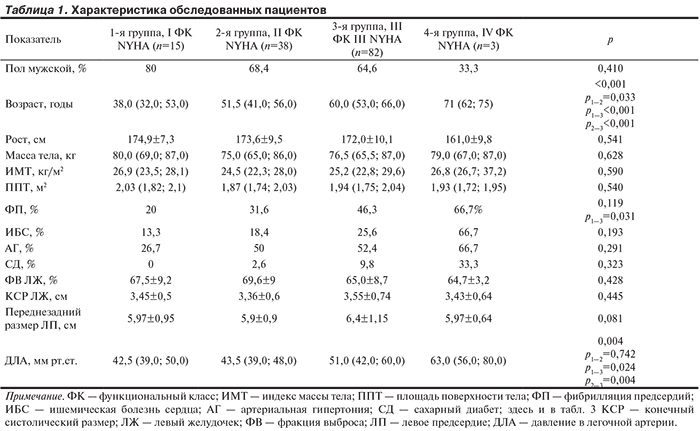
Всего в исследование включены 138 последовательно оперированных пациентов старше 18 лет с изолированной МН (ФЭД или болезнь Барлоу) в период с 01.09.11 по 31.12.13. Средний возраст включенных больных составил 54,7±12,6 года. Среди пациентов было 92 (66,7%) мужчины и 46 (33,3%) женщин. Все больные были распределены на 4 группы в зависимости от ФК ХСН по классификации NYHA: 1-я группа — 15 больных с I ФК, 2-я группа — 38 больных с II ФК, 3-я группа — 82 больных с III ФК, 4-я группа — 3 больных с IV ФК (табл. 1).
Выполнимость пластики в 4 группах составила 93,5%. Период наблюдения составил 6—60 дней, средняя продолжительность исследования 18 (15; 24) дней.
Критериями исключения стали сопутствующие органические поражения аортального, трикуспидального клапанов (пациенты с относительной, т.е. функциональной трикуспидальной недостаточностью не исключались из исследования), патология аорты и ее ветвей, ишемическая болезнь сердца (ИБС), требующие хирургического лечения; инфаркт миокарда (ИМ), острое нарушение мозгового кровообращения (ОНМК) в анамнезе, любые предшествующие операции на сердце и магистральных сосудах.
Исследование одобрено локальным Этическим комитетом. Перед включением в исследование все пациенты подписывали специально разработанную форму информированного согласия на участие в исследовании.
Всем пациентам до операции выполняли стандартное обследование: общеклинический и биохимический анализы крови, коагулограмма, электрокардиограмма, ультразвуковое исследование (УЗИ) брахиоцефальных артерий, УЗИ артерий нижних конечностей, трансторакальная эхокардиография (ЭхоКГ), селективная коронарография (пациенты старше 45 лет), чреспищеводная ЭхоКГ (ЧП-ЭхоКГ) в операционной перед началом операции и после завершения основного этапа для оценки выполненного вмешательства.
В табл. 1 отражены основные антропометрические параметры, наиболее часто встречавшиеся сопутствующие заболевания и ранее указанные эхокардиографические предикторы исхода хирургического лечения, такие как ФВ ЛЖ, КСР ЛЖ, размеры ЛП, систолическое давление в ЛА. Сравнение по исходным параметрам с 4-й группой не проводилось ввиду малого числа пациентов в данной группе. В дальнейшем 4-я группа представлена методами описательной статистики без расчета уровня значимости при сравнении с другими группами.
Как представлено в табл. 1, сравниваемые группы не отличались по полу, частоте развития ИБС, артериальной гипертонии и сахарного диабета. В группе пациентов с ХСН III ФК статистически значимо чаще, чем у пациентов 1-й группы без клинических симптомов, встречались нарушения ритма сердца по типу ФП (р=0,031).
Сравниваемые группы статистически значимо отличались по таким факторам риска, как возраст пациентов и систолическое давление в ЛА, что вероятно, объясняется тяжестью и длительностью основного заболевания до момента операции. У пациентов всех 4 групп по данным ЭхоКГ имелось увеличенное ЛП >55 мм и отсутствовали признаки дисфункции миокарда ЛЖ (КСР ЛЖ ≥45 мм, ФВ ЛЖ ≤60). По всем количественным признакам (за исключением возраста и уровня давления в ЛА) сравниваемые группы статистически значимо не различались.
Таким образом, пациенты без клинических признаков заболевания были достоверно более молодого возраста, реже страдали ФП, были с более низким систолическим давлением в ЛА и не имели нарушений сократительной способности миокарда ЛЖ; из факторов риска в данной когорте представлена только атриомегалия. С повышением ФК пациентов статистически значимо увеличиваются количество и выраженность предикторов неблагоприятного исхода операции.
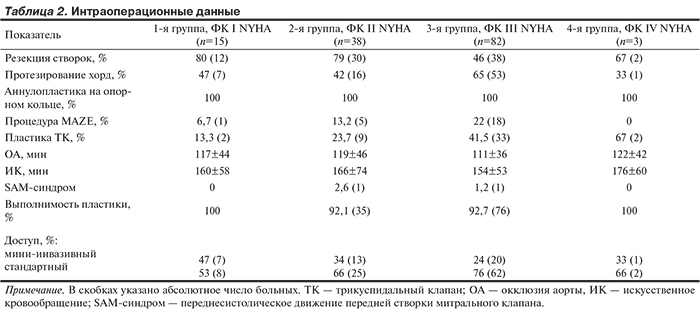
Виды хирургических вмешательств. В зависимости от анатомических особенностей поражения отдельных сегментов передней или задней створок выполняли резекционные методики, протезирование хорд отдельными нитями или группой петель или сочетание методов. Сводные данные представлены в табл. 2. Обзор существующих методов хирургической коррекции МН при болезни Барлоу как наиболее сложной и трудоемкой операции (по сравнению с ФЭД) был представлен ранее [17]. Во всех случаях для ремоделирования и создания стабильности нативного фиброзного кольца пластика МК дополнялась имплантацией опорного кольца. В настоящее время в практике наиболее часто мы используем замкнутые кольца D-ring, полукольца C-ring/Flex, реже — частично разомкнутые полужесткие опорные кольца Standard. Следует отметить, что идеального по всем характеристикам опорного устройства в мире нет. Основные споры в настоящее время развернуты о применении первых двух типов колец [18].
Модифицированную процедуру MAZE или лабиринт выполняли у пациентов с пароксизмальной, персистирующей и длительно персистирующей формами ФП [19—22]. У большинства пациентов для этой цели применяли биполярную радиочастотную абляцию ЛП [21—25] с использованием коммерческой системы [26]. Результаты хирургического лечения ФП при пороках МК представлены ранее [20—22, 27].
Пластику трикуспидального клапана во всех случаях выполняли путем имплантации опорного кольца Standard.
SAM-синдром (переднесистолическое движение передней створки митрального клапана) развился у 2 пациентов. В одном случае удалось выполнить коррекцию возникшей МН [28], в другом случае у пациента из 3-й группы выполнено протезирование клапана механическим протезом. При выявлении умеренной или выраженной МН по данным контрольной ЧП-ЭхоКГ пациентам выполняли на повторной окклюзии аорты протезирование МК двустворчатыми механическими протезами «МедИнж-2» с сохранением подклапанных структур с целью профилактики разрывов ЛЖ [29] согласно рекомендациям [10].
Длительность искусственного кровообращения и окклюзии аорты в сравниваемых группах статистически значимо не различалась (p=0,897 и р=0,922 соответственно). Из боковой мини-торакотомии или с использованием роботизированного комплекса da Vinci прооперированы 47 и 34% пациентов 1-й и 2-й групп соответственно.
Статистическую обработку данных проводили с помощью пакета программ Statistica v6.1 для Windows. Для проверки статистических гипотез о виде распределения был применен критерий Шапиро—Уилка. При выполнении основной задачи сравнения 3 независимых групп и более по одному количественному или порядковому признаку были использованы методы непараметрической статистики (ранговый анализ вариаций Крускала—Уоллиса). При выявлении статистически значимых различий в группах проводили парное сравнение групп с использованием непараметрического теста Манна—Уитни с поправкой Бонферрони для преодоления проблем множественных сравнений. Для оценки результатов лечения по количественному или качественному порядковому признаку до и после операции применены методы непараметрической статистики (критерий Вилкоксона). Выборочные параметры представлены в таблицах как среднее ± стандартное отклонение. При распределении, отличном от нормального, данные представляли в виде медианы и интерквартильного размаха. Различия считали статистически значимыми при p<0,05.
Результаты и обсуждение
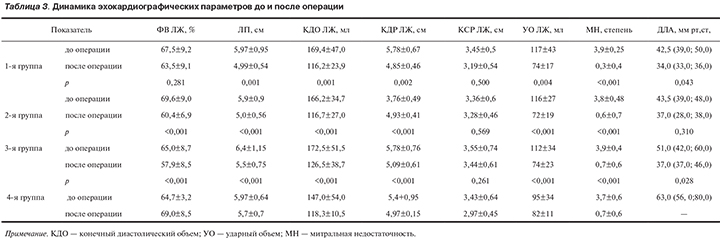
В табл. 3 представлено сравнение до- и послеоперационных основных ЭхоКГ-параметров. Исходя из полученных данных, можно сделать вывод об эффективности клапансохраняющих операций: у всех пациентов к моменту выписки установлено благоприятное влияние на процессы ремоделирования левых отделов сердца, а именно статистически значимое уменьшение размеров ЛП, конечного диастолического объема, конечного диастолического размера, ударного объема ЛЖ, степени МН, а также систолического давления в ЛА у пациентов 1-й и 3-й групп. У пациентов 2-й группы также отмечено снижение давления в ЛА с 43,5 до 37,0 мм рт.ст., отсутствие статистически значимых различий объясняется числом пропущенных данных (доступно 7 из 38). Снижение ФВ в послеоперационном периоде объясняется устранением патологической гемодинамики порока (МР). Также отмечено некоторое статистически незначимое уменьшение КСР ЛЖ.
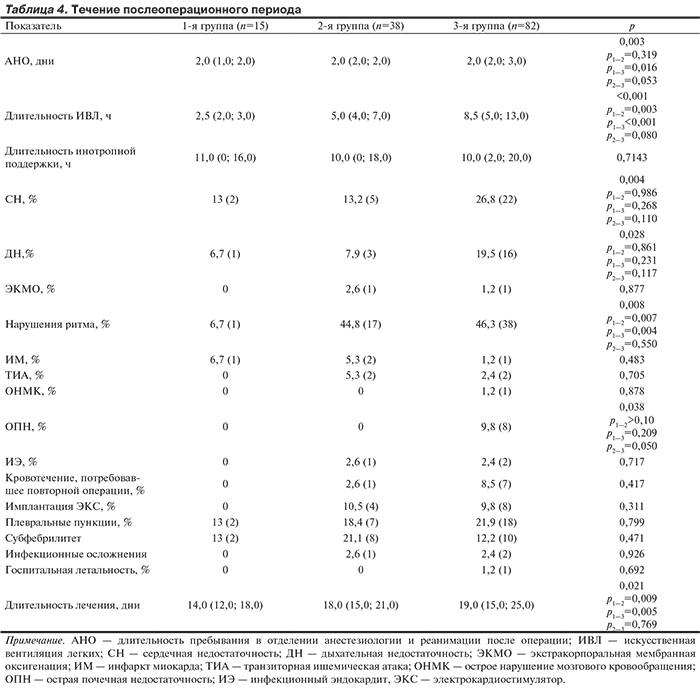
При сравнении групп по временны'м параметрам (длительность пребывания в отделении анестезиологии и реанимации после операции; продолжительность искусственной вентиляции легких — ИВЛ, длительность лечения в стационаре) выявлены статистически значимые различия (табл. 4). Пациенты без клинических симптомов пребывали в палате реанимации статистически значимо меньше, чем пациенты 3-й группы, имели меньше длительность ИВЛ и продолжительность пребывания в стационаре по сравнению с пациентами 2-й и 3-й групп. По необходимости в инотропной поддержке группы не различались. Данные показатели так или иначе отражают затраты на лечение пациентов каждой конкретной группы.
Течение послеоперационного периода при оценке по таким показателям, как необходимость в подключении экстракорпоральной мембранной оксигенации, развитие острого ИМ, транзиторной ишемической атаки, ОНМК, инфекционного эндокардита, кровотечения, потребовавшего хирургического вмешательства, при имплантации постоянного водителя ритма, гидротораксе, потребовавшем выполнения плевральной пункции, при длительной лихорадке, инфекционных осложнениях хирургического доступа, летальность у больных сравниваемых групп статистически значимо не различалась. Однако следует отметить, что в группе пациентов без клинических симптомов реже требовались такие вмешательства, как хирургический гемостаз (0 против 8,5% в 3-й группе), плевральные пункции (13% против 18,4 и 21,9% во 2-й и 3-й группах соответственно), имплантации электрокардиостимулятора (0 против 10,5 и 9,8% во 2-й и 3-й группах соответственно), реже наблюдался субфебрилитет (13% против 21,1% во 2-й группе). У пациентов без клинических симптомов имелось статистически значимо меньше эпизодов преходящих нарушений ритма сердца (атриовентрикулярная блокада, синдром слабости синусного узла, ФП, трепетание предсердий) в послеоперационном периоде — 6,7% против 44,8 и 46,3% соответственно. По ряду показателей пациенты без клинических симптомов не имели осложнений в отличие от сравниваемых групп (табл. 4).
Заключение
С ростом ФК ХСН по классификации NYHA увеличиваются количество известных предикторов неблагоприятного исхода операции, частота развития послеоперационных осложнений, длительность и тяжесть послеоперационного периода, и, соответственно, стоимость лечения. Пациенты молодого и среднего возраста с выраженной бессимптомной митральной недостаточностью дегенеративного генеза в настоящее время могут быть прооперированы с высокой вероятностью реконструкции клапана (до 100), с низкой частотой возможных осложнений послеоперационного периода (до 0), меньшими сроками пребывания в стационаре (2 нед) и по своим исходным характеристикам являются кандидатами для менее травматичных операций из боковой мини-торакотомии. Пациенты со II—IV ФК также могут быть оперированы с высокой вероятностью сохранения митрального клапана (>90), послеоперационный период у таких пациентов протекает более «драматично», но с достаточно низким риском развития тяжелых осложнений. Эффект от хирургического лечения подтверждается уже к моменту выписки пациентов — субъективно в виде регресса клинических проявлений, объективно — в процессах обратного ремоделирования левых отделов сердца и отсутствии значимой митральной недостаточности (≥2/4) по данным эхокардиографии.
Все пациенты с клиническими симптомами были оперированы согласно европейским рекомендациям по показаниям IB, пациенты без симптомов — по IIbC. Уровень С — мнение экспертов и/или результаты небольших ретроспективных исследований, IIb — польза/эффективность менее доказана (чем IIa) и погранична с классом III, где «вред» от вмешательства превышает возможную «пользу» [11]. Исходя из проведенного исследования нам представляется оправданным более широкое распространение хирургических методов лечения, чем стратегия наблюдения за пациентами. Для укрепления позиций активного хирургического лечения возможно использование непопулярных в настоящее время методов — определение содержания мозгового натрийуретического пептида в крови и волюмометрия левого предсердия по данным ЭхоКГ как более объективного показателя атриомегалии. В настоящее время нет ни одного рандомизированного исследования, сравнивающего инвазивный (хирургический) и консервативный методы лечения; отбор пациентов осуществляется еще на догоспитальном этапе, а в хирургическую клинику пациенты поступают целенаправленно на хирургическое лечение. Совместное кардиологическое и хирургическое, амбулаторное и стационарное крупное рандомизированное и, желательно, многоцентровое исследование с оценкой непосредственных и отдаленных результатов может изменить в будущем уровень рекомендаций и класс доказательств для пациентов без клинических симптомов.



