Несмотря на очевидные успехи катетерных технологий в лечении фибрилляции предсердий (ФП), эксперты по-прежнему рекомендуют изоляцию легочных вен лишь в случае неэффективности предшествующей антиаритмической терапии [1].
Антиаритмические препараты (ААП) традиционно принято разделять на 4 класса в зависимости от механизма действия: блокада натриевых (I класс) и кальциевых (IV класс) токов, удлинение реполяризации (преимущественно за счет блокады калиевых токов) — III класс и подавление симпатических влияний (II класс) на сердце. β-Адреноблокаторы и антагонисты кальция традиционно используются для нормализации частоты сокращения желудочков преимущественно при хронической ФП. Собственно с антиаритмической целью при ФП используют препараты I и III классов. Однако их недостаточная эффективность, а также риск развития кардиальных (прежде всего аритмогенных) и внекардиальных побочных эффектов побудил ведущие фармацевтические компании к поиску новых ААП.
Более 2 десятилетий назад было сформулировано представление об «идеальном» антиаритмическом средстве для лечения ФП. Это должен быть препарат III класса, обладающий следующими свойствами: 1) умеренное подавление синусовой тахикардии до нормальных значений; 2) поддержание частоты сокращения желудочков при рецидиве ФП; 3) удлинение потенциала действия (ПД) и рефрактерности преимущественно в предсердиях с минимальным риском удлинения QT и развития torsade de pointes (TdP); 4) подавление ранних постдеполяризаций в М-клетках и волокнах Пуркинье; 5) снижение собственной и лекарственной гетерогенности рефрактерных периодов миокарда; 6) отсутствие аритмогенности; 7) эффективность и безопасность в отношении как предсерд ных, так и желудочковых аритмий; 8) благоприятное или нейтральное влияние на выживаемость; 9) сохранение эффективности без развития побочных эффектов при длительном применении [2].
Результатом прогресса в последние десятилетия в фармацевтической индустрии стала большая группа препаратов III класса, разделяемая на подгруппы: 1. Производные амиодарона; 2. Неселективные блокаторы калиевых каналов (так называемые новые препараты III класса); 3. «Предсердно-селективные» калиевые блокаторы («новейшие» препараты III класса). Данная классификация весьма условна, поскольку для большинства современных препаратов III класса мишенью является более одного ионного тока (мультиканальные блокаторы). Их по-прежнему объединяет основной признак — удлинение ПД за счет замедления фаз реполяризации и увеличения рефрактерных периодов как основного механизма анти аритмического действия.
В настоящем обзоре дана характеристика препаратам III класса, применяемым или находящимся на различных стадиях экспериментальных и клинических исследований, в том числе двум отечественным препаратам этого класса — нибентану и ниферидилу.
Производные амиодарона
Амиодарон и соталол синтезированы как антиангинальные средства в 1962 г., но их уникальные электрофизиологические свойства были открыты только к 1970 г., а как ААП они стали применяться десятилетие спустя [3].
Уникальные свойства этих первых препаратов III класса — удлинение ПД и рефрактерности как в предсердиях, так и в желудочках — легли в основу концепции одновременного контроля предсердных и желудочковых аритмий. По прошествии 40 лет амиодарон и соталол являются самыми часто назначаемыми препаратами III класса, особенно при ФП.
Однако хорошо известная способность амиодарона накапливаться в тканях при длительном применении с проявлением хронической органной токсичности (чаще всего, индуцированный амиодароном гипотиреоз) нередко ограничивают возможности препарата. В настоящее время имеется несколько производных амиодарона, близких по химической структуре и электрофизиологическим свойствам.
Дронедарон
Дронедарон, как и амиодарон, является производным бензофуранила, в котором удалены 2 атома йода, что устранило тиреотропность. Сульфонамидный радикал, добавленный к исходному веществу, устранил свойство амиодарона накапливаться в тканях, что ускорило кинетику препарата и, как предполагалось, позволило бы избежать побочных эффектов, присущих амиодарону.
Дронедарон, как и амиодарон, демонстрирует электрофизиологические эффекты мультиканального блокатора [4, 5]. Дронедарон подавляет быстрый Ikr и медленный Iks компоненты выходящего калиевого тока IK+ задержанного выпрямления, L-тип кальциевого тока, входящий натриевый INa+ ток и входящий калиевый Ik1 ток аномального выпрямления (рис. 1).
Кроме того, он блокирует активируемый ацетилхолином калиевый ток IKAch, ток пейсмейкерных клеток (If) и проявляет свойства неконкурентного α- и β-адренергического антагониста. Препарат вызывает умеренную брадикардию, замедляет предсердно-желудочковое проведение и увеличивает рефрактерные периоды предсердий и желудочков. В ряде экспериментальных исследований под влиянием дронедарона отмечено повышение порога фибрилляции желудочков. Дронедарон изучался в нескольких многоцентровых клинических исследованиях [6—10].
В исследованиях EURIDIS и ADONIS оценивалась эффективность дронедарона в дозе 400 мг в предотвращении рецидива ФП. В группе дронедарона рецидив ФП возникал в среднем на 96-е сутки против 41-х суток в группе плацебо (EURIDIS), и на 158-е сутки против 59-х суток соответственно в исследовании ADONIS. Препарат достоверно был эффективнее у пациентов с органическим поражением сердца, при артериальной гипертензии, сердечной недостаточности. Дронедaрон не удлинял интервал QT, что, вероятно, объясняет низкий риск проаритмических эффектов. Кроме того, в обоих исследованиях в группе дронедaрона в случае рецидива ФП регистрировалась достоверно более низкая частота сокращений желудочков (на 12—15 в минуту по сравнению с группой плацебо).
В следующем исследовании ERATO в группе больных с постоянной ФП (принимающих также β-адреноблокаторы или дигоксин) и частотой сердечных сокращений (ЧСС) в покое более 80 уд/мин дронедарон также подтвердил способность снижать частоту сокращений желудочков на 12 в минуту по сравнению с плацебо.
Следующим в серии стало клиническое исследование ANDROMEDA, в котором планировалось изучить влияние дронедарона на общую смертность и частоту госпитализаций среди больных группы высокого риска — с прогрессирующей сердечной недостаточностью III и IV функционального класса по классификации NYHA. Исследование было прекращено досрочно, так как смерт ность в группе дронедарона составила 8% против 3,8% в группе плацебо (р=0,027). При ретроспективном анализе оказалось, что дронедарон подавлял канальцевую абсорбцию креатинина, приводя к увеличению его содержания в плазме. Это, в свою очередь, заставляло врачей отменять ингибиторы ангиотензинпревращающего фермента или блокаторы ангиотензиновых рецепторов, что могло приводить к прогрессированию сердечной недостаточности и смерти больных.
Целью исследования III фазы ATHENA была оценка эффективности дронедарона в дозе 400 мг по предотвращению госпитализаций и влиянию на общую смертность у больных с пароксизмальной или персистирующей ФП и трепетанием предсердий (ТП). По сравнению с предыдущим исследованием контингент больных в ATHENA не был столь тяжелым. Помимо ФП у пациентов имелся один из следующих факторов риска: артериальная гипертензия, возраст старше 70 лет, сахарный диабет, перенесенный ранее инсульт или тромбоэмболия, фракция выброса левого желудочка менее 40%.
Дронедарон в этом исследовании достоверно превосходил плацебо по влиянию на конечные точки. Под действием препарата на 24% снизился риск смерти и госпитализаций в связи с осложнениями сердечно-сосудистых заболеваний. После опубликования результатов ATHENA дронедарон под торговым наименованием Multaq был одобрен Администрацией США по контролю за качеством пищевых продуктов и лекарственных препаратов (FDA) и Европейским медицинским агентством.
Последним в серии стало клиническое исследование PALLAS [11]. В ходе исследования планировалось подтвердить гипотезу о том, что положительное действие дронедарона на общую и сердечно-сосудистую смертность связано не только с собственно антиаритмическим эффектом (восстановление и удержание синусового ритма), но и с дополнительными влияниями препарата — снижением ЧСС, антифибрилляторным и гипотензивным эффектами. У пациентов в исследовании PALLAS имелись практически те же факторы риска, что и в исследовании ATHENA, но при этом у всех была постоянная (перманентная) форма ФП. В июле 2011 г. по соображениям безопасности исследование PALLAS было досрочно прекращено. Среди пациентов, получавших дронедарон, было зарегистрировано двукратное превышение числа госпитализаций и смертности от сердечно-сосудистых заболеваний, в том числе инфарктов и инсультов.
Столь драматическая разница в результатах 2 исследований может быть объяснена положительным прямым антиаритмическим влиянием препарата на восстановление и поддержание синусового ритма в исследовании ATHENA [12] и отсутствием этого влияния при хронической ФП в исследовании PALLAS и, соответственно, сохраняющимся высоким риском развития осложнений ФП в последнем исследовании.
К сожалению, дронедарон показал потенциальную токсичность в отношении печени и легких. Это обстоятельство и неблагоприятные результаты исследования PALLAS заставили Европейское Агентство по лекарственным препаратам выпустить в 2011 г. специальный релиз по ограничению клинического использования дронедарона [http://ema/chmp/718819/2011]. Дронедарон рекомендуется использовать для поддержания синусового ритма только у лиц с пароксизмальной или персистирующей формой ФП после успешной кардиоверсии. Препарат не следует применять при хронической ФП и при сердечной недостаточности на фоне нарушенной функции левого желудочка. Препарат также не должен использоваться у лиц с нарушениями функции печени и легких. Перед назначением дронедарона рекомендуется рассмотреть варианты альтернативного медикаментозного лечения, а его прием должен сопровождаться контролем ферментов печени.
Целиварон и другие производные амиодарона
Целиварон — нейодированное бензофурановое производное амиодарона, разрабатываемое компанией Sanofi Aventis. Целиварон — мультиканальный блокатор, показавший в эксперименте 100% эффективность в купировании и 60% в предотвращении вагозависимой ФП у собак. Эффективность в дозах от 50 до 300 мг/сут изучалась в исследовании II фазы MAIA. Целиварон в дозе 50 мг/сут предотвращал рецидив ФП в течение 90 дней в 58% случаев по сравнению с 37% в группе плацебо [13]. Результаты исследования CОRYFREE по оценке возможности использования препарата для медикаментозной кардиоверсии ФП/ТП в дозах от 300 до 600 мг еще не опубликованы.
Ряд производных амиодарона представляют улучшенные преимущественно с точки зрения безопасности и более удобной фармакокинетики средства. При этом потерпели неудачу попытки синтеза Amio-Aqueous (Wyeth-Ayers) — амиодарона с повышенной растворимостью в воде.
ATI-2042 — пероральный, быстро метаболизируемый аналог амиодарона с периодом полувыведения около 7 ч. Как и родительское вещество, он содержит в структуре своей молекулы йод, однако быстрая фармакокинетика препарата позволяет в значительной степени избежать присущих амиодарону внекардиальных побочных эффектов. В пилотном исследовании ANI-2042 на 87% сокращал количество эпизодов ФП [14].
РМ 101 — амиодарон, комбинированный с циклодекстрином. Препарат быстро проявляет свое действие при внутривенном введении. Проходит I фазу клинических испытаний.
Неселективные блокаторы калиевых каналов
Сформулированная в конце XX века концепция «удлиненной реполяризации» как основного механизма антиаритмического действия препаратов III класса легла на благодатную почву [15]. Дело в том, что по мере накопления клинических данных о потенциальной угрозе препаратов I класса для больных, перенесших ИМ, интерес исследователей естественным образом сосредоточился на препаратах, преимущественно влияющих на удлинение реполяризации и оказывающих минимально выраженное действие на проводимость, обладающих антифибрилляторным и весьма желательным симпатолитическим потенциалом. Следует помнить, что в 90-е годы прошлого века не существовало имплантируемых антифибрилляторных устройств для борьбы с наиболее опасными угрожающими жизни желудочковыми тахиаритмиями. Это первоначально и определило интерес к данному классу ААП.
Концепция «удлинения реполяризации» предусматривала баланс между полезными антиаритмическими свойствами и потенциальным аритмогенным (TdP) потенциалом этих новых препаратов. Синтезированные в последующее десятилетие соединения некоторые исследователи условно разделили на мультиканальные блокаторы (воздействующие на 2 ионных тока и более) и на так называемые чистые препараты, подавляющие исключительно или преимущественно выходящие калиевые токи реполяризации (табл. 1).
Таблица 1. «Неселективные» антиаритмические препараты III класса
Ибутилид блокирует быстрый компонент выходящего калиевого тока IKr (см. рис. 1; см. табл. 1), что замедляет реполяризацию и удлиняет ПД в предсердиях и желудочках [16]. Препарат увеличивает рефрактерность в предсердиях, желудочках, системе Гиса—Пуркинье, дополнительных аномальных путях проведения и атриовентрикулярном узле. Препарат не влияет на проводимость. Ибутилид умеренно замедляет синусовый ритм и зависимо от дозы удлиняет интервал QT/QTc [17].
Ибутилид существует в виде раствора и сразу же рассматривался как препарат для медикаментозной кардиоверсии ФП и ТП. Ибутилид купировал ФП продолжительностью от 3 до 48 ч в 77% случаев, а ТП — в 87% [18], достоверно не отличаясь по эффективности от амиодарона. Заметно ниже была эффективность при персистирующей аритмии. При длительности ФП менее 90 дней эффективность ибутилида (0,015 мг/кг) варьировала от 31 до 44% [19, 20]. Кроме того, обнаружено, что ибутилид во всех исследованиях купировал ТП более эффективно, чем ФП соответствующей продолжительности.
Наиболее опасным побочным действием ибутилида была полиморфная желудочковая тахикардия, риск развития которой составлял около 4% [21]. Предикторами развития TdP являлись брадикардия, сердечная недостаточность, небольшая масса тела, женский пол [21]. В 1995 г. ибутилид получил одобрение FDA в качестве препарата для медикаментозной кардиоверсии в условиях специализированных отделений. Препарат в России не зарегистрирован.
Азимилид блокирует быстрый IKr и медленный IKs выходящий калиевый ток, замедляет реполяризацию и увеличивает рефрактерность в предсердиях и желудочках (см. рис. 1). Блокада IKs (помимо IKr) калиевого тока теоретически предполагала высокую эффективность при частой предсердной импульсации фибриллирующих предсердий. Однако, несмотря на первые обнадеживающие результаты, в исследованиях COMET I, COMET II и A-STAR при персистирующей ФП азимилид не только показал крайне низкую способность удерживать синусовый ритм, но и проявил аритмогенный потенциал в виде TdP [22—24]. Кроме того, в исследовании ALIVE азимилид не улучшал прогноз у постинфарктных больных c ФП [25].
Тедисамил является типичным мультиканальным блокатором. Препарат ингибирует быстрый IKr, кратковременный Ito, а также АТФ-чувствительный IK/ATP калиевые токи. Кроме того, он предотвращает тахисистолию при ФП за счет замедления предсердно-желудочкового проведения. Как оказалось, тедисамил при длительном применении вызывал диарею и, как следствие, TdP на фоне гипокалиемии, что исключило использование препарата в виде таблеток. Возможность его применения для медикаментозной кардиоверсии ФП также оказалась под вопросом. Тедисамил при испытании у 175 больных с недавно возникшей ФП в дозах 0,4—0,5 мг на 1 кг массы тела восстанавливал синусовый ритм в 40—50% случаев, при этом в 2 случаях наблюдалось развитие полиморфной желудочковой тахикардии [26].
Нифекалант — блокатор быстрого калиевого тока IKr с отчетливо выраженным феноменом обратной частотной зависимости антиаритмического действия. Применяется для купирования желудочковых тахикардий, устойчивых к другим ААП. Увеличивая рефрактерность в предсердиях, нифекалант купирует ТП в 75% случаев, однако он неэффективен при ФП [27].
Нибентан — первый отечественный ААП III класса, синтезированный в НИХФИ (Москва). В эксперименте нибентан блокировал калиевые токи задержанного выпрямления Ik+ и активируемый ацетилхолином калиевый ток Ik (Ach). Это приводило к удлинению реполяризации ПД и соответствующему увеличению рефрактерности в предсердиях и желудочках [28]. Препарат вызывал умеренное отрицательное хронотропное действие за счет прямого влияния на клетки синусного узла. Показана высокая антиаритмическая активность нибентана на моделях холинергической ФП у животных [29].
Первые клинические испытания, проведенные в 1993—1996 гг. в Институте клинической кардиологии им. А.Л. Мясникова, показали, что препарат демонстрирует отчетливые электрофизиологические эффекты, присущие «неселективным» ААП III класса [30, 31]. В дозе 0,125 мг на 1 кг массы тела препарат удлинял интервал QT/QTc в среднем на 21%, не влияя на продолжительность интервалов PQ и QRS. Рефрактерные периоды предсердий и желудочков возрастали на 19 и 16% соответственно; препарат умеренно снижал частоту синусового ритма и не влиял на показатели проводимости [32].
Значительное удлинение интервала QT и риск проаритмических побочных эффектов, обусловленных блокадой Ikr в желудочках, были особенно выражены на фоне синусовой брадикардии, при использовании больших доз препарата и у лиц с органическим поражением сердца. Так, при использовании нибентана с целью купирования желудочковых аритмий в остром периоде инфаркта миокарда в дозе от 0,125 мг/кг и более TdP возникала в 6% случаев [33, 34].
При этом препарат оказался высокоэффективным для восстановления ритма при персистирующей форме ФП и ТП. Нибентан стал первым отечественным препаратом, зарегистрированным и рекомендованным для медикаментозной кардиоверсии при персистирующей ФП и купировании пароксизмальных наджелудочковых тахикардий. В исследовании с участием 64 больных с ФП и ТП продолжительностью 6,7±6,8 мес (от 8 сут до 36 мес) нибентан в дозе 0,06 мг/кг восстанавливал синусовый ритм в 29,7% случаев при полном отсутствии аритмогенности. В дозе до 0,125 мг/кг эффективность препарата возрастала до 72% (68% — при ФП, 100% — при ТП), при этом риск развития TdP составил около 3% [35, 36].
Ниферидил — новый отечественный препарат III класса. В экспериментальном исследовании [37] ниферидил подавлял калиевый ток задержанного выпрямления Ik. Препарат снижал входящий кальциевый ток большой проводимости IСа, L, что приводило к снижению частоты синусового ритма [38]. Как и нибентан, ниферидил оказывал антихолинергическое действие, возможно, опосредуемое влиянием на М2-холинорецепторы. Препарат удлинял реполяризацию как в предсердиях, так и в желудочках. При этом увеличение рефрактерности в предсердиях начиналось с дозы 5 мкг/кг, тогда как достоверное увеличение рефрактерности желудочков отмечалось при дозе 40 мкг/кг. Эти различия имеют принципиальное значение, поскольку указывают на вполне отчетливые различия в действии препарата на ионные токи в предсердиях и желудочках. Это позволило предположить, что угроза появления аритмогенных проявлений типа TdP при использовании ниферидила могла быть существенно меньше, и поэтому его применение может оказаться более безопасным [39]. Эффективность нового препарата на моделях вагоиндуцируемой ФП у животных превысила эффективность нибентана: ниферидил в дозе 20—40 мкг/кг купировал ФП в 100% случаев, а предотвращал ее в 80% [40].
В ходе I фазы клинических испытаний (внутрисердечное электрофизиологическое исследование) ниферидил изучался в дозах от 5 до 20 мкг/кг внутривенно. В дозах 5 и 10 мкг/кг препарат не оказывал достоверного влияния на показатели предсердной и предсердно-желудочковой проводимости, автоматической функции синусного узла и рефрактерные периоды миокарда предсердий и желудочков, не влиял на интервалы PQ и QRS. При этом интервалы QT и корригированного QTc возрастали в среднем на 10%.
В дозах 15 и 20 мкг/кг ниферидил приводил к значительному и достоверному увеличению рефрактерности как предсердий, так и желудочков. В большей степени возрастала рефрактерность в предсердиях: на 29% в правом и на 38% в левом. Эффективный рефрактерный период правого желудочка возрастал в среднем на 22,6%. Отражением удлинения реполяризации в желудочках было удлинение интервала QT на 22%, что сопровождалось появлением в 50% случаев волны «u». Ниферидил в дозах 5—20 мкг/кг хорошо переносился, не проявлял побочных, в том числе аритмогенных, эффектов.
Спектр электрофизиологических эффектов ниферидила типичен для препаратов III класса. При этом следует обратить внимание, что клинические данные в определенной степени подтвердили экспериментальные результаты. Ниферидил не обладает выраженной предсердной «селективностью», однако влияние препарата на предсердную рефрактерность все же преобладает [41].
В рамках II фазы клинических испытаний у 30 больных с персистирующей формой ФП/ТП ниферидил применялся с целью восстановления синусового ритма [42]. Средняя продолжительность текущего эпизода аритмии составляла 6,1±4,8 мес (от 2 нед до 24 мес). Длительность заболевания, определяемая как время от первого возникновения ФП или ТП до момента включения в настоящее исследование, составила 41,5±88,35 мес. У 28 из 30 больных имелась персистирующая форма ФП, у 2 других — ТП. В исследование не включали больных после перенесенного ИМ, со сниженной фракцией выброса или выраженной гипертрофией миокарда. Препарат вводили внутривенно в дозе от 10 до 30 мкг/кг в виде трех последовательных болюсов по 10 мкг/кг с интервалом 15 мин с одновременной регистрацией суточного 12-канального холтеровского мониторирования электрокардиограммы. Введение препарата прекращали на любом из этапов, как только достигалось устранение ФП.
Ниферидил в дозе 10 мкг/кг восстановил синусовый ритм у 18 (60%) пациентов, включенных в исследование, в том числе в 2 случаях с ТП (рис. 2). Суммарная доза в 20 мкг/кг повысила эффективность до 70%, а после введения третьего болюса (суммарно 30 мкг/кг) ФП была купирована еще у 20% больных. Таким образом, суммарная эффективность ниферидила составила 90% (см. рис. 2).
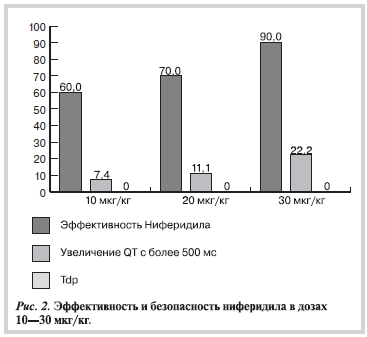
Во всех случаях препарат вызывал удлинение интервала QT. При этом превышение длительности QT более 500 мс после восстановления синусового ритма регистрировалось у 22% больных (см. рис. 2). Важно отметить, что ни в одном случае не было зарегистрировано проаритмии в виде TdP. Синусовая брадикардия (после купирования ФП) с ЧСС менее 50 уд/мин в дневное время отмечалась в 37% случаев, была гемодинамически незначимой, пациентами не ощущалась и коррекции не требовала. В настоящее время проводится многоцентровое клиническое исследование ниферидила в рамках III фазы клинических испытаний.
«Предсердно-селективные» блокаторы калиевых каналов
Формирование ПД в предсердиях и желудочках протекает в значительной степени одинаково. Однако имеются и различия: 1) фаза плато ПД в предсердиях достигается при более отрицательном значении трансмембранного потенциала; 2) продолжительность предсердного ПД короче. Эти различия связаны с некоторой разницей в распределении ионных каналов и соответствующих токов в предсердиях и желудочках (см. рис. 1). Например, ультрабыстрый калиевый ток задержанного выпрямления IKur и активируемый ацетилхолином калиевый ток IKAch имеется в предсердиях и отсутствует в желудочках. Только в предсердиях имеются белки ионных каналов Kv1.5 и GIRK4 [43, 44].
Таким образом, потенциально активные препараты, мишенью действия которых являлись бы ионные токи и рецепторы предсердий, могли бы исключить опасное влияние на желудочки (удлинение интервала QT и развитие TdP), характерное для ААП III класса [45]. Подобные препараты, демонстрирующие «селективное» влияние на предсердие, известны также как ARDAs (atrial repolarization-delaying agents), т.е. средства, замедляющие реполяризацию предсердий [46]. В последние годы синтезированы десятки потенциально «предсердно-селективных» препаратов, и некоторые из них находятся на стадиях экспериментальных исследований in vivo или клинических испытаний [47].
Вернакалант (Vernakalant, Cardiome and Astellas) — наиболее изученный препарат. Основной мишенью вернакаланта является ультрабыстрый калиевый ток. Кроме того, препарат оказывает незначительное влияние на быстрый Ikr и медленный Iks калиевый ток, блокирует кратковременный калиевый Ito и натриевый токи INa (см. табл. 2). Препарат был изучен в серии рандомизированных исследований ACTs (Atrial Arrhythmia Conversion Trials) I, II, III и IV у больных с ФП продолжительностью от 3 ч до 45 дней (рис. 3).
Таблица 2. Препараты, удлиняющие реполяризацию предсердий — «предсердно-селективные» препараты III класса
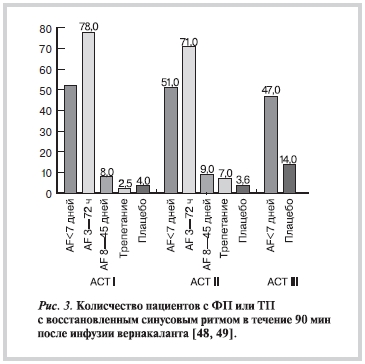
В исследование ACT II были включены больные с продолжительностью ФП 3—72 ч, возникшей после коронарного шунтирования или протезирования клапанов (см. рис. 3). С целью восстановления синусового ритма (АСТ I, II, и III) назначался вернакалант (или плацебо) в виде последовательных инфузий в дозе 3 и 2 мг/кг. При ФП до 7 сут вернакалант восстанавливал синусовый ритм в 51,7% (АСТ I), 51,2 % (АСТ II) и 50% (АСТ IV) наблюдений [48, 49]. При этом максимальная эффективность (70—80%) отмечена у больных с непродолжительной (не более 72 ч) аритмией (см. рис. 3).
Препарат, однако, был малоэффективен при персистирующей ФП длительностью более 7 дней, а также при ТП: 8 и 2,5% соответственно, успешной кардиоверсии в исследовании АСТ I и 9 и 7% в АСТ III. Препарат хорошо переносился, не вызывал ни достоверного (по сравнению с плацебо) удлинения QTc, ни TdP. Вернакалант был одобрен в FDA в качестве средства для медикаментозной кардиоверсии ФП.
Пероральная форма вернакаланта также проходит клинические испытания. В рандомизированном двойном слепом исследовании вернакалант (150, 300 или 500 мг 2 раза в день) назначался после медикаментозной или электрической кардиоверсии. Через 3 мес синусовый ритм сохранялся у 52% больных, принимавших 500 мг препарата, по сравнению с 39% в группе плацебо. Время до рецидива ФП в группе активного лечения превышало 90 дней по сравнению с 39 днями в группе плацебо [46]. Ни у одного пациента не были отмечены проаритмические эффекты препарата.
EN-D0101 (Xention) — ингибирует токи, опосредуемые Kv1.5 (аналог IKur у человека), которые участвуют в реполяризации мембраны кардиомиоцитов в предсердиях у ряда животных. Вероятно, XEN-D0101 является исключительно селективным калиевым блокатором. Препарат в экспериментальных исследованиях удлинял рефрактерность предсердий у собак на 49%, не удлиняя при этом интервал QT [50]. Препарат существенно снижал воспроизводимость и продолжительность ФП у животных. Данных о фармакокинетике и безопасности препарата нет. Находится в I фазе клинических испытаний (см. табл. 2).
AVEO 118 (Sanofi Aventis) блокирует IKur, а также кратковременный калиевый Ito и активируемый ацетилхолином калиевый ток IKACh (см. табл. 2). В экспериментальных исследованиях AVEO 118 значительно (на 56%) удлинял рефрактерность в левом предсердии, не влияя на продолжительность интервала QT/QTc. Препарат купировал персистирующую ФП у коз в 60% случаев [51]. Препарат плохо растворим, быстро метаболизируется печенью с периодом полувыведения около 20 мин. Клинические испытания II фазы завершены.
AZD7009 (Astra Zeneca) помимо IKur блокирует и другие неселективные выходящие калиевые токи, а также входящий натриевый ток INa (см. табл. 2). В доклинических испытаниях препарат преимущественно влиял на предсердную рефрактерность. Действие на желудочки сопровождалось уменьшением трансмуральной дисперсии рефрактерности. AZD7009 был эффективен на животных моделях. У человека препарат дозозависимо восстанавливал синусовый ритм в 58% случаев при продолжительности ФП 2—90 дней и в 78% случаев при продолжительности ФП не более недели [52]. Клинические испытания препарата были остановлены из-за экстракардиальных побочных эффектов и потенциально опасного удлинения интервала QT (без проявления TdP).
Заключение
Одним из путей повышения эффективности и безопасности ААП III класса является повышение селективности препаратов, для которых мишенями являлись бы предсерд ные реполяризующие токи IKur и IAch. Показано, что в предсердиях под действием ремоделирования базовый ток IAch возрастает, и, возможно, это играет ключевую роль в поддержании ФП [44]. Вероятно, отчасти механизмы антиаритмического действия амиодарона и дронедарона обусловлены подавлением IAch [44]. Предполагается, что селективные блокаторы предсердного IAch будут оказывать антиаритмическое действие [53].
Однако многочисленные клинические данные свидетельствуют, что эффективность «предсердноселективных» препаратов имеет довольно отчетливую обратную зависимость от продолжительности аритмии. Так, вернакалант почти 10-кратно снижает вероятность восстановления ритма, если ФП превышает 4 cут (см. рис. 3). Причиной этого, вероятно, является тахиаритмическое ремоделирование, индуцируемое фибрилляцией предсердий [54]. Резкое (8-кратное) увеличение частоты сокращений предсердий при возникновении фибрилляции предсердий приводит к кальциевой перегрузке кардиомиоцитов. Цитотоксическое действие Ca2+ п риводит к подавлению входящего тока ICaL, укорочению ПД, предсердной рефрактерности и формированию условий для устойчивой фибрилляции.
Помимо этого, доказано, что фибрилляция ремоделирует калиевые токи реполяризации. Оказалось, что ток Ikur крайне чувствителен к оксидантам, образующимся в клетке при возникновении фибрилляции предсердий и существенно угнетающим этот ток. Этим может объясняться быстрая утрата эффективности «селективными» калиевыми блокаторами. В экспериментальных исследованиях показана устойчивость токов Iks и Ikr к ATR ремоделированию [56]. Вероятно, неповрежденные и чувствительные токи Iks и Ikr как мишени для воздействия неселективных блокаторов и определяют крайне высокую эффективность нибентана и ниферидила при длительной персистирующей фибрилляции предсердий.
Можно предположить, что будущий «идеальный» антиаритмический препарат III класса — это мультиканальный блокатор калиевых токов IK+ реполяризации с преобладающим влиянием на рефрактерность предсердий (за счет блокады предсердных токов IKur и IAch), незначительным влиянием на рефрактерность желудочков, интервал QT и, соответственно, минимальным риском развития torsade de pointes.



