В структуре общей смертности населения Российской Федерации, по данным Росстата от 2010 г., болезни системы кровообращения (БСК) составляют 56,5% [1]. Причиной более 50% смертности от БСК и 29,1% общей смертности в России служит ишемическая болезнь сердца (ИБС). Не вызывает сомнения, что своевременная эффективная помощь данному контингенту и возможность профилактики острых расстройств коронарного кровообращения в определенной степени зависят от диспансерного наблюдения пациентов с ИБС. Согласно полученным данным, в 2009 г. доля больных ИБС, находящихся под диспансерным наблюдением, была на уровне 50%, что нельзя считать удовлетворительным.
Одной из главных проблем кардиологии и кардиохирургии была и остается внезапная сердечная смерть (ВСС), от которой в России ежегодно умирают более 350 тыс. человек. Тогда как во всех других экономически развитых странах этот показатель экспоненциально растет с возрастом, в России высока смертность лиц молодого и среднего возраста — именно в РФ зарегистрирована самая высокая смертность от БСК среди мужчин в возрасте от 30 до 50 лет. Внезапная смерть — результат кумуляции различных патогенных факторов, однако ее непосредственной причиной чаще всего служит нарушение ритма сердца (НРС). В то же время НРС — одно из самых тяжелых осложнений всех БСК, которое ухудшает клиническое течение и прогноз, способствует инвалидности, сокращает продолжительность жизни пациентов. Фатальные желудочковые тахиаритмии являются причиной ВСС почти в 80% случаев.
Развитию опасных для жизни аритмий сердца способствует хроническая сердечная недостаточность (ХСН). В целом сердечная недостаточность (СН) регистрируется у 0,5–2% населения во всем мире, при этом в России распространенность данного заболевания в несколько раз выше и, согласно результатам проведенных эпидемиологических исследований, в стране насчитывают более 8 млн человек с признаками ХСН, из которых более 3 млн имеют клинические проявления СН [2]. Декомпенсация ХСН становится причиной госпитализаций в кардиологические стационары почти каждого второго больного [3]. Серьезность ситуации с ХСН усугубляется крайне неблагоприятным прогнозом: годичная смертность больных клинически выраженной ХСН достигает 26—29%, т.е. за один год в РФ умирают от 880 до 986 тыс. больных ХСН.
Все указанные категории больных остро нуждаются в динамическом наблюдении, в постоянном мониторинге их состояния.
Технология персонального телемониторинга состояния больных. Развитие информационных и телекоммуникационных технологий привело к рождению принципиально нового медицинского сервиса, основанного на мобильном дистанционном мониторинге состояния пациентов с имплантированными антиаритмическими устройствами. Для клиник и их пациентов с электрокардиостимуляторами (ЭКС) и имплантируемыми кардиовертерами-дефибрилляторами (ИКД) создана замкнутая информационная сеть пациент — сервисный центр — врач — пациент (рисунок), которая обеспечивает принципиально новый уровень диагностики и оптимизации электротерапии сердца. Современные имплантаты снабжены телеметрической связью со специальным прибором, находящимся у пациента. Этот прибор обеспечивает передачу в сервисный центр данных о функционировании имплантированной системы и обширной информации о состоянии пациента, включая многоканальные внутрисердечные электрограммы высокого разрешения в режиме реального времени. Благодаря использованию телеметрических функций имплантатов, мобильных передающих устройств и развитию информационных сетей на базе Интернета мониторинг состояния пациента перестал ограничиваться процедурами амбулаторного осмотра в клинике, а охватил и время между ними, т.е. стал непрерывным (on-line). Это открыло возможности применения новых лечебных подходов, значительно расширяющих круг пациентов, находящихся под амбулаторным наблюдением, сокращающих число визитов пациентов в клинику.
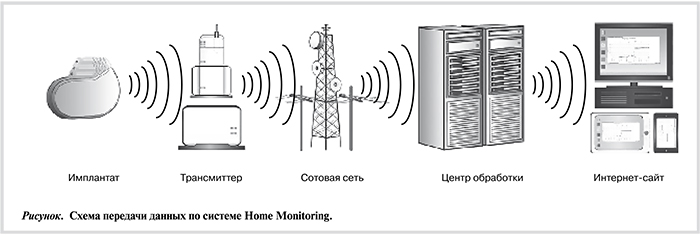
Основой медицинского сервиса Home Monitoring (домашний мониторинг) [4] является установление телеметрической связи между электронным имплантатом (ЭКС или ИКД) и прибором у пациента, трансмиттером, для создания единой замкнутой информационной системы имплантат — сервисный центр — лечащий врач — пациент. Прибор пациента получает телеметрические сообщения от имплантированного аппарата — регулярные (ежедневные) и триггерные (запущенные важным с клинической точки зрения событием, например, эпизодом аритмии) — и передает их, например через систему мобильной телефонной связи, в сервисный центр. Спустя несколько минут сервисный центр размещает обработанные данные в электронной форме на своем Интернет-сайте. Врач, наблюдающий пациентов с помощью удаленного мониторинга, имеет защищенный доступ к информации о своих пациентах на своей странице сайта сервисного центра. Для этого у врача имеется пароль, с которым он может в любое время посмотреть данные пациентов во всех деталях. На обзорной странице в первую очередь выделены те пациенты, на которых необходимо обратить внимание в связи с новыми сообщениями, вызванными эпизодом аритмии или состоянием имплантата.
Таким образом, врач получает постоянный оперативный доступ к разносторонней информации о состоянии пациента и его прибора в режиме on-line без участия пациента. Получая данные об эпизодах аритмий [5] и изменениях терапии, о состоянии системы электрокардиотерапии [6], в случае необходимости врач может внести коррективы в ход лечения пациента, вызвав его на внеочередное амбулаторное обследование [7]. У пациентов с ИКД сообщение генерируется и передается незамедлительно после прекращения каждого эпизода тахикардии. Такая функция повышает безопасность и эффективность электрокардиотерапии, своевременно информирует врача о возникших осложнениях, верифицирует аритмические события.
Важно, что удаленный мониторинг дает возможность врачу вмешаться в ход терапии до того, как состояние пациента ухудшится в результате непредвиденных осложнений. Например, при мониторинге передаются данные об эпизодах переключения режима стимуляции Mode Switch. Благодаря этому можно на ранней стадии обнаружить развитие фибрилляции предсердий, которая во многих случаях не сопровождается ярко выраженными симптомами, заметными самому пациенту, но увеличивает число госпитализаций до 76% [8].
Новая технология эффективна в диагностике НРС, значительно сокращает время, затрачиваемое на амбулаторное наблюдение пациентов, и дает значительный экономический эффект. Новый медицинский сервис позволяет врачу проводить своевременную оптимизацию режимов и параметров стимуляции, корректировать медикаментозное лечение, своевременно предупреждать осложнения у пациентов с быстрой динамикой течения заболевания, например ХСН.
Особенностью технологии Home Monitoring, в частности является ежедневная передача данных при малом потреблении энергии, что создает широкие возможности для проведения научных исследований. Завершенные рандомизированные исследования, включающие более 3000 пациентов (TRUST [9], COMPAS [10], REFORM [11], ECOST [12], IN-TIME [13]) доказали преимущество телемониторинга перед стандартной процедурой наблюдения. Дальнейшие исследования, включающие более 2000 пациентов (IMPACTi, EUROECO, Quantum) находятся в стадии анализа и публикации результатов.
В последние годы для лечения больных ХСН все шире применяется ресинхронизирующая терапия сердца — Cardiac Resynchronization Therapy (CRT). Она значительно улучшает качество жизни пациентов, но большой проблемой остаются при этом осложнения, вызванные прогрессированием заболевания. Постоянный мониторинг состояния больных этой категории может частично решить эту проблему при правильном выборе характеристик, которые объективно отражают развитие заболевания и угрозу возникновения аритмий. Такой набор характеристик объединен в единую опцию, названную Heart Failure Monitor (HFM — монитор сердечной недостаточности), которая имеется у трехкамерных имплантатов (ЭКС и ИКД), используемых для лечения больных ХСН. Анализируя динамическое изменение набора параметров (средний ритм сердца за сутки в целом, средний ритм сердца в состоянии покоя, вариабельность ритма сердца, число желудочковых экстрасистол в час, эпизоды фибрилляции предсердий, длительность физической активности пациента в течение дня), врач заблаговременно может предотвратить декомпенсацию состояния пациента путем внесения корректив в медикаментозное лечение или программу стимуляции, добиваясь оптимизации терапии.
Анализ достоверности сообщений показал, что в 97% случаев клинические решения, принимаемые на основе данных удаленного мониторинга, коррелируют с решениями, принимаемыми в ходе стандартного амбулаторного обследования [14].
В исследовании TRUST (1450 пациентов) [9] оценивалось среднее время, прошедшее от начала осложнения до момента регистрации врачом этого факта при двух различных методах наблюдения пациента (стандартного амбулаторного и телемониторинга). Время, выигранное при использовании удаленного мониторинга для выявления таких эпизодов, как фибрилляция желудочков, желудочковая тахикардия, наджелудочковая тахикардия, фибрилляция предсердий, составило более 30 дней [9, 10, 15, 16]. Мгновенная диагностика НРС позволяет предотвратить такие серьезные последствия для здоровья пациента, как инсульт, и резко снизить их количество [9, 10, 16, 17].
В то же время результаты обширного анализа, проведенного на основе 3 004 763 сообщений, полученных от 11 624 имплантированных устройств (от 4631 ЭКС, 6548 ИКД и 445 систем ИКД с функцией CRT; длительность мониторинга пациентов составила от 1 до 49 мес при суммарной длительности 10 057 лет), показали, что 47,6% больных не имели никаких аритмических событий [15]. Это означает, что почти 50% больных, в принципе, могли бы наблюдаться только с применением функции Home Monitoring без необходимости являться на процедуру наблюдения в клинику. Исследования TRUST [9], COMPAS [10], REFORM [11] продемонстрировали снижение числа визитов пациентов в клинику соответственно на 45%, 55 и 63%.
По данным исследования ECOST, телемониторинг сокращает число неадекватных шоковых разрядов на 52% и число связанных с ними госпитализаций на 72% [12]. Обеспечивается снижение числа набранных шоковых зарядов на 76% и снижение нанесенных шоковых разрядов на 71%, что оказывает значительное положительное влияние на долговечность батареи и удлиняет срок службы имплантата.
Применение удаленного мониторинга может дать значительную экономию средств по сравнению со стандартной процедурой наблюдения благодаря предупреждению инсультов, лечение которых, например в Германии, обходится в среднем в 43 129 евро [17] в расчете на одного пациента. Исследование MoniC показало эффективность централизованного мониторинга состояния пациентов [18]. Благодаря персоналу центра мониторинга, активно работавшего в случае возникновения перерывов в получении сообщений от имплантатов, эффективность передачи сообщений составила почти 90%. Таким образом, можно предотвращать большинство случаев инсульта, связанных с персистирующей формой фибрилляции предсердий.
Повышение выживаемости пациентов и организация клинической работы. Как показали исследования, клинические результаты улучшаются при телемониторинге по сравнению со стандартной процедурой наблюдения благодаря раннему обнаружению сердечно-сосудистых осложнений, снижению риска развития тяжелых осложнений (например, инсульта), раннему распознаванию и лечению при усилении симптомов СН,существенному снижению числа неадекватных шоковых разрядов; соблюдению режима наблюдения, удовлетворенности и спокойствию пациентов; повышению безопасности в конце срока службы имплантата. Более того, публикация результатов исследования IN-TIME [13] свидетельствует почти о трехкратном снижении общей смертности и смертности от сердечно-сосудистых заболеваний. Таким образом, наблюдение больных с применением технологии удаленного мониторинга становится важной составляющей эффективной электрокардиотерапии.
Исследование MoniC продемонстрировало важную роль организации работы по мониторингу состояния пациентов в рамках единого скринингового центра, который «фильтрует» сообщения [18].
Отечественные исследования. Целью начатого под эгидой Всероссийского научного общества специалистов по клинической электрофизиологии, аритмологии и кардиостимуляциии (ВНОА) в марте 2014 г. исследования ReHoming является оценка клинических результатов и экономической эффективности наблюдения больных с помощью технологии персонального телемониторинга в России. В ходе исследования регистрируются и анализируются параметры удаленного мониторинга, генерирующие сообщения о клинически важных событиях. Тренды физиологически значимых параметров служат основой для принятия врачом решения о необходимости вмешательства, предупреждающего развитие осложнений. В протоколах исследования регистрируются нежелательные явления, такие как госпитализация, осложнения сердечно-сосудистых заболеваний, необходимость изменения терапии, нарушения в работе имплантата.
Для оценки эффекта применения телемониторинга в структуре организации медицинской помощи в России определяется эффективность технологии в скорейшем выявлении нежелательных клинических явлений.
К ноябрю 2014 г. в 10 крупнейших центрах Российской Федерации в исследование включены более 50% запланированных исследованием 100 пациентов. Выводы исследования ReHoming могут быть использованы в дальнейшем для выработки клинических рекомендаций по наблюдению больных с помощью технологии телемониторинга для предупреждения осложнений и ятрогенных эффектов электрокардиостимуляции.
Одной из целей исследования ReHoming является дальнейшее развитие технологии персонального телемониторинга в России. В ходе реализации проекта создан сайт исследования rehoming.dicoming.com, являющийся частью интернет-платформы HELTERBOOK, и организован единый скрининговый центр. Создана основа для дальнейшего развития технологии телемониторинга физиологически значимых параметров больных и для интеграции медицинских данных, получаемых с применением различных приборов и датчиков. Платформа HELTERBOOK поддерживает все основные типы медицинских датчиков для анализа таких параметров, как ЭКГ, артериальное давление (АД), уровень глюкозы в крови, температура и масса тела, показатели пульсоксиметрии (SpO2), физическая активность, фазы сна.
Проект ReHoming локализует технологию Home Monitoring в структуре организации медицинской помощи в России и способствует выработке клинических рекомендаций по наблюдению больных с помощью технологии мобильного телемониторинга. Платформа новой персонифицированной медицины, в центре которой находятся пациент и его взаимоотношения с врачом, создает предпосылки для дальнейшего развития медицины на основе комплексного анализа интегрированных медицинских данных. HELTERBOOK — это инструмент для повышения эффективности лечения, в том числе медикаментозного, широкого внедрения различных видов удаленной диагностики, помощник в профилактике заболеваний и поддержании здорового образа жизни человека.
Концепция проекта может быть расширена и применена в четырех разделах новой сферы медицины и медицинской техники: 1) медицинская информационная система «Диспетчерский сервисный центр» (ДСЦ); 2) сервисная служба холтеровского мониторинга и скрининга населения; 3) сервисная служба мобильного мониторинга пользователей индивидуальных приборов; 4) сервисная служба мониторинга приверженности пациентов терапии.
1. Медицинская информационная система «Диспетчерский сервисный центр» (ДСЦ) создается как для диспетчерского контроля, мониторинга и анализа бизнес-процессов в системе здравоохранения, так и обеспечения указанных сервисных служб. Информационная инфраструктура должна формироваться в тесном сотрудничестве с региональными органами здравоохранения и российскими компаниями, работающими над созданием региональных и межрегиональных медицинских информационных систем, связывающих лечебно-профилактические учреждения (ЛПУ) в едином информационном пространстве.
2. Сервисная служба холтеровского мониторинга и скрининга населения обеспечивает визуализацию для экспертов скринингового центра всех регистраторов ЭКГ и АД, подключенных к центральным клиническим системам (ЦКС) ЛПУ.
ЦКС может включать центральную станцию ЛПУ, состоящую из одного или двух персональных компьютеров, к которой могут быть подключены до нескольких десятков пациентов с носимыми регистраторами данных ЭКГ, АД, передаваемых на ЦКС по радиоканалам. Комплекс помещений ЛПУ может быть оборудован беспроводной сетью Wi-Fi, в которой регистраторы представляют собой клиентские устройства, отправляющие и получающие данные по сети. Эксперты единого межрегионального скринингового центра будут обеспечивать амбулаторный скрининг населения в регионах и удаленную диагностику пациентов по требованию персонала на периферии. При этом будет использован клинический опыт ведущих медицинских центров России.
3. Сервисная служба персонального телемониторинга (СПТМ) обеспечивает непрерывный (24 ч в сут/7 дней в нед) мобильный мониторинг данных у пациентов с высоким риском ВСС и осложнений БСК, носителей наружных приборов персонального телемониторинга и имплантатов с функцией телемониторинга. Система обеспечивает раннюю диагностику аритмий и ИБС, а также экстренное оповещение об угрожающих состояниях пациентов для оказания им неотложной скорой помощи. В режиме амбулаторного наблюдения индивидуальный монитор передает сообщения с физиологически значимыми данными как в связи с сердечно-сосудистыми осложнениями, так и периодически, с интервалом, определяемым врачом. Приборную оснастку для удаленной диагностики и мобильного телемониторинга необходимо определять на основе имеющегося в России и в регионе клинического опыта, в сотрудничестве с компаниями, имеющими опыт не только разработки и производства сенсоров для регистрации физиологических показателей состояния человека, но и локализации технологий удаленной диагностики и телемониторинга в Российской Федерации.
4. Сервисная служба мониторинга приверженности пациентов лечению обеспечивает лечащего врача и соответствующее ЛПУ данными о соблюдении пациентами назначенной лекарственной терапии. Создание единого информационного пространства на основе созданных Интернет-платформ предполагает расширение технологических возможностей системы, в частности до уровня контроля соблюдения пациентами назначений врача, что обеспечит передачу пациенту, наблюдающему врачу, клиническому центру данных о приверженности для оптимизации терапии. Такая система способствует усилению взаимодействия врача и пациента, хорошо подходит для проведения обширных наблюдений эффективности того или иного лекарственного препарата, повышает эффективность медикаментозной терапии, сокращает сроки излечения и существенно уменьшает потребление малоэффективных препаратов.
Неотъемлемой частью проекта должно стать обеспечение приборной основы центра удаленной диагностики и персонального телемониторинга, включая программное обеспечение телемедицинского сервиса.
В проекте необходимо координировать деятельность медицинских учреждений с участием провайдеров мобильной связи, компаний, создающих информационные системы в сфере здравоохранения, в рамках единой системы общих организационных мероприятий.
В условиях страны с большой территорией, большими расстояниями до центров высокотехнологичной помощи телемониторинг может стать стратегическим решением проблем на периферии, связанных с ранней диагностикой и оказанием помощи больным в остром периоде заболевания, например поможет решить проблему «золотого терапевтического окна» при остром коронарном синдроме.
Направления развития персонального телемониторинга. Объем передаваемых с имплантата данных меняется как количественно, так и качественно по мере улучшения технических возможностей как самих имплантатов, так и средств мобильной телекоммуникации. По-видимому, дальнейшее развитие телеметрии в медицинской практике будет идти по пути развития технологий, как требующих участия пациента, так и не требующих или даже исключающих его. Развитие технических возможностей имплантируемых устройств и средств телекоммуникации создает предпосылки для расширения функций диагностики симптомов или заболеваний, незаметных пациенту или проявляющихся эпизодически. Ярким примером эффективности применения ЭКС или ИКД с функцией мобильного удаленного мониторинга является диагностика пароксизмальной фибрилляции предсердий. Опыт работы сервисного центра Home Monitoring с применением диагностического имплантата BioMonitor (имплантируемый монитор ЭКГ) свидетельствует также о широких возможностях телемониторинга в оценке эффективности лекарственной терапии, в верификации этиологии синкопальных состояний.
В современных ЭКС и ИКД заложены многие опции, которые со временем позволят еще больше расширить показания к применению электронных имплантатов. К этим опциям относятся такие параметры, как вариабельность интервалов RR, средний и максимальный желудочковый ритм при предсердной аритмии, рассчитываемые самими устройствами на основе измеряемых сигналов внутрисердечных электрограмм. Несомненно, более частая передача сигналов внутрисердечных электрограмм на основе четких медицинских критериев позволила бы расширить диагностические возможности электронных имплантатов. Достоверное определение текущего клинического статуса пациента с помощью удаленного мониторинга открывает путь к созданию методов и приборов, способных путем незамедлительного выявления экстренных ситуаций предотвращать осложнения заболеваний сердца.
Вариабельность ритма сердца (ВРС). Анализ ВРС стал эффективным диагностическим методом [19] для изучения механизмов контроля функций сердца автономной нервной системой. ВРС широко применяется в клинической практике для оценки состояния различных звеньев системы вегетативной регуляции [19, 20]: она отражает изменения баланса симпатического и парасимпатического тонуса при остром эмоциональном стрессе, оказывающих значительное воздействие на работу сердца и приводящих к дисфункции сократительной функции левого желудочка сердца, ишемии миокарда или НРС. Неблагоприятное патологическое воздействие факторов окружающей среды вызывает общий адаптационный синдром, основой развития которого является повышение активности симпатико-адреналовой системы. Система кровообращения как чувствительный индикатор адаптационных реакций организма [20] и ВРС как генерализованный параметр отражают степень напряжения регуляторных систем, обусловленную активацией системы гипофиз—надпочечники и реакцией симпатико-адреналовой системы.
Уменьшение параметров ВРС, особенно тех, которые отражают долговременную вариабельность — индекс треугольности TI, мощность VLF (0,0033-0,04 Гц), мощность ULF (<0,0033 Гц) и соотношение LF/HF (мощность диапазона частот 0,04—0,15 Гц к мощности диапазона частот 0,15—0,4 Гц), — является независимым предиктором сердечной смерти. У больных с гемодинамической нестабильностью (симптоматическая гипотензия) ВРС может существенно снижаться по сравнению с таковым у больных со стабильной гемодинамикой (без симптоматической гипотензии). Предполагается, что гемодинамическая нестабильность тесно коррелирует со сниженной ВРС и с нарушенным симпатическим/парасимпатическим балансом, что характеризует пациентов с ишемией миокарда. Пациенты с ИБС, сниженной систолической функцией левого желудочка и сниженной ВРС имеют наибольший риск ВСС.
ВРС как индекс автономного симпатического/парасимпатического баланса сердца, имеющий прогностическое значение, является независимым предиктором смерти у больных СН [21]. Создание имплантируемых приборов, способных постоянно регистрировать параметры ВРС, преодолело барьер на пути к получению долговременных данных о ВРС [22].
Было показано, что параметр ВРС — стандартное отклонение средних значений длины сердечных циклов SDANN (Standard Deviation of the Averages of NN intervals) — постоянно измеряемый имплантируемым устройством, является независимым предиктором возникновения сердечно-сосудистых осложнений в длительном периоде наблюдения [23]. Больные СН с высоким риском смерти или госпитализации имеют существенно более низкие SDANN. Следует отметить также, что снижение SDANN предшествует возникновению клинически значимой декомпенсации СН по времени в среднем на 16 дней — от времени пересечения определенного порогового значения параметра до госпитализации. Поэтому, постоянный мониторинг SDANN имплантируемым или наружным устройством может быть использован для подачи сигнала о приближающемся остром ухудшении состояния больного СН. Регистрация параметров ВРС предоставляет диагностическую информацию, имеющую большое клиническое значение и позволяющую провести стратификацию риска и оценку состояния больного СН.
Анализ ВРС может быть использован для разработки прогностических заключений на основе оценки текущего функционального состояния организма, выраженности его адаптационных ответов и состояния отдельных звеньев регуляторного механизма. В исследовании Home-CARE с применением имплантатов для электрокардиотерапии с функцией телемониторинга [24] использовалась оценка ВРС: ежедневно определялось стандартное отклонение средних сердечных интервалов среди всех сегментов NN продолжительностью 5 мин (SDANN) для построения тренда ВРС. Результаты, полученные в исследовании, показывают возможность применения этого подхода для широкого круга пациентов с различными заболеваниями, сопутствующими или связанными с СН, дают новый клинический материал для разработки алгоритма предиктора осложнений для большого числа заболеваний.
ЭКГ, снятые на поверхности тела пациента (поверхностная ЭКГ), позволяют обнаружить изменения в ориентации электрической оси сердца. У здорового человека среднее направление электрической оси сердца совпадает с его анатомической осью. Отклонения от этого направления могут быть вызваны различными патологиями, например изменениями массы миокарда (левостороннее смещение у больных артериальной гипертонией, правостороннее смещение при гипертрофии правого желудочка), блокады проведения и инфаркт миокарда.
Один из методов анализа ЭКГ для выявления инфаркта миокарда основан на анализе высокочастотных компонентов (100—500 Гц) комплекса QRS (который отражает длительность периода возбуждения миокарда) и его вариабельности [25], уменьшение которых может указывать на ишемию миокарда [26].
Другой метод дифференциальной диагностики ИБС [27] основан на регистрации ЭКГ с высоким разрешением и анализом ритма для выявления уменьшения ВРС. Уменьшение ВРС и стабилизация на низком уровне считаются признаками ишемии миокарда.
Таким образом, выявление инфаркта и ишемии миокарда может стать возможным на основе регистрации сигналов ЭКГ высокого разрешения для выявления относительных изменений сигналов в условиях нагрузки.
Мониторы для диагностики НРС и нарушений реполяризации, включая ишемию миокарда. На протяжении десятилетия в клинической практике применяются различные имплантируемые мониторы ЭКГ, отличающиеся небольшим размером и удобством подкожной имплантации. Они применяются для выяснения природы синкопальных состояний неясной этиологии и могут работать без замены в течение нескольких лет. Приборы не имеют внешних электродов и регистрируют ЭКГ, автоматически распознавая эпизоды нерегулярного ритма сердца. Эти эпизоды записываются в память прибора и могут быть рассмотрены врачом в ходе амбулаторного визита пациента в клинику или переданы в сервисный центр мониторинга для определения их истинного характера в режиме on-line.
Для выявления быстрых изменений сегмента ST, которые могут быть обусловлены острым коронарным синдромом или прогрессированием СН, разработана система, состоящая из имплантируемого подкожно прибора и тонкого электрода.
После выявления смещения сегмента ST система подает пациенту сигналы тревоги в форме вибрации, звука или изображений на наружный прибор. Возможна также телеметрическая передача информации от имплантата на другие внешние приемники.
С октября 2012 г. в клинической практике европейских стран для регистрации НРС широко применяется имплантируемый регистратор событий BioMonitor, имеющий на своем корпусе 3 наружных электрода. Биомонитор регистрирует эпизоды НРС, запоминает длительные записи ЭКГ высокого разрешения и передает данные в сервисный центр телемониторинга через трансмиттер. Данные автоматически анализируются для подготовки кардио-отчета и выработки предварительного клинического решения. Они мгновенно становятся доступны врачу на его персональной странице для просмотра и принятия решения для оптимизации лекарственной терапии или другого врачебного вмешательства.
Основываясь на накопленном опыте в области удаленного мониторинга состояния пациентов и использования имплантируемых приборов для регистрации электрической активности сердца, ВНОА совместно с ООО «Инжиниринговый Центр НИЯУ МИФИ» разрабатывает универсальный имплантируемый монитор ЭКГ для выявления как НРС, так и патологических изменений электрического возбуждения сердца, с оценкой фаз деполяризации и реполяризации, которые позволяют оценить ишемические изменения миокарда.
Техническими и функциональными особенностями разрабатываемого прибора, отличающими его от ранее существующих моделей, являются следующие:
- сочетание малых габаритов с функцией удаленного мониторинга;
- наличие акселерометра для определения уровня нагрузки пациента;
- возможность выявления достоверного смещения сегмента ST;
- новые алгоритмы для выявления клинически значимых и экстренных ситуаций.



