Среди всех суправентрикулярных тахикардий (СВТ) на долю атриовентрикулярной узловой реципрокной тахикардии (АВУРТ) приходится 35–40% случаев при исключении мерцательной аритмии [1–4]. Среди пациентов с АВУРТ соотношение между женщинами и мужчинами составляет 3:2 [1, 5, 6]. Считается, что АВУРТ является доброкачественной аритмией, которая встречается у относительно молодых лиц (выраженные клинические проявления приходятся на возраст 32±18 года) без структурной патологии миокарда и не характеризуется высоким риском развития внезапной сердечной смерти [1, 3, 4].
Известно, что высокая частота сердечных сокращений у больных на фоне пароксизмального течения СВТ может приводить сначала к диастолической, а затем и систолической дисфункции миокарда с последующим развитием аритмогенно обусловленной кардиомиопатии и сердечной недостаточности, что повышает риск развития тромбоэмболических осложнений [2–4]. Подобный характер течения заболевания весьма вероятен у пациентов, страдающих тахисистолическими формами фибрилляции предсердий (ФП) или трепетания предсердий (ТП), и маловероятен у больных с АВреципрокными
тахикардиями [3–5].
Целью настоящего исследования явилось изучение основных показателей центральной гемодинамики
методом эхокардиографии (ЭхоКГ) у пациентов с АВУРТ в межприступном периоде до радиочастотной
абляции (РЧА) медленной части АВсоединения и в течение одного года после выполнения операции.
Материал и методы
Пациенты с АВУРТ (n=81) были разделены на 2 группы: основную (исследуемую) и контрольную . Основную группу (n=81) составили пациенты с АВУРТ типичного течения (slowfast), средний возраст — 45,3±15,1 года, мужчин — 44 (72%), женщин — 17 (28%). Аритмический анамнез составил 10,7±8,5 года. Средняя частота сердечных сокращений на фоне пароксизма АВУРТ равнялась 168±14 уд/мин.
Основными жалобами пациентов исследуемой группы были приступообразные сердцебиения и замирание в области сердца (см. таблицу).
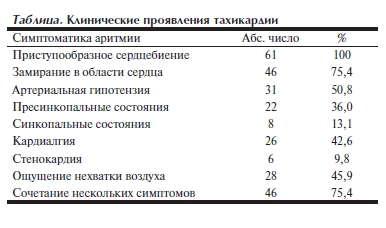
У большинства пациентов приступы АВУРТ имели выраженную клиническую симптоматику и расценивались нами как гемодинамически значимые: у 8 (13,1%) пациентов на фоне приступа аритмии развивались синкопальные состояния, у 6 (9,8%) — стенокардия и у 31 (50,8%) — артериальная гипотензия, что требовало оказания ургентной медицинской помощи. Помимо АВУРТ, у 13 (21%) пациентов (3 женщины) диагностировались сопутствующие заболевания сердечнососудистой системы: ишемическая болезнь сердца — у 3, постмиокардитический кардиосклероз — у 2 и артериальная гипертензия — у 8.
Всем пациентам исследуемой группы проводили эндокардиальное электрофизиологическое исследование (ЭФИ) и РЧА — модификацию медленной части атриовентрикулярного соединения (АВсоединения).
В контрольную группу вошли 20 практически здоровых лиц (15 мужчин, 5 женщин) в возрасте
41,9±5,3 года, у которых в результате проведенного обследования не было выявлено структурной патологии сердечнососудистой системы. Обе группы были сопоставимы по возрасту и полу.
Под местной анестезией по методике Сельдингера выполняли пункцию левой подключичной вены, правой и левой общих бедренных вен. В левую общую бедренную вену устанавливался интродьюсер трипорт диаметром 12 Fr. В правую общую бедренную вену, в левую подключичную вену устанавливались интродьюсеры диаметром 8 Fr. Через интродьюсер трипорт диаметром 14 Fr вводили 3 диагностических электрода, которые устанавливали в верхнелатеральном отделе правого предсердия, области пучка Гиса и верхушке правого желудочка. Через подключичный интродьюсер диаметром 8 Fr вводили диагностический 10полюсный электрод, который устанавливали в коронарном синусе [7, 8].
Протокол ЭФИ включал определение антеро- и ретроградного эффективного рефрактерного периодов медленной и быстрой части АВсоединения, точки Венкебаха, режима индукции и купирования тахикардии, методику введения синхронизированного желудочкового экстрастимула из верхушки правого желудочка, парагисиальную стимуляцию для верификации АВУРТ и дифференциальной диагностики с другими СВТ. В отсутствие индукции АВУРТ протокол ЭФИ повторяли
после внутривенного введения атропина сульфата в дозе 0,02–0,04 мг/кг массы тела больного [7, 8].
После эндокардиальной верификации диагноза АВУРТ переходили к следующему этапу операции —
РЧА медленной части АВсоединения [7, 8].
Область интереса для нанесения эффективной РЧ-аппликации определяли на основании бииуниполярной регистрации потенциалов медленной части атриовентрикулярного соединения на фоне синусового ритма. При достижении оптимального позиционирования и стабилизации картирующего электрода в области регистрации потенциалов медленной части АВ-соединения
проводили РЧ-воздействие. Параметры мощности и температуры нагрева устанавливали в режиме «контроль по температуре»; они составляли 45 Вт и 50 ˚С соответственно [7, 9–12].
После РЧ-воздействий в области медленной части АВ-соединения проводился контрольный протокол
ЭФИ, заключавшийся в проведении программированной и асинхронной электрокардиостимуляции предсердий в режиме индукции клинической аритмии (не менее 10 сессий). Если пароксизм АВУРТ не воспроизводился, то протокол электрокардиостимуляции предсердий повторяли после внутривенного введения атропина из расчета 0,01–0,02 мг/кг массы тела пациента [12].
Параметры центральной гемодинамики в основной и контрольной группах изучали с помощью трансторакальной ЭхоКГ, которую выполняли на аппаратах Acuson 512 Sequoia фирмы Acuson (США) и Vivid3 фирмы GE (США). При проведении ЭхоКГ пациент находился в горизонтальном положении (на спине и на левом боку). Обследование выполняли в режимах М, 2D, PW и CW (цветового допплеровского картирования кровотока). Обработка изображений осуществлялась с помощью специального пакета программ для кардиологических расчетов на соответствующем ультразвуковом аппарате. В ходе проведения протокола трансторакального эхокардиографического исследования измеряли следующие параметры левого желудочка (ЛЖ): конечный диастолический диаметр, конечный систолический диаметр, конечный диастолический объем, конечный систолический объем,
фракция выброса по формуле Teichholz, систолодиастолическое укорочение, а также конечный диастолический диаметр правого желудочка и размер левого предсердия. Определяли признаки, свидетельствующие о наличии соединительнотканной дисплазии и малых аномалий развития сердца (пролапс митрального клапана — ПМК, дополнительные хорды ЛЖ и т.д.).
Анализ параметров центральной гемодинамики, изученных методом ЭхоКГ у 61 пациента с типичной
АВУРТ, проводили до операции и через 2, 6 и 12 мес после РЧА, а в контрольной группе — однократно.
Расчет выполняли на персональном компьютере с использованием приложения пакета статистического
анализа данных Statistica 6.0 for Windows. Для оценки количественных показателей применяли непараметрические критерии (Вилкоксона, Ньюмена—Кейлса). Данные представлены в виде среднего значения ± стандартное отклонение. Различия считали статистически значимыми при р<0,05.
Результаты
Нами проведен комплексный анализ ближайших и отдаленных (до 1 года) результатов РЧА у 61 больного с типичной формой АВУРТ. Эффектность РЧА за 1 год наблюдения составила 95,1%. Рецидив тахикардии в периоде наблюдения возник у 3 (4,9%) больных. Повторная РЧА была эффективна во всех случаях. В ближайшем послеоперационном периоде у 2 (3,3%) пациентов развились следующие осложнения: у одного (1,6%) — проксимальная полная АВблокада, потребовавшая имплантации постоянного водителя ритма, и у одной (1,6%) пациентки сформировалось артериовенозное соустье между общей бедренной артерией и общей бедренной веной (в месте пункции), потребовавшее
хирургического вмешательства — лигирования артериовенозного шунта.
Анализ параметров центральной гемодинамики, изученных методом ЭхоКГ у 61 пациента с типичной формой АВУРТ до и через 2, 6 и 12 мес после РЧА, продемонстрировал, что у больных с типичной АВУРТ до хирургического вмешательства не было выявлено достоверных различий по изучаемым параметрам с контрольной группой.
Это может свидетельствовать о том, что у пациентов с 10-летним анамнезом типичной формы АВУРТ
(в среднем 10,3±5,5 года) отсутствуют признаки структурного ремоделирования миокарда. Это еще более интересно в связи с тем, что у 21% из них были сопутствующие структурные заболевания сердечнососудистой системы (в том числе ишемическая болезнь сердца – 5%), а аритмический синдром характеризовался выраженной гемодинамической значимостью (гипотензия — в 50,8% случаев, эпизоды пресинкопе — у 36% больных, стенокардия — в 9,8% случаев; см. таблицу).
В ходе динамического наблюдения за пациентами исследуемой группы было установлено, что через 2, 6 и 12 мес после операции изучаемые эхокардиографические параметры не претерпели существенных изменений по сравнению с исходными.
Малые аномалии развития соединительной ткани сердца у пациентов с АВУРТ. В ходе проведения эхокардиографического обследования у пациентов с типичной формой АВУРТ малые аномалии развития соединительной ткани сердца были диагностированы в 28 (45%) случаях. Самым распространенным из них являлся ПМК, который был верифицирован у 21 (34%) пациента. В ходе трансторакальной ЭхоКГ у больных с АВУРТ также были выявлены следующие аномалии развития клапанного аппарата: утолщение, «избыточность створок» (n=4), удлинение хорд (n=3), аномально расположенные хорды (n=4) (см. рисунок). По данным трансторакальной ЭхоКГ у 5 (8%) больных было верифицировано открытое овальное окно. У 8 (13%) пациентов обнаруживалось сочетание нескольких малых аномалий сердца (удлинение хорд левого желудочка и патентное овальное окно — у 3, ПМК и аномально расположенные хорды — у 5).
Рисунок. Малые аномалии соединительной ткани сердца у пациентов с АВУРТ.
У пациентов контрольной группы малые аномалии развития соединительной ткани сердца были диагностированы в 2 (10%) случаях (ПМК).
Среди пациентов исследуемой группы (n=45), у которых приступ АВУРТ сопровождался гемодинамически значимой клинической симптоматикой (синкопе, стенокардия, артериальная гипотензия), малые аномалии сердца встречались у 20 (44%), тогда как среди остальных
больных (n=16), входивших в основную группу исследования, — у 8 (50%). Статистический анализ,
проведенный внутри группы больных с АВУРТ, не выявил достоверных различий между этими подгруппами пациентов. Не было получено также достоверных различий в изучаемых нами эхокардиографических показателях у пациентов с малыми аномалиями (n=28) и без них (n=31).
Обсуждение
На современном этапе развития интервенционной кардиологии радиочастотная модификация «медленной » части АВ-соединения благодаря высокой эффективности и безопасности является методом выбора при лечении больных с АВУРТ [3, 4, 7, 9]. Существующий тактический подход к лечению пациентов с АВУРТ основан на результатах нескольких крупных многоцентровых исследований, посвященных оценке эффективности и безопасности РЧА в ближайшем и отдаленном
периодах наблюдения [13–15]. Динамическое наблюдение за пациентами этой категории продемонстрировало, что первичная эффективность радиочастотной модификации медленной части АВ-соединения составляет 93–95%, частота развития осложнений не превышает 5% (включая развитие полной АВблокады, тампонады сердца, формирование артериовенозной фистулы и др.)
[3–5, 13–15]. Кроме того, интервенционное вмешательство, как правило, ассоциируется со значительным улучшением качества жизни пациентов и не требует поддерживающей антиаритмической терапии [13–15].
Нами было установлено, что у 74% пациентов, страдающих АВУРТ, приступы аритмии сопровождаются
серьезными нарушениями центральной гемодинамики (артериальная гипотензия, пресинкопе, стенокардия). Выраженность клинической симптоматики аритмии обусловлена тахисистолией желудочков, снижением ударного объема, совпадением систол желудочков и предсердий, рефлекторной дилатацией периферических сосудов, опосредованной через активацию карди опульмонального компонента барорефлекторной регуляции [16–21]. Косвенным образом в пользу последнего положения свидетельствуют данные Ю.Н. Гришкина и соавт. (2004), которые, изучив параметры центральной гемодинамики методом трансторакальной ЭхоКГ, выявили, что во время приступа АВУРТ наблюдается отчетливое увеличение переднезаднего диаметра левого предсердия с 32±0,5 мм (во время синусового ритма) до 35±1,1 мм (во время приступа тахикардии). Аналогичные изменения претерпевал поперечный диаметр правого предсердия, увеличивающийся во время
тахикардии с 36±0,9 до 39±1,5 мм [22].
Принято считать, что АВУРТ является доброкачественной аритмией идиопатического характера и изменения показателей центральной гемодинамики на фоне синусового ритма у пациентов этой категории не выявляются. Следует отметить, что исследования, посвященные данной клинической проблеме, в современной медицинской литературе чрезвычайно ограничены. Зачастую в них на первый план выходит собственно образ аритмии, а не клинические характеристики пациентов, и тем
более не длительность клинического мониторирования больных с АВУРТ после РЧА аритмии [3–4].
На основании данных трансторакальной ЭхоКГ нами было установлено, что у относительно молодых
пациентов с типичной формой АВУРТ (средний возраст 45,3±15,1 года) в межприступном периоде
не выявляются грубые структурные изменения сердца, и основные эхокардиографические показатели центральной гемодинамики сопоставимы с аналогичными характеристиками здоровых лиц.
Однако практически у 45% пациентов, страдающих АВУРТ, при проведении ЭхоКГ визуализируются
малые аномалии развития соединительной ткани сердца (ПМК, удлиненная заслонка нижней полой
вены, ложные хорды желудочков и др.), в то время как среди пациентов контрольной группы только у 2 (10%) пациентов диагностировался ПМК. Эти данные согласуются с результатами исследования M. Josephson и соавт., в котором было показано, что признаки дисплазии соединительной ткани (ПМК, ложные хорды левого желудочка, бикуспидальная аорта) верифицировались у 40–60% больных с пароксизмальными СВТ. Тем не менее авторы считают, что аритмия (в частности, АВУРТ) не рассматривается как признак соединительнотканной дисплазии [23]. В настоящий момент неизвестно, какие именно факторы определяют тяжесть гемодинамических нарушений, характер клинического течения аритмии и отдаленный прогноз у больных с этой формой аритмии.
В группе пациентов со средней частотой сердечных сокращений 168±14 уд/мин во время пароксизмов
АВУРТ нам не удалось выявить достоверных различий по частоте выявления малых аномалий развития
соединительной ткани между подгруппами пациентов с выраженными клиническими проявлениями
аритмического синдрома и пациентами, у которых пароксизмы тахикардии не были столь гемодинамически значимы. Полученные нами данные позволяют предположить, что наличие малых аномалий сердца не определяет выраженность клинических проявлений АВУРТ, по крайней мере в 45летней возрастной группе пациентов с 10-летним аритмическим анамнезом. Можно предположить, что это положение будет дискутироваться по мере увеличения возраста больных с АВУРТ и длительности их аритмического анамнеза.
По нашему мнению, эхокардиографическая верификация малых аномалий сердца, тем не менее, требует от лечащего врача настороженного отношения к этой категории пациентов как на этапе подготовки к операции, так и в ходе последующего динамического наблюдения [24–26].
В медицинской литературе имеется небольшое число публикаций, касающихся изучения возможных структурных изменений сердца после РЧА у пациентов с АВУРТ [24–26]. В этой связи нами проанализированы результаты трансторакальной ЭхоКГ, выполненной пациентам с АВУРТ через 2, 6 и 12 мес после операции. Полученные данные показали, что РЧА по поводу АВУРТ, требующая точного картирования аритмического субстрата, сопровождается небольшой площадью повреждения. Так, при повторной ЭхоКГ после эффективной РЧА не регистрируются зоны нарушений локальной сократимости миокарда, клапанный аппарат у всех больных остается неизмененным. Не было получено также данных о снижении инотропной функции сердца и увеличении размеров его полостей. Это свидетельствует о безопасности и малой травматичности метода РЧА, что позволяет рассматривать его как метод выбора в лечении этой аритмической патологии.
Заключение
Морфофункциональные характеристики миокарда у пациентов с атриовентрикулярной узловой
реципрокной тахикардией, изученные методом трансторакальной эхокардиографии, сопоставимы с аналогичными параметрами здоровых лиц и остаются без изменений в течение одного года наблюдения после проведения операции катетерной радиочастотной модификации медленной части
атриовентрикулярного соединения.



