В соответствии с рекомендациями Всемирной организации здравоохранения (ВОЗ) и Международного
общества и Федерации кардиологов (МОФК) (1996)в качестве одной из клинических форм кардиомио-
патий выделяется послеродовая, или перипартальная,кардиомиопатия (ПКМП), характеризующаяся развитием необъяснимой дисфункции левого желудочка (ЛЖ)и хронической сердечной недостаточности (ХСН), связанной с беременностью и родами [1, 2]. Она развивается в конце беременности или в течение первых месяцевпосле родов у женщин без подтвержденных заболеваний
сердечно-сосудистой системы [3]. Термин ПКМП былвпервые предложен J.G. Demakis в 1971 г. [4]. По мнению некоторых исследователей, ПКМП имеет весьма сходные черты с идиопатической дилатационнойкардиомиопатией (ДКМП). Вместе с тем особенност иклинического течения и параметры гемодинамики данных состояний по имеющимся сведениям несколько различаются [5, 6]. Низкая распространенность, относительно недолгая история изучения и недостаточная
осведомленность специалистов о данном заболевании способствуют сохранению множества нерешенных вопросов, касающихся его определения, классификации, особенностей клинического течения и прогноза. В связи с изложенным целью настоящего исследования явилась сравнительная оценка клинического статуса и параметров центральной гемодинамики у больных ПКМП и идиопатической ДКМП.
Материал и методы
Материалом исследования послужили данные 273 больных с ДКМП, наблюдавшихся в отделе некоро-
нарогенной патологии миокарда и сердечной недостаточности Республиканского специализированного центра кардиологии (РСЦК) МЗ РУз. Соотношение мужчин и женщин составило 177/96, при этом у 26 (9,5%) пациенток констатирована ПКМП. Данный диагноз во всех
случаях установлен в нашем центре, в том числе беременным и родильницам, направленных из родильных комплексов. Для постановки диагноза использовали критерии Объединенной рабочей группы ВОЗ/МОФК (1996): развитие симптомов ХСН в конце беременности или в течение первых 5 мес после родов; исключение других причин развития данного состояния и отсутствие документированных заболеваний сердца до беременности.
Всем больным помимо оценки клинического состояния с помощью шкалы ШОКС, верифицирования среднего функционального класса (ФК) ХСН согласно критериям Нью-Йоркской ассоциации сердца (NYHA) и определения толерантности к физическим нагрузкам с помощью теста с 6-минутной ходьбой (ТШХ) проводили рентгенокардиометрию с определением кардиоторакального индекса (КТИ), стандартную электрокардиографию в 12 отведениях с помощью компьютерного комплекса
Кардиолаб-2000, суточное мониторирование электрокардиограммы (ЭКГ) по Холтеру (ХМ ЭКГ), трансторакальную эхокардиографию (ЭхоКГ) при помощи ультразвукового аппарата Sonoline Versa-Pro (Siemens, Германия), имеющего электронные секторные датчики с частотой 2,5 и 3,75 МГц, по стандартной методике с использованием рекомендаций ASE (American Society of Echocardiography)
в М- и В-режимах. Дополнительно проводили биохимическое исследование крови, включавшее определение неспецифических маркеров воспаления (С-реактивный белок — СРБ), мочевой кислоты и липидного состава. Ретроспективно изучался 2-летний прогноз у пациенток с кардиомиопатиями.
Для сравнительной оценки клинико-функциональных и гемодинамических параметров 96 пациенток были разделены на 2 группы: 1-я — больные с ПКМП (n=26) и 2-я — с идиопатической ДКМП (n=70) (табл. 1).

Необходимо отметить, что при констатации ПКМП немедленно решали вопрос о прерывании беременности или родоразрешении, а в случае развития заболевания после родов — о прекращении кормления грудью с последующим назначением оптимальной терапии ХСН (ингибиторы ангиотензинпревращающего фермента или блокаторы рецепторов ангиотензина II, β-адреноблокаторы, диуретики, спиронолактон и по показаниям — дигоксин, амиодарон).
Статистическую обработку данных проводили с использованием пакета прикладных программ Statistica 6.0. Вычисляли среднее арифметическое (М) и стандартную ошибку среднего арифметического (m). Значимость различий определяли с помощью t-критерия Стьюдента. Для анализа достоверности различий между качественными признаками использовали критерий χ2. Различия считали статистически значимыми при р<0,05.
Результаты
При анализе демографических характеристик отмечено, что средний возраст больных с ПКМП, который составил 28,2±0,9 года, оказался достоверно меньше, чем в группе сравнения (43,4±2,3 года; р=0,01) (табл. 2). Оценка клинического статуса с помощью ШОКС показала, что состояние больных обеих групп к моменту поступления в стационар характеризовалось как тяжелое, о чем свидетельствовали средняя сумма баллов по данной шкале. При этом данный показатель был недостоверно выше
(на 8,5%) в группе больных с идиопатической ДКМП. Средний ФК ХСН (3,3±0,1 против 3,4±0,1; р>0,05)
и сроки от начала манифестации симптомов заболевания до поступления в стационар (8,6±2,5 и 10,6±2,8 мес; р>0,05) также достоверно не различались между группами. Оказалось характерным, что ПКМП развивалась в основном после родов (у 21 пациентки), при этом у 67% из них — спустя 3 мес и более. И лишь у 5 (19,2%) больных симптомы ХСН стали развиваться и прогрессировать во время последнего триместра беременности.
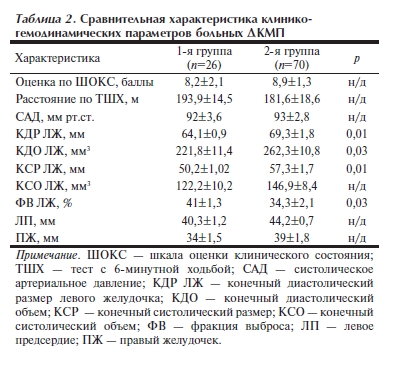
Результаты рентгенокардиометрии в большинстве случаев как у больных с ПКМП, так и идиопатической ДКМП отражали III степень кардиомегалии по КТИ (63,9±1,2 и 64,05±1,1% соответственно; р>0,05). Пройденное расстояние по результатам ТШХ в обеих группах также достоверно не различалось, составляя 193,9±14,5 и 181,6±18,6 м соответственно (р>0,05) (табл. 3). При анализе данных биохимического исследования крови выявлено некоторое повышение концентрации СРБ у больных 1-й и 2-й групп (5,6±1,2 и 6,6±1,2 мг/л соответственно; р>0,05) и мочевой кислоты (6,8±1,2 и 6,9±1,1 мг/дл соответственно; р>0,05), диагностическое и прогностическое значение которых у больных с ХСН активно обсуждается; при этом межгрупповые различия отсутствовали. Однако уровень общего холестерина, снижение которого также рассматривается как показатель тяжести ХСН, в группе больных с идиопатической ДКМП оказался
ниже, чем в группе с ПКМП (162,1±6,6 и 204,2±7,3 мг/дл соответственно; р<0,01).
Параметры внутрисердечной гемодинамики по результатам ЭхоКГ отражали сравнительное превалирование линейных размеров левых отделов сердца у женщин с идиопатической ДКМП (см. табл. 2). Так, у пациентов данной группы линейный размер левого предсердия на 8,8% (40,3±1,2 и 44,2±0,7 мм соответственно; р<0,01), конечного диастолического размера (КДР) ЛЖ — на 7,5%
(64,1±0,9 и 69,3±1,8 мм соответственно; р<0,01), конечного систолического размера ЛЖ — на 12,4% (50,2±1,02 и 57,3±1,7 мм соответственно; р<0,01) были достоверно больше, чем в группе ПКМП. Фракция выброса (ФВ) ЛЖ у последних на 6,7% превышала аналогичный показатель больных с идиопатической ДКМП (41±1,3 и 34,3±2,1% соответственно; р=0,03). Линейные размеры правых отделов сердца и отдельные параметры диастолической функции ЛЖ между группами больных значимо не различались.
Анализ показателей вариабельности ритма сердца по результатам ХМ ЭКГ показал, что у пациенток с ПКМП отмечается увеличение SDNN на 12% (р<0,05) и RMSSD на 18% (р<0,05), увеличение общей мощности спектра на 32% (р<0,01). Данные изменения сопровождались увеличением мощности высокочастотной составляющей спектра — HF на 28% (р<0,01) и снижением соотношения LF/HF на 26,5% (р<0,01) статистически значимого характера по сравнению с таковыми у пациенток 2-й группы. Вместе с тем другие выявляемые различия, такие как увеличение циркадного индекса (на 8,6%) и снижение мощности низкочастотной составляющей спектра LF (на 12,1%) у больных с ПКМП не имели статистически значимых различий (р>0,05).
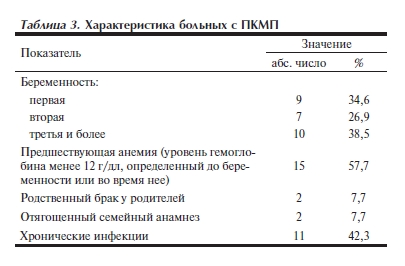
Помимо приведенного анализа показателей в группе пациенток с ПКМП нами изучались возможные предикторы развития данной патологии сердечно-сосудистой системы у исследуемых больных (см. табл. 3). Так, выявлено, что кардиомиопатия у женщин, включенных в наше исследование, в основном развилась в связи с первой или второй беременностью (у 61,5%). Отмечено также, что более чем у половины пациенток в до- и послеродовый период при развитии ХСН имелась анемия и у 42,3%
были сопутствующие хронические инфекции, в том числе вирусной этиологии (хроническая обструктивная болезнь легких, хронический пиелонефрит, хронические гепатиты В, С, инфекции группы TORCH). Такие показатели, как родственные браки между родителями и случаи развития кардиомиопатии среди членов семьи регистрировались в 2 случаях соответственно.
Изучение прогноза у женщин с кардиомиопатиями показало, что в группе ПКМП в 15,4% случаев отмечалось полное восстановление функции ЛЖ со значительной регрессией симптомов ХСН (табл. 4). Обнаружены также достоверные различия по частоте повторных госпитализаций по поводу дестабилизации состояния. Так, более ⅓ больных с идиопатической ДКМП госпитализировались 2 раза
и более в течение года, в то время как в группе ПКМП только 2 пациентки имели подобное число госпитализаций. Одной из особенностей ПКМП является относительно благоприятное течение заболевания. Согласно полученным результатам, в группе ПКМП число женщин со стабильным
течением ХСН на фоне приема оптимальной медикаментозной терапии было выше на 20%, чем в группе ДКМП.

Число смертельных исходов заболевания в группе с идиопатической ДКМП было недостоверно больше,
чем в группе ПКМП.
Обсуждение
Существует ряд определений ПКМП (табл. 5). Так, рабочие рекомендации Национального института сердца, легких, крови и Комитета по редким заболеваниям (2000) помимо 3 основных критериев ВОЗ/МОФК включило дисфункцию ЛЖ, установленную согласно классическим эхокардиографическим критериям: ФВ ЛЖ <45% и/или фракция укорочения ЛЖ <30%, с увеличением индексированного КДР ЛЖ >2,7 см/м2 или без такового [7, 8].
Таблица 5. Определение/классификация перипартальной ДКМП.
Научное положение Американской ассоциации сердца по современному определению и классификации кардиомиопатий (2006) определяет ПКМП как редко встречающуюся форму приобретенной первичной кардиомиопатии, ассоциированную с дисфункцией ЛЖ и ХСН [9]. В настоящее время ввиду углубления представлений о происхождении различных заболеваний миокарда возникла необходимость изменений существующей классификации кардиомиопатий в целом и дилатационной, в частности. В основу новой классификации, предложенной Рабочей группой по заболеваниям миокарда и перикарда ЕОК (2008), был положен этиологический принцип с отчетливой геномной направленностью. Согласно ей ПКМП отнесена к первичным негенетическим несемейным формам ДКМП и попадает в группу приобретенных кардиомиопатий, связанных с беременностью [10]. Последние рекомендации Рабочей группы по перипартальной кардиомиопатии Ассоциации
сердечной недостаточности ЕОК (2010) вносят значительные поправки и дополнения к критериям диагноза. ПКМП является идиопатической кардиомиопатией с признаками ХСН, обусловленной дисфункцией ЛЖ, которая развивается в течение последних месяцев беременности или после
родов, при исключении других причин развития ХСН. При этом не всегда может наблюдаться дилатация ЛЖ, но ФВ обычно ниже 45% [3]. Как видно, критерии диагноза ПКМП, претерпевая за последние 15 лет неоднократные пересмотры, стали значительно объемнее и шире.
Непосредственный анализ результатов нашего исследования свидетельствует, что в структуре ДКМП перипартальная форма составляет около 9%. Истинная частота развития ПКМП неизвестна, так как к настоящему времени не проведено ни одного крупного популяционного исследования. Вместе с тем есть сообщения, что ПКМП развивается в 1 случае на 3000—4000 живорожденных [2], а также известно, что более высокая распространенность отмечается в африканских странах. Частота случаев 1:1000 живорожденных регистрируется в частности в Южной Африке, а в США данный показатель составляет от 1:2289 до 1:4000 случаев живорождения [11, 12].
По результатам нашего исследования, возраст пациенток с ПКМП в среднем составил 28 лет. Ранее считалось, что ПКМП чаще развивается у женщин, чей возраст приближается либо к нижней, либо к верхней границе детородного возраста [13]. Тем не менее результаты нашего исследования согласуются с мнениями ряда ученых, которые отмечают, что в 24—37% случаев ПКМП
развивается у молодых и первобеременных женщин [14]. Непосредственная причина развития ПКМП точно не установлена. Однако описаны предрасполагающие, связанные с беременностью факторы (возраст роженицы, количество беременностей и родов, анемия, недостаточное питание, применение лекарственных препаратов при родовспоможении и т.д.). Наиболее заслуживающими внимание теориями патогенеза являются следующие:
1) развитие так называемого каскада оксидантный стресс — протеаза пролактина (катепсин D) — пролактин, роль воспаления (в плазме крови женщин с ПКМП часто обнаруживали повышение уровней СРБ, провоспалительных цитокинов);
2) аутоиммунные нарушения (in vitro доказано, что сыворотка больных ПКМП по-иному влияет на созревание дендритов, чем сыворотка здоровых родильниц, и в крови женщин с ПКМП выявляется достоверно больший титр IgG и его подклассов);
3) роль фетального микрохимеризма (наличие в крови матери эмбриональных клеток во время беременности и после ее завершения); 4) вирусной инфекции [15—18].
В нашем исследовании также более чем у 50% женщин с ПКМП имелась анемия и 42,3% пациенток в перипартальный период были подвержены хроническим, в том числе вирусным инфекциям.
Анализ литературы показывает, что в проведенных в данной области исследованиях заболевание характеризовалось подострым началом с клиническими симптомами застойной сердечной недостаточности (преимущественно левожелудочковой), нарушениями ритма сердца, кардиомегалией
и тромбоэмболическими осложнениями (Е.Н. Амосова). Как свидетельствуют результаты нашего исследования, в большинстве случаев промежуток времени с момента появления первых симптомов ХСН до госпитализации в тяжелом состоянии с ХСН III—IV ФК в среднем составил 8,6±2,5 мес
а КТИ — 63%; это соответствует III степени кардиомегалии. Согласно данным Е.Н. Амосовой, по изменениям показателей гемодинамики и морфологическому субстрату ПКМП идентична идиопатической ДКМП [6]. Результаты нашего исследования не совпадают с данным мнением, так
как установлено, что исходные параметры внутрисердечной гемодинамики характеризовались сравнительно сохранными, в отдельных случаях с достоверной разницей, значениями у больных с ПКМП, в отличие от группы женщин с идиопатической ДКМП, что являлось свидетельством
отсутствия выраженной дилатации полости ЛЖ и его дисфункции. Сходный взгляд на проблему имели также и другие авторы, отметившие большую гетерогенность клинических и гемодинамических показателей при ПКМП, чем при идиопатической ДКМП [14, 18]. Более того, нам импонируют
рекомендации упомянутой выше Рабочей группы по ПКМП (2010), которые позволили дополнить имеющуюся картину заболевания, выделяя, что не всегда может развиться дилатация ЛЖ, а ФВ ЛЖ обычно ниже 45% [3]. Изучение прогноза жизни у женщин показало, что у 15,4% пациенток с ПКМП,
включенных в наше исследование, в отличие от больных с ДКМП, в последующем отмечена полная регрессия заболевания с восстановлением функции ЛЖ. По данным литературы, стойкое клиническое улучшение встречается в 30—50% случаев (J. Sanderson и соавт., 1986; М. Roife и соавт., 1992;
G. Cloatre и соавт., 1996). Как было указано выше, женщинам с подтвержденной ПКМП мы назначали стандартную терапию ХСН. Вместе с тем в небольших клинических исследованиях доказана эффективность препаратов, подавляющих синтез пролактина (бромокриптин, каберголин),
и оказывающего ингибирующее влияние на цитокины — пентоксифиллина, которые могут рассматриваться в качестве новых препаратов специфической терапии ПКМП [19, 20]. Летальность в течение 2 лет среди больных с ПКМП в нашем исследовании составила 11,5%, также несколько
уступая данному показателю в группе ДКМП (17,2%). При этом во всех случаях женщины с ПКМП умирали от тяжелой декомпенсации ХСН. Существующие данные о смертности при ПКМП различаются в зависимости от географии исследований. Так, наименьшая смертность зафиксирована в США. Тем не менее К.А. Modi и соавт. отмечают, что данные по выживаемости и частоте восстановления функции
ЛЖ, поступающие из США, Гаити и ЮАР, несколько схожи [21]. Описания случаев ПКМП в ЮАР демонстрируют, что смертность несколько увеличивается с течением времени: 6-месячная и 2-летняя смертность составляет соответственно 10 и 28%. Клинические (одноцентровые) исследования,
проведенные в Бразилии и Гаити, сообщают о 6-месячной смертности 14—16%. Смертность по результатам 4-летнего наблюдения больных с ПКМП в Турции составила 30% [3].
Заключение
У женщин, страдающих послеродовой (перипартальной) кардиомиопатией, по сравнению с больными идиопатической дилатационной кардиомиопатией отмечаются менее выраженная дилатация левых отделов сердца и относительная сохранность сократительной функции левого желудочка при более благоприятном течении хронической сердечной недостаточности и меньшей частоте ее декомпенсации. Оказалось характерным также то, что послеродовая (перипартальная) кардиомиопатия развивалась в основном в послеродовой период и у женщин с предшествующей
анемией. Отсутствуют ясность в понимании этиологии, а также единодушное мнение исследователей
о гемодинамических критериях и сроках развития послеродовой (перипартальной) кардиомиопатии, что предопределяет продолжение исследований в данном направлении.



